Chủ đề mô hình cấu tạo nguyên tử oxygen: Mô hình cấu tạo nguyên tử oxygen là chìa khóa để hiểu rõ cấu trúc và tính chất của một trong những nguyên tố quan trọng nhất trong hóa học. Bài viết này sẽ giúp bạn khám phá chi tiết về cách sắp xếp các thành phần trong nguyên tử oxygen và vai trò của chúng trong các phản ứng hóa học.
Mục lục
Mô Hình Cấu Tạo Nguyên Tử Oxygen
Nguyên tử oxygen là một trong những nguyên tử quan trọng và phổ biến nhất trong hóa học. Để hiểu rõ hơn về cấu trúc và đặc tính của nguyên tử này, việc xây dựng mô hình cấu tạo nguyên tử oxygen là một phương pháp trực quan và hữu ích. Dưới đây là hướng dẫn chi tiết về mô hình này.
1. Thành Phần Của Nguyên Tử Oxygen
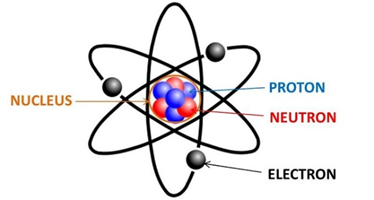
- Proton (p): Nguyên tử oxygen có 8 proton, mang điện tích dương.
- Neutron (n): Nguyên tử oxygen có 8 neutron, không mang điện tích.
- Electron (e): Nguyên tử oxygen có 8 electron, mang điện tích âm, phân bố ở các lớp vỏ electron.
2. Cấu Trúc Lớp Vỏ Electron
Electron trong nguyên tử oxygen được sắp xếp thành hai lớp vỏ:
- Lớp vỏ thứ nhất: Gồm 2 electron, tương ứng với quỹ đạo \(1s^2\).
- Lớp vỏ thứ hai: Gồm 6 electron, được sắp xếp trong các quỹ đạo \(2s^2\) và \(2p^4\).
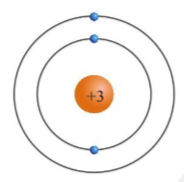
3. Mô Hình Bohr Cho Nguyên Tử Oxygen
Mô hình Bohr là một cách tiếp cận đơn giản nhưng hiệu quả để mô tả cấu trúc nguyên tử. Trong mô hình này, các electron được sắp xếp thành các quỹ đạo tròn xung quanh hạt nhân:
- Hạt nhân: Bao gồm 8 proton và 8 neutron.
- Các quỹ đạo: Lớp vỏ thứ nhất chứa 2 electron, lớp vỏ thứ hai chứa 6 electron.
Biểu thức cấu hình electron cho nguyên tử oxygen là:
\[1s^2 2s^2 2p^4\]
4. Vai Trò Của Mô Hình Nguyên Tử Oxygen
Mô hình nguyên tử oxygen giúp chúng ta hiểu rõ hơn về các khái niệm cơ bản như năng lượng ion hóa, liên kết hóa học, và cách thức mà oxygen tương tác trong các phản ứng hóa học. Mô hình này không chỉ quan trọng trong giáo dục mà còn trong các lĩnh vực như y học, công nghiệp, và nghiên cứu môi trường.
5. Ứng Dụng Thực Tiễn
Mô hình nguyên tử oxygen được ứng dụng rộng rãi trong nhiều lĩnh vực, từ thiết kế vật liệu mới trong công nghiệp đến nghiên cứu các phương pháp điều trị trong y học. Nó cung cấp một nền tảng để phát triển các công nghệ tiên tiến và cải thiện hiệu suất trong nhiều quá trình công nghiệp.
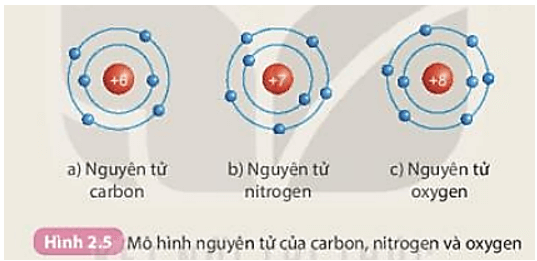
1. Giới Thiệu Về Nguyên Tử Oxygen
Nguyên tử oxygen là một trong những nguyên tử cơ bản và quan trọng nhất trong vũ trụ, đặc biệt là trong hóa học và sinh học. Với số hiệu nguyên tử là 8, oxygen nằm ở vị trí thứ hai trong bảng tuần hoàn sau hydro và là nguyên tố phổ biến thứ ba trong vũ trụ sau hydro và helium.
Oxygen đóng vai trò then chốt trong quá trình hô hấp của sinh vật sống và là thành phần chính trong nhiều hợp chất hóa học, bao gồm nước (H2O) và carbon dioxide (CO2). Oxygen có cấu trúc bao gồm 8 proton, 8 neutron trong hạt nhân và 8 electron phân bố trên hai lớp vỏ điện tử.
Các electron này được sắp xếp theo cấu hình electron \([1s^2 2s^2 2p^4]\), với hai electron ở lớp vỏ thứ nhất và sáu electron ở lớp vỏ thứ hai. Oxygen là một nguyên tố phi kim mạnh mẽ, có khả năng kết hợp với nhiều nguyên tố khác để tạo thành các hợp chất hóa học phức tạp.
- Proton (p): 8 proton trong hạt nhân mang điện tích dương.
- Neutron (n): 8 neutron trung hòa điện tích.
- Electron (e): 8 electron mang điện tích âm, phân bố ở hai lớp vỏ.
Cấu trúc của nguyên tử oxygen làm cho nó trở thành một nguyên tố cực kỳ phản ứng, tham gia vào nhiều phản ứng hóa học, đặc biệt là quá trình oxy hóa. Oxygen cũng là một phần quan trọng của khí quyển Trái Đất, chiếm khoảng 21% khí quyển theo thể tích, và là nguyên tố cần thiết cho sự sống.
2. Các Mô Hình Nguyên Tử Đã Được Phát Triển
Qua lịch sử nghiên cứu khoa học, nhiều mô hình nguyên tử đã được phát triển nhằm giải thích cấu trúc và tính chất của các nguyên tử, bao gồm nguyên tử oxygen. Dưới đây là một số mô hình quan trọng đã đóng góp vào sự hiểu biết của chúng ta về nguyên tử:
- Mô Hình Nguyên Tử Của John Dalton:
Mô hình của John Dalton vào đầu thế kỷ 19 là một trong những mô hình nguyên tử đầu tiên. Ông hình dung nguyên tử như những quả cầu rắn, không thể chia nhỏ hơn. Theo Dalton, mỗi nguyên tố hóa học được cấu thành từ những nguyên tử có khối lượng và tính chất riêng biệt.
- Mô Hình "Bánh Bao Nho" Của J.J. Thomson:
Vào cuối thế kỷ 19, J.J. Thomson đề xuất mô hình "bánh bao nho", trong đó nguyên tử được mô tả như một khối cầu tích điện dương với các electron âm nằm rải rác bên trong như các hạt nho trong bánh.
- Mô Hình Hành Tinh Của Rutherford:
Ernest Rutherford đã cải tiến mô hình của Thomson bằng cách giới thiệu hạt nhân nguyên tử. Trong mô hình này, nguyên tử có một hạt nhân nhỏ, tích điện dương ở trung tâm, và các electron quay xung quanh nó theo các quỹ đạo, giống như các hành tinh quay quanh Mặt Trời.
- Mô Hình Nguyên Tử Bohr:
Niels Bohr đã phát triển mô hình hành tinh của Rutherford bằng cách đưa vào các mức năng lượng cho electron. Theo mô hình Bohr, electron chỉ có thể tồn tại ở các quỹ đạo cố định với năng lượng nhất định và có thể nhảy từ mức năng lượng này sang mức năng lượng khác.
- Mô Hình Cơ Học Lượng Tử:
Mô hình hiện đại nhất về nguyên tử là mô hình cơ học lượng tử, trong đó các electron không còn được coi là các hạt điểm trên quỹ đạo mà là các đám mây xác suất. Mô hình này cho phép mô tả vị trí và năng lượng của electron bằng các hàm sóng \(\Psi(x, y, z)\).
Các mô hình này không chỉ là các bước tiến quan trọng trong việc hiểu cấu trúc của nguyên tử oxygen mà còn mở đường cho nhiều phát hiện khác trong hóa học và vật lý học hiện đại.

3. Cấu Hình Electron Của Nguyên Tử Oxygen
Nguyên tử Oxygen có số hiệu nguyên tử là 8, điều này có nghĩa là nó có 8 proton trong hạt nhân và 8 electron phân bố xung quanh hạt nhân. Cấu hình electron của nguyên tử Oxygen là một trong những yếu tố quan trọng nhất để hiểu rõ về tính chất hóa học của nó.
3.1 Phân Bố Electron Ở Các Lớp Vỏ
Cấu hình electron của nguyên tử Oxygen được biểu diễn theo quy tắc phân bố electron vào các lớp vỏ theo thứ tự năng lượng tăng dần:
- Lớp vỏ thứ nhất (\(n=1\)): 2 electron
- Lớp vỏ thứ hai (\(n=2\)): 6 electron
Do đó, cấu hình electron của Oxygen có thể được viết là:
\(1s^2 2s^2 2p^4\)
Điều này có nghĩa là trong lớp vỏ \(n=1\), có 2 electron chiếm chỗ trong orbital \(1s\). Trong lớp vỏ \(n=2\), có 2 electron trong orbital \(2s\) và 4 electron trong orbital \(2p\).
3.2 Cách Đọc Cấu Hình Electron Oxygen
Khi đọc cấu hình electron của nguyên tử Oxygen, chúng ta cần chú ý đến các orbital và số electron có mặt trong mỗi orbital. Mỗi orbital được biểu diễn bằng một chỉ số (1s, 2s, 2p) và số electron được biểu diễn bằng số mũ phía trên (ví dụ, \(2s^2\) nghĩa là có 2 electron trong orbital \(2s\)).
Chúng ta có thể minh họa cấu hình electron của Oxygen theo dạng bảng sau:
| Orbital | Số Electron |
| 1s | 2 |
| 2s | 2 |
| 2p | 4 |
Qua cách đọc này, ta có thể dễ dàng xác định số lượng electron trong từng orbital, giúp hiểu rõ hơn về cấu trúc và tính chất của nguyên tử Oxygen.
4. Tầm Quan Trọng Của Nguyên Tử Oxygen
Oxygen là một trong những nguyên tố thiết yếu nhất đối với sự sống trên Trái Đất. Nguyên tử oxygen không chỉ cần thiết cho sự hô hấp mà còn đóng vai trò quan trọng trong nhiều quá trình hóa học và công nghiệp khác nhau.
- Hô hấp và sự sống: Oxygen là thành phần chính của quá trình hô hấp, giúp duy trì sự sống của tất cả các sinh vật. Khi hít thở, oxygen được hấp thụ vào máu và phân phối tới các tế bào, nơi nó tham gia vào quá trình chuyển hóa năng lượng.
- Quá trình cháy: Oxygen là chất duy trì sự cháy, cần thiết cho các quá trình đốt cháy nhiên liệu. Khi có đủ lượng oxygen, quá trình cháy diễn ra mạnh mẽ hơn và hiệu quả hơn, giúp tạo ra năng lượng cần thiết cho nhiều hoạt động công nghiệp và hàng ngày.
- Ứng dụng trong y học: Oxygen được sử dụng rộng rãi trong y học để cung cấp hỗ trợ thở cho bệnh nhân, đặc biệt là trong các trường hợp cấp cứu hoặc khi bệnh nhân không thể tự thở. Hơn nữa, khí oxygen còn được sử dụng trong các liệu pháp giảm đau khi kết hợp với nitơ oxit.
- Ứng dụng trong công nghiệp: Oxygen là yếu tố quan trọng trong nhiều ngành công nghiệp, từ hàn cắt kim loại đến sản xuất thép. Oxygen giúp tăng cường quá trình đốt cháy trong các lò cao và lò mở, duy trì nhiệt độ cao cần thiết cho việc sản xuất các kim loại chất lượng cao.
Nhìn chung, oxygen là nguyên tố không thể thiếu cho sự sống và nhiều lĩnh vực khác nhau trong cuộc sống và công nghiệp. Sự hiện diện của nó là một phần quan trọng trong việc duy trì và phát triển các hoạt động sống và sản xuất.

5. Kết Luận
Nguyên tử oxygen đóng một vai trò cực kỳ quan trọng trong nhiều lĩnh vực khoa học và ứng dụng thực tiễn. Với cấu trúc gồm 8 proton, 8 neutron trong hạt nhân, và 8 electron sắp xếp trong hai lớp vỏ điện tử, nguyên tử oxygen là nền tảng cho nhiều phản ứng hóa học và sinh học quan trọng.
Việc hiểu rõ cấu trúc của nguyên tử oxygen giúp chúng ta giải thích được các tính chất hóa học, bao gồm khả năng tạo liên kết và tham gia phản ứng, đặc biệt là trong quá trình oxy hóa, một phần không thể thiếu trong các hệ thống sinh học và công nghiệp.
Không chỉ dừng lại ở lý thuyết, mô hình cấu trúc nguyên tử oxygen còn mang lại những giá trị ứng dụng thực tiễn. Từ việc thiết kế các vật liệu mới cho đến các ứng dụng trong y học và bảo vệ môi trường, oxygen luôn là yếu tố trung tâm trong các nghiên cứu và phát triển công nghệ.
Qua việc nghiên cứu sâu hơn về nguyên tử oxygen, chúng ta không chỉ hiểu thêm về các đặc điểm của nó mà còn mở ra những cơ hội mới trong việc cải tiến các quy trình công nghệ và cải thiện chất lượng cuộc sống. Như vậy, có thể khẳng định rằng, việc hiểu biết và ứng dụng kiến thức về nguyên tử oxygen là một trong những yếu tố then chốt giúp thúc đẩy sự phát triển của khoa học và công nghệ hiện đại.



.png)