Chủ đề đặc điểm cấu tạo vỏ nguyên tử khí hiếm: Khám phá những đặc điểm cấu tạo vỏ nguyên tử của khí hiếm và tầm quan trọng của chúng trong các ứng dụng khoa học. Bài viết này sẽ giúp bạn hiểu rõ hơn về các yếu tố làm nên tính chất ổn định của khí hiếm, tại sao chúng ít phản ứng và cách chúng được sử dụng trong nhiều lĩnh vực khác nhau.
Mục lục
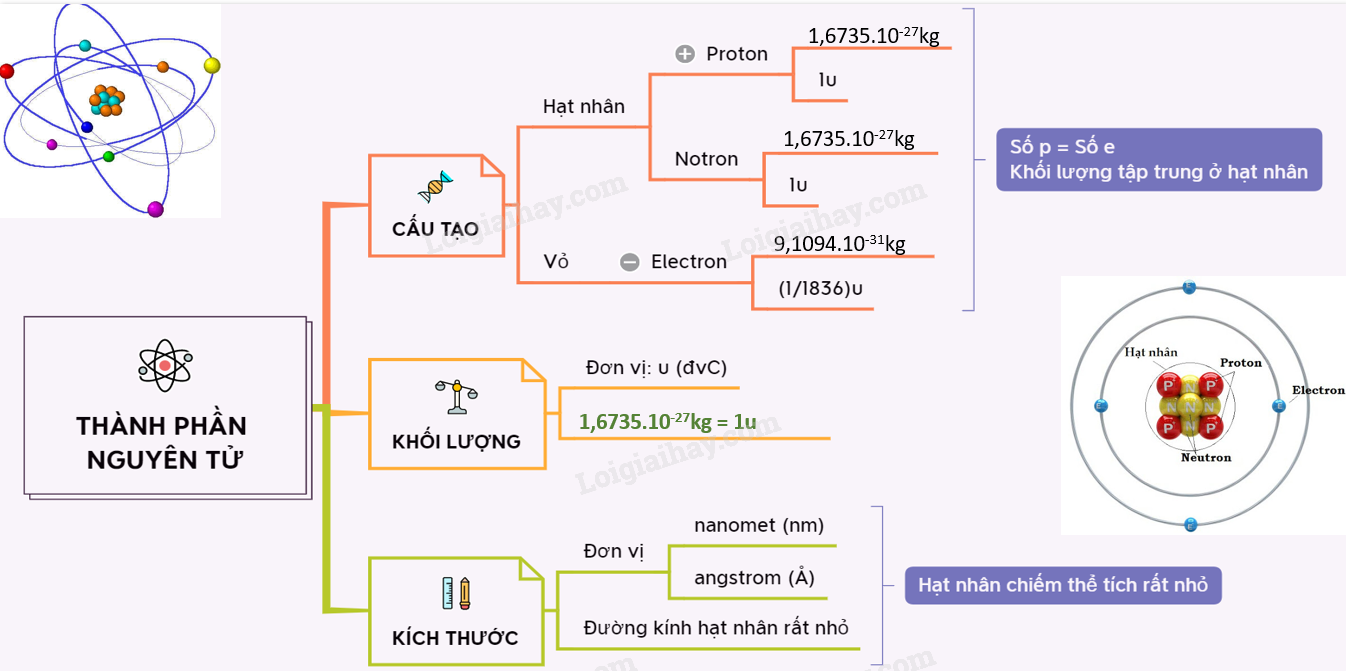
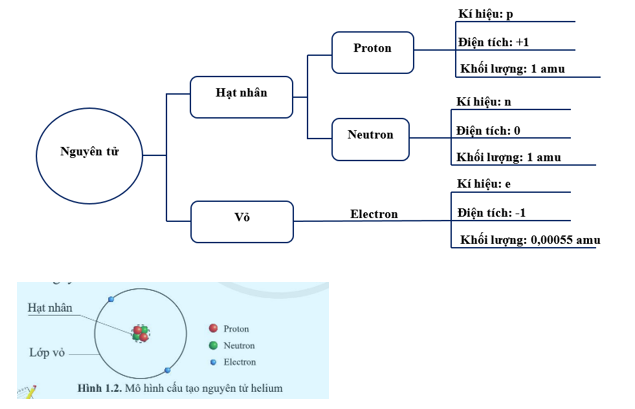
Đặc Điểm Cấu Tạo Vỏ Nguyên Tử Khí Hiếm
Khí hiếm là nhóm các nguyên tố hóa học nằm trong nhóm 18 của bảng tuần hoàn, bao gồm Helium (He), Neon (Ne), Argon (Ar), Krypton (Kr), Xenon (Xe), và Radon (Rn). Các nguyên tố này có cấu trúc vỏ electron hoàn chỉnh, khiến chúng trở nên rất ít phản ứng với các nguyên tố khác.
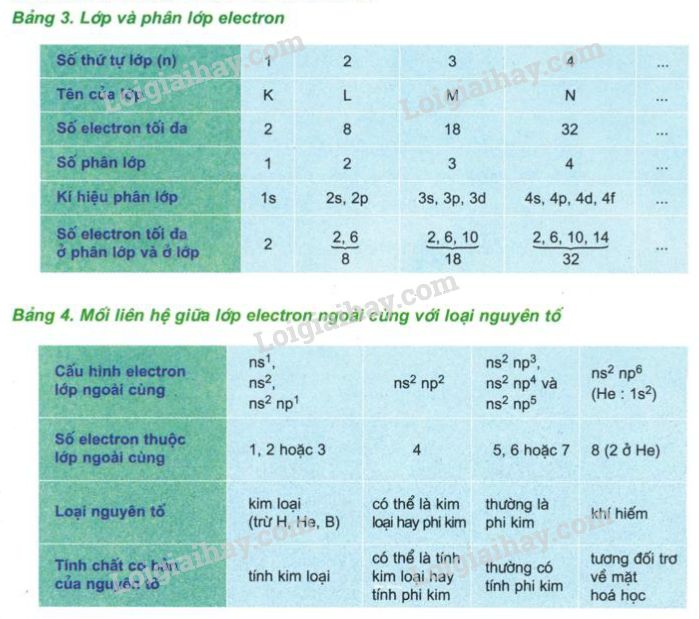
1. Cấu Trúc Vỏ Nguyên Tử
Nguyên tử của khí hiếm có cấu hình electron bão hòa, nghĩa là lớp vỏ ngoài cùng của chúng đã được lấp đầy hoàn toàn với các electron, tạo nên tính chất hóa học đặc biệt của nhóm này. Dưới đây là số electron của mỗi nguyên tố khí hiếm theo từng lớp:
| Tên Nguyên Tố | Số Proton | Cấu Hình Electron |
|---|---|---|
| Helium (He) | 2 | \(1s^2\) |
| Neon (Ne) | 10 | \(1s^2 2s^2 2p^6\) |
| Argon (Ar) | 18 | \(1s^2 2s^2 2p^6 3s^2 3p^6\) |
| Krypton (Kr) | 36 | \(1s^2 2s^2 2p^6 3s^2 3p^6 4s^2 3d^{10} 4p^6\) |
| Xenon (Xe) | 54 | \(1s^2 2s^2 2p^6 3s^2 3p^6 4s^2 3d^{10} 4p^6 5s^2 4d^{10} 5p^6\) |
| Radon (Rn) | 86 | \(1s^2 2s^2 2p^6 3s^2 3p^6 4s^2 3d^{10} 4p^6 5s^2 4d^{10} 5p^6 6s^2 4f^{14} 5d^{10} 6p^6\) |
2. Đặc Tính Hóa Học
Khí hiếm có đặc tính hóa học rất đặc biệt vì chúng không có xu hướng tạo liên kết với các nguyên tố khác do lớp vỏ electron đã hoàn chỉnh. Tuy nhiên, trong một số trường hợp, đặc biệt là với Xenon và Krypton, chúng có thể tạo ra một số hợp chất hóa học như xenon hexafluoride (XeF6).
3. Ứng Dụng Của Khí Hiếm
- Helium: Được sử dụng trong các bóng đèn huỳnh quang, khí cầu, và làm môi trường bảo quản trong các thí nghiệm khoa học.
- Neon: Được sử dụng trong các biển quảng cáo neon và trong một số thiết bị điện tử.
- Argon: Sử dụng trong hàn kim loại và trong các bóng đèn sợi đốt.
- Krypton và Xenon: Sử dụng trong các bóng đèn flash và trong một số thiết bị y tế.
- Radon: Có ứng dụng trong một số thiết bị phát hiện động đất và nghiên cứu phóng xạ.
Khí hiếm đóng vai trò quan trọng trong nhiều ngành công nghiệp và nghiên cứu khoa học nhờ vào tính chất hóa học ổn định của chúng.
.png)
Tổng quan về các khí hiếm
Các khí hiếm là nhóm nguyên tố hóa học thuộc nhóm 18 trong bảng tuần hoàn, bao gồm Helium (He), Neon (Ne), Argon (Ar), Krypton (Kr), Xenon (Xe), và Radon (Rn). Chúng có những đặc tính đặc biệt, chủ yếu là tính trơ hóa học và không màu, không mùi, không vị trong điều kiện tiêu chuẩn.
- Helium (He): Khí này được biết đến với khả năng làm mát mạnh mẽ, thường được sử dụng trong công nghệ làm mát, y tế và nghiên cứu khoa học. Helium cũng là thành phần chính trong khí thở của các thợ lặn biển sâu để ngăn ngừa độc tính của các khí khác.
- Neon (Ne): Neon nổi tiếng với ánh sáng đỏ rực rỡ khi phóng điện qua nó, thường được dùng trong các bảng hiệu quảng cáo và đèn chỉ thị điện cao thế.
- Argon (Ar): Đây là khí không màu và không phản ứng, được sử dụng rộng rãi trong các bóng đèn không xả khí để bảo vệ dây tóc vonfram khỏi bị oxy hóa.
- Krypton (Kr): Krypton được sử dụng trong đèn phóng điện và laser, đặc biệt trong các laser florua krypton có ứng dụng trong nghiên cứu khoa học và y tế.
- Xenon (Xe): Xenon có thể phát ra ánh sáng đa màu sắc khi bị kích thích điện, được sử dụng trong bóng đèn không xả khí, máy phát tia X, và làm khí gây mê trong y tế.
- Radon (Rn): Radon là khí phóng xạ, thường phát sinh từ sự phân rã của các nguyên tố phóng xạ như uranium và thorium. Nó chủ yếu được nghiên cứu trong lĩnh vực địa chất và vật lý hạt nhân.
Mỗi loại khí hiếm có cấu trúc vỏ electron hoàn toàn đầy đủ, khiến chúng rất ít khả năng tham gia vào các phản ứng hóa học thông thường. Điều này làm cho các khí hiếm cực kỳ ổn định và được sử dụng rộng rãi trong các ứng dụng không cần hoặc không muốn sự phản ứng hóa học.
| Tên khí hiếm | Số proton | Cấu hình electron |
|---|---|---|
| Helium (He) | 2 | 2 |
| Neon (Ne) | 10 | 2, 8 |
| Argon (Ar) | 18 | 2, 8, 8 |
| Krypton (Kr) | 36 | 2, 8, 18, 8 |
| Xenon (Xe) | 54 | 2, 8, 18, 18, 8 |
| Radon (Rn) | 86 | 2, 8, 18, 32, 18, 8 |
Các khí hiếm được thu thập và tinh chế qua nhiều phương pháp khác nhau, như chưng cất phân đoạn của không khí hóa lỏng (Neon, Argon, Krypton, Xenon) hoặc khai thác từ các mỏ khí tự nhiên (Helium). Radon thường được phân lập do sự phân rã phóng xạ của các nguyên tố nặng như radium.
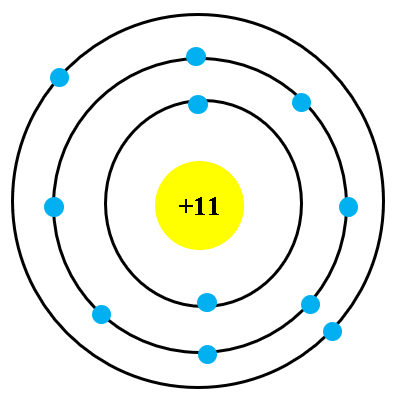
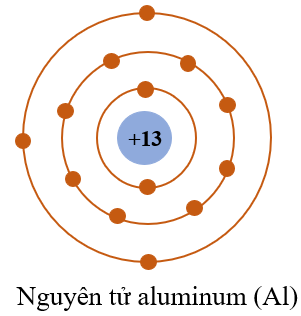
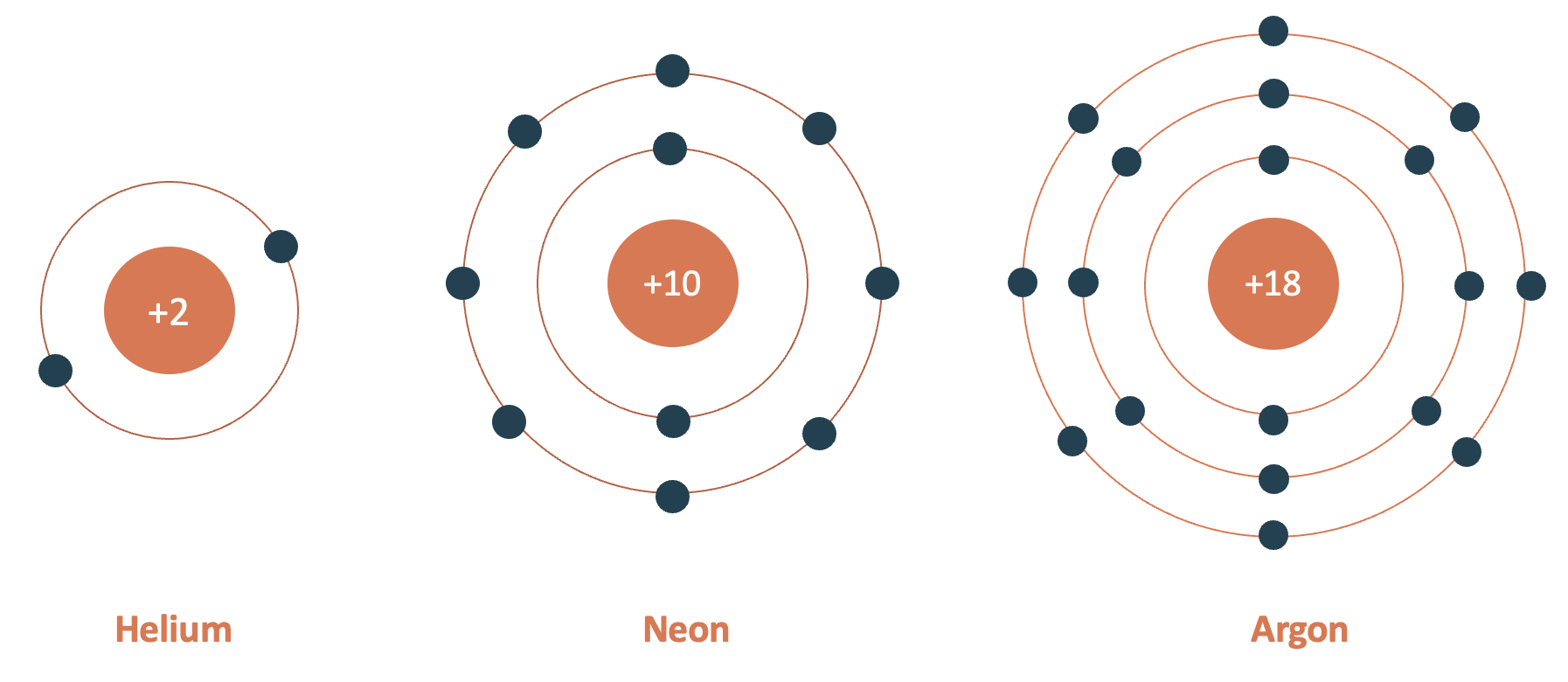
Cấu tạo vỏ nguyên tử của khí hiếm
Nguyên tử khí hiếm là những nguyên tố thuộc nhóm 18 trong bảng tuần hoàn, bao gồm helium (He), neon (Ne), argon (Ar), krypton (Kr), xenon (Xe), và radon (Rn). Các nguyên tố này có cấu trúc vỏ electron đặc biệt ổn định, khiến chúng ít tham gia vào các phản ứng hóa học ở điều kiện bình thường.
- Helium (He): Có số electron là 2, nằm hoàn toàn trong lớp vỏ đầu tiên. Cấu hình electron của He là \(1s^2\).
- Neon (Ne): Có 10 electron, với cấu hình electron là \(1s^2 2s^2 2p^6\). Lớp vỏ ngoài cùng có 8 electron, tạo thành một lớp vỏ hoàn chỉnh và ổn định.
- Argon (Ar): Có 18 electron, với cấu hình electron là \(1s^2 2s^2 2p^6 3s^2 3p^6\). Lớp vỏ ngoài cùng của Ar cũng có 8 electron, tương tự như Ne.
- Krypton (Kr): Có 36 electron, với cấu hình electron là \(1s^2 2s^2 2p^6 3s^2 3p^6 4s^2 3d^{10} 4p^6\). Lớp vỏ ngoài cùng có 8 electron, góp phần tạo nên tính chất trơ của Kr.
- Xenon (Xe): Có 54 electron, với cấu hình electron là \(1s^2 2s^2 2p^6 3s^2 3p^6 4s^2 3d^{10} 4p^6 5s^2 4d^{10} 5p^6\). Lớp vỏ ngoài cùng chứa 8 electron, giúp Xe ổn định về mặt hóa học.
- Radon (Rn): Có 86 electron, với cấu hình electron là \(1s^2 2s^2 2p^6 3s^2 3p^6 4s^2 3d^{10} 4p^6 5s^2 4d^{10} 5p^6 6s^2 4f^{14} 5d^{10} 6p^6\). Lớp vỏ ngoài cùng có 8 electron, tương tự như các khí hiếm khác.
Nhìn chung, các khí hiếm đều có lớp vỏ ngoài cùng với 8 electron, trừ Helium chỉ có 2 electron. Cấu hình này làm cho các khí hiếm trở nên rất ổn định và ít tham gia phản ứng hóa học, chính vì thế chúng thường tồn tại dưới dạng đơn nguyên tử.

Vai trò và ứng dụng của khí hiếm
Khí hiếm, còn được gọi là khí trơ, là nhóm các nguyên tố bao gồm Helium (He), Neon (Ne), Argon (Ar), Krypton (Kr), Xenon (Xe), và Radon (Rn). Những khí này có tính chất hóa học rất đặc biệt do có lớp vỏ electron ngoài cùng đầy đủ, khiến chúng hầu như không tham gia phản ứng hóa học. Do tính chất này, khí hiếm có nhiều vai trò và ứng dụng quan trọng trong cuộc sống và công nghiệp.
1. Ứng dụng trong công nghiệp và khoa học
- Helium (He): Được sử dụng rộng rãi trong các ứng dụng làm mát siêu dẫn, như trong các máy cộng hưởng từ (MRI) và thiết bị y tế. Helium lỏng được dùng để làm lạnh siêu dẫn và các thiết bị cần nhiệt độ cực thấp.
- Neon (Ne): Chủ yếu được sử dụng trong các biển hiệu phát sáng và đèn Neon. Neon phát ra ánh sáng đặc trưng khi bị kích thích bằng điện, tạo ra các hiệu ứng ánh sáng màu sắc rực rỡ.
- Argon (Ar): Thường được dùng trong bóng đèn không xả khí để ngăn chặn oxy hóa dây tóc vonfram, giúp kéo dài tuổi thọ của đèn. Argon cũng được sử dụng trong hàn kim loại để bảo vệ mối hàn khỏi sự xâm nhập của không khí.
- Krypton (Kr) và Xenon (Xe): Được sử dụng trong các bóng đèn không xả khí cao cấp và laser. Xenon còn được dùng làm khí gây mê trong y học và trong các nghiên cứu năng lượng hạt nhân.
2. Vai trò trong đời sống hàng ngày
- Kinh khí cầu và bóng bay: Helium được sử dụng để làm đầy kinh khí cầu và bóng bay vì nó nhẹ hơn không khí, giúp chúng bay lên cao.
- Ứng dụng trong y tế: Helium được dùng trong hỗn hợp khí thở của các thợ lặn biển sâu để ngăn ngừa các vấn đề sức khỏe do khí ni-tơ gây ra. Ngoài ra, khí này cũng được dùng trong điều trị hen suyễn và các bệnh về hô hấp.
3. Ứng dụng trong nghiên cứu khoa học và công nghệ cao
Các khí hiếm, với tính chất trơ và ổn định, thường được dùng trong các nghiên cứu khoa học và công nghệ cao, bao gồm nghiên cứu về cấu trúc nguyên tử, nghiên cứu vật liệu, và phát triển các công nghệ mới trong lĩnh vực y tế, không gian và năng lượng.
Kết luận
Với tính chất hóa học đặc biệt và đa dạng ứng dụng, khí hiếm đóng vai trò quan trọng trong nhiều lĩnh vực từ công nghiệp, y tế cho đến nghiên cứu khoa học. Chúng không chỉ giúp cải thiện chất lượng cuộc sống mà còn thúc đẩy sự phát triển của nhiều ngành công nghiệp và công nghệ hiện đại.
Kết luận
Khí hiếm là nhóm nguyên tố độc đáo với cấu tạo vỏ nguyên tử hoàn chỉnh, khiến chúng hầu như không tham gia phản ứng hóa học. Sự ổn định và tính chất hóa học đặc biệt này làm cho khí hiếm trở thành yếu tố quan trọng trong nhiều lĩnh vực khác nhau.
Trong công nghiệp, khí hiếm như Helium, Neon, và Argon được sử dụng rộng rãi từ làm mát siêu dẫn cho đến các ứng dụng chiếu sáng và bảo vệ mối hàn. Điều này cho thấy sự linh hoạt và giá trị không thể thay thế của khí hiếm trong việc cải tiến công nghệ và sản xuất.
Trong đời sống hàng ngày, vai trò của khí hiếm cũng không thể thiếu, từ việc làm đầy bóng bay bằng Helium đến việc hỗ trợ y tế cho các thợ lặn biển sâu. Khí hiếm cũng góp phần quan trọng trong lĩnh vực nghiên cứu khoa học, từ việc phân tích cấu trúc nguyên tử đến phát triển công nghệ mới.
Như vậy, với những đặc tính hóa học độc đáo và ứng dụng rộng rãi, khí hiếm không chỉ đóng góp vào sự phát triển của khoa học và công nghệ mà còn nâng cao chất lượng cuộc sống. Sự hiện diện của chúng trong nhiều lĩnh vực khác nhau khẳng định vai trò không thể thiếu trong thế giới hiện đại.