Chủ đề cấu tạo nguyên tử natri: Cấu tạo nguyên tử Natri không chỉ là kiến thức cơ bản trong hóa học mà còn đóng vai trò quan trọng trong nhiều lĩnh vực. Bài viết này sẽ cung cấp cho bạn cái nhìn chi tiết về cấu trúc, tính chất hóa học, và ứng dụng của Natri trong đời sống hàng ngày cũng như trong công nghiệp hiện đại.
Mục lục
Cấu Tạo Nguyên Tử Natri
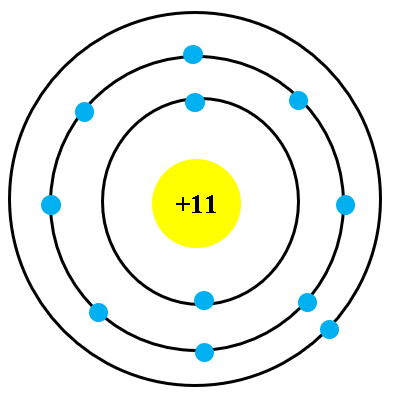
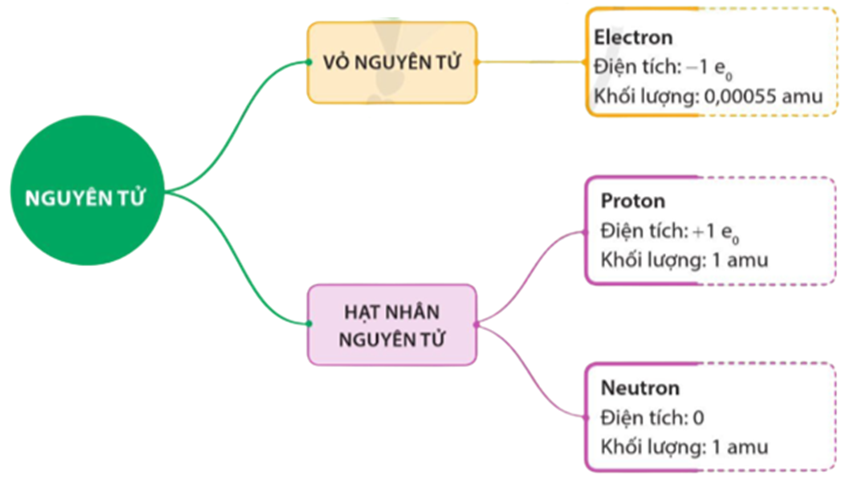
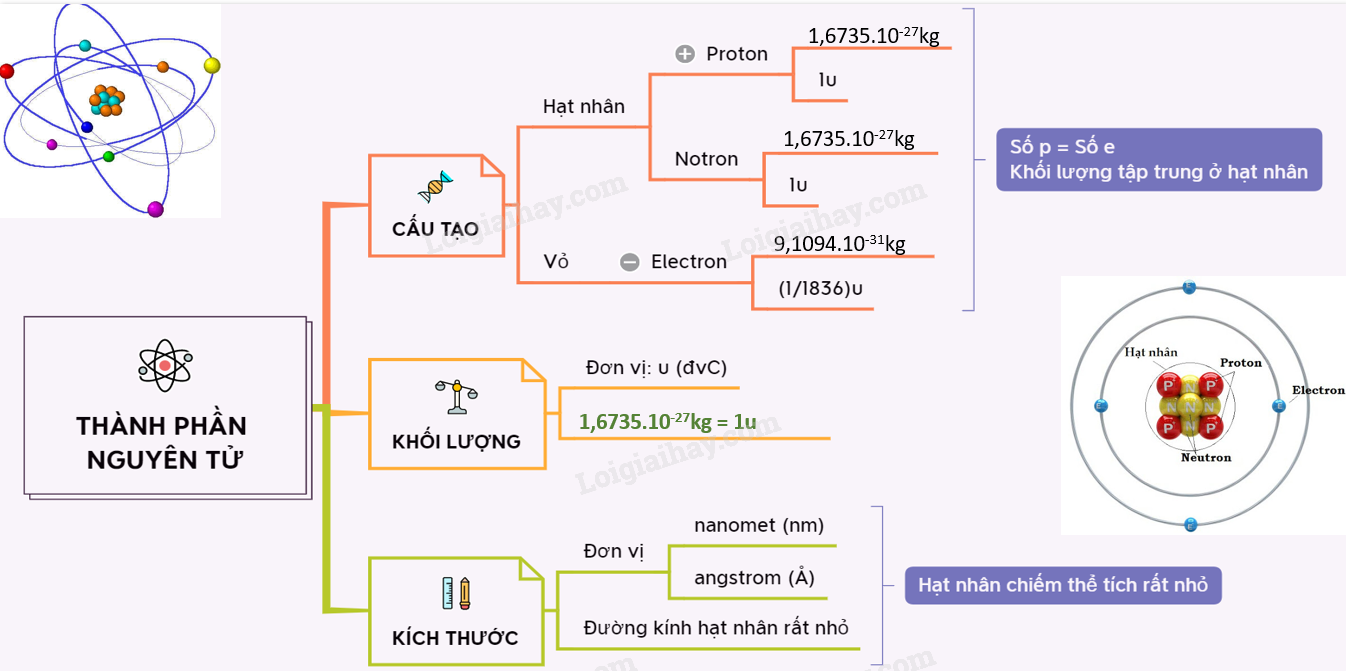
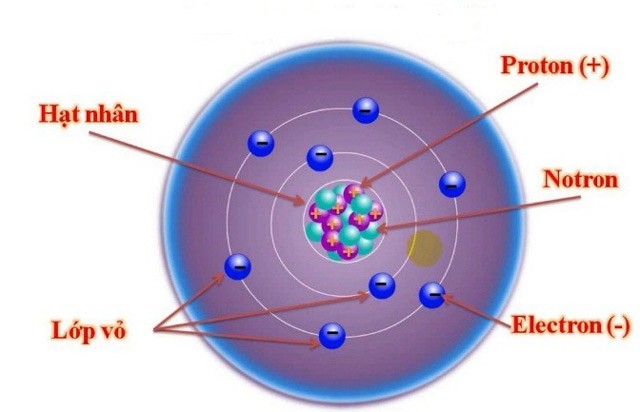
Nguyên tử natri (Na) là một nguyên tố thuộc nhóm kim loại kiềm với số hiệu nguyên tử là 11. Nguyên tử này có cấu trúc đặc biệt, gồm một hạt nhân chứa proton và neutron, và các electron quay xung quanh theo các lớp electron.
1. Cấu Hình Electron Của Natri
Cấu hình electron của nguyên tử natri được biểu diễn như sau:
\[ 1s^{2}2s^{2}2p^{6}3s^{1} \]
Điều này có nghĩa là natri có tổng cộng 11 electron được sắp xếp vào ba lớp vỏ electron, trong đó lớp ngoài cùng chỉ chứa một electron duy nhất.
2. Cấu Trúc Nguyên Tử
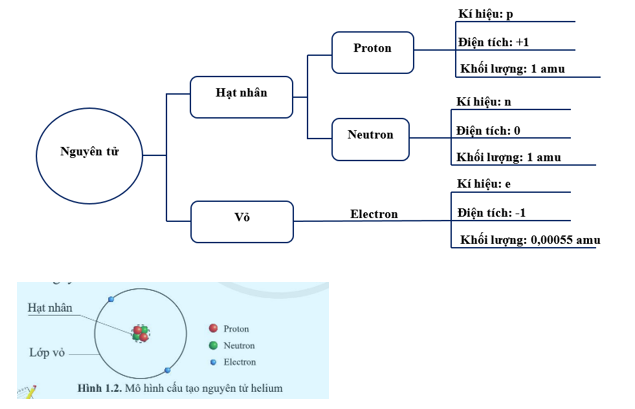
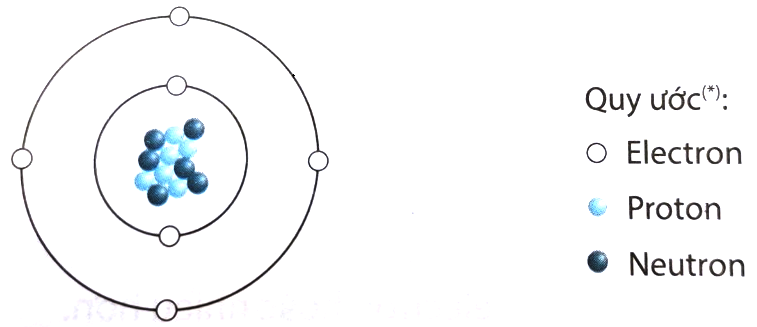
- Hạt nhân: Hạt nhân của nguyên tử natri chứa 11 proton và 12 neutron.
- Lớp vỏ electron: Các electron được sắp xếp theo ba lớp vỏ:
- Lớp thứ nhất (K): 2 electron
- Lớp thứ hai (L): 8 electron
- Lớp thứ ba (M): 1 electron
3. Tính Chất Hóa Học Của Natri
Natri là một kim loại có tính khử mạnh do nó có xu hướng nhường electron ngoài cùng để đạt cấu hình bền vững. Một số phản ứng tiêu biểu của natri bao gồm:
- Phản ứng với oxy: Natri phản ứng với oxy tạo ra oxit natri:
- Phản ứng với nước: Natri tác dụng với nước tạo ra natri hydroxide và khí hydro:
- Phản ứng với axit: Natri phản ứng mạnh với axit, đặc biệt là HCl:
\[ 4Na + O_{2} → 2Na_{2}O \]
\[ 2Na + 2H_{2}O → 2NaOH + H_{2} \]
\[ 2Na + 2HCl → 2NaCl + H_{2} \]
4. Ứng Dụng Của Natri
Natri có nhiều ứng dụng quan trọng trong công nghiệp và đời sống:
- Sử dụng trong sản xuất xà phòng, thủy tinh, và giấy.
- Làm chất truyền nhiệt trong lò phản ứng hạt nhân.
- Ứng dụng trong sản xuất natri clorua (muối ăn), natri hydroxide (dùng trong công nghiệp hóa chất).
- Sử dụng trong các hợp chất tẩy rửa, như natri bicarbonate (baking soda).
5. Phương Pháp Điều Chế Natri
Natri được điều chế chủ yếu bằng phương pháp điện phân muối natri clorua (NaCl) trong điều kiện nóng chảy. Quá trình này tạo ra natri kim loại và khí clo:
\[ 2NaCl_{(nc)} → 2Na_{(r)} + Cl_{2(g)} ↑ \]
6. Kết Luận
Nguyên tử natri là một thành phần quan trọng trong hóa học với nhiều ứng dụng thiết thực. Cấu trúc và tính chất hóa học của nó đã đóng góp vào nhiều lĩnh vực từ công nghiệp đến đời sống hàng ngày.
1. Giới thiệu về nguyên tử Natri
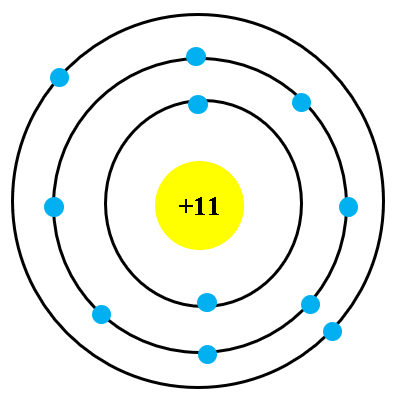
Nguyên tử Natri là một trong những nguyên tử cơ bản trong bảng tuần hoàn, thuộc nhóm kim loại kiềm. Với ký hiệu hóa học là \( \text{Na} \), Natri có số nguyên tử là 11, tức là trong nguyên tử Natri có 11 proton trong hạt nhân.
Natri tồn tại chủ yếu ở dạng hợp chất, đặc biệt là dưới dạng muối (như \( \text{NaCl} \)). Do có một electron ở lớp ngoài cùng, Natri rất dễ mất đi electron này để trở thành ion \( \text{Na}^+ \), từ đó tham gia vào nhiều phản ứng hóa học quan trọng.
- Số nguyên tử: 11
- Ký hiệu hóa học: \( \text{Na} \)
- Cấu hình electron: \( 1s^2 2s^2 2p^6 3s^1 \)
- Nhóm: Kim loại kiềm, nhóm 1
Nguyên tử Natri có cấu trúc đơn giản nhưng đóng vai trò quan trọng trong nhiều lĩnh vực khoa học và công nghệ. Với tính chất hoạt động mạnh, Natri được sử dụng rộng rãi trong các phản ứng hóa học và ứng dụng công nghiệp khác nhau.
2. Cấu trúc của nguyên tử Natri
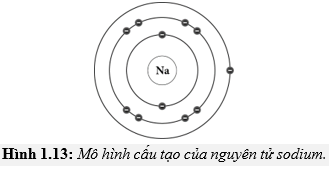
Nguyên tử natri (Na) có số nguyên tử là 11, nghĩa là nó có 11 proton trong hạt nhân và 11 electron quay xung quanh. Các electron này được sắp xếp vào các lớp vỏ electron khác nhau theo cấu hình: \(1s^2 2s^2 2p^6 3s^1\). Trong đó, lớp ngoài cùng chỉ chứa 1 electron, làm cho natri dễ dàng mất đi electron này để trở thành ion Na+, tham gia vào nhiều phản ứng hóa học quan trọng.
Các electron trong nguyên tử natri được phân bố như sau:
- Lớp thứ nhất: 2 electron
- Lớp thứ hai: 8 electron
- Lớp thứ ba: 1 electron
Sự phân bố này giải thích tại sao natri có tính chất hóa học mạnh mẽ và thường phản ứng với các nguyên tố khác để đạt được cấu hình bền vững hơn.

3. Tính chất hóa học của Natri
Natri (Na) là một kim loại kiềm có tính hoạt động hóa học rất mạnh. Đặc điểm nổi bật của natri là khả năng mất đi electron lớp ngoài cùng, tạo thành ion Na+. Điều này làm cho natri có những tính chất hóa học đặc trưng sau:
- Phản ứng với nước: Natri phản ứng mạnh với nước, tạo ra natri hydroxide (NaOH) và khí hydro (H2). Phản ứng này rất mãnh liệt, kèm theo tỏa nhiệt mạnh: \[ 2Na + 2H_2O \rightarrow 2NaOH + H_2 \uparrow \]
- Phản ứng với oxy: Natri dễ dàng phản ứng với oxy trong không khí, tạo thành natri oxide (Na2O) hoặc natri peroxide (Na2O2): \[ 4Na + O_2 \rightarrow 2Na_2O \]
- Phản ứng với halogen: Natri kết hợp với các halogen như clo (Cl2) để tạo thành muối natri chloride (NaCl): \[ 2Na + Cl_2 \rightarrow 2NaCl \]
- Tính khử mạnh: Natri có khả năng khử mạnh, được dùng để khử các kim loại khác ra khỏi hợp chất của chúng trong các phản ứng điều chế kim loại.
Nhờ những tính chất hóa học này, natri được ứng dụng rộng rãi trong công nghiệp và đời sống, từ việc sản xuất xà phòng, pin, đến việc xử lý nước và nhiều ứng dụng khác.
4. Ứng dụng của Natri trong đời sống và công nghiệp
Natri (Na) là một kim loại có vai trò quan trọng trong cả đời sống và công nghiệp. Dưới đây là một số ứng dụng tiêu biểu của natri:
- Sản xuất muối ăn: Natri kết hợp với clo tạo thành natri chloride (NaCl), còn gọi là muối ăn. Đây là một trong những sản phẩm không thể thiếu trong đời sống hàng ngày, được sử dụng trong nấu nướng, bảo quản thực phẩm và các mục đích y tế.
- Sản xuất xà phòng: Natri hydroxide (NaOH) là chất chính trong quá trình sản xuất xà phòng, giúp xà phòng hóa dầu mỡ để tạo ra các sản phẩm làm sạch.
- Ngành công nghiệp hóa chất: Natri là chất khử mạnh được sử dụng trong nhiều quá trình sản xuất hóa chất, bao gồm cả sản xuất kim loại như titan, nhôm từ quặng của chúng.
- Pin natri: Natri được sử dụng trong các loại pin công suất cao như pin natri-lưu huỳnh (Na-S) và pin natri-niken chloride (Na-NiCl2), giúp lưu trữ năng lượng hiệu quả.
- Xử lý nước: Natri carbonate (Na2CO3) được sử dụng trong xử lý nước để làm mềm nước cứng, loại bỏ ion canxi và magie.
- Đèn natri cao áp: Natri được sử dụng trong đèn chiếu sáng đường phố và các khu vực công cộng, nhờ khả năng phát sáng màu vàng đặc trưng và hiệu suất cao.
Với các ứng dụng đa dạng này, natri đóng góp không nhỏ vào sự phát triển của nhiều ngành công nghiệp cũng như cải thiện chất lượng cuộc sống hàng ngày.

5. Phương pháp điều chế Natri
Việc điều chế natri, một kim loại kiềm có hoạt tính hóa học mạnh, chủ yếu được thực hiện qua phương pháp điện phân nóng chảy của muối natri clorua (NaCl) trong các điều kiện đặc biệt. Quá trình này được gọi là phương pháp điện phân nóng chảy, mang đến hiệu quả cao trong công nghiệp.
- Nguyên tắc: Điện phân nóng chảy NaCl ở nhiệt độ cao để giải phóng natri kim loại tại catốt và khí clo tại anot.
- Công thức:
\[2NaCl (nóng chảy) \xrightarrow{điện phân} 2Na (lỏng) + Cl_2 (khí)\]
- Thiết bị và điều kiện:
Một điện phân bể lớn có lớp lót đặc biệt để chịu được nhiệt độ cao.
Nhiệt độ khoảng 800-900°C để duy trì trạng thái nóng chảy của NaCl.
Sử dụng dòng điện một chiều với cường độ cao để tạo ra phản ứng điện phân.
- Quá trình thực hiện:
Điện phân: NaCl được nạp vào bể và làm nóng chảy. Khi áp dụng dòng điện, các ion Na+ di chuyển về catốt, tại đây chúng nhận electron và chuyển thành natri kim loại.
Tách natri: Natri lỏng được tách ra khỏi hỗn hợp và thu thập trong các buồng tách biệt.
Thu khí clo: Khí clo sinh ra tại anot được thu lại và có thể sử dụng cho các quá trình công nghiệp khác.
Phương pháp điện phân nóng chảy natri clorua được sử dụng rộng rãi do hiệu quả kinh tế và khả năng sản xuất natri với độ tinh khiết cao, phục vụ cho nhiều ngành công nghiệp quan trọng như sản xuất hợp kim, chất làm lạnh, và trong sản xuất đèn natri.
XEM THÊM:
6. Kết luận
Natri là một nguyên tố hóa học thiết yếu với nhiều ứng dụng quan trọng trong đời sống và công nghiệp. Qua việc nghiên cứu về cấu tạo nguyên tử, tính chất hóa học, và các phương pháp điều chế natri, chúng ta có thể thấy rõ được vai trò to lớn của nguyên tố này trong các ngành công nghiệp hiện đại, từ sản xuất kim loại đến các hợp chất hóa học cần thiết cho đời sống hằng ngày.
Việc hiểu rõ về natri không chỉ giúp chúng ta ứng dụng hiệu quả trong sản xuất mà còn giúp tối ưu hóa quy trình công nghệ, giảm thiểu chi phí và tăng năng suất. Những kiến thức này đóng vai trò nền tảng trong việc phát triển các công nghệ tiên tiến, đảm bảo sự bền vững và tiến bộ của ngành công nghiệp hóa chất nói chung.
Trong tương lai, với sự phát triển của khoa học và công nghệ, có thể chúng ta sẽ khám phá thêm nhiều ứng dụng mới của natri, góp phần vào sự phát triển của nhân loại. Việc nghiên cứu sâu hơn về nguyên tố này chắc chắn sẽ mang lại những đột phá quan trọng, mở ra những hướng đi mới cho các lĩnh vực khoa học khác nhau.