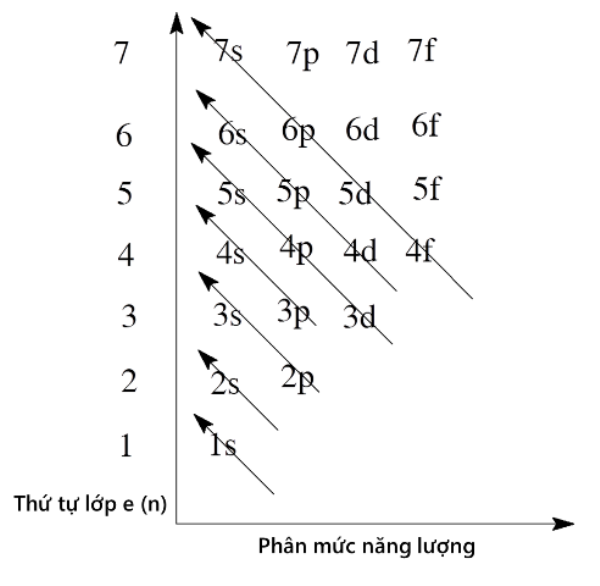Chủ đề bài tập cấu tạo nguyên tử lớp 10: Bài viết này cung cấp tổng hợp bài tập về cấu tạo nguyên tử lớp 10, từ cơ bản đến nâng cao, giúp học sinh nắm vững kiến thức quan trọng và rèn luyện kỹ năng giải bài tập một cách hiệu quả. Cùng khám phá các dạng bài tập tiêu biểu và phương pháp giải chi tiết.
Mục lục
Bài Tập Cấu Tạo Nguyên Tử Lớp 10
Trong phần này, chúng ta sẽ tổng hợp các bài tập và lý thuyết quan trọng liên quan đến cấu tạo nguyên tử, giúp các em học sinh lớp 10 nắm vững kiến thức cơ bản và nâng cao về chủ đề này.
1. Lý Thuyết Trọng Tâm
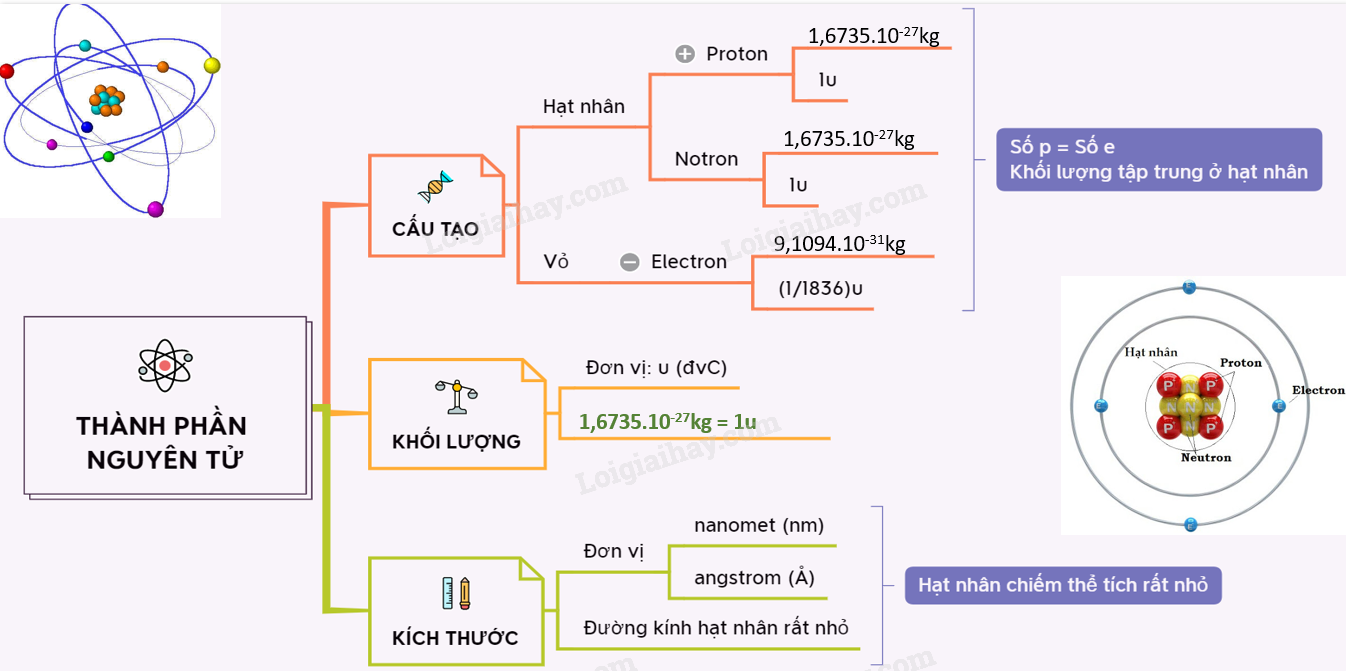
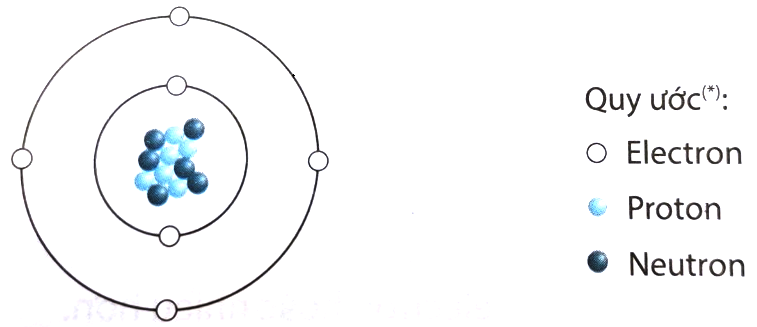
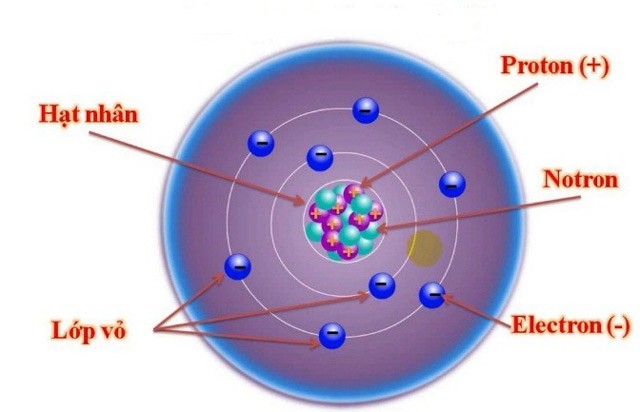
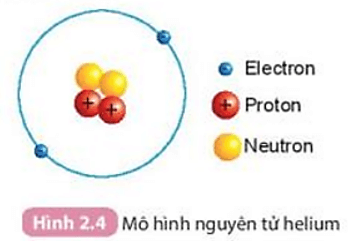
- Thành phần của nguyên tử bao gồm: electron, proton và neutron. Electron mang điện tích âm, proton mang điện tích dương, và neutron không mang điện.
- Các nguyên tử có cấu tạo từ một hạt nhân trung tâm chứa proton và neutron, xung quanh là các electron chuyển động trên các quỹ đạo xác định.
- Khối lượng nguyên tử chủ yếu tập trung ở hạt nhân, do khối lượng của electron rất nhỏ so với proton và neutron.
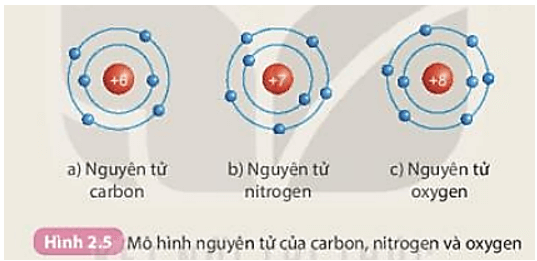
- Số proton trong hạt nhân quyết định nguyên tố hóa học và gọi là số hiệu nguyên tử.
2. Các Dạng Bài Tập Cấu Tạo Nguyên Tử
Dưới đây là các dạng bài tập phổ biến về cấu tạo nguyên tử, từ cơ bản đến nâng cao:
- Bài tập tính số hạt trong nguyên tử: Cho biết số proton, neutron và electron của nguyên tử. Tính khối lượng nguyên tử và xác định nguyên tố hóa học.
- Bài tập về đồng vị: Xác định số lượng proton, neutron trong các đồng vị khác nhau của một nguyên tố và tính khối lượng nguyên tử trung bình.
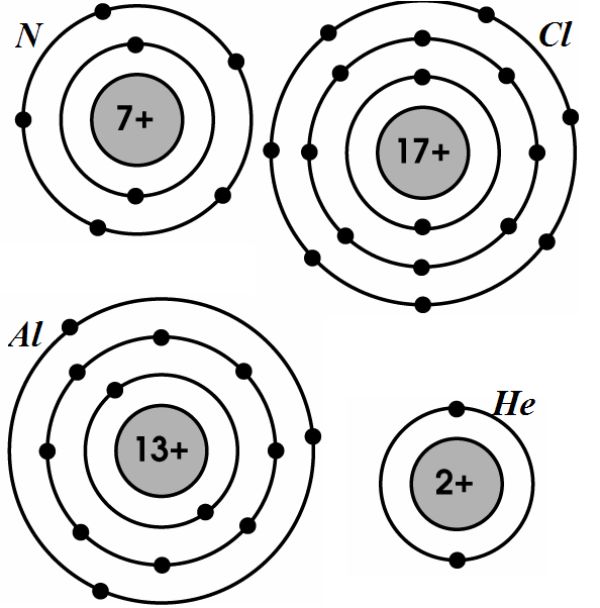
- Bài tập về cấu trúc electron: Phân bố electron vào các lớp và phân lớp, xác định cấu hình electron của nguyên tử.
3. Ví Dụ Bài Tập
Dưới đây là một số ví dụ cụ thể:
| Câu 1 | Tính tổng số electron, proton và neutron trong một phân tử nước \(H_2O\). Biết rằng: nguyên tử \(H\) có 1 proton và 1 electron, nguyên tử \(O\) có 8 proton, 8 neutron và 8 electron. |
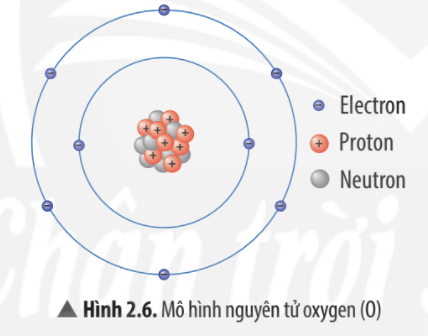
| Câu 2 | Nguyên tử oxygen-16 có 8 proton, 8 neutron và 8 electron. Tính khối lượng nguyên tử oxygen theo đơn vị gam và amu. |
| Câu 3 | Nguyên tử aluminium \(Al\) gồm 13 proton và 14 neutron. Tính khối lượng proton, neutron và electron. |
4. Phương Pháp Giải Bài Tập
- Phân tích đề bài để xác định các dữ kiện cần thiết như số proton, neutron, electron, và áp dụng các công thức liên quan.
- Sử dụng các công thức vật lý và hóa học để tính toán khối lượng, số khối, và cấu hình electron.
- Đối với các bài tập phức tạp hơn, cần lập bảng phân tích để dễ dàng theo dõi các giá trị tính toán.

Tổng Quan Về Cấu Tạo Nguyên Tử
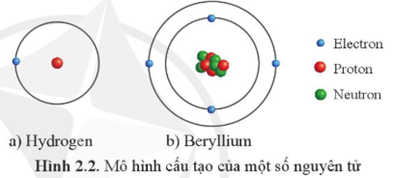
Nguyên tử là đơn vị cơ bản của vật chất, bao gồm ba loại hạt cơ bản: proton, neutron và electron. Proton và neutron nằm trong hạt nhân của nguyên tử, trong khi electron chuyển động xung quanh hạt nhân theo các quỹ đạo xác định.
- Proton: Proton mang điện tích dương \((+1)\) và có khối lượng xấp xỉ \[1.6726 \times 10^{-27}\] kg.
- Neutron: Neutron không mang điện tích \((0)\) và có khối lượng gần bằng proton, khoảng \[1.6750 \times 10^{-27}\] kg.
- Electron: Electron mang điện tích âm \((-1)\) và có khối lượng rất nhỏ so với proton và neutron, xấp xỉ \[9.1094 \times 10^{-31}\] kg.
Hạt nhân của nguyên tử tập trung hầu hết khối lượng của nguyên tử và được liên kết chắc chắn bởi các lực hạt nhân. Electron, với khối lượng nhỏ, chuyển động quanh hạt nhân và chịu tác động của lực điện từ từ proton. Sự phân bố của các electron trên các lớp và phân lớp tạo thành cấu trúc electron của nguyên tử, quyết định tính chất hóa học của nguyên tố.
Phân Loại Bài Tập Cấu Tạo Nguyên Tử
Bài tập về cấu tạo nguyên tử lớp 10 thường được chia thành nhiều dạng khác nhau, nhằm giúp học sinh nắm vững các khái niệm cơ bản cũng như ứng dụng của chúng trong việc giải các bài toán cụ thể. Dưới đây là một số phân loại bài tập phổ biến:
- Bài Tập Tính Số Hạt: Dạng bài tập này yêu cầu học sinh tính toán số proton, neutron, và electron trong một nguyên tử dựa trên số hiệu nguyên tử và số khối. Công thức tính cơ bản là:
- \(\text{Số proton} = \text{Số hiệu nguyên tử}\)
- \(\text{Số neutron} = \text{Số khối} - \text{Số hiệu nguyên tử}\)
- \(\text{Số electron} = \text{Số proton} \, (nếu \, nguyên tử \, trung hòa)\)
- Bài Tập Về Đồng Vị: Học sinh được yêu cầu phân tích các đồng vị của một nguyên tố, tính toán phần trăm tỉ lệ và khối lượng trung bình của nguyên tử dựa trên các đồng vị này. Công thức khối lượng trung bình của nguyên tử là:
- \(\text{Khối lượng trung bình} = \frac{\sum (\text{khối lượng đồng vị} \times \text{tỉ lệ phần trăm})}{100}\)
- Bài Tập Cấu Trúc Electron: Dạng bài tập này yêu cầu học sinh viết cấu hình electron của các nguyên tố, xác định số lớp và phân lớp electron dựa trên số hiệu nguyên tử. Cấu hình electron được viết theo nguyên tắc:
- \(1s^2, 2s^2, 2p^6, 3s^2, 3p^6, ...\)
- Bài Tập Khối Lượng Nguyên Tử: Bài tập tính toán khối lượng của một nguyên tử hoặc phân tử dựa trên số mol, số Avogadro và khối lượng mol. Công thức liên quan là:
- \(\text{Khối lượng} = \text{Số mol} \times \text{Khối lượng mol}\)
Việc phân loại và rèn luyện các dạng bài tập trên giúp học sinh củng cố kiến thức lý thuyết, đồng thời phát triển kỹ năng giải quyết vấn đề trong thực tiễn.

Phương Pháp Giải Bài Tập
Để giải bài tập về cấu tạo nguyên tử, học sinh cần nắm vững các bước cơ bản và phương pháp tiếp cận từng dạng bài tập cụ thể. Dưới đây là một số phương pháp giải chi tiết:
- Bước 1: Đọc kỹ đề bài và xác định yêu cầu.
- Bước 2: Áp dụng công thức thích hợp.
- \(\text{Số proton} = \text{Số hiệu nguyên tử}\)
- \(\text{Số neutron} = \text{Số khối} - \text{Số hiệu nguyên tử}\)
- Bước 3: Giải bài tập theo từng bước.
- Giải thích từng bước tính toán số proton, neutron, và electron dựa trên các thông tin đã cho.
- Bước 4: Kiểm tra lại kết quả.
- Bước 5: Luyện tập nhiều dạng bài tập.
Trước tiên, học sinh cần đọc kỹ đề bài, xác định rõ yêu cầu là tính số hạt, viết cấu hình electron, hay tính khối lượng nguyên tử. Việc hiểu đúng yêu cầu giúp học sinh chọn đúng phương pháp giải.
Học sinh cần lựa chọn công thức phù hợp với yêu cầu của bài toán, ví dụ như công thức tính số hạt:
Sau khi xác định công thức, học sinh cần giải bài tập từng bước một cách cẩn thận, chú ý đến đơn vị và kết quả cuối cùng. Ví dụ, nếu bài yêu cầu tính số proton và neutron:
Sau khi hoàn thành bài tập, học sinh nên kiểm tra lại các bước tính toán để đảm bảo không có sai sót và kết quả là chính xác.
Cuối cùng, học sinh nên thực hành nhiều dạng bài tập khác nhau để làm quen với các tình huống và cách giải bài tập về cấu tạo nguyên tử, từ đó cải thiện kỹ năng và hiệu suất học tập.
Với phương pháp tiếp cận chi tiết và luyện tập thường xuyên, học sinh sẽ dễ dàng nắm vững và giải quyết hiệu quả các bài tập về cấu tạo nguyên tử.

Ví Dụ Minh Họa
Dưới đây là một ví dụ minh họa chi tiết về cách giải bài tập cấu tạo nguyên tử lớp 10, giúp học sinh nắm vững phương pháp giải và áp dụng vào thực tế.
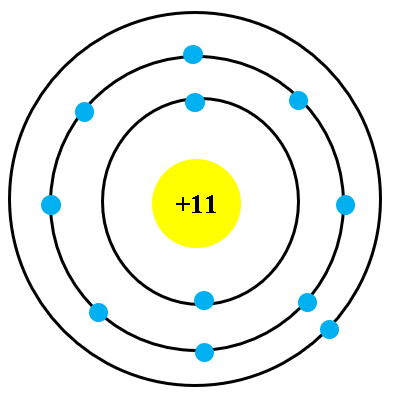
Ví dụ: Xác định số proton, neutron và electron của nguyên tử \(\ce{^{23}_{11}Na}\).
- Bước 1: Xác định số proton.
- Bước 2: Tính số neutron.
- Bước 3: Xác định số electron.
- Bước 4: Kết luận.
- 11 proton
- 12 neutron
- 11 electron
Số proton trong nguyên tử \(\ce{^{23}_{11}Na}\) chính là số hiệu nguyên tử (Z) của nguyên tố Na (Natri). Vậy số proton là:
\[ Z = 11 \]
Số neutron được tính bằng cách lấy số khối (A) trừ đi số proton (Z). Với nguyên tử \(\ce{^{23}_{11}Na}\), ta có:
\[ \text{Số neutron} = A - Z = 23 - 11 = 12 \]
Vì nguyên tử \(\ce{^{23}_{11}Na}\) ở trạng thái trung hòa điện, nên số electron sẽ bằng với số proton. Do đó, số electron là:
\[ \text{Số electron} = 11 \]
Vậy nguyên tử \(\ce{^{23}_{11}Na}\) có:
Qua ví dụ này, học sinh có thể hiểu rõ hơn cách áp dụng các công thức và phương pháp tính toán trong bài tập cấu tạo nguyên tử. Luyện tập nhiều ví dụ tương tự sẽ giúp nâng cao kỹ năng giải bài tập hóa học.

Tổng Kết Và Luyện Tập
Sau khi đã nắm vững các khái niệm và phương pháp giải bài tập cấu tạo nguyên tử, bước cuối cùng là ôn tập và luyện tập để củng cố kiến thức. Dưới đây là một số gợi ý để bạn tổng kết lại toàn bộ kiến thức đã học và áp dụng chúng vào thực tế qua các bài tập.
Ôn Tập Kiến Thức Cấu Tạo Nguyên Tử
Hãy dành thời gian ôn tập lại các khái niệm cơ bản về cấu tạo nguyên tử, bao gồm:
- Thành phần của nguyên tử: Proton, neutron và electron.
- Số hiệu nguyên tử và số khối: Khái niệm và cách tính.
- Đồng vị: Định nghĩa và ví dụ minh họa.
- Cấu trúc electron: Các lớp electron và cấu hình electron của nguyên tử.
Ôn tập lại các công thức quan trọng liên quan đến cấu tạo nguyên tử, chẳng hạn như công thức tính số hạt proton, neutron và electron:
- Số proton: \( Z \)
- Số neutron: \( N = A - Z \)
- Số electron: \( Z \) (đối với nguyên tử trung hòa về điện)
- Số khối: \( A = Z + N \)
Luyện Tập Các Dạng Bài Tập
Sau khi đã ôn tập kiến thức, bạn nên thực hành giải các dạng bài tập liên quan để kiểm tra và củng cố kiến thức:
- Bài tập tính số hạt: Tính số proton, neutron và electron dựa trên các dữ liệu đề bài cho.
- Bài tập về đồng vị: Tính khối lượng nguyên tử trung bình dựa trên phần trăm đồng vị.
- Bài tập cấu trúc electron: Xác định cấu hình electron của các nguyên tử và ion.
- Bài tập khối lượng nguyên tử: Tính khối lượng nguyên tử dựa trên số khối và số hiệu nguyên tử.
Cuối cùng, bạn có thể thực hiện các bài kiểm tra hoặc bài tập trắc nghiệm để đánh giá mức độ nắm vững kiến thức của mình. Điều này sẽ giúp bạn chuẩn bị tốt hơn cho các kỳ thi sắp tới.