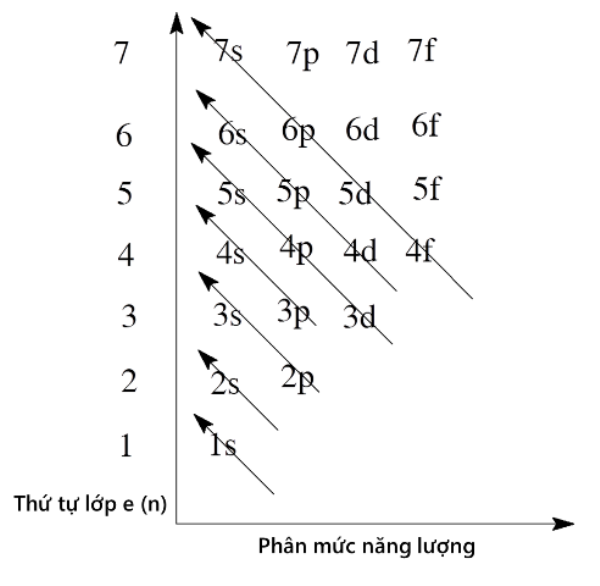Chủ đề cấu tạo nguyên tử cacbon: Cấu tạo nguyên tử cacbon là một chủ đề quan trọng trong hóa học, mở ra hiểu biết về nguyên tố cơ bản của sự sống. Bài viết này sẽ giúp bạn khám phá chi tiết về cấu trúc, đồng vị, và ứng dụng thực tế của nguyên tử cacbon trong khoa học và đời sống hàng ngày.
Mục lục
Cấu Tạo Nguyên Tử Cacbon
Nguyên tử cacbon là một nguyên tố hóa học thuộc nhóm 14 trong bảng tuần hoàn, có ký hiệu hóa học là C và số hiệu nguyên tử là 6. Cấu tạo của nguyên tử cacbon bao gồm:
1. Số Proton, Nơtron, và Electron
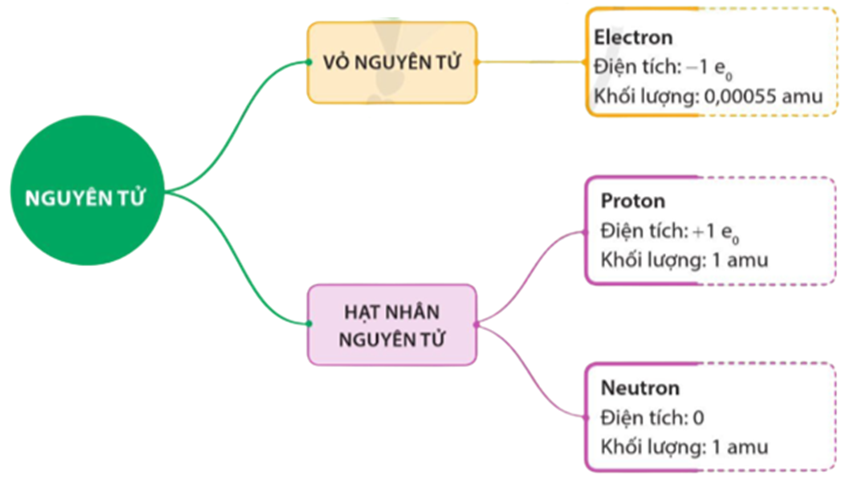
- Số proton: 6
- Số nơtron: Thường là 6 (đối với đồng vị phổ biến nhất, Cacbon-12)
- Số electron: 6
Nguyên tử cacbon có tổng cộng 6 electron, được phân bố theo cấu hình electron:
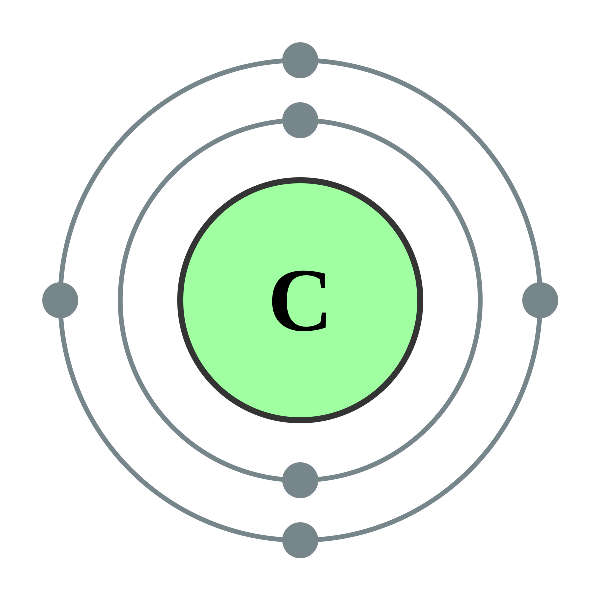
Cấu hình này cho thấy nguyên tử cacbon có hai lớp electron. Lớp thứ nhất chứa 2 electron, và lớp thứ hai chứa 4 electron, trong đó có 2 electron ở phân lớp 2s và 2 electron ở phân lớp 2p.
2. Cấu Trúc Vỏ Electron
Với 4 electron ở lớp ngoài cùng, cacbon có khả năng tạo 4 liên kết hóa học cộng hóa trị, điều này làm cho nó trở thành một nguyên tố rất linh hoạt trong việc hình thành các hợp chất khác nhau. Các electron này có thể được hình dung dưới dạng các orbital s và p:
- Orbital 2s: Chứa 2 electron.
- Orbital 2p: Chứa 2 electron, với mỗi electron chiếm một trong ba orbital p_x, p_y, và p_z.
3. Đồng Vị của Cacbon
Cacbon có hai đồng vị ổn định chính:
- Cacbon-12 (12C): Chiếm khoảng 98,89% trong tự nhiên, với 6 proton và 6 nơtron.
- Cacbon-13 (13C): Chiếm khoảng 1,11%, với 6 proton và 7 nơtron.
4. Ứng Dụng của Nguyên Tử Cacbon
Cacbon là một nguyên tố cơ bản trong hóa học hữu cơ và có vai trò quan trọng trong sự sống. Nó tham gia vào nhiều hợp chất và vật liệu quan trọng như:
- Kim cương: Cấu trúc tinh thể của cacbon ở trạng thái này tạo ra một trong những chất cứng nhất được biết đến.
- Than chì: Cấu trúc lớp của cacbon trong than chì cho phép các lớp trượt qua nhau, ứng dụng trong bút chì và làm chất bôi trơn.
- Cacbon vô định hình: Dạng này của cacbon bao gồm than hoạt tính, than gỗ, than cốc, có tính hấp thụ cao và được dùng trong nhiều ngành công nghiệp.
5. Kết Luận
Nguyên tử cacbon với cấu trúc đơn giản nhưng linh hoạt đã tạo ra một thế giới đa dạng các hợp chất hữu cơ và vật liệu quý giá. Nhờ vào cấu tạo này, cacbon đã trở thành một trong những nguyên tố quan trọng nhất, không chỉ trong hóa học mà còn trong nhiều lĩnh vực khác của khoa học và đời sống.
1. Giới Thiệu Về Nguyên Tử Cacbon
Nguyên tử cacbon là một trong những nguyên tố cơ bản nhất trong bảng tuần hoàn, đóng vai trò quan trọng trong việc cấu thành các hợp chất hữu cơ. Với số nguyên tử là 6, cacbon thuộc nhóm IVA, chu kỳ 2 trong bảng tuần hoàn.
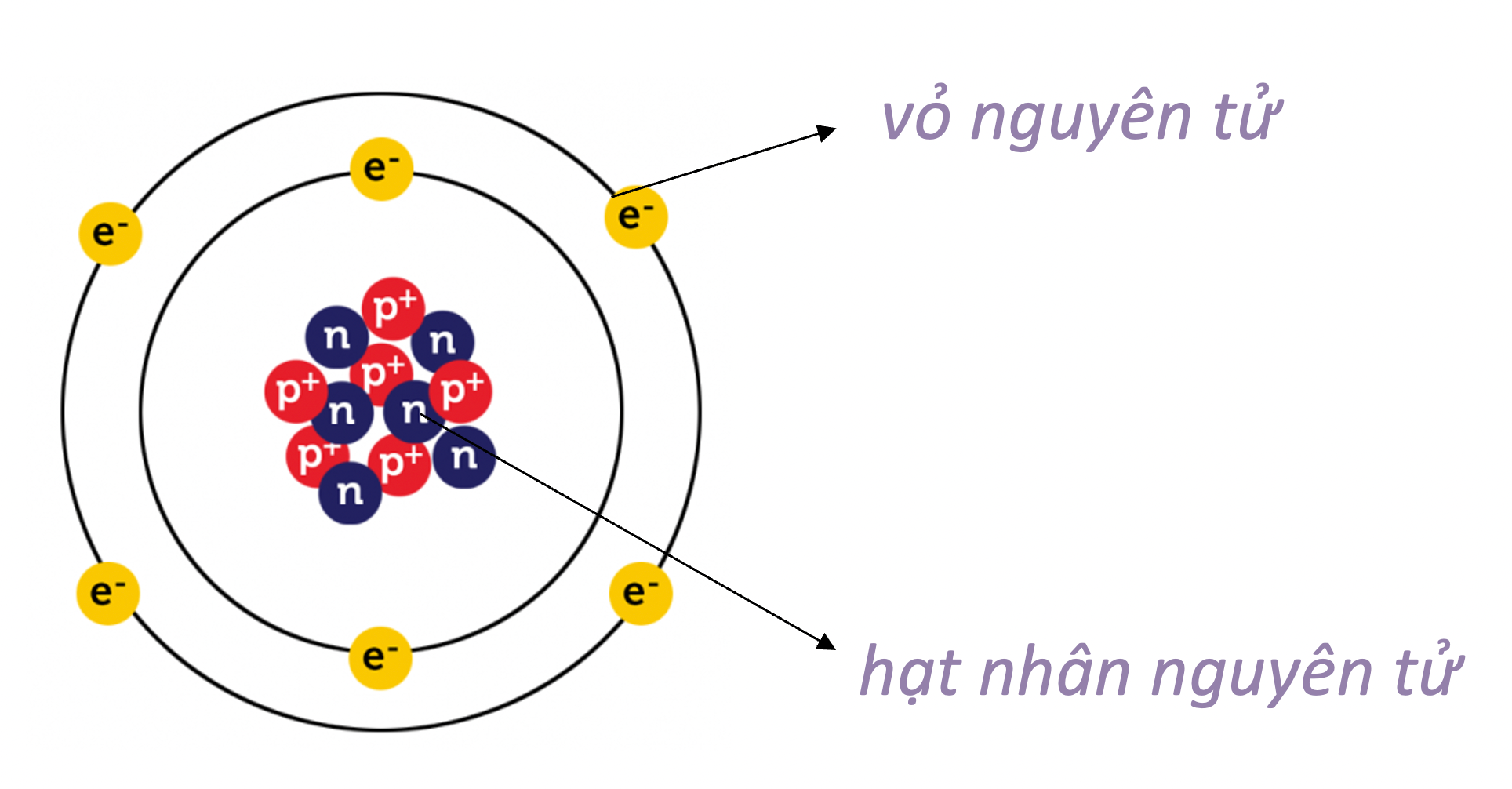
Cấu trúc của nguyên tử cacbon gồm có 6 proton, 6 neutron trong hạt nhân và 6 electron phân bố trên hai lớp vỏ điện tử. Lớp thứ nhất chứa 2 electron, lớp thứ hai chứa 4 electron, tạo nên cấu hình electron \([1s^2 2s^2 2p^2]\). Đây là cấu hình cơ bản tạo nên tính chất hóa học đặc trưng của nguyên tố này.
Với khả năng liên kết đa dạng, cacbon có thể tạo ra nhiều dạng hợp chất khác nhau, từ các hợp chất đơn giản như \(CO_2\) (carbon dioxide) cho đến các hợp chất phức tạp như chuỗi polymer dài. Chính vì vậy, nguyên tử cacbon là yếu tố quan trọng không chỉ trong hóa học mà còn trong các ngành khoa học khác như sinh học, vật lý, và công nghệ vật liệu.
2. Cấu Hình Electron và Vỏ Nguyên Tử Cacbon
Nguyên tử cacbon có cấu hình electron đặc trưng với tổng cộng 6 electron được sắp xếp trong hai lớp vỏ điện tử. Lớp thứ nhất chứa 2 electron trong orbital \(1s\), và lớp thứ hai chứa 4 electron phân bố trong các orbital \(2s\) và \(2p\), cụ thể là \([1s^2 2s^2 2p^2]\). Cấu hình này giúp cacbon có khả năng tạo ra bốn liên kết cộng hóa trị, điều này giải thích tại sao cacbon có thể tham gia vào rất nhiều loại phản ứng hóa học khác nhau.
Vỏ nguyên tử của cacbon đóng vai trò quan trọng trong việc xác định tính chất hóa học của nó. Với 4 electron ở lớp vỏ ngoài cùng, cacbon có xu hướng đạt được cấu hình bền vững giống như khí hiếm bằng cách chia sẻ electron với các nguyên tử khác, tạo ra liên kết đơn, đôi, hoặc ba. Điều này làm cho cacbon trở thành một nguyên tố rất linh hoạt trong việc hình thành các hợp chất hữu cơ phức tạp.
Khả năng tạo liên kết đa dạng của cacbon là lý do tại sao nó là nền tảng của hóa học hữu cơ, từ các phân tử nhỏ đơn giản đến các phân tử sinh học phức tạp như DNA và protein. Điều này thể hiện rõ ràng trong các ứng dụng thực tiễn của cacbon trong nhiều lĩnh vực khác nhau như công nghệ vật liệu, y học, và môi trường.

4. Dạng Thù Hình của Cacbon
Cacbon là nguyên tố có khả năng tạo ra nhiều dạng thù hình khác nhau, mỗi dạng có cấu trúc và tính chất riêng biệt. Các dạng thù hình chính của cacbon bao gồm kim cương, than chì và cacbon vô định hình. Dưới đây là mô tả chi tiết về các dạng thù hình này:
4.1. Kim Cương: Cấu Trúc và Tính Chất
Kim cương là một dạng thù hình của cacbon có cấu trúc tinh thể đặc biệt, trong đó các nguyên tử cacbon liên kết với nhau bằng liên kết cộng hóa trị mạnh mẽ, tạo thành một mạng lưới ba chiều. Đây là lý do tại sao kim cương có độ cứng rất cao và có thể cắt được hầu hết các vật liệu khác.
- Cấu trúc: Các nguyên tử cacbon trong kim cương được sắp xếp theo cấu trúc hình lập phương, tạo thành một mạng lưới ba chiều.
- Tính chất: Kim cương có độ cứng cao nhất trong các vật liệu tự nhiên, dẫn điện kém, và có khả năng khúc xạ ánh sáng mạnh mẽ, tạo ra ánh sáng lấp lánh đặc trưng.
4.2. Than Chì: Cấu Trúc và Ứng Dụng
Than chì là một dạng thù hình của cacbon mà trong đó các nguyên tử cacbon sắp xếp thành các lớp phẳng giống như tổ ong, các lớp này chỉ liên kết với nhau bằng liên kết Van der Waals yếu. Đây là lý do tại sao than chì có thể dễ dàng bị tách lớp và là vật liệu lý tưởng cho các ứng dụng bôi trơn và làm chì viết.
- Cấu trúc: Các lớp trong than chì được cấu thành từ các vòng sáu cạnh liên kết với nhau bằng liên kết cộng hóa trị mạnh, trong khi các lớp thì liên kết với nhau bằng liên kết Van der Waals yếu.
- Ứng dụng: Than chì được sử dụng rộng rãi trong các ứng dụng như bút chì, vật liệu bôi trơn, và trong các linh kiện điện tử như pin và siêu tụ.
4.3. Cacbon Vô Định Hình: Đặc Điểm và Công Dụng
Cacbon vô định hình không có cấu trúc tinh thể cụ thể như kim cương hay than chì, và bao gồm các dạng như than hoạt tính và bột cacbon. Cacbon vô định hình có nhiều ứng dụng trong các ngành công nghiệp và y học nhờ vào khả năng hấp thụ và tính linh hoạt cao của nó.
- Đặc điểm: Cacbon vô định hình có cấu trúc không đều và không có mạng lưới tinh thể rõ ràng. Đặc điểm này giúp cacbon vô định hình có khả năng hấp thụ chất lỏng và khí tốt.
- Công dụng: Các dạng cacbon vô định hình như than hoạt tính được sử dụng trong xử lý nước và không khí, trong khi bột cacbon được ứng dụng trong sản xuất cao su và các sản phẩm nhựa.
5. Ứng Dụng Thực Tế của Cacbon
Cacbon, với tính chất và dạng thù hình đa dạng của nó, đóng vai trò quan trọng trong nhiều lĩnh vực khác nhau. Dưới đây là những ứng dụng thực tế nổi bật của cacbon trong các ngành công nghiệp và công nghệ hiện đại:
5.1. Ứng Dụng Trong Ngành Công Nghiệp
Cacbon được sử dụng rộng rãi trong ngành công nghiệp nhờ vào các tính chất vật lý và hóa học của nó. Các ứng dụng chính bao gồm:
- Vật liệu chế tạo: Kim cương được sử dụng trong các công cụ cắt và mài do độ cứng vượt trội. Than chì được dùng làm điện cực trong các quá trình điện phân và trong các ứng dụng bôi trơn nhờ khả năng trơn trượt của nó.
- Chất xúc tác: Than hoạt tính được dùng làm chất xúc tác trong nhiều phản ứng hóa học và trong các hệ thống xử lý khí thải để hấp thụ các hợp chất độc hại.
- Vật liệu composite: Sợi cacbon được ứng dụng trong sản xuất các vật liệu composite nhẹ nhưng bền, dùng trong ngành hàng không vũ trụ và ô tô để cải thiện hiệu suất và tiết kiệm nhiên liệu.
5.2. Ứng Dụng Trong Công Nghệ Vật Liệu
Cacbon không chỉ quan trọng trong ngành công nghiệp mà còn có nhiều ứng dụng trong công nghệ vật liệu hiện đại:
- Pin và siêu tụ: Graphene và các vật liệu cacbon khác được sử dụng trong pin và siêu tụ nhờ vào khả năng dẫn điện và hiệu suất lưu trữ năng lượng cao.
- Công nghệ y học: Cacbon vô định hình và graphene đang được nghiên cứu và ứng dụng trong công nghệ y học, đặc biệt là trong các hệ thống delivery thuốc và các thiết bị chẩn đoán nhờ vào tính tương thích sinh học của chúng.
- Chất liệu bảo vệ: Các vật liệu cacbon như sợi cacbon và graphene được sử dụng trong việc chế tạo các lớp bảo vệ và thiết bị chống va đập, bảo vệ người sử dụng khỏi các tác động cơ học.

6. Kết Luận
Nguyên tử cacbon không chỉ là nền tảng của hóa học hữu cơ mà còn đóng vai trò quan trọng trong nhiều lĩnh vực khác nhau. Các đặc điểm nổi bật của cacbon, từ cấu trúc tinh thể đến tính chất hóa học, đã mở ra nhiều ứng dụng thực tế có giá trị trong khoa học và công nghệ.
6.1. Tầm Quan Trọng của Nguyên Tử Cacbon Trong Hóa Học Hữu Cơ
Cacbon là nguyên tố chủ chốt trong hóa học hữu cơ, nơi nó hình thành liên kết với các nguyên tố khác để tạo ra hàng triệu hợp chất hữu cơ. Các hợp chất này đóng vai trò quan trọng trong sinh học, dược học và công nghiệp. Tính linh hoạt của cacbon trong việc tạo ra các liên kết đơn, đôi và ba với các nguyên tố khác cho phép hình thành các phân tử có cấu trúc đa dạng, từ các hợp chất đơn giản như metan đến các hợp chất phức tạp như protein và DNA.
6.2. Những Tiềm Năng Nghiên Cứu Liên Quan Đến Cacbon
Các nghiên cứu về cacbon tiếp tục mang lại nhiều phát hiện và ứng dụng mới. Từ các vật liệu tiên tiến như graphene và cacbon nanotubes đến việc cải thiện các công nghệ hiện có như pin và công nghệ xử lý nước, cacbon vẫn là một lĩnh vực nghiên cứu đầy triển vọng. Những nghiên cứu này không chỉ mở rộng kiến thức khoa học mà còn góp phần vào sự phát triển của các công nghệ mới, cải thiện chất lượng cuộc sống và bảo vệ môi trường.