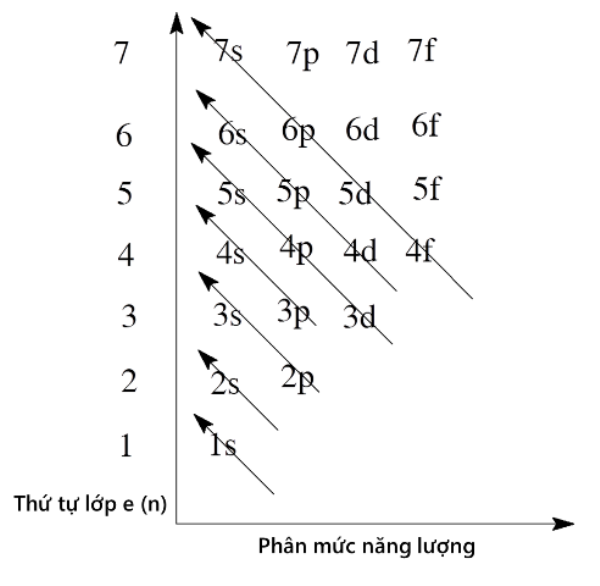Chủ đề mô hình cấu tạo nguyên tử carbon: Khám phá sâu sắc về mô hình cấu tạo nguyên tử carbon, từ các mô hình cơ bản như Bohr và Orbital đến ứng dụng thực tiễn trong hóa học, công nghệ vật liệu và y học. Bài viết này cung cấp cái nhìn toàn diện và chi tiết về cách cấu tạo của nguyên tử carbon ảnh hưởng đến các lĩnh vực khoa học và công nghệ hiện đại.
Mục lục
Tổng hợp thông tin về mô hình cấu tạo nguyên tử carbon
Mô hình cấu tạo nguyên tử carbon là một chủ đề quan trọng trong hóa học và vật lý. Dưới đây là tổng hợp thông tin chi tiết về chủ đề này từ kết quả tìm kiếm trên Bing tại Việt Nam:
1. Giới thiệu về nguyên tử carbon
Carbon là nguyên tố hóa học có ký hiệu C và số nguyên tử 6. Đây là nguyên tố cơ bản trong hóa học hữu cơ, tham gia vào nhiều phản ứng hóa học và hình thành các phân tử quan trọng như protein, DNA, và carbohydrates.
2. Các mô hình cấu tạo nguyên tử carbon
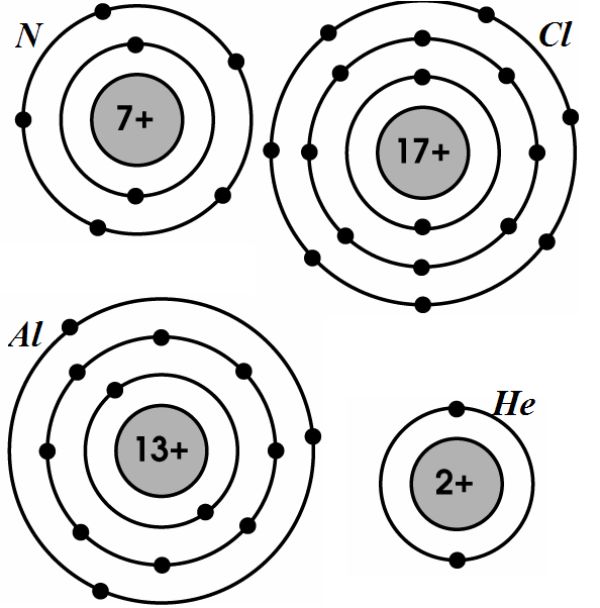
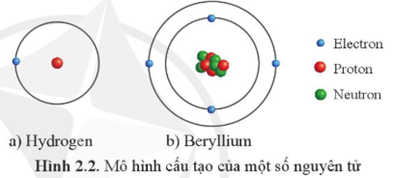
- Mô hình Bohr: Mô hình Bohr mô tả nguyên tử carbon với các lớp electron xung quanh hạt nhân. Trong mô hình này, các electron được phân bố vào các lớp khác nhau, với lớp ngoài cùng chứa 4 electron.
- Mô hình Orbital: Mô hình này mô tả cách các electron phân bố trong các orbital của nguyên tử carbon. Theo mô hình này, carbon có 4 orbital sp³, cho phép nó tạo liên kết với các nguyên tử khác.
- Mô hình Hybridization: Carbon có khả năng lai hóa để tạo ra các liên kết bền vững. Các loại lai hóa phổ biến là sp³ (liên kết đơn), sp² (liên kết đôi) và sp (liên kết ba).
3. Ứng dụng của mô hình cấu tạo nguyên tử carbon
Mô hình cấu tạo nguyên tử carbon được ứng dụng rộng rãi trong nhiều lĩnh vực:
- Hóa học hữu cơ: Hiểu cách carbon liên kết với các nguyên tố khác giúp nghiên cứu và phát triển các hợp chất hữu cơ.
- Công nghệ vật liệu: Mô hình cấu tạo carbon giúp thiết kế các vật liệu mới như graphene và carbon nanotubes.
- Y học: Mô hình cấu tạo nguyên tử carbon hỗ trợ trong việc nghiên cứu cấu trúc phân tử của các thuốc và sinh phẩm.
4. Bảng so sánh các mô hình cấu tạo nguyên tử carbon
| Mô hình | Đặc điểm | Ứng dụng |
|---|---|---|
| Mô hình Bohr | Electron phân bố theo lớp | Cung cấp nền tảng cho việc hiểu cấu trúc cơ bản của nguyên tử |
| Mô hình Orbital | Các orbital electron | Phân tích cấu trúc phân tử và liên kết hóa học |
| Mô hình Hybridization | La hóa electron | Phát triển các loại liên kết trong hóa học hữu cơ |
5. Tài liệu tham khảo
Các tài liệu liên quan đến mô hình cấu tạo nguyên tử carbon có thể được tìm thấy trong sách giáo khoa hóa học, tài liệu nghiên cứu và các bài báo khoa học.
Hy vọng thông tin trên giúp bạn hiểu rõ hơn về mô hình cấu tạo nguyên tử carbon và ứng dụng của nó trong các lĩnh vực khác nhau.
1. Giới thiệu về Nguyên Tử Carbon
Nguyên tử carbon là một trong những thành phần cơ bản nhất trong hóa học và sinh học. Carbon có ký hiệu hóa học là C và số nguyên tử là 6. Đây là nguyên tố đa dụng, đóng vai trò quan trọng trong nhiều phân tử sinh học và hóa học. Dưới đây là một số thông tin chi tiết về nguyên tử carbon:
1.1. Đặc Điểm Cơ Bản
- Số nguyên tử: 6
- Ký hiệu hóa học: C
- Khối lượng nguyên tử: khoảng 12 amu (đơn vị khối lượng nguyên tử)
- Cấu hình electron: 1s² 2s² 2p²
1.2. Tầm Quan Trọng Trong Hóa Học
Carbon là nguyên tố chính trong hóa học hữu cơ và là thành phần của tất cả các hợp chất hữu cơ, như protein, lipit, carbohydrate và axit nucleic. Do khả năng tạo liên kết với nhiều nguyên tử khác, carbon có thể hình thành nhiều loại phân tử với cấu trúc phức tạp.
1.3. Các Dạng Đồng Vị của Carbon
- Carbon-12 (¹²C): Chiếm khoảng 98.89% lượng carbon tự nhiên. Đây là dạng đồng vị ổn định của carbon.
- Carbon-13 (¹³C): Chiếm khoảng 1.11% lượng carbon tự nhiên. Đồng vị này cũng ổn định và được sử dụng trong các nghiên cứu phân tích đồng vị.
- Carbon-14 (¹⁴C): Là đồng vị phóng xạ, có thời gian bán rã khoảng 5730 năm, được sử dụng trong phương pháp định tuổi carbon.
1.4. Ứng Dụng của Carbon
- Công Nghệ Vật Liệu: Carbon được sử dụng trong các vật liệu như graphene và carbon nanotubes, nổi bật với tính chất cơ học và điện tử đặc biệt.
- Y Học: Carbon là thành phần chính trong nhiều hợp chất thuốc và sinh phẩm.
- Công Nghiệp: Carbon được sử dụng trong sản xuất nhựa, cao su, và các sản phẩm hóa học khác.
1.5. Bảng So Sánh Các Đồng Vị Carbon
| Đồng Vị | Phần Trăm Xuất Hiện | Thời Gian Bán Rã | Ứng Dụng |
|---|---|---|---|
| Carbon-12 | 98.89% | Ổn định | Không có ứng dụng đặc biệt, là đồng vị chính trong tự nhiên |
| Carbon-13 | 1.11% | Ổn định | Được sử dụng trong phân tích đồng vị và nghiên cứu hóa học |
| Carbon-14 | Vô cùng nhỏ | 5730 năm | Định tuổi carbon trong khảo cổ học và địa chất học |
2. Các Mô Hình Cấu Tạo Nguyên Tử Carbon
Các mô hình cấu tạo nguyên tử carbon giúp chúng ta hiểu cách các electron phân bố quanh hạt nhân và cách carbon hình thành các liên kết hóa học. Dưới đây là các mô hình chính và chi tiết về mỗi mô hình:
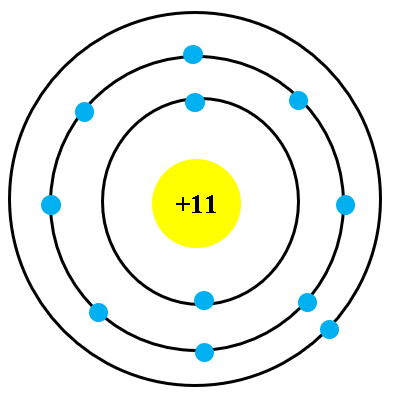
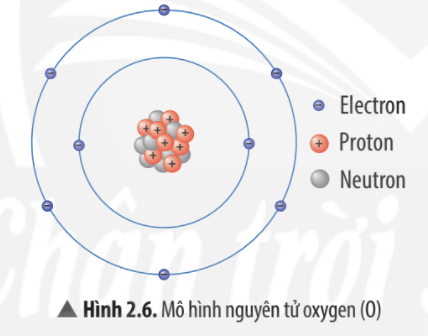
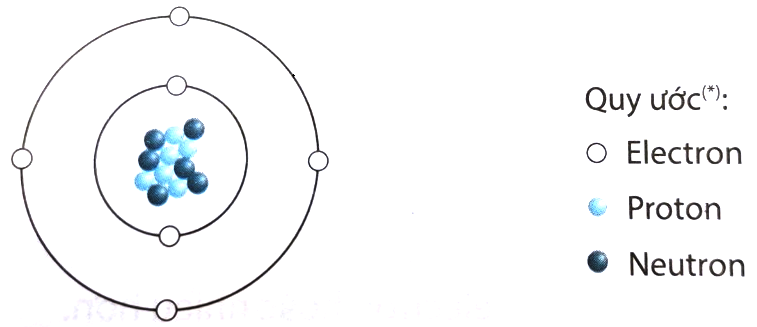
2.1. Mô Hình Bohr
Mô hình Bohr, được đề xuất bởi Niels Bohr, mô tả cấu trúc nguyên tử với các electron phân bố vào các lớp khác nhau quanh hạt nhân. Trong mô hình này, các electron nằm trên các quỹ đạo cụ thể và mỗi lớp chứa một số lượng electron nhất định. Mô hình Bohr là cơ sở cho việc hiểu cấu trúc của nguyên tử và sự phân bố của các electron.
- Electron trong lớp K: 2 electron
- Electron trong lớp L: 8 electron
- Electron trong lớp M: 4 electron
2.2. Mô Hình Orbital
Mô hình orbital mô tả cách các electron phân bố trong các orbital quanh hạt nhân. Các orbital này bao gồm s, p, d, và f. Trong nguyên tử carbon, các electron nằm chủ yếu trong các orbital sp³, cho phép carbon tạo ra bốn liên kết với các nguyên tử khác.
- Orbital s: Một orbital hình cầu, chứa 2 electron.
- Orbital p: Ba orbital hình số 8, mỗi orbital chứa 2 electron, tổng cộng 6 electron.
- Orbital sp³: Sự lai hóa giữa một orbital s và ba orbital p, tạo ra bốn orbital sp³ đồng đều, giúp carbon hình thành các liên kết đơn bền vững.
2.3. Mô Hình Hybridization
Mô hình hybridization giải thích sự kết hợp của các orbital nguyên tử để tạo ra các liên kết hóa học. Carbon có khả năng lai hóa để tạo ra các liên kết đa dạng:
| Loại Lai Hóa | Orbital Lai Hóa | Liên Kết Tạo Ra | Cấu Trúc Ví Dụ |
|---|---|---|---|
| sp³ | 1s + 3p | Liên kết đơn | Metan (CH₄) |
| sp² | 1s + 2p | Liên kết đôi | Ethene (C₂H₄) |
| sp | 1s + 1p | Liên kết ba | Acetylene (C₂H₂) |
2.4. So Sánh Các Mô Hình
Các mô hình khác nhau cung cấp cái nhìn sâu sắc về cấu trúc nguyên tử carbon và cách thức nó tương tác với các nguyên tử khác. Dưới đây là sự so sánh giữa các mô hình:
- Mô hình Bohr: Tập trung vào phân bố lớp electron, dễ hiểu nhưng không giải thích được các liên kết hóa học phức tạp.
- Mô hình Orbital: Cung cấp cái nhìn chi tiết về các orbital và cách các electron phân bố, giúp hiểu rõ hơn về cấu trúc phân tử.
- Mô hình Hybridization: Giải thích khả năng tạo liên kết của carbon, quan trọng trong việc hiểu cấu trúc và phản ứng hóa học của các hợp chất carbon.

3. Ứng Dụng của Các Mô Hình Cấu Tạo Carbon
Các mô hình cấu tạo nguyên tử carbon không chỉ giúp hiểu về cấu trúc của nguyên tử mà còn có nhiều ứng dụng thực tiễn trong các lĩnh vực khoa học và công nghệ. Dưới đây là các ứng dụng chính của các mô hình này:
3.1. Hóa Học Hữu Cơ
Trong hóa học hữu cơ, mô hình cấu tạo nguyên tử carbon là cơ sở để hiểu cách carbon tạo ra các liên kết với các nguyên tố khác, tạo thành các hợp chất hữu cơ. Một số ứng dụng bao gồm:
- Phát triển thuốc: Mô hình cấu tạo giúp thiết kế và tổng hợp các phân tử thuốc mới, cải thiện hiệu quả điều trị và giảm tác dụng phụ.
- Phân tích chất hữu cơ: Hiểu cấu trúc của các phân tử hữu cơ giúp phân tích và xác định các chất trong mẫu vật liệu và sinh phẩm.
- Sản xuất polymer: Các mô hình giúp trong việc thiết kế các polymer mới với tính chất cơ lý đặc biệt cho ngành công nghiệp nhựa và cao su.
3.2. Công Nghệ Vật Liệu
Các mô hình cấu tạo nguyên tử carbon đóng vai trò quan trọng trong việc phát triển các vật liệu mới với các đặc tính nổi bật:
- Graphene: Mô hình hybridization giải thích cấu trúc của graphene, một loại vật liệu carbon hai chiều với tính dẫn điện và cơ học cực kỳ tốt, được ứng dụng trong điện tử, pin và cảm biến.
- Carbon Nanotubes: Các mô hình orbital giúp hiểu cấu trúc của carbon nanotubes, được sử dụng trong công nghệ nano, vật liệu composite và y học.
3.3. Y Học
Trong y học, các mô hình cấu tạo nguyên tử carbon hỗ trợ trong việc nghiên cứu và phát triển các công nghệ y sinh:
- Hóa chất y sinh: Các mô hình giúp thiết kế các phân tử thuốc và sinh phẩm để cải thiện hiệu quả điều trị bệnh.
- Hình ảnh y học: Graphene và các vật liệu carbon khác được sử dụng trong các kỹ thuật hình ảnh y học như MRI và CT scan để cải thiện độ chính xác và hiệu quả của chẩn đoán.
3.4. Năng Lượng
Trong lĩnh vực năng lượng, mô hình cấu tạo carbon cũng có những ứng dụng đáng kể:
- Pin và ắc quy: Carbon được sử dụng trong các loại pin và ắc quy để tăng cường hiệu suất và tuổi thọ của thiết bị.
- Chất xúc tác: Các vật liệu carbon được sử dụng làm chất xúc tác trong các phản ứng hóa học để chuyển đổi năng lượng và giảm ô nhiễm.
3.5. Môi Trường
Các mô hình cấu tạo carbon cũng giúp trong việc phát triển các giải pháp bảo vệ môi trường:
- Hấp phụ chất ô nhiễm: Các vật liệu carbon, như than hoạt tính, được sử dụng để loại bỏ các chất ô nhiễm từ không khí và nước.
- Khử CO₂: Công nghệ dựa trên vật liệu carbon giúp giảm lượng CO₂ trong khí quyển, hỗ trợ trong việc chống biến đổi khí hậu.

4. So Sánh Các Mô Hình Cấu Tạo
Các mô hình cấu tạo nguyên tử carbon cung cấp những cái nhìn khác nhau về cách các electron phân bố quanh hạt nhân và cách carbon tạo liên kết hóa học. Việc so sánh các mô hình này giúp hiểu rõ hơn về ưu và nhược điểm của từng mô hình cũng như ứng dụng của chúng trong các lĩnh vực khoa học và công nghệ. Dưới đây là sự so sánh giữa các mô hình cấu tạo chính:
4.1. So Sánh Mô Hình Bohr và Mô Hình Orbital
| Tiêu Chí | Mô Hình Bohr | Mô Hình Orbital |
|---|---|---|
| Phân Bố Electron | Electron phân bố theo các lớp cụ thể quanh hạt nhân. | Electron phân bố trong các orbital hình học (s, p, d, f) với xác suất cao hơn. |
| Độ Chính Xác | Phù hợp với nguyên tử đơn giản nhưng không giải thích được sự hình thành liên kết hóa học phức tạp. | Giải thích chi tiết về hình dạng các orbital và cách các electron tương tác với nhau. |
| Ứng Dụng | Thích hợp cho các phân tử đơn giản và nguyên tử có số lượng electron nhỏ. | Cung cấp cái nhìn rõ ràng về cấu trúc phân tử và các phản ứng hóa học phức tạp. |
4.2. So Sánh Mô Hình Orbital và Mô Hình Hybridization
| Tiêu Chí | Mô Hình Orbital | Mô Hình Hybridization |
|---|---|---|
| Phân Bố Electron | Electron phân bố trong các orbital độc lập (s, p, d). | Orbital nguyên tử kết hợp để tạo ra các orbital lai hóa với khả năng liên kết tốt hơn. |
| Độ Chính Xác | Cung cấp cái nhìn về cách các electron phân bố trong các orbital nhưng không mô tả sự lai hóa của các orbital. | Giải thích rõ ràng cách các orbital lai hóa hình thành liên kết hóa học và cấu trúc phân tử. |
| Ứng Dụng | Hữu ích trong việc hiểu cấu trúc các orbital và phân tử có liên kết đơn giản. | Rất quan trọng trong việc mô tả cấu trúc phân tử và liên kết hóa học phức tạp, như trong các hợp chất hữu cơ. |
4.3. Tóm Tắt Sự Khác Biệt Chính
- Mô hình Bohr tập trung vào các lớp electron, cung cấp cái nhìn cơ bản nhưng thiếu chi tiết về cấu trúc liên kết.
- Mô hình Orbital cung cấp thông tin về phân bố các electron trong các orbital và hình dạng của chúng, nhưng không giải thích sự lai hóa của các orbital.
- Mô hình Hybridization giải thích sự lai hóa của các orbital nguyên tử để tạo ra các liên kết hóa học bền vững và cấu trúc phân tử cụ thể, phù hợp với phân tử carbon phức tạp.

5. Tài Liệu và Nguồn Tham Khảo
Để hiểu sâu về mô hình cấu tạo nguyên tử carbon và các ứng dụng của nó, có nhiều tài liệu và nguồn tham khảo hữu ích mà bạn có thể tham khảo. Dưới đây là một số tài liệu và nguồn tham khảo quan trọng:
5.1. Sách Giáo Khoa và Chuyên Ngành
- Hóa Học Đại Cương - Đây là sách cơ bản giúp bạn hiểu về các khái niệm cơ bản trong hóa học, bao gồm cấu trúc nguyên tử và mô hình liên kết hóa học.
- Các Mô Hình Cấu Tạo Nguyên Tử - Tài liệu chuyên sâu về các mô hình cấu tạo nguyên tử, giải thích chi tiết về các mô hình Bohr, Orbital và Hybridization.
- Hóa Học Hữu Cơ - Cung cấp cái nhìn sâu về hóa học hữu cơ, nơi carbon đóng vai trò trung tâm trong cấu trúc phân tử.
5.2. Các Tạp Chí Khoa Học
- Tạp Chí Hóa Học - Đăng tải các bài viết nghiên cứu và bài báo liên quan đến cấu trúc nguyên tử và các ứng dụng của carbon trong khoa học và công nghệ.
- Tạp Chí Vật Liệu Nano - Cung cấp thông tin về các ứng dụng của carbon trong công nghệ nano, bao gồm graphene và carbon nanotubes.
5.3. Các Nguồn Trực Tuyến
- Wikipedia - Cung cấp các bài viết tổng quan và dễ hiểu về các mô hình cấu tạo nguyên tử carbon và ứng dụng của chúng.
- PubMed - Nơi tìm kiếm các nghiên cứu và bài báo khoa học về ứng dụng của carbon trong y học và công nghệ.
- Google Scholar - Cung cấp các tài liệu nghiên cứu khoa học về các mô hình cấu tạo nguyên tử và các ứng dụng của chúng.
5.4. Các Tài Nguyên Học Tập
- Kênh Youtube Khoa Học - Cung cấp video giải thích về các mô hình cấu tạo nguyên tử và ứng dụng của chúng.
- Khóa Học Trực Tuyến - Nhiều nền tảng học trực tuyến cung cấp khóa học về hóa học hữu cơ và cấu tạo nguyên tử.
Các tài liệu và nguồn tham khảo này sẽ cung cấp thông tin phong phú và chi tiết giúp bạn hiểu rõ hơn về mô hình cấu tạo nguyên tử carbon và ứng dụng của chúng trong các lĩnh vực khác nhau.
XEM THÊM:
6. Kết Luận
Các mô hình cấu tạo nguyên tử carbon cung cấp cái nhìn sâu sắc về cách các electron phân bố xung quanh hạt nhân và ảnh hưởng của chúng đến khả năng tạo liên kết hóa học của carbon. Việc hiểu các mô hình này không chỉ giúp chúng ta giải thích cấu trúc của nguyên tử mà còn mở ra nhiều ứng dụng trong các lĩnh vực khác nhau.
Những mô hình cấu tạo nguyên tử carbon chính như mô hình Bohr, mô hình Orbital và mô hình Hybridization đều có những ưu điểm và hạn chế riêng. Mô hình Bohr cung cấp cái nhìn cơ bản về phân bố lớp electron nhưng chưa giải thích được cấu trúc liên kết phức tạp. Mô hình Orbital đưa ra cái nhìn chi tiết hơn về các orbital và sự phân bố electron, trong khi mô hình Hybridization giúp giải thích khả năng tạo liên kết của carbon và cấu trúc phân tử phức tạp.
Ứng dụng của các mô hình này rất phong phú, từ hóa học hữu cơ, công nghệ vật liệu, y học đến các giải pháp bảo vệ môi trường. Việc hiểu rõ các mô hình này giúp các nhà khoa học và kỹ sư thiết kế và cải thiện các sản phẩm và công nghệ, từ thuốc chữa bệnh đến vật liệu nano và công nghệ năng lượng.
Trong tương lai, nghiên cứu và phát triển các mô hình cấu tạo nguyên tử sẽ tiếp tục đóng vai trò quan trọng trong việc khám phá và phát triển các công nghệ mới. Sự tiến bộ trong lĩnh vực này không chỉ mở ra những cơ hội mới cho khoa học và công nghệ mà còn góp phần vào việc giải quyết các thách thức toàn cầu.
Tóm lại, việc nắm vững các mô hình cấu tạo nguyên tử carbon không chỉ giúp hiểu rõ hơn về bản chất của nguyên tử carbon mà còn tạo điều kiện cho sự phát triển của các ứng dụng thực tiễn trong nhiều lĩnh vực khác nhau.