Chủ đề bảng tuần hoàn và cấu tạo nguyên tử: Bảng tuần hoàn và cấu tạo nguyên tử là nền tảng quan trọng trong hóa học, giúp hiểu rõ tính chất các nguyên tố và mối quan hệ giữa chúng. Bài viết này sẽ đưa bạn khám phá chi tiết về cấu trúc, ý nghĩa và ứng dụng thực tiễn của bảng tuần hoàn trong học tập và đời sống.
Mục lục
- Bảng Tuần Hoàn và Cấu Tạo Nguyên Tử
- 1. Giới thiệu về Bảng Tuần Hoàn
- 2. Cấu Tạo Nguyên Tử và Mối Quan Hệ Với Vị Trí Trong Bảng Tuần Hoàn
- 3. Phân Loại Các Nhóm Nguyên Tố Trong Bảng Tuần Hoàn
- 4. Ý Nghĩa Của Bảng Tuần Hoàn
- 5. Các Quy Ước và Phân Loại Khác Trong Bảng Tuần Hoàn
- 6. Các Ví Dụ Thực Tiễn và Bài Tập Liên Quan
Bảng Tuần Hoàn và Cấu Tạo Nguyên Tử
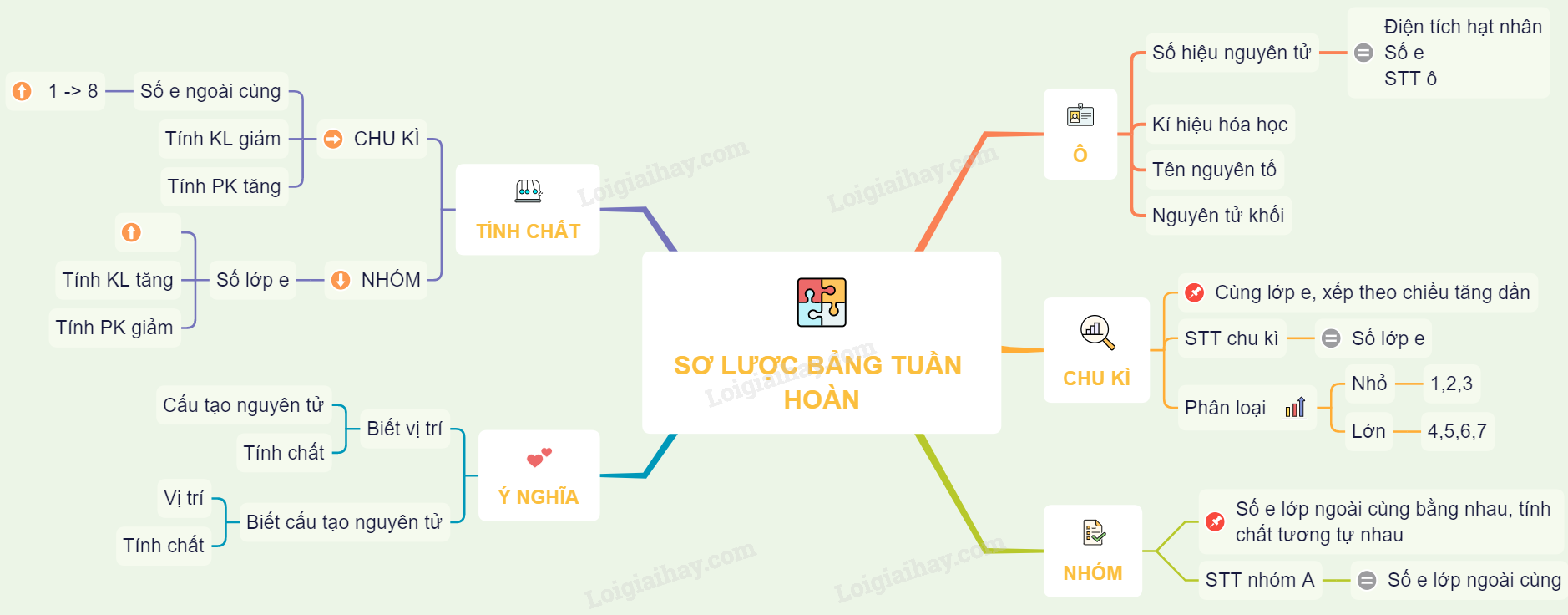
Bảng tuần hoàn là một công cụ quan trọng trong hóa học, giúp chúng ta hiểu rõ hơn về cấu trúc và tính chất của các nguyên tố hóa học. Dưới đây là một cái nhìn tổng quan về bảng tuần hoàn và cấu tạo nguyên tử.
1. Cấu Trúc của Bảng Tuần Hoàn
Bảng tuần hoàn bao gồm các nguyên tố hóa học được sắp xếp theo số hiệu nguyên tử tăng dần. Các nguyên tố trong cùng một cột (nhóm) có tính chất hóa học tương tự nhau, trong khi các nguyên tố trong cùng một hàng (chu kỳ) có cùng số lớp electron.
- Nhóm: Nguyên tố trong cùng một nhóm có số electron hóa trị bằng nhau. Ví dụ, các nguyên tố trong nhóm IA có một electron hóa trị.
- Chu Kỳ: Số chu kỳ cho biết số lớp electron trong nguyên tử. Từ trái sang phải trong cùng một chu kỳ, bán kính nguyên tử giảm dần và năng lượng ion hóa tăng lên.
2. Cấu Tạo Nguyên Tử và Liên Kết
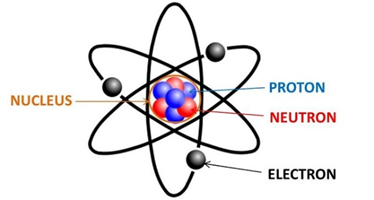
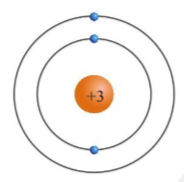
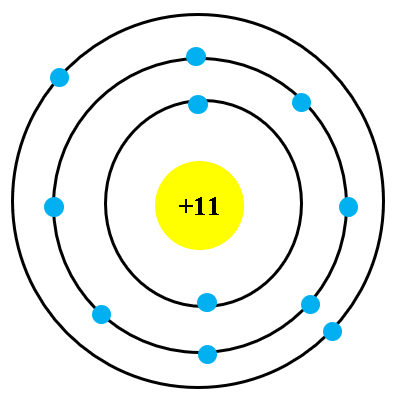
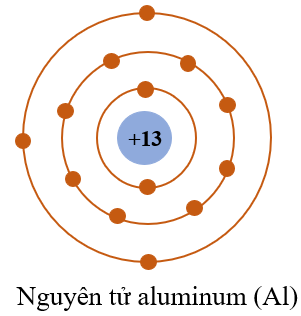
Nguyên tử gồm có hạt nhân ở trung tâm và các electron quay quanh. Số proton trong hạt nhân xác định nguyên tố và vị trí của nó trong bảng tuần hoàn.
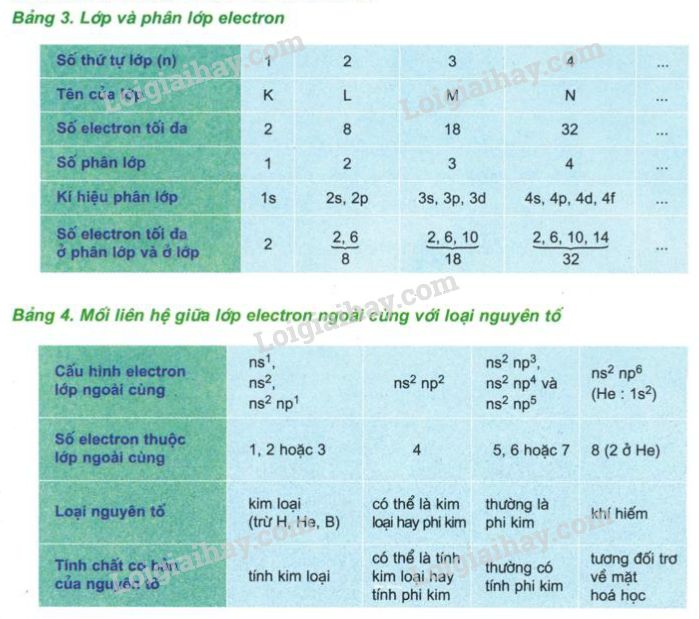
- Cấu hình electron: Xác định vị trí của nguyên tố trong bảng tuần hoàn. Các electron được sắp xếp vào các phân lớp s, p, d, f theo thứ tự năng lượng tăng dần.
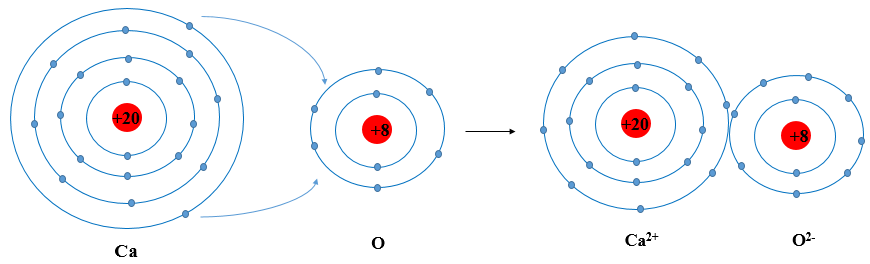
- Liên kết hóa học: Các nguyên tố tham gia vào các liên kết hóa học để đạt được cấu hình electron bền vững. Liên kết ion hình thành giữa kim loại và phi kim, trong khi liên kết cộng hóa trị thường gặp giữa các phi kim.
3. Phân Loại Nguyên Tố
| Kim loại | Chiếm phần lớn bảng tuần hoàn, thường dẫn điện và nhiệt tốt, có ánh kim, nằm ở bên trái bảng. |
| Phi kim | Thường là khí hoặc chất rắn giòn, không dẫn điện, nằm ở phía bên phải bảng tuần hoàn. |
| Á kim | Có tính chất trung gian giữa kim loại và phi kim, nằm giữa hai loại này trên bảng tuần hoàn. |
4. Mối Liên Hệ Giữa Vị Trí và Tính Chất Nguyên Tố
Vị trí của một nguyên tố trong bảng tuần hoàn cho phép dự đoán các tính chất vật lý và hóa học của nó. Ví dụ:
- Các nguyên tố trong nhóm IA là kim loại kiềm, rất dễ mất electron để tạo thành ion dương.
- Các nguyên tố nhóm VIIA là halogen, dễ dàng nhận thêm một electron để tạo thành ion âm.
- Kim loại chuyển tiếp (các nguyên tố nhóm B) có khả năng tạo nhiều loại ion khác nhau và có các tính chất hóa học phức tạp.
Bảng tuần hoàn không chỉ là một công cụ sắp xếp các nguyên tố mà còn phản ánh các quy luật tự nhiên trong hóa học, giúp chúng ta hiểu sâu hơn về cấu trúc và hoạt động của thế giới vi mô.

1. Giới thiệu về Bảng Tuần Hoàn
Bảng tuần hoàn là một công cụ quan trọng trong hóa học, được phát triển bởi nhà khoa học người Nga Dmitri Mendeleev vào năm 1869. Nó sắp xếp các nguyên tố hóa học dựa trên số hiệu nguyên tử, cấu hình electron, và các tính chất hóa học lặp lại của chúng. Điều này giúp dễ dàng dự đoán tính chất của các nguyên tố và mối quan hệ giữa chúng.
Bảng tuần hoàn hiện đại được chia thành các hàng ngang gọi là chu kỳ và các cột dọc gọi là nhóm. Mỗi nguyên tố trong cùng một nhóm thường có các tính chất hóa học tương tự nhau, ví dụ như các kim loại kiềm ở nhóm IA đều có một electron lớp ngoài cùng.
Thông qua bảng tuần hoàn, ta có thể hiểu rõ hơn về:
- Cấu trúc nguyên tử: Vị trí của nguyên tố trong bảng tuần hoàn phản ánh cấu hình electron của nó, từ đó giúp dự đoán được các tính chất hóa học.
- Sự biến đổi tính chất hóa học: Các tính chất hóa học của nguyên tố biến đổi có quy luật khi di chuyển từ trái sang phải trong một chu kỳ và từ trên xuống dưới trong một nhóm.
Ví dụ, khi di chuyển từ trái sang phải trong một chu kỳ, bán kính nguyên tử thường giảm do số proton trong hạt nhân tăng lên, kéo các electron lại gần hạt nhân hơn. Đồng thời, năng lượng ion hóa và độ âm điện của nguyên tố cũng tăng lên.
Một trong những đặc điểm nổi bật của bảng tuần hoàn là khả năng dự đoán tính chất của các nguyên tố chưa được phát hiện. Dựa trên cấu trúc bảng, Mendeleev đã dự đoán chính xác sự tồn tại và tính chất của các nguyên tố như gallium và germanium trước khi chúng được khám phá.
2. Cấu Tạo Nguyên Tử và Mối Quan Hệ Với Vị Trí Trong Bảng Tuần Hoàn
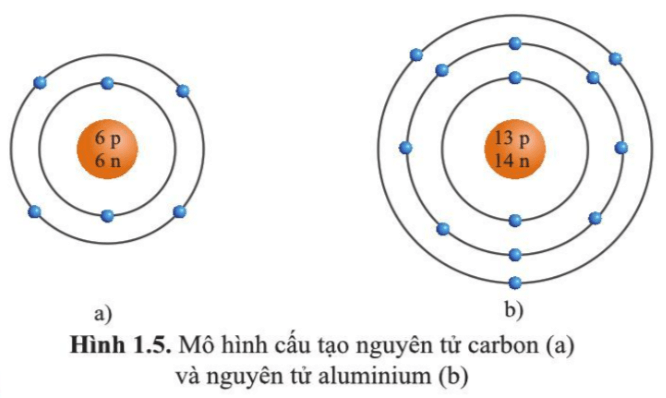
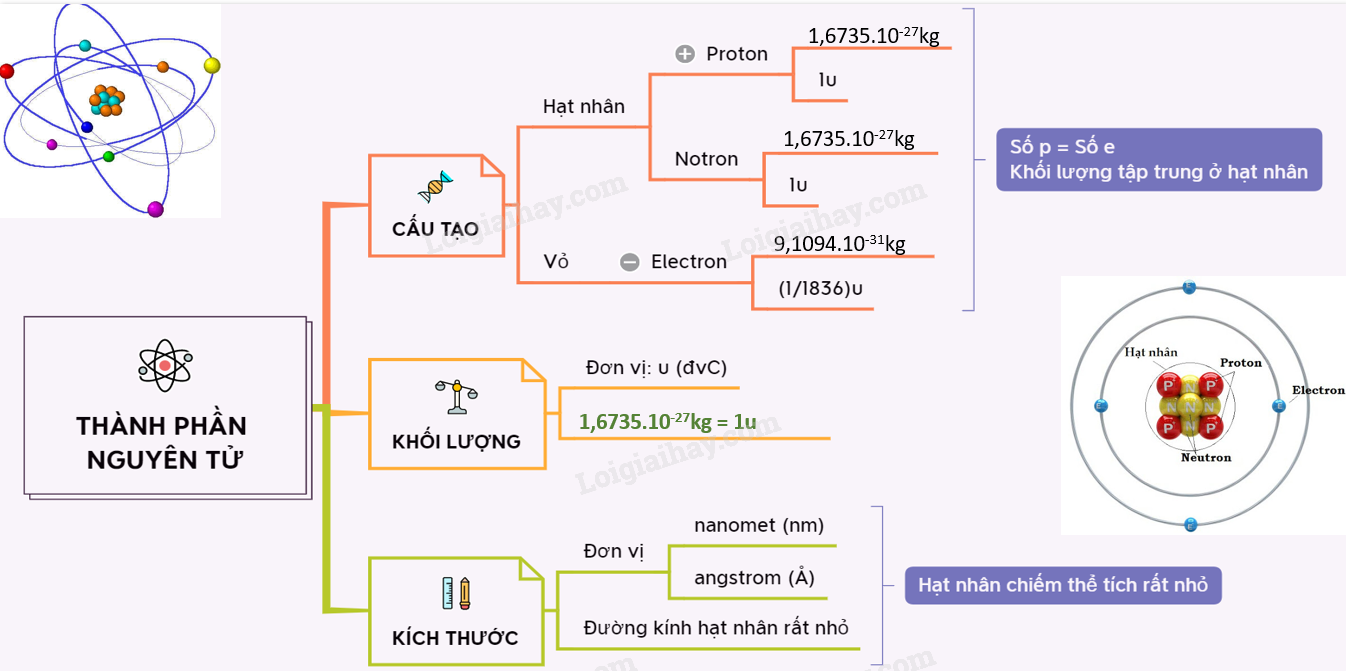
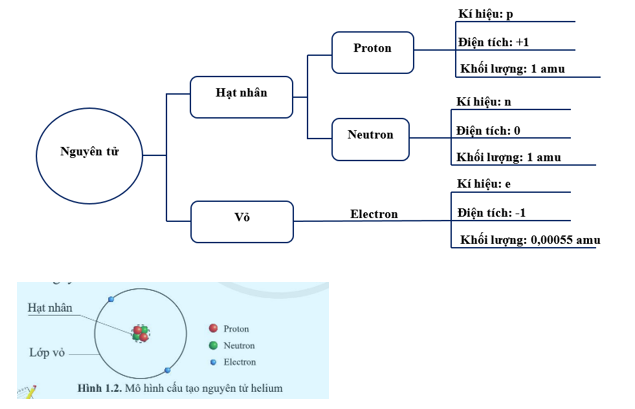
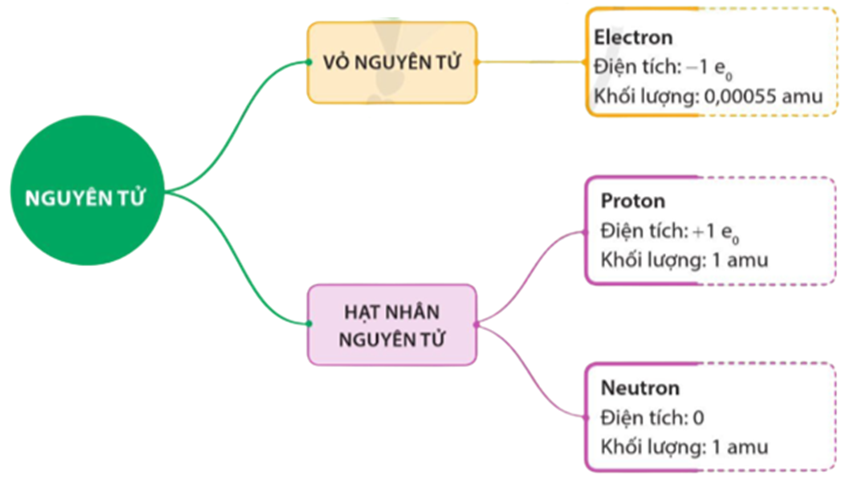
Nguyên tử là đơn vị cơ bản của vật chất, bao gồm ba loại hạt chính: proton, neutron và electron. Cấu tạo của nguyên tử được xác định bởi số lượng và vị trí của các hạt này, đặc biệt là electron, trong các lớp vỏ electron. Vị trí của nguyên tố trong bảng tuần hoàn phản ánh cấu trúc electron của nó, từ đó ảnh hưởng đến tính chất hóa học và vật lý.
Mỗi nguyên tố có một số hiệu nguyên tử (Z) tương ứng với số proton trong hạt nhân. Số hiệu nguyên tử cũng chính là số electron trong nguyên tử trung hòa điện. Các electron được phân bố vào các lớp và phân lớp theo nguyên lý Pauli, nguyên lý Hund và quy tắc Aufbau.
Bảng tuần hoàn chia các nguyên tố thành các nhóm và chu kỳ. Các nguyên tố trong cùng một nhóm có cùng số electron lớp ngoài cùng, dẫn đến các tính chất hóa học tương tự. Ví dụ, các nguyên tố trong nhóm IA đều có một electron ở lớp ngoài cùng, điều này làm cho chúng có xu hướng mất đi electron này để đạt cấu hình bền vững của khí hiếm.
Ngược lại, các nguyên tố trong cùng một chu kỳ có cùng số lượng lớp electron, nhưng số electron lớp ngoài cùng tăng dần khi đi từ trái sang phải. Điều này dẫn đến sự thay đổi dần dần về bán kính nguyên tử, năng lượng ion hóa, và độ âm điện:
- Bán kính nguyên tử: Khi đi từ trái sang phải trong cùng một chu kỳ, bán kính nguyên tử giảm dần do lực hút giữa hạt nhân và các electron tăng lên.
- Năng lượng ion hóa: Năng lượng cần thiết để loại bỏ một electron ra khỏi nguyên tử tăng dần từ trái sang phải, do lực hút hạt nhân mạnh hơn.
- Độ âm điện: Khả năng của một nguyên tử trong phân tử hút electron về phía mình tăng dần khi đi từ trái sang phải trong cùng một chu kỳ.
Mối quan hệ giữa cấu tạo nguyên tử và vị trí trong bảng tuần hoàn cho phép chúng ta dự đoán được tính chất của các nguyên tố, cũng như giải thích các hiện tượng hóa học cơ bản.

3. Phân Loại Các Nhóm Nguyên Tố Trong Bảng Tuần Hoàn
Bảng tuần hoàn hóa học chia các nguyên tố thành các nhóm dựa trên cấu hình electron và các tính chất hóa học tương tự. Mỗi nhóm nguyên tố trong bảng tuần hoàn đại diện cho một tập hợp các nguyên tố có những đặc điểm chung, được sắp xếp theo chiều dọc.
Các nhóm nguyên tố chính bao gồm:
- Nhóm nguyên tố s: Các nguyên tố thuộc nhóm này có electron cuối cùng nằm trong orbital \(s\). Các nguyên tố này bao gồm kim loại kiềm (nhóm IA) và kim loại kiềm thổ (nhóm IIA). Chúng có tính chất hóa học tương tự, chẳng hạn như có tính khử mạnh và phản ứng mạnh với nước.
- Nhóm nguyên tố p: Các nguyên tố có electron cuối cùng nằm trong orbital \(p\), bao gồm các phi kim như oxygen, nitrogen, và các halogen, cũng như các á kim như boron và silicon. Các nguyên tố này thường có độ âm điện cao và có tính oxi hóa mạnh.
- Nhóm nguyên tố d: Nhóm này bao gồm các kim loại chuyển tiếp như sắt (Fe), đồng (Cu), và kẽm (Zn), với electron cuối cùng nằm trong orbital \(d\). Các nguyên tố này có khả năng tạo phức chất và có nhiều trạng thái oxi hóa khác nhau.
- Nhóm nguyên tố f: Nhóm này bao gồm các nguyên tố đất hiếm và các nguyên tố actini, với electron cuối cùng nằm trong orbital \(f\). Chúng thường có cấu trúc electron phức tạp và thể hiện nhiều tính chất hóa học đặc biệt.
Việc phân loại các nhóm nguyên tố trong bảng tuần hoàn giúp chúng ta hiểu rõ hơn về tính chất hóa học và vật lý của từng nguyên tố, cũng như dự đoán cách chúng sẽ phản ứng trong các hợp chất khác nhau. Sự hiểu biết này là cơ sở để nghiên cứu và ứng dụng các nguyên tố trong nhiều lĩnh vực khoa học và công nghệ.

4. Ý Nghĩa Của Bảng Tuần Hoàn
Bảng tuần hoàn không chỉ đơn thuần là một công cụ sắp xếp các nguyên tố hóa học, mà còn mang lại nhiều ý nghĩa quan trọng đối với khoa học và đời sống.
- Ý nghĩa về cấu tạo nguyên tử: Bảng tuần hoàn giúp chúng ta hiểu rõ hơn về cấu trúc của nguyên tử, bao gồm số proton, neutron và electron của mỗi nguyên tố. Vị trí của nguyên tố trong bảng tuần hoàn cung cấp thông tin về cấu hình electron, từ đó xác định được tính chất hóa học của nguyên tố.
- Ý nghĩa về tính chất hóa học: Các nguyên tố trong cùng một nhóm có tính chất hóa học tương tự, giúp dự đoán cách mà chúng phản ứng với các chất khác. Điều này rất quan trọng trong việc phát triển các hợp chất mới và ứng dụng chúng trong công nghiệp, y học, và nông nghiệp.
- Ứng dụng thực tiễn: Bảng tuần hoàn là cơ sở để tìm hiểu và ứng dụng các nguyên tố trong nhiều lĩnh vực như sản xuất, dược phẩm, và nghiên cứu khoa học. Ví dụ, hiểu rõ tính chất của kim loại chuyển tiếp giúp tối ưu hóa quá trình chế tạo hợp kim và chất xúc tác trong công nghiệp.
Bảng tuần hoàn không chỉ là một công cụ học tập quan trọng mà còn là nền tảng cho nhiều nghiên cứu và phát minh khoa học. Khả năng dự đoán và giải thích các tính chất hóa học của nguyên tố từ vị trí của chúng trong bảng tuần hoàn là một trong những thành tựu vĩ đại của hóa học hiện đại.

5. Các Quy Ước và Phân Loại Khác Trong Bảng Tuần Hoàn
Bảng tuần hoàn không chỉ sắp xếp các nguyên tố theo số hiệu nguyên tử, mà còn áp dụng các quy ước và phân loại khác nhau để làm rõ tính chất và mối quan hệ giữa các nguyên tố. Dưới đây là một số quy ước và phân loại phổ biến:
- Phân loại theo nhóm: Các nguyên tố được chia thành nhóm dựa trên số electron lớp ngoài cùng và tính chất hóa học tương tự. Ví dụ, các nguyên tố trong nhóm IA (kim loại kiềm) đều có một electron lớp ngoài cùng và có tính chất hóa học giống nhau.
- Phân loại theo chu kỳ: Bảng tuần hoàn được chia thành các chu kỳ dựa trên số lớp electron trong nguyên tử. Các nguyên tố trong cùng một chu kỳ có số lớp electron bằng nhau, nhưng tính chất hóa học thay đổi khi đi từ trái sang phải.
- Phân loại theo trạng thái vật lý: Các nguyên tố cũng được phân loại dựa trên trạng thái vật lý tại điều kiện thường, bao gồm kim loại, phi kim và á kim. Kim loại thường dẫn điện và dẫn nhiệt tốt, trong khi phi kim có tính chất đối ngược.
- Quy ước về kí hiệu hóa học: Mỗi nguyên tố được biểu thị bằng một ký hiệu hóa học, thường là một hoặc hai chữ cái viết tắt từ tên tiếng Latin của nguyên tố đó. Ví dụ, \( \text{Fe} \) là ký hiệu của sắt (Ferrum), \( \text{Na} \) là ký hiệu của natri (Natrium).
- Phân loại theo khối lượng nguyên tử: Các nguyên tố cũng được sắp xếp theo khối lượng nguyên tử, giúp xác định sự ổn định và các đồng vị của nguyên tố đó. Khối lượng nguyên tử thường được hiển thị dưới dạng số thập phân trên bảng tuần hoàn.
Những quy ước và phân loại này giúp cho việc học tập và nghiên cứu hóa học trở nên hệ thống và dễ dàng hơn, đồng thời cung cấp những công cụ quan trọng để dự đoán và giải thích các hiện tượng hóa học trong tự nhiên.
XEM THÊM:
6. Các Ví Dụ Thực Tiễn và Bài Tập Liên Quan
Để hiểu rõ hơn về bảng tuần hoàn và cấu tạo nguyên tử, chúng ta có thể áp dụng kiến thức này vào một số ví dụ thực tiễn và bài tập sau đây.
Ví dụ 1: Xác định tính chất hóa học của các nguyên tố thuộc nhóm IA
- Giả sử bạn có các nguyên tố Lithium (\( \text{Li} \)), Natri (\( \text{Na} \)), và Kali (\( \text{K} \)). Hãy so sánh các tính chất hóa học của chúng dựa trên vị trí của chúng trong bảng tuần hoàn.
- Gợi ý: Do chúng đều thuộc nhóm IA, các nguyên tố này có một electron ở lớp ngoài cùng, dẫn đến tính chất hóa học tương tự nhau, như khả năng phản ứng mạnh với nước để tạo thành hydroxide kim loại và giải phóng khí hydro.
Bài tập 1: Tính số electron, proton, và neutron của một nguyên tử
- Cho nguyên tố X có số hiệu nguyên tử là 12 và khối lượng nguyên tử là 24. Hãy xác định số lượng electron, proton, và neutron của nguyên tử này.
- Giải:
- Số electron = Số proton = Số hiệu nguyên tử = 12
- Số neutron = Khối lượng nguyên tử - Số proton = 24 - 12 = 12
Ví dụ 2: Dự đoán tính chất của một nguyên tố dựa trên vị trí của nó trong bảng tuần hoàn
- Hãy dự đoán tính chất vật lý và hóa học của nguyên tố Brom (\( \text{Br} \)) dựa trên vị trí của nó trong bảng tuần hoàn.
- Gợi ý: Brom là một halogen thuộc nhóm VIIA. Nó có tính oxi hóa mạnh và thường tham gia vào các phản ứng để nhận electron và tạo thành ion bromide (\( \text{Br}^- \)). Ở nhiệt độ phòng, Brom tồn tại dưới dạng lỏng và có màu nâu đỏ.
Bài tập 2: Xác định vị trí của nguyên tố trong bảng tuần hoàn
- Nguyên tố Y có cấu hình electron: \( 1s^2 2s^2 2p^6 3s^2 3p^5 \). Hãy xác định vị trí của nguyên tố Y trong bảng tuần hoàn.
- Giải:
- Số electron: 2 + 2 + 6 + 2 + 5 = 17
- Số hiệu nguyên tử = 17, vậy nguyên tố Y là Chlorine (\( \text{Cl} \)).
- Vị trí trong bảng tuần hoàn: Chu kỳ 3, nhóm VIIA.
Những ví dụ và bài tập này sẽ giúp bạn củng cố kiến thức về bảng tuần hoàn và cấu tạo nguyên tử, đồng thời nâng cao kỹ năng giải quyết các bài toán hóa học thực tiễn.