Chủ đề electron energy levels: Mức năng lượng electron là yếu tố then chốt trong nhiều lĩnh vực khoa học và công nghệ. Bài viết này sẽ giúp bạn khám phá sâu hơn về các mức năng lượng electron, từ cơ bản đến ứng dụng thực tiễn, đồng thời cung cấp kiến thức cần thiết để hiểu rõ hơn về thế giới vi mô đầy thú vị này.
Mục lục
Mức Năng Lượng Electron
Mức năng lượng electron là một khái niệm cơ bản trong vật lý và hóa học, liên quan đến các trạng thái năng lượng mà một electron có thể chiếm giữ trong một nguyên tử hoặc phân tử. Electron có thể chuyển đổi giữa các mức năng lượng khác nhau bằng cách hấp thụ hoặc phát ra năng lượng dưới dạng photon.
Các Khái Niệm Chính
- Mức Năng Lượng: Mỗi mức năng lượng đại diện cho một trạng thái cố định mà electron có thể tồn tại. Các mức năng lượng này được lượng tử hóa, nghĩa là electron chỉ có thể tồn tại ở các mức cụ thể, không phải ở giữa các mức đó.
- Quỹ Đạo Electron: Quỹ đạo là khu vực xung quanh hạt nhân nơi electron có khả năng xuất hiện cao nhất. Các quỹ đạo này được sắp xếp theo mức năng lượng từ thấp đến cao.
- Sự Chuyển Dịch Năng Lượng: Khi electron chuyển từ mức năng lượng cao xuống mức năng lượng thấp hơn, nó phát ra năng lượng dưới dạng photon. Ngược lại, khi electron hấp thụ năng lượng, nó có thể nhảy lên mức năng lượng cao hơn.
Công Thức Liên Quan
Công thức liên quan đến mức năng lượng của electron trong nguyên tử hydrogen là:
Trong đó:
- \(E_n\) là năng lượng của mức năng lượng thứ \(n\).
- \(n\) là số lượng tử chính, đại diện cho các mức năng lượng (n=1, 2, 3,...).
- 13.6 eV là năng lượng ion hóa của nguyên tử hydrogen, tương ứng với mức năng lượng thấp nhất.
Ứng Dụng Trong Thực Tế
Mức năng lượng của electron là cơ sở cho nhiều hiện tượng và ứng dụng trong thực tế:
- Quang Phổ Hấp Thụ và Phát Xạ: Mỗi nguyên tố có một tập hợp các mức năng lượng riêng, tạo ra các dải quang phổ đặc trưng khi electron chuyển dịch giữa các mức năng lượng này. Điều này được ứng dụng trong việc phân tích thành phần của các chất.
- Pin Năng Lượng Mặt Trời: Hiểu biết về mức năng lượng giúp cải thiện hiệu suất của các vật liệu bán dẫn trong pin mặt trời, nơi electron được kích thích để tạo ra dòng điện.
- Điện Tử Học: Mức năng lượng electron cũng quan trọng trong thiết kế các linh kiện điện tử, như transistor, nơi việc kiểm soát chuyển động của electron giữa các mức năng lượng là cơ bản.
Kết Luận
Mức năng lượng electron là một khái niệm quan trọng trong nhiều lĩnh vực khoa học và công nghệ. Hiểu rõ về các mức năng lượng này không chỉ giúp giải thích các hiện tượng vật lý và hóa học mà còn mở ra các ứng dụng mới trong công nghệ cao.

Giới Thiệu Về Mức Năng Lượng Electron
Mức năng lượng electron là một khái niệm quan trọng trong vật lý lượng tử và hóa học, đóng vai trò nền tảng trong việc hiểu về cấu trúc nguyên tử và phân tử. Mỗi electron trong một nguyên tử tồn tại ở các mức năng lượng cụ thể, được xác định bởi số lượng tử chính \(n\). Các mức năng lượng này không liên tục mà được lượng tử hóa, nghĩa là electron chỉ có thể tồn tại ở những mức năng lượng nhất định.
Trong nguyên tử, electron quay quanh hạt nhân ở các quỹ đạo nhất định, tương ứng với các mức năng lượng khác nhau. Khi electron chuyển dịch từ mức năng lượng này sang mức năng lượng khác, nó có thể hấp thụ hoặc phát ra năng lượng dưới dạng photon. Công thức tính năng lượng của electron trong nguyên tử hydro là:
Trong đó:
- \(E_n\) là năng lượng của mức năng lượng thứ \(n\).
- \(n\) là số lượng tử chính, biểu thị các mức năng lượng (n=1, 2, 3,...).
- 13.6 eV là năng lượng ion hóa của nguyên tử hydro, tương ứng với mức năng lượng cơ bản.
Hiểu rõ về các mức năng lượng electron không chỉ giúp giải thích nhiều hiện tượng vật lý, như quang phổ của các nguyên tố, mà còn có ứng dụng quan trọng trong công nghệ, chẳng hạn như trong pin năng lượng mặt trời và các thiết bị điện tử. Điều này mở ra một thế giới vi mô đầy thú vị và đóng góp vào sự phát triển của khoa học và công nghệ hiện đại.
Các Mức Năng Lượng Của Electron Trong Nguyên Tử
Trong một nguyên tử, các electron không chuyển động tự do mà bị ràng buộc trong các quỹ đạo xung quanh hạt nhân. Mỗi quỹ đạo tương ứng với một mức năng lượng cụ thể, và các electron trong cùng một nguyên tử có thể tồn tại ở các mức năng lượng khác nhau. Các mức năng lượng này được xác định bởi số lượng tử chính \(n\), với giá trị \(n = 1, 2, 3,...\), từ mức năng lượng thấp nhất trở lên.
Mỗi mức năng lượng có một khoảng cách cụ thể so với hạt nhân và năng lượng của các electron tại các mức này cũng khác nhau. Electron ở mức năng lượng cao hơn có nhiều năng lượng hơn và ở xa hạt nhân hơn so với electron ở mức năng lượng thấp hơn. Khi một electron chuyển từ một mức năng lượng cao xuống mức năng lượng thấp hơn, nó phát ra một photon có năng lượng tương ứng với sự chênh lệch giữa hai mức năng lượng. Ngược lại, khi một electron hấp thụ năng lượng, nó có thể nhảy lên một mức năng lượng cao hơn.
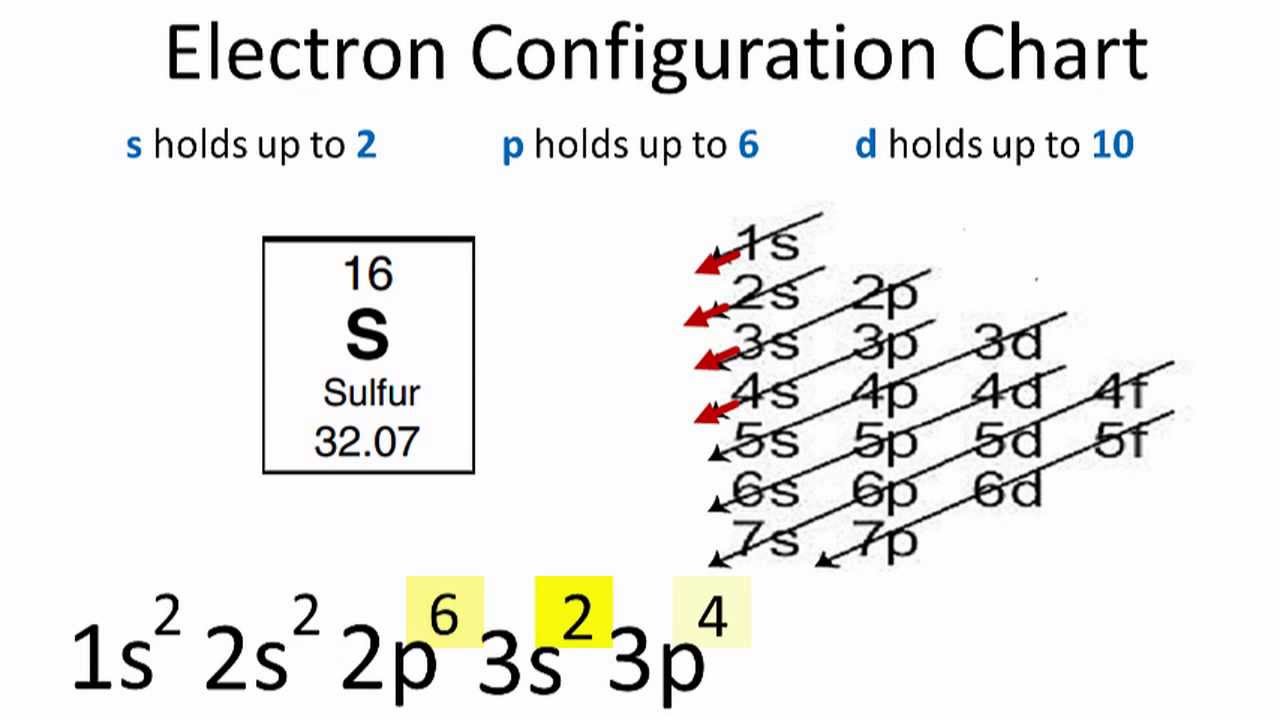
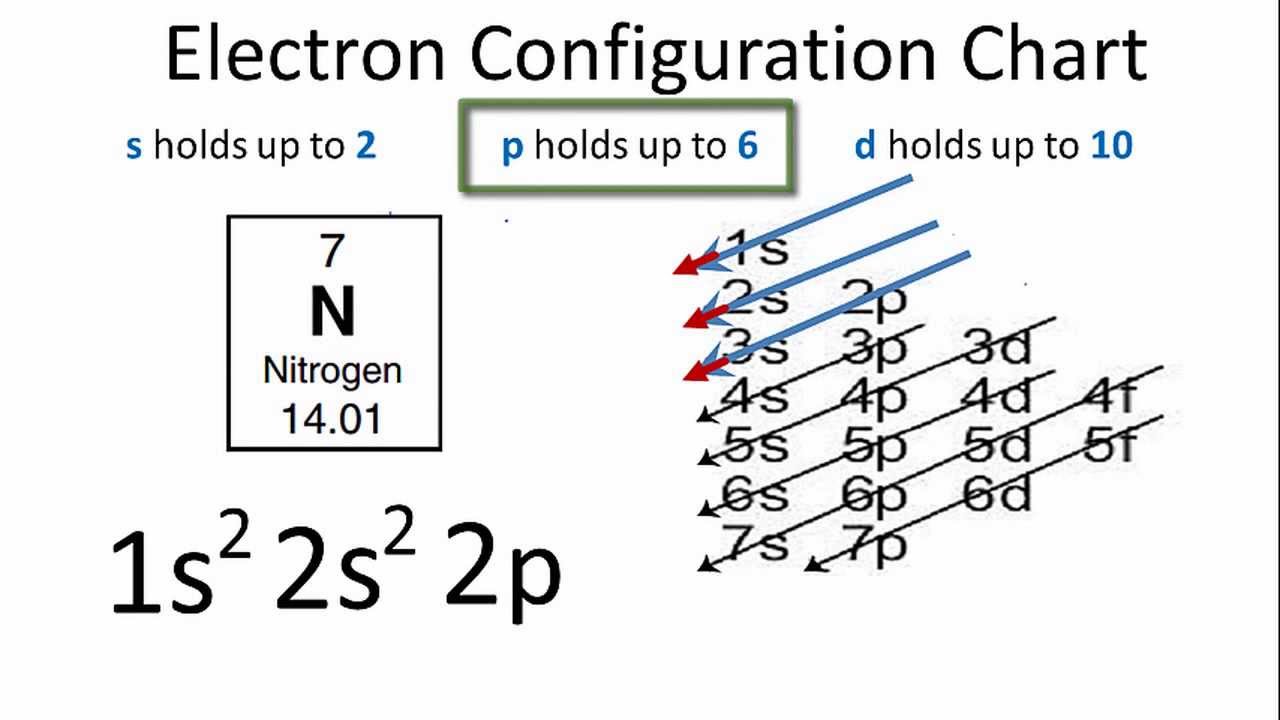
Nguyên tắc sắp xếp các electron vào các mức năng lượng được quy định bởi các quy tắc như nguyên lý loại trừ Pauli và quy tắc Hund:
- Nguyên lý loại trừ Pauli: Không có hai electron nào trong cùng một nguyên tử có thể có cùng bốn số lượng tử giống nhau. Điều này có nghĩa là mỗi quỹ đạo chỉ có thể chứa tối đa hai electron, và chúng phải có spin ngược chiều.
- Quy tắc Hund: Khi các electron điền vào các quỹ đạo có cùng mức năng lượng, chúng sẽ được điền vào từng quỹ đạo một cách độc lập trước khi ghép cặp với nhau.
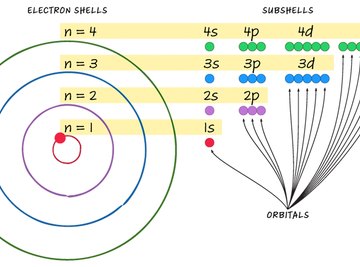
Các mức năng lượng của electron trong nguyên tử được biểu diễn qua các sơ đồ năng lượng, giúp minh họa rõ ràng vị trí của các electron trong nguyên tử. Sơ đồ này cũng giúp chúng ta hiểu rõ hơn về cấu trúc điện tử của các nguyên tố và sự tương tác giữa các electron với nhau.
Hiểu về các mức năng lượng của electron là cơ sở để nắm bắt nhiều khía cạnh của hóa học và vật lý hiện đại, bao gồm quang phổ học, hóa học lượng tử, và nhiều ứng dụng công nghệ khác.

Sự Chuyển Dịch Giữa Các Mức Năng Lượng
Sự chuyển dịch giữa các mức năng lượng của electron trong nguyên tử là một quá trình quan trọng, diễn ra khi electron di chuyển từ một mức năng lượng này sang một mức năng lượng khác. Quá trình này có thể xảy ra khi electron hấp thụ hoặc phát ra một lượng năng lượng tương ứng với sự chênh lệch giữa hai mức năng lượng đó.
Quá trình chuyển dịch có thể được chia thành hai loại chính:
- Chuyển Dịch Hấp Thụ: Khi một electron nhận đủ năng lượng từ một nguồn bên ngoài (chẳng hạn như photon ánh sáng), nó có thể nhảy lên một mức năng lượng cao hơn. Năng lượng của photon hấp thụ phải khớp với sự chênh lệch năng lượng giữa hai mức này, tuân theo công thức: \[ \Delta E = E_2 - E_1 = h\nu \] Trong đó, \(\Delta E\) là năng lượng hấp thụ, \(h\) là hằng số Planck, và \(\nu\) là tần số của photon.
- Chuyển Dịch Phát Xạ: Khi một electron trở về mức năng lượng thấp hơn từ mức năng lượng cao hơn, nó phát ra năng lượng dưới dạng photon. Quá trình này có thể diễn ra tự phát hoặc được kích thích. Năng lượng của photon phát ra cũng khớp với sự chênh lệch năng lượng giữa hai mức, theo công thức: \[ E_{\text{photon}} = E_{\text{cao}} - E_{\text{thấp}} \]
Trong một số trường hợp đặc biệt, sự chuyển dịch giữa các mức năng lượng có thể không chỉ liên quan đến một photon duy nhất mà có thể liên quan đến nhiều photon hoặc quá trình tương tác phức tạp khác. Những chuyển dịch này là cơ sở cho nhiều hiện tượng vật lý quan trọng, như quang phổ hấp thụ và phát xạ của các nguyên tố, cũng như là nguyên lý hoạt động của các thiết bị quang học và điện tử, bao gồm laser và đèn LED.
Hiểu rõ về sự chuyển dịch giữa các mức năng lượng giúp chúng ta nắm bắt được cách các nguyên tử và phân tử tương tác với ánh sáng và năng lượng, từ đó mở ra các ứng dụng thực tiễn trong khoa học và công nghệ.
Ứng Dụng Thực Tế Của Mức Năng Lượng Electron
Mức năng lượng electron đóng vai trò quan trọng trong nhiều ứng dụng công nghệ và khoa học hiện đại. Sự hiểu biết về các mức năng lượng này không chỉ giúp giải thích các hiện tượng vật lý mà còn tạo nền tảng cho sự phát triển của nhiều lĩnh vực công nghệ tiên tiến.
- Quang Phổ và Phân Tích Thành Phần: Sự chuyển dịch giữa các mức năng lượng của electron là cơ sở cho các kỹ thuật quang phổ học. Quang phổ hấp thụ và phát xạ của các nguyên tử và phân tử được sử dụng để xác định thành phần hóa học của các chất. Điều này rất hữu ích trong nhiều ngành công nghiệp, từ hóa học phân tích đến thiên văn học, nơi mà quang phổ của ánh sáng từ các ngôi sao và hành tinh có thể tiết lộ thành phần của chúng.
- Pin Mặt Trời: Hiệu ứng quang điện, nơi mà ánh sáng kích thích electron từ mức năng lượng thấp lên mức năng lượng cao hơn, là nguyên lý hoạt động của pin mặt trời. Khi các electron này di chuyển qua chất bán dẫn, chúng tạo ra dòng điện, cung cấp năng lượng tái tạo và thân thiện với môi trường.
- Vật Liệu Bán Dẫn: Các mức năng lượng electron trong chất bán dẫn quyết định cách chúng dẫn điện. Sự điều chỉnh các mức năng lượng này, thông qua quá trình pha tạp (doping) hoặc bằng cách tạo ra các cấu trúc bán dẫn đặc biệt như điốt hoặc transistor, là cơ sở cho toàn bộ ngành công nghiệp điện tử hiện đại. Các thiết bị như vi xử lý, bộ nhớ và các cảm biến đều hoạt động dựa trên nguyên lý này.
- Laser: Công nghệ laser hoạt động dựa trên nguyên lý phát xạ kích thích, trong đó electron trong các nguyên tử hoặc phân tử được kích thích để phát ra ánh sáng đồng pha. Các laser có ứng dụng rộng rãi trong y học, viễn thông, và công nghệ quân sự, nhờ khả năng tạo ra chùm sáng mạnh và chính xác.
- Đèn LED: Đèn LED (Light Emitting Diode) phát sáng khi electron chuyển từ mức năng lượng cao về mức năng lượng thấp trong một chất bán dẫn, phát ra ánh sáng. Đèn LED đã cách mạng hóa ngành công nghiệp chiếu sáng nhờ hiệu suất cao và tuổi thọ dài, đồng thời cũng được sử dụng rộng rãi trong các thiết bị hiển thị và công nghệ thông tin.
Những ứng dụng thực tế của mức năng lượng electron đã và đang góp phần thúc đẩy sự phát triển của nhiều lĩnh vực công nghệ và khoa học. Từ năng lượng tái tạo đến công nghệ thông tin, sự hiểu biết sâu sắc về các mức năng lượng electron mang lại nhiều lợi ích to lớn cho cuộc sống hiện đại.

Kết Luận Về Mức Năng Lượng Electron
Mức năng lượng electron là một khái niệm quan trọng và cốt lõi trong vật lý lượng tử, đóng vai trò quan trọng trong việc hiểu cấu trúc và tính chất của nguyên tử và phân tử. Qua việc phân tích và nghiên cứu các mức năng lượng này, chúng ta có thể giải thích được nhiều hiện tượng khoa học và ứng dụng chúng trong nhiều lĩnh vực khác nhau như quang phổ học, công nghệ bán dẫn, và năng lượng tái tạo.
Việc nắm bắt được cách thức các electron chuyển dịch giữa các mức năng lượng khác nhau giúp chúng ta hiểu sâu hơn về bản chất của vật chất, cũng như phát triển các công nghệ tiên tiến như laser, đèn LED, và pin mặt trời. Những ứng dụng này không chỉ nâng cao chất lượng cuộc sống mà còn góp phần vào sự phát triển bền vững của nhân loại.
Nhìn chung, nghiên cứu về mức năng lượng electron mở ra những cơ hội lớn trong khoa học và công nghệ, cung cấp nền tảng vững chắc cho các tiến bộ trong tương lai. Đây là một minh chứng cho thấy tầm quan trọng của việc hiểu biết về cơ cấu vi mô của vật chất, từ đó áp dụng vào thực tiễn để tạo ra những giá trị to lớn cho xã hội.