Chủ đề electron bằng proton: Electron và proton là hai thành phần cơ bản tạo nên nguyên tử. Bài viết này sẽ giúp bạn hiểu rõ hơn về mối quan hệ giữa electron và proton, cũng như tầm quan trọng của chúng trong cấu trúc và phản ứng hóa học của vật chất.
Mục lục
- Thông tin về Electron và Proton
- 1. Giới thiệu về Electron và Proton
- 2. Khối lượng và Điện tích của Electron và Proton
- 3. Cấu trúc Nguyên tử và Sự cân bằng giữa Electron và Proton
- 4. Ứng dụng của Electron và Proton trong cuộc sống
- 5. Vai trò của Proton và Electron trong Phản ứng Hóa học
- 6. Những Khám phá và Nghiên cứu nổi bật về Proton và Electron
Thông tin về Electron và Proton
Electron và proton là hai hạt cơ bản cấu tạo nên nguyên tử, với những đặc điểm quan trọng như sau:
1. Cấu tạo của nguyên tử
Một nguyên tử bao gồm hạt nhân ở trung tâm và các electron chuyển động xung quanh. Hạt nhân được cấu thành từ các proton (mang điện tích dương) và neutron (không mang điện tích), trong khi các electron mang điện tích âm chuyển động quanh hạt nhân.
2. Khối lượng và điện tích của Proton và Electron
| Hạt | Ký hiệu | Khối lượng | Điện tích |
|---|---|---|---|
| Proton | \(p\) | \(1,6726 \times 10^{-27}\) kg \(\approx 1\)u | +1,602 \times 10^{-19}\) C |
| Electron | \(e\) | \(9,1094 \times 10^{-31}\) kg | -1,602 \times 10^{-19}\) C |
3. Tương quan giữa Electron và Proton
Trong một nguyên tử trung hòa về điện, số lượng proton trong hạt nhân bằng với số lượng electron quay quanh hạt nhân. Do đó, tổng điện tích dương của các proton cân bằng với tổng điện tích âm của các electron.
4. Vai trò của Electron và Proton trong nguyên tử
Proton xác định tính chất hóa học của nguyên tố (số nguyên tử), trong khi electron tham gia vào các liên kết hóa học, quyết định tính chất hóa học và vật lý của nguyên tử. Khối lượng của proton lớn hơn nhiều so với electron, nhưng electron lại đóng vai trò quan trọng trong các phản ứng hóa học và tương tác với các nguyên tử khác.
5. Các ứng dụng của Proton và Electron
- Proton: Được sử dụng trong các máy gia tốc hạt và nghiên cứu vật lý hạt nhân.
- Electron: Đóng vai trò quan trọng trong các thiết bị điện tử như bóng bán dẫn, màn hình CRT và trong các phản ứng hóa học.
Với những đặc điểm nổi bật trên, electron và proton không chỉ là các thành phần cơ bản của vật chất mà còn là đối tượng nghiên cứu quan trọng trong khoa học hiện đại.

1. Giới thiệu về Electron và Proton
Electron và proton là hai hạt cơ bản cấu thành nên nguyên tử, đại diện cho hai loại điện tích khác nhau. Electron mang điện tích âm \((-1)\), trong khi proton mang điện tích dương \((+1)\). Hai hạt này tương tác với nhau thông qua lực điện từ, giữ nguyên tử ở trạng thái ổn định.
Proton được tìm thấy trong hạt nhân của nguyên tử và có khối lượng lớn hơn electron khoảng 1836 lần. Trái lại, electron có khối lượng rất nhỏ và di chuyển xung quanh hạt nhân trong các quỹ đạo xác định, tạo nên các lớp vỏ electron.
Về mặt hóa học, số lượng proton trong hạt nhân xác định nguyên tố của nguyên tử, trong khi số lượng electron quyết định tính chất hóa học và khả năng tham gia phản ứng của nguyên tử đó. Sự cân bằng giữa số lượng electron và proton trong nguyên tử là yếu tố quan trọng để duy trì tính trung hòa điện của nguyên tử.
Vì vậy, hiểu rõ về electron và proton không chỉ giúp chúng ta nắm bắt được cấu trúc của vật chất mà còn hiểu được cách thức các nguyên tử tương tác và liên kết với nhau để tạo ra các phân tử phức tạp hơn.
2. Khối lượng và Điện tích của Electron và Proton
Electron và proton, dù cùng tồn tại trong cấu trúc nguyên tử, lại có những đặc điểm khác biệt rõ rệt về khối lượng và điện tích.
- Khối lượng của Electron: Electron là một hạt hạ nguyên tử có khối lượng rất nhỏ, chỉ khoảng \[9.109 \times 10^{-31}\] kg. Khối lượng này thường được coi là không đáng kể so với các hạt khác trong nguyên tử, như proton hoặc neutron.
- Khối lượng của Proton: Proton nặng hơn electron rất nhiều, với khối lượng khoảng \[1.672 \times 10^{-27}\] kg. Khối lượng của proton tương đương với khoảng 1 đơn vị khối lượng nguyên tử (u), và gấp khoảng 1836 lần khối lượng của electron.
- Điện tích của Electron: Electron mang điện tích âm với giá trị \(-1.602 \times 10^{-19}\) coulomb. Điện tích này là đơn vị cơ bản của điện tích âm trong tự nhiên.
- Điện tích của Proton: Proton mang điện tích dương với giá trị tương tự \(+1.602 \times 10^{-19}\) coulomb. Đây là đơn vị điện tích dương cơ bản, cân bằng hoàn toàn với điện tích của electron.
Sự khác biệt về khối lượng và điện tích giữa electron và proton là yếu tố quan trọng trong việc hình thành và duy trì cấu trúc của nguyên tử. Khối lượng lớn của proton đóng vai trò quan trọng trong việc xác định khối lượng của nguyên tử, trong khi điện tích của electron quyết định tính chất hóa học và khả năng liên kết của nguyên tử đó.

3. Cấu trúc Nguyên tử và Sự cân bằng giữa Electron và Proton
Nguyên tử là đơn vị cơ bản của vật chất, bao gồm một hạt nhân trung tâm chứa các proton và neutron, xung quanh là các electron chuyển động trong các quỹ đạo. Hạt nhân nguyên tử có kích thước rất nhỏ nhưng chứa gần như toàn bộ khối lượng của nguyên tử nhờ vào các proton và neutron.
Proton, mang điện tích dương, nằm trong hạt nhân và chịu trách nhiệm xác định số hiệu nguyên tử của nguyên tố. Electron, mang điện tích âm, di chuyển xung quanh hạt nhân trong các lớp vỏ electron. Số lượng electron trong một nguyên tử thường bằng số lượng proton, tạo nên sự cân bằng về điện tích, khiến nguyên tử trở nên trung hòa về điện.
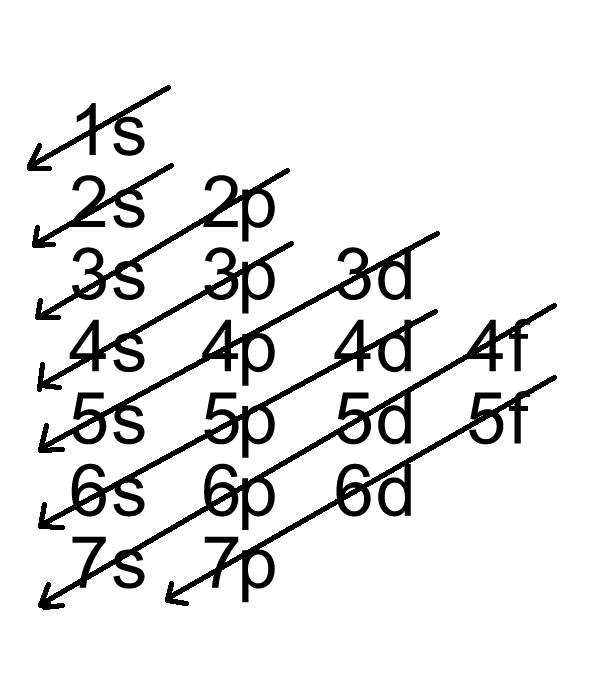
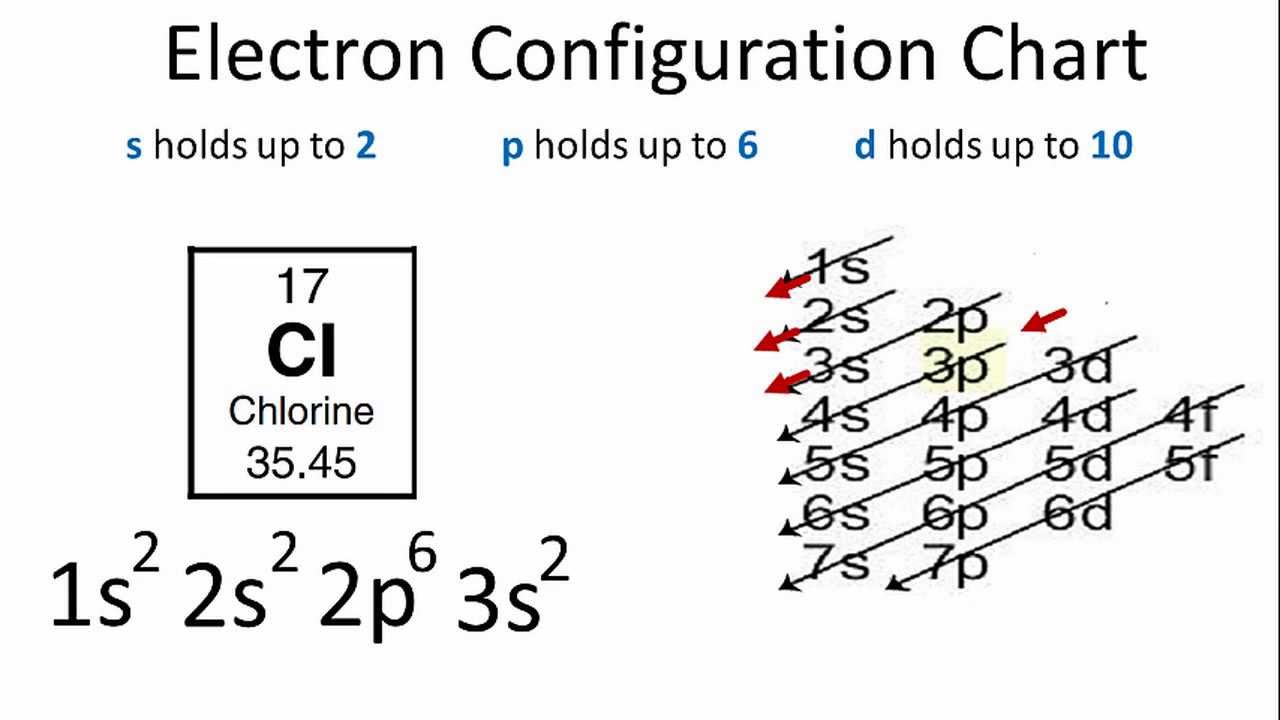
Các electron được sắp xếp trong các lớp vỏ khác nhau dựa trên mức năng lượng của chúng. Lớp vỏ gần hạt nhân nhất có mức năng lượng thấp nhất, và các electron có xu hướng lấp đầy các lớp vỏ này theo thứ tự tăng dần. Sự sắp xếp này đóng vai trò quan trọng trong việc xác định tính chất hóa học của nguyên tố.
Sự cân bằng giữa số lượng proton và electron là điều kiện cần để nguyên tử tồn tại ở trạng thái ổn định. Nếu một nguyên tử mất đi hoặc nhận thêm electron, nó sẽ trở thành một ion, với điện tích dương (cation) nếu mất electron và điện tích âm (anion) nếu nhận thêm electron. Các ion này có vai trò quan trọng trong các phản ứng hóa học và các hiện tượng vật lý khác nhau.

4. Ứng dụng của Electron và Proton trong cuộc sống
Electron và proton, ngoài vai trò cấu thành nguyên tử, còn có những ứng dụng rộng rãi trong nhiều lĩnh vực khác nhau của cuộc sống, từ công nghệ, y học đến khoa học vật liệu.
- Ứng dụng của Electron:
- Thiết bị điện tử: Electron đóng vai trò chính trong các mạch điện và các thiết bị điện tử. Các dòng điện trong dây dẫn thực chất là dòng chuyển động của các electron. Nhờ sự chuyển động này, các thiết bị như máy tính, điện thoại, và vô số các thiết bị công nghệ khác có thể hoạt động.
- Chụp ảnh điện tử: Kỹ thuật hiển vi điện tử sử dụng electron thay vì ánh sáng để tạo ra các hình ảnh có độ phân giải cực cao, giúp quan sát cấu trúc tế bào và các vật thể siêu nhỏ khác với chi tiết tinh vi.
- Truyền tải thông tin: Các electron trong các dây dẫn quang học và cáp truyền thông chịu trách nhiệm cho việc truyền tải dữ liệu trên các mạng lưới viễn thông, đảm bảo sự liên lạc và kết nối toàn cầu.
- Ứng dụng của Proton:
- Y học: Proton được sử dụng trong xạ trị proton, một phương pháp điều trị ung thư hiệu quả nhờ khả năng nhắm chính xác vào các khối u mà không gây tổn hại nhiều đến các mô xung quanh. Phương pháp này được xem là tiên tiến hơn so với xạ trị bằng tia X truyền thống.
- Máy gia tốc hạt: Proton được sử dụng trong các máy gia tốc hạt như máy gia tốc Large Hadron Collider (LHC) để nghiên cứu cấu trúc hạt nhân và các hiện tượng vật lý cơ bản, giúp con người hiểu rõ hơn về vũ trụ và các hạt cơ bản.
- Nghiên cứu vật liệu: Proton được sử dụng trong các kỹ thuật như phân tán proton để nghiên cứu và phân tích các vật liệu, giúp cải tiến và phát triển các vật liệu mới với tính năng vượt trội.
Các ứng dụng của electron và proton không chỉ giới hạn trong các lĩnh vực trên mà còn mở ra nhiều tiềm năng phát triển trong tương lai, đặc biệt trong việc giải quyết các thách thức về công nghệ và y tế.

5. Vai trò của Proton và Electron trong Phản ứng Hóa học
Trong các phản ứng hóa học, proton và electron đóng vai trò trung tâm trong việc thay đổi cấu trúc và tính chất của các nguyên tử và phân tử tham gia. Cả hai hạt này đều liên quan chặt chẽ đến các quá trình oxi hóa - khử, sự tạo thành liên kết hóa học, và sự thay đổi năng lượng trong các phản ứng.
- Vai trò của Proton:
- Phản ứng Axit - Bazơ: Trong các phản ứng axit-bazơ, proton (\(H^+\)) là thành phần chính. Axit là chất có khả năng cho proton, trong khi bazơ là chất có khả năng nhận proton. Quá trình trao đổi proton này là cơ sở của nhiều phản ứng trong hóa học hữu cơ và vô cơ.
- Tạo thành các Liên kết: Proton trong hạt nhân nguyên tử đóng vai trò quyết định trong việc tạo thành các liên kết hóa học giữa các nguyên tử. Số lượng proton xác định khả năng của một nguyên tử trong việc thu hút và giữ các electron, từ đó ảnh hưởng đến việc hình thành các liên kết cộng hóa trị hoặc ion.
- Vai trò của Electron:
- Phản ứng Oxi hóa - Khử: Trong phản ứng oxi hóa - khử, sự chuyển dời electron giữa các nguyên tử và phân tử dẫn đến sự thay đổi trạng thái oxi hóa của các nguyên tố. Nguyên tử hoặc phân tử nhận electron sẽ bị khử, trong khi nguyên tử hoặc phân tử mất electron sẽ bị oxi hóa.
- Liên kết Hóa học: Electron nằm ở lớp vỏ ngoài của nguyên tử và tham gia vào việc tạo thành các liên kết hóa học. Sự chia sẻ hoặc chuyển giao electron giữa các nguyên tử dẫn đến việc hình thành các liên kết cộng hóa trị hoặc ion, giữ các nguyên tử lại với nhau để tạo thành phân tử.
- Định hình Phân tử: Sự sắp xếp của electron trong các quỹ đạo của nguyên tử quyết định hình dạng của phân tử. Các mô hình phân tử như thuyết VSEPR (Valence Shell Electron Pair Repulsion) giúp dự đoán hình dạng phân tử dựa trên sự đẩy giữa các cặp electron trong lớp vỏ ngoài cùng của nguyên tử.
Nhờ vào vai trò quan trọng của proton và electron trong phản ứng hóa học, chúng ta có thể hiểu rõ hơn về cách thức các chất tương tác và biến đổi trong tự nhiên, cũng như ứng dụng những hiểu biết này vào các lĩnh vực như hóa học, y học, và vật liệu học.
XEM THÊM:
6. Những Khám phá và Nghiên cứu nổi bật về Proton và Electron
Trong hành trình khám phá thế giới vi mô, proton và electron đã trở thành những hạt cơ bản không thể thiếu trong việc hiểu biết về cấu trúc nguyên tử và các hiện tượng vật lý. Dưới đây là một số cột mốc quan trọng trong lịch sử khám phá và nghiên cứu về hai hạt này:
6.1 Lịch sử khám phá Proton
Proton được phát hiện bởi nhà vật lý người Anh, Ernest Rutherford, vào năm 1917 trong một loạt các thí nghiệm bắn phá hạt nhân nitơ bằng hạt alpha. Đây là lần đầu tiên một nguyên tử khác ngoài hydro bị phân rã nhân tạo. Rutherford nhận ra rằng các hạt thu được sau thí nghiệm là hạt nhân của nguyên tử hydro và từ đó, ông đặt tên chúng là "proton", từ tiếng Hy Lạp "protos", có nghĩa là "đầu tiên". Proton sau đó được xác định là thành phần cơ bản của hạt nhân nguyên tử, đóng vai trò chính trong việc xác định tính chất hóa học của các nguyên tử.
6.2 Lịch sử khám phá Electron
Electron là hạt mang điện tích âm đầu tiên được phát hiện vào năm 1897 bởi J.J. Thomson, một nhà vật lý người Anh. Thí nghiệm của ông với ống tia âm cực đã dẫn đến việc phát hiện ra electron, khi ông nhận thấy các tia phát ra từ ống có khả năng bị lệch trong điện trường, cho thấy chúng mang điện tích âm. Khám phá này đã mở ra một kỷ nguyên mới trong lĩnh vực vật lý, làm thay đổi cách chúng ta hiểu về cấu trúc của nguyên tử và sự tương tác giữa các hạt cơ bản.
Trong những năm sau đó, các nghiên cứu về proton và electron đã tiếp tục phát triển mạnh mẽ. Điển hình là việc xác định khối lượng và điện tích của các hạt này với độ chính xác cao, đóng góp vào sự phát triển của mô hình nguyên tử hiện đại và các lý thuyết vật lý về tương tác cơ bản. Các ứng dụng của những khám phá này đã có tác động to lớn đến nhiều lĩnh vực, từ công nghệ điện tử đến y học, góp phần nâng cao chất lượng cuộc sống của con người.