Chủ đề hf có phân cực không: HF có phân cực không? Đây là câu hỏi phổ biến trong hóa học khi xét đến tính chất của phân tử hydrofluoride. Trong bài viết này, chúng ta sẽ cùng khám phá cấu trúc phân tử, tính phân cực và những ứng dụng quan trọng của HF trong đời sống hàng ngày và công nghiệp.
Mục lục
HF Có Phân Cực Không?
Hydrofluoric acid (HF) là một hợp chất có chứa liên kết giữa nguyên tử hydro (H) và nguyên tử fluorine (F). Để hiểu rõ hơn về tính phân cực của HF, chúng ta cần phân tích các yếu tố quan trọng như độ âm điện và cấu trúc phân tử.
1. Độ Âm Điện
Fluorine (F) là nguyên tố có độ âm điện cao nhất trong bảng tuần hoàn, với giá trị khoảng 3.98 theo thang độ âm điện của Pauling. Ngược lại, độ âm điện của hydro (H) chỉ vào khoảng 2.20. Do sự chênh lệch đáng kể về độ âm điện này, liên kết giữa H và F là một liên kết cộng hóa trị phân cực, trong đó các electron liên kết bị hút về phía fluorine, tạo ra một momen lưỡng cực lớn.
2. Cấu Trúc Phân Tử
Phân tử HF có cấu trúc tuyến tính với chỉ một liên kết H-F. Điều này có nghĩa là momen lưỡng cực không bị triệt tiêu bởi bất kỳ yếu tố nào khác và toàn bộ phân tử trở nên phân cực.
3. Kết Luận
Vì sự chênh lệch lớn về độ âm điện giữa H và F cùng với cấu trúc phân tử đơn giản, HF là một phân tử phân cực. Momen lưỡng cực của nó được xác định bằng công thức:
\[
\mu = Q \times r
\]
trong đó:
- \(\mu\): Momen lưỡng cực
- Q: Điện tích
- r: Khoảng cách giữa các tâm điện tích dương và âm
4. Ứng Dụng Và Tính Chất
Nhờ vào tính phân cực, HF dễ dàng hòa tan trong nước, tạo thành dung dịch acid mạnh. Tuy nhiên, HF là một acid yếu so với các hydrohalic acid khác (như HCl, HBr, HI) vì liên kết H-F rất bền vững, dẫn đến khả năng phân ly thấp hơn trong dung dịch.
5. Bảng Tóm Tắt
| Yếu tố | Mô tả |
|---|---|
| Độ âm điện của H | 2.20 |
| Độ âm điện của F | 3.98 |
| Momen lưỡng cực của HF | Có, phân tử phân cực |
| Tính hòa tan trong nước | Dễ tan |
| Loại acid | Acid yếu |
Với những phân tích trên, có thể khẳng định rằng HF là một phân tử phân cực với nhiều ứng dụng quan trọng trong công nghiệp và nghiên cứu hóa học.
Mục Lục Tổng Hợp Về Tính Phân Cực Của HF
Tính phân cực của HF (Hydrofluoride) là một chủ đề quan trọng trong hóa học vì ảnh hưởng của nó đến nhiều tính chất vật lý và hóa học của phân tử. Dưới đây là một mục lục tổng hợp về các khía cạnh khác nhau liên quan đến tính phân cực của HF:
- 1. Tính Phân Cực Của HF Là Gì?
- 2. Cấu Trúc Phân Tử HF Và Độ Âm Điện
- 3. Ứng Dụng Thực Tế Của HF Dựa Trên Tính Phân Cực
- 4. So Sánh Tính Phân Cực Của HF Với Các Hydrohalide Khác
- 5. Tác Động Của Tính Phân Cực Đến Tính Chất Hóa Lý Của HF
- 6. Phân Tích Momen Lưỡng Cực Của HF
- 7. Tính Acid Của HF Và Sự Ảnh Hưởng Của Phân Cực
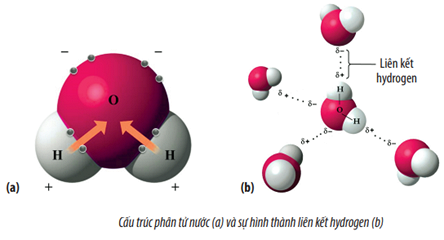
- 8. Liên Kết Hydro Trong HF
- 9. Sự Phân Bố Điện Tích Trong Phân Tử HF
- 10. Thực Hành Tính Toán Và Thí Nghiệm Với HF
Phân tích và giải thích về khái niệm tính phân cực, lý do vì sao HF là một phân tử phân cực, bao gồm cách tính toán momen lưỡng cực \(\mu\).
Phân tích cấu trúc phân tử HF, đặc biệt là sự khác biệt về độ âm điện giữa nguyên tử H và F, dẫn đến sự phân bố không đều của mật độ electron.
Khám phá cách tính phân cực của HF được ứng dụng trong các ngành công nghiệp như khắc kính và xử lý bề mặt.
Sự khác biệt về tính phân cực giữa HF và các hợp chất tương tự như HCl, HBr, và HI, từ đó đánh giá độ mạnh yếu của liên kết hydrogen.
Ảnh hưởng của tính phân cực đến nhiệt độ sôi, độ tan trong nước và khả năng dẫn điện của HF.
Cách tính toán và ứng dụng momen lưỡng cực của HF trong các bài toán hóa học, đặc biệt là trong các phản ứng acid-base.
Cách tính phân cực tác động đến tính acid của HF, so sánh với các acid khác trong nhóm halide.
Giải thích về liên kết hydro trong HF và cách nó đóng góp vào độ mạnh của liên kết cũng như các tính chất hóa học khác của phân tử.
Phân tích sự phân bố điện tích trong HF dựa trên mô hình phân tử, ảnh hưởng đến tính chất điện tử của phân tử.
Các bài tập và thí nghiệm liên quan đến tính phân cực của HF, bao gồm tính toán momen lưỡng cực và các phép đo thực tế trong phòng thí nghiệm.
10 Dạng Bài Tập Có Lời Giải Hoàn Chỉnh Về Tính Phân Cực Của HF
-
Bài tập 1: Tính momen lưỡng cực của phân tử HF
Giải thích cách tính toán momen lưỡng cực \(\mu\) của HF dựa trên độ âm điện của H và F. Sử dụng công thức: \(\mu = q \times d\), trong đó \(q\) là điện tích và \(d\) là khoảng cách giữa các hạt nhân.
-
Bài tập 2: So sánh tính phân cực của HF với HCl
So sánh tính phân cực của HF và HCl bằng cách phân tích độ âm điện của các nguyên tử liên kết và momen lưỡng cực của các phân tử.
-
Bài tập 3: Phân tích cấu trúc phân tử HF bằng lý thuyết VSEPR
Áp dụng lý thuyết đẩy cặp electron vùng hóa trị (VSEPR) để mô tả hình học và tính phân cực của HF.
-
Bài tập 4: Ảnh hưởng của tính phân cực đến nhiệt độ sôi của HF
Giải thích tại sao tính phân cực của HF lại ảnh hưởng đến nhiệt độ sôi của nó so với các hợp chất cùng nhóm.
-
Bài tập 5: Liên kết hydrogen trong HF và các hợp chất tương tự
Phân tích cách liên kết hydrogen trong HF ảnh hưởng đến tính chất phân cực và đặc điểm hóa học của phân tử.
-
Bài tập 6: Tính phân cực và độ tan của HF trong nước
Giải thích mối quan hệ giữa tính phân cực của HF và khả năng tan của nó trong nước. Dự đoán độ tan của HF dựa trên phân tích phân cực.
-
Bài tập 7: Mô phỏng phân tử HF bằng phần mềm hóa học
Thực hành sử dụng phần mềm mô phỏng phân tử để xem sự phân bố mật độ electron và tính phân cực của HF.
-
Bài tập 8: Xác định độ phân cực của HF trong trạng thái khí
Sử dụng dữ liệu thực nghiệm để tính toán và so sánh độ phân cực của HF trong trạng thái khí so với khi ở trong dung dịch.
-
Bài tập 9: Ứng dụng của tính phân cực HF trong công nghiệp
Phân tích ứng dụng thực tiễn của tính phân cực của HF trong các quy trình công nghiệp như sản xuất và xử lý hóa chất.
-
Bài tập 10: Tính toán năng lượng liên kết trong phân tử HF
Sử dụng dữ liệu về độ phân cực để tính toán năng lượng liên kết trong phân tử HF và so sánh với các hợp chất halogen khác.