Chủ đề que es un electron en quimica: Electron là một trong những hạt cơ bản của nguyên tử, đóng vai trò quan trọng trong hóa học và vật lý. Bài viết này sẽ giúp bạn khám phá chi tiết về khái niệm, vai trò và ứng dụng của electron trong các phản ứng hóa học, cũng như các hiện tượng vật lý. Hãy cùng tìm hiểu sâu hơn về thế giới vi mô này!
Mục lục
Electron trong Hóa học
Electron là một hạt hạ nguyên tử có điện tích âm, tồn tại trong tất cả các nguyên tử và là một phần cơ bản trong cấu trúc của vật chất. Dưới đây là những thông tin chi tiết về electron trong hóa học:
1. Cấu tạo và thuộc tính của Electron
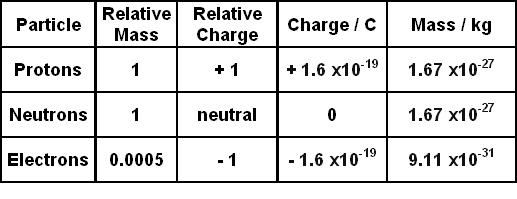
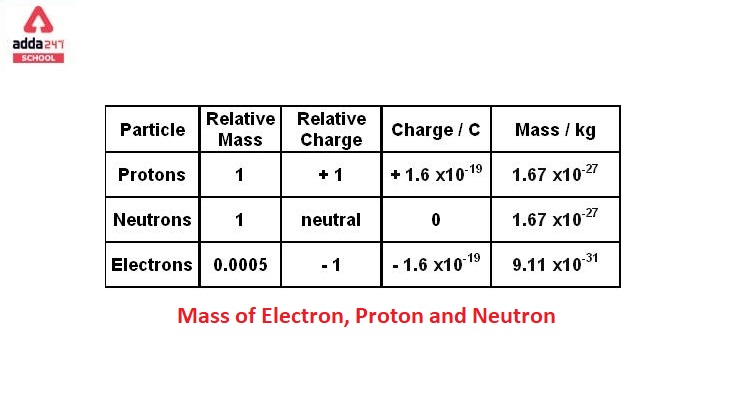
Electron có khối lượng rất nhỏ so với proton và neutron, khoảng \(9.109 \times 10^{-31}\) kg. Nó có điện tích âm đơn vị \(1.602 \times 10^{-19}\) coulombs. Các electron di chuyển xung quanh hạt nhân trong các quỹ đạo hoặc mức năng lượng nhất định, được sắp xếp thành các lớp và phân lớp.
- Phân lớp s: Chứa tối đa 2 electron.
- Phân lớp p: Chứa tối đa 6 electron.
- Phân lớp d: Chứa tối đa 10 electron.
- Phân lớp f: Chứa tối đa 14 electron.
2. Vai trò của Electron trong phản ứng hóa học
Electron đóng vai trò quan trọng trong các phản ứng hóa học. Các phản ứng này thường liên quan đến sự chuyển động của electron giữa các nguyên tử, làm thay đổi cấu hình electron và hình thành các liên kết hóa học.
Khi các nguyên tử tham gia phản ứng, chúng có thể:
- Nhường electron: Nguyên tử kim loại thường nhường electron để trở thành ion dương.
- Nhận electron: Nguyên tử phi kim thường nhận electron để trở thành ion âm.
3. Thuyết Electron
Thuyết electron giải thích các hiện tượng điện dựa trên sự di chuyển của electron:
- Khi một nguyên tử mất electron, nó trở thành ion dương.
- Khi một nguyên tử nhận thêm electron, nó trở thành ion âm.
- Vật chất dẫn điện chứa các electron tự do có thể di chuyển dễ dàng trong cấu trúc của chúng.
4. Ứng dụng của Electron trong Hóa học và Vật lý
Electron không chỉ quan trọng trong hóa học mà còn trong vật lý, đặc biệt là trong các ứng dụng liên quan đến điện và điện tử. Ví dụ, dòng điện trong các dây dẫn là dòng chảy của các electron. Electron cũng là yếu tố chính trong việc hình thành các liên kết hóa học giữa các nguyên tử, quyết định tính chất hóa học của các nguyên tố và hợp chất.
Cấu hình electron của một nguyên tố xác định vị trí của nó trong bảng tuần hoàn, và do đó, xác định tính chất hóa học và vật lý của nguyên tố đó.
Kết luận
Electron là thành phần cơ bản và cực kỳ quan trọng trong hóa học và vật lý, quyết định nhiều tính chất của vật chất và các hiện tượng điện từ. Hiểu biết về electron giúp chúng ta nắm bắt được bản chất của các phản ứng hóa học và tính chất của các nguyên tố trong bảng tuần hoàn.

Mục lục Tổng Hợp
Dưới đây là mục lục tổng hợp về chủ đề "Electron trong hóa học", được xây dựng từ việc tham khảo các kết quả tìm kiếm chi tiết. Mục lục này giúp người đọc dễ dàng tiếp cận và hiểu rõ hơn về vai trò, cấu trúc và ứng dụng của electron trong các phản ứng hóa học và hiện tượng vật lý.
- 1. Khái niệm Electron:
1.1. Electron là gì?
1.2. Vai trò của Electron trong nguyên tử
- 2. Cấu trúc của Electron:
2.1. Đặc điểm và tính chất của Electron
2.2. Phân lớp và quỹ đạo Electron trong nguyên tử
2.3. Sự phân bố Electron trong các nguyên tố
- 3. Vai trò của Electron trong các phản ứng hóa học:
3.1. Liên kết hóa học và sự tham gia của Electron
3.2. Electron và phản ứng oxi hóa - khử
3.3. Ảnh hưởng của cấu hình Electron đến tính chất hóa học của nguyên tố
- 4. Thuyết Electron và ứng dụng:
4.1. Thuyết Electron trong vật lý hiện đại
4.2. Vai trò của Electron trong công nghệ và đời sống
4.3. Electron trong các thiết bị điện tử và công nghệ bán dẫn
- 5. Kết luận:
5.1. Tầm quan trọng của Electron trong khoa học và đời sống
1. Electron là gì?
Electron là một trong ba loại hạt cơ bản cấu tạo nên nguyên tử, bên cạnh proton và neutron. Đây là hạt mang điện tích âm, được ký hiệu là \( e^- \), và có khối lượng rất nhỏ, khoảng \[9.109 \times 10^{-31}\] kg, chỉ bằng khoảng 1/1836 khối lượng của proton. Electron di chuyển xung quanh hạt nhân nguyên tử theo các quỹ đạo được xác định bởi năng lượng của chúng.
Vai trò của electron trong nguyên tử là cực kỳ quan trọng, bởi chúng quyết định đến tính chất hóa học của nguyên tố. Cấu hình electron – tức cách mà các electron được sắp xếp trong các lớp vỏ nguyên tử – là yếu tố quyết định đến khả năng phản ứng của một nguyên tố trong các phản ứng hóa học.
Trong khi proton xác định danh tính của nguyên tố, electron chịu trách nhiệm cho hầu hết các tính chất hóa học của nguyên tử, bao gồm khả năng tạo liên kết và phản ứng với các nguyên tử khác. Khi một nguyên tử mất hoặc nhận thêm electron, nó trở thành ion, một phần tử mang điện tích và có tính chất hóa học khác biệt so với nguyên tử trung hòa.
Các electron không chỉ quan trọng trong hóa học, mà còn có vai trò thiết yếu trong các hiện tượng vật lý, từ hiện tượng điện đến các ứng dụng trong công nghệ như điện tử, bán dẫn và truyền thông. Sự di chuyển của electron trong dây dẫn là cơ sở của dòng điện – một khái niệm nền tảng trong điện học.

2. Cấu trúc của electron trong nguyên tử
Electron trong nguyên tử không tồn tại tự do mà di chuyển xung quanh hạt nhân theo các quỹ đạo cụ thể, được gọi là các lớp vỏ electron hoặc lớp năng lượng. Các lớp vỏ này được sắp xếp theo mức năng lượng tăng dần, từ lớp gần hạt nhân nhất đến lớp xa nhất.
Mỗi lớp vỏ electron chứa một số lượng tối đa các electron, tuân theo nguyên tắc phân bố electron (nguyên lý Pauli) và quy tắc Hund. Số lượng electron tối đa trong một lớp vỏ được tính theo công thức \[2n^2\], với \(n\) là số thứ tự của lớp vỏ.
Ví dụ, lớp vỏ đầu tiên (n=1) có thể chứa tối đa \[2 \times 1^2 = 2\] electron, lớp vỏ thứ hai (n=2) chứa tối đa \[2 \times 2^2 = 8\] electron, và cứ thế tiếp tục. Electron trong cùng một lớp vỏ có cùng mức năng lượng, nhưng có thể chiếm các quỹ đạo khác nhau trong lớp đó.
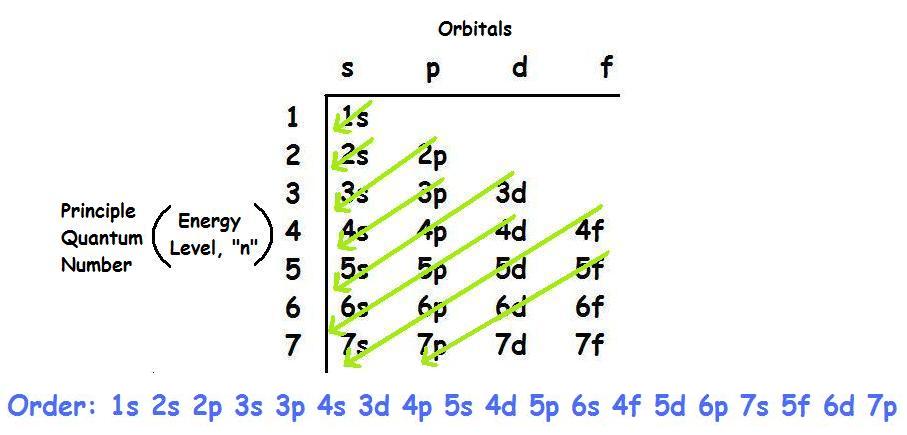
Cấu trúc của electron trong nguyên tử cũng tuân theo quy tắc cấu hình electron, theo đó các electron sẽ lấp đầy các lớp vỏ theo thứ tự mức năng lượng từ thấp đến cao. Điều này ảnh hưởng trực tiếp đến tính chất hóa học của nguyên tố, bởi các electron ở lớp vỏ ngoài cùng (còn gọi là electron hóa trị) là những hạt tham gia vào các liên kết hóa học.
Trong một số nguyên tử, các lớp vỏ electron có thể bị chia nhỏ thành các phân lớp, mỗi phân lớp chứa các quỹ đạo với hình dạng khác nhau (s, p, d, f) và mức năng lượng khác nhau. Sự phân bố và cấu trúc của các electron trong các phân lớp này quyết định các đặc tính quang học, từ tính và hóa học của nguyên tố.

3. Vai trò của electron trong các phản ứng hóa học
Electron đóng vai trò then chốt trong các phản ứng hóa học, vì chúng là những hạt chủ yếu tham gia vào quá trình hình thành và phá vỡ các liên kết hóa học giữa các nguyên tử. Trong các phản ứng hóa học, các nguyên tử trao đổi hoặc chia sẻ electron để đạt được cấu hình electron bền vững hơn, thường là cấu hình giống với cấu hình của các khí hiếm.
Các loại liên kết hóa học chính gồm liên kết ion và liên kết cộng hóa trị. Trong liên kết ion, một nguyên tử nhường electron cho nguyên tử khác, tạo ra các ion tích điện trái dấu, sau đó hút nhau bằng lực tĩnh điện. Ngược lại, trong liên kết cộng hóa trị, các nguyên tử chia sẻ một hoặc nhiều cặp electron để tạo thành liên kết giữa chúng.
Quá trình oxy hóa và khử cũng là một dạng phản ứng quan trọng, nơi electron được chuyển từ chất khử (chất nhường electron) sang chất oxy hóa (chất nhận electron). Quá trình này được thể hiện qua phương trình phản ứng oxy hóa - khử, trong đó sự mất hoặc nhận electron dẫn đến sự thay đổi hóa trị của các nguyên tử liên quan.
Ví dụ, trong phản ứng của natri (\(Na\)) với clo (\(Cl_2\)), natri nhường một electron để trở thành ion \(Na^+\), trong khi mỗi nguyên tử clo nhận một electron để trở thành ion \(Cl^-\). Hai ion này sau đó liên kết với nhau tạo thành natri clorua (\(NaCl\)), hay còn gọi là muối ăn.
Vai trò của electron trong các phản ứng hóa học không chỉ giới hạn ở việc hình thành liên kết mà còn ảnh hưởng đến năng lượng của phản ứng. Khi electron chuyển từ mức năng lượng cao xuống mức năng lượng thấp hơn, năng lượng sẽ được giải phóng dưới dạng nhiệt hoặc ánh sáng, như thấy trong các phản ứng cháy hoặc phản ứng quang hợp.

4. Thuyết electron và ứng dụng trong vật lý
Thuyết electron là một trong những nền tảng quan trọng của vật lý hiện đại. Theo thuyết này, electron là các hạt mang điện tích âm và di chuyển xung quanh hạt nhân nguyên tử theo các quỹ đạo xác định. Thuyết electron giải thích các hiện tượng vật lý liên quan đến điện tích, từ trường và các phản ứng hạt nhân.
Trong vật lý, thuyết electron được ứng dụng rộng rãi, đặc biệt trong việc giải thích cơ chế dẫn điện trong các vật liệu. Trong chất dẫn điện như kim loại, các electron tự do có thể di chuyển dễ dàng dưới tác động của điện trường, tạo ra dòng điện. Điều này là cơ sở của các thiết bị điện tử, từ bóng đèn, máy tính đến các thiết bị viễn thông hiện đại.
Các electron cũng đóng vai trò quan trọng trong hiện tượng quang điện, nơi ánh sáng chiếu vào một vật liệu làm bật các electron ra khỏi bề mặt. Hiện tượng này là nguyên lý hoạt động của các tế bào quang điện trong pin mặt trời, giúp chuyển đổi năng lượng ánh sáng thành điện năng.
Thuyết electron còn giải thích hiện tượng từ tính trong các vật liệu như sắt, nơi các electron tạo ra các moment từ, kết hợp lại để tạo thành từ trường tổng thể. Hiện tượng từ tính này là nền tảng cho các ứng dụng trong động cơ điện, máy phát điện, và các thiết bị lưu trữ dữ liệu như ổ cứng.
Trong lĩnh vực hạt nhân, thuyết electron giúp hiểu rõ về các phản ứng hạt nhân và sự phân rã phóng xạ, nơi các electron và các hạt khác tương tác ở mức năng lượng cao, dẫn đến sự biến đổi hạt nhân và phát ra năng lượng dưới dạng bức xạ.
XEM THÊM:
5. Ứng dụng của electron trong công nghệ và đời sống
5.1. Electron và công nghệ bán dẫn
Electron đóng vai trò quan trọng trong công nghệ bán dẫn, đặc biệt là trong việc tạo ra các thiết bị điện tử như transistor và diode. Trong các vật liệu bán dẫn, electron di chuyển tự do giữa các lớp vật liệu, cho phép các thiết bị này hoạt động như công tắc hoặc bộ khuếch đại tín hiệu. Các công nghệ này là cơ sở của mọi thiết bị điện tử hiện đại, từ máy tính, điện thoại di động đến các thiết bị gia dụng thông minh.
5.2. Vai trò của electron trong y học và khoa học vật liệu
Trong y học, electron được sử dụng trong các công nghệ hình ảnh y khoa, chẳng hạn như máy chụp cộng hưởng từ (MRI) và máy chụp cắt lớp phát xạ positron (PET). Các kỹ thuật này cho phép các bác sĩ quan sát chi tiết các cấu trúc bên trong cơ thể mà không cần phẫu thuật xâm lấn.
Trong khoa học vật liệu, electron đóng vai trò trong việc xác định tính chất của vật liệu. Ví dụ, kính hiển vi điện tử sử dụng electron để tạo ra hình ảnh có độ phân giải cao của các cấu trúc nhỏ hơn nhiều so với giới hạn của kính hiển vi quang học truyền thống.
5.3. Electron trong các thiết bị hàng ngày
Electron có vai trò quan trọng trong các thiết bị điện tử hàng ngày như TV, điện thoại di động, và máy tính. Những thiết bị này hoạt động dựa trên sự chuyển động của electron trong các mạch điện và các linh kiện như tụ điện và điện trở. Electron còn được sử dụng trong các màn hình hiển thị như màn hình LED và OLED, mang lại chất lượng hình ảnh sắc nét và tiêu thụ điện năng thấp.
Tầm quan trọng của electron trong công nghệ và đời sống
Electron không chỉ là thành phần cơ bản của vật chất mà còn là yếu tố chủ chốt trong sự phát triển của công nghệ và khoa học hiện đại. Từ công nghệ bán dẫn đến y học và khoa học vật liệu, electron giúp chúng ta hiểu sâu hơn về thế giới xung quanh và phát triển những ứng dụng mới, cải thiện chất lượng cuộc sống.