Chủ đề lawrencium electron configuration: Lawrencium, một nguyên tố hiếm trong bảng tuần hoàn, có cấu hình electron đặc biệt và phức tạp. Bài viết này sẽ đi sâu vào cấu hình electron của Lawrencium, khám phá các tính chất hóa học, và ứng dụng tiềm năng của nó trong nghiên cứu khoa học hiện đại.
Mục lục
Cấu Hình Electron Của Lawrencium
Lawrencium (ký hiệu hóa học là Lr) là nguyên tố cuối cùng trong nhóm Actinide, có số nguyên tử là 103. Cấu hình electron của Lawrencium đóng vai trò quan trọng trong việc hiểu rõ các đặc tính hóa học của nguyên tố này, đặc biệt là sự phân bố electron trong các orbital.
Cấu Hình Electron Cơ Bản
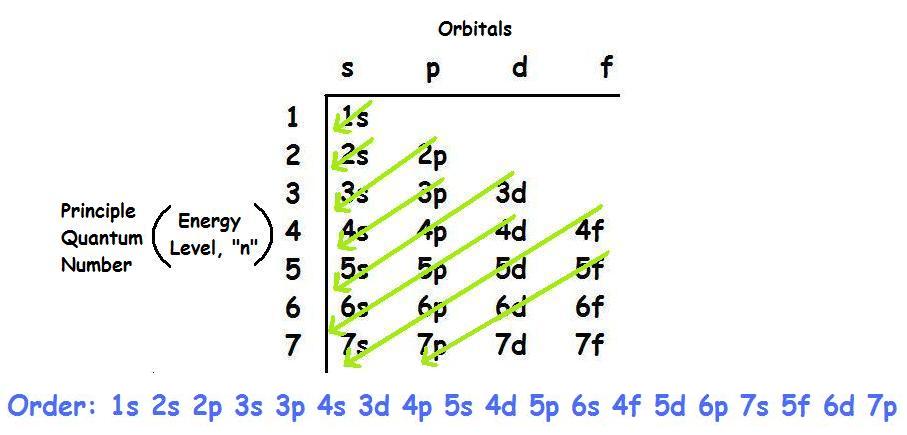
Cấu hình electron của Lawrencium được biểu diễn như sau:
\[\text{[Rn]} 5f^{14} 6d^{1} 7s^{2}\]
Trong đó, [Rn] đại diện cho cấu hình electron của nguyên tố radon (Z=86), 5f là các orbital f của lớp vỏ thứ năm, 6d là các orbital d của lớp vỏ thứ sáu, và 7s là orbital s của lớp vỏ thứ bảy.
Cấu Trúc Orbital
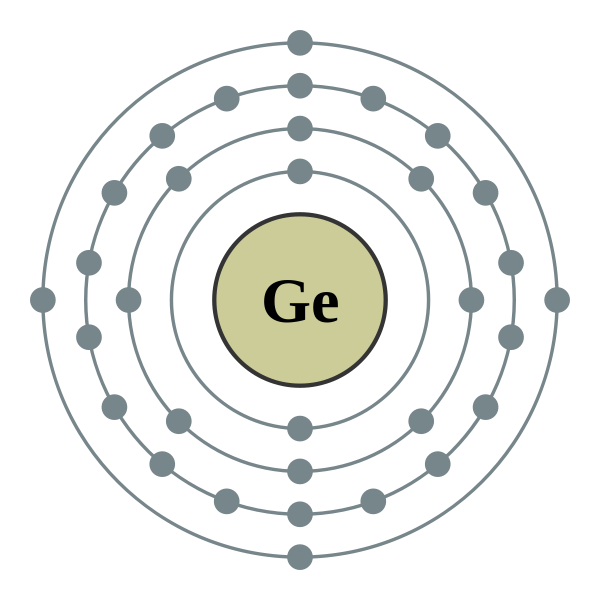
Các electron của Lawrencium phân bố theo các orbital như sau:
- Orbital 5f: chứa 14 electron, là orbital chứa đầy đủ electron, đặc trưng cho các nguyên tố Actinide.
- Orbital 6d: chỉ chứa 1 electron, tạo nên tính chất đặc biệt của Lawrencium trong nhóm Actinide.
- Orbital 7s: chứa 2 electron, tương tự như các nguyên tố khác trong nhóm này.
Tính Chất Hóa Học
Do cấu hình electron độc đáo, Lawrencium có một số tính chất hóa học đặc trưng:
- Lawrencium có thể dễ dàng mất các electron ở orbital 6d và 7s, dẫn đến việc hình thành ion Lr3+, đặc trưng cho các nguyên tố nhóm Actinide.
- Tính chất hóa học của Lawrencium cũng gần giống với các nguyên tố khác trong nhóm Actinide, như sự hình thành các hợp chất với trạng thái oxy hóa +3.
Ứng Dụng Của Lawrencium
Do tính phóng xạ cao và khó chế tạo, Lawrencium chủ yếu được sử dụng trong nghiên cứu khoa học để khám phá các đặc tính của các nguyên tố nặng và hành vi của electron trong các nguyên tố nhóm Actinide.
Kết Luận
Cấu hình electron của Lawrencium là một ví dụ tiêu biểu cho sự phức tạp của các nguyên tố nhóm Actinide. Việc hiểu rõ cấu hình electron của nguyên tố này giúp chúng ta khám phá sâu hơn về các tính chất hóa học và vật lý của nó.

Giới Thiệu Về Lawrencium
Lawrencium là nguyên tố hóa học có ký hiệu Lr và số nguyên tử 103, thuộc nhóm Actinide trong bảng tuần hoàn. Được phát hiện vào năm 1961, Lawrencium là một trong những nguyên tố nặng nhất và ít được biết đến nhất.
Lawrencium được đặt theo tên của nhà vật lý người Mỹ Ernest O. Lawrence, người đã phát minh ra máy gia tốc hạt cyclotron. Nguyên tố này chỉ tồn tại ở dạng tổng hợp trong các phòng thí nghiệm và có tính phóng xạ cao.
- Vị trí trong bảng tuần hoàn: Lawrencium nằm ở vị trí cuối cùng của nhóm Actinide, thuộc chu kỳ 7.
- Trạng thái tự nhiên: Lawrencium không tồn tại trong tự nhiên mà chỉ được tạo ra thông qua các phản ứng hạt nhân.
- Tính chất vật lý: Lawrencium có tính kim loại, nhưng do tính phóng xạ cao, các đặc tính vật lý chi tiết của nó vẫn chưa được nghiên cứu đầy đủ.
Cấu hình electron của Lawrencium là \[\text{[Rn]} 5f^{14} 6d^{1} 7s^{2}\], thể hiện sự phân bố electron trong các lớp vỏ nguyên tử. Đây là một cấu hình phức tạp, đặc trưng cho các nguyên tố trong nhóm Actinide.
Cấu Hình Electron Chi Tiết Của Lawrencium
Lawrencium, với số nguyên tử 103, có cấu hình electron phức tạp đặc trưng cho các nguyên tố thuộc nhóm Actinide. Cấu hình electron của Lawrencium được viết dưới dạng:
\[\text{[Rn]} 5f^{14} 6d^{1} 7s^{2}\]
Trong đó:
- \[\text{[Rn]}\]: Cấu hình electron của Radon, nguyên tố thuộc chu kỳ 6, đóng vai trò là nền tảng.
- \[5f^{14}\]: Cho biết 14 electron chiếm các orbital 5f, đầy đủ các mức năng lượng f.
- \[6d^{1}\]: Một electron nằm trong orbital 6d, thể hiện sự chuyển đổi từ phân lớp f sang d.
- \[7s^{2}\]: Hai electron chiếm các orbital 7s, lớp ngoài cùng của nguyên tố này.
Việc xác định cấu hình electron của Lawrencium không chỉ quan trọng trong việc hiểu rõ hơn về tính chất hóa học của nó mà còn giúp giải thích các đặc điểm đặc trưng của nguyên tố này so với các thành viên khác trong nhóm Actinide. Đặc biệt, sự hiện diện của electron trong orbital 6d là một điểm khác biệt so với các nguyên tố trước đó trong cùng nhóm.
Mặc dù cấu hình electron của Lawrencium đã được xác định, các nghiên cứu tiếp tục được tiến hành để làm rõ hơn về các trạng thái năng lượng và khả năng tương tác của nguyên tố này trong các phản ứng hóa học.

Tính Chất Hóa Học Của Lawrencium
Lawrencium (Lr) là nguyên tố thứ 103 trong bảng tuần hoàn và thuộc nhóm Actinide. Tính chất hóa học của Lawrencium khá độc đáo và được đặc trưng bởi sự phức tạp của cấu hình electron.
Một số tính chất hóa học của Lawrencium bao gồm:
- Trạng thái oxi hóa: Lawrencium thường xuất hiện ở trạng thái oxi hóa +3, giống như các nguyên tố Actinide khác. Trạng thái này được hình thành do sự mất electron từ các orbital 7s và 6d.
- Tính chất kim loại: Lawrencium có tính kim loại, với đặc điểm dễ dàng tạo thành hợp chất ion. Tính chất này chủ yếu do cấu hình electron của nó, với các electron dễ mất từ các lớp ngoài cùng.
- Phản ứng hóa học: Trong các phản ứng, Lawrencium có thể tạo thành các hợp chất với các nguyên tố khác, chủ yếu là trong các dạng oxit và halide. Do tính phóng xạ cao, các phản ứng hóa học của Lawrencium thường được tiến hành trong điều kiện kiểm soát nghiêm ngặt.
Một đặc điểm đáng chú ý của Lawrencium là khả năng hình thành liên kết với các nguyên tố phi kim, đặc biệt là oxy, để tạo ra \(\text{Lr}_2\text{O}_3\) - oxit của Lawrencium. Phản ứng tổng quát có thể được viết như sau:
\[\text{4 Lr + 3 O}_2 \rightarrow \text{2 Lr}_2\text{O}_3\]
Tuy nhiên, do tính phóng xạ mạnh, việc nghiên cứu chi tiết về tính chất hóa học của Lawrencium vẫn còn hạn chế và đang được các nhà khoa học tiếp tục khám phá.