Chủ đề electron yield: Electron yield là một khái niệm quan trọng trong hóa học, liên quan đến sự phân bố và sắp xếp các electron trong nguyên tử và phân tử. Hiểu rõ về electron yield giúp giải thích các tính chất hóa học và vật lý của các nguyên tố, từ cấu trúc phân tử đến phản ứng hóa học. Bài viết này sẽ đưa bạn qua một hành trình khám phá chi tiết về electron yield và những ứng dụng thực tiễn trong nghiên cứu khoa học.
Mục lục
- Electron Yield: Khái niệm và Ứng dụng trong Khoa học Vật liệu
- Mục lục
- 1. Khái niệm Electron Yield
- 2. Cấu tạo và tính chất của Electron
- 3. Các công thức tính liên quan đến Electron Yield
- 4. Ứng dụng của Electron Yield trong khoa học và công nghệ
- 5. Thuyết Electron và Định luật Bảo toàn Điện tích
- 6. Các ví dụ minh họa và bài tập liên quan
- 7. Kết luận
Electron Yield: Khái niệm và Ứng dụng trong Khoa học Vật liệu
Electron yield là một khái niệm quan trọng trong vật lý và hóa học, liên quan đến khả năng phát xạ electron từ một vật liệu khi nó được chiếu xạ bằng một nguồn năng lượng như tia X, tia cực tím hoặc hạt nhân. Dưới đây là các thông tin chi tiết về khái niệm và ứng dụng của electron yield:
1. Định nghĩa Electron Yield
Electron yield thường được định nghĩa là số lượng electron phát ra trên mỗi hạt năng lượng tương tác với vật liệu. Quá trình này có thể xảy ra trong các vật liệu như kim loại, bán dẫn và các màng mỏng. Electron yield phụ thuộc vào nhiều yếu tố, bao gồm năng lượng và loại hạt chiếu xạ, cũng như tính chất của vật liệu bị chiếu xạ.
2. Các Yếu Tố Ảnh Hưởng Đến Electron Yield
- Năng lượng của nguồn chiếu xạ: Năng lượng cao hơn thường dẫn đến electron yield lớn hơn.
- Góc tới của nguồn chiếu xạ: Góc tới càng nhỏ, electron yield càng cao do đường đi của hạt năng lượng dài hơn trong vật liệu.
- Tính chất của vật liệu: Vật liệu với độ dẫn điện tốt thường có electron yield cao hơn.
3. Ứng Dụng của Electron Yield
Electron yield có nhiều ứng dụng trong các lĩnh vực khoa học và công nghệ, bao gồm:
- Phân tích bề mặt vật liệu: Electron yield được sử dụng trong các kỹ thuật như quang phổ điện tử tia X (XPS) để nghiên cứu thành phần và cấu trúc của bề mặt vật liệu.
- Phát triển vật liệu mới: Hiểu rõ electron yield giúp các nhà khoa học phát triển các vật liệu có khả năng tự bảo vệ hoặc tăng cường các tính chất điện tử.
- Ứng dụng trong công nghệ bán dẫn: Trong sản xuất vi mạch, electron yield có thể ảnh hưởng đến quá trình khắc và xử lý bề mặt.
4. Phương Trình Tính Electron Yield
Electron yield, ký hiệu \(\eta\), được tính bằng công thức:
Trong đó:
- \(N_{out}\): Số lượng electron phát ra.
- \(N_{in}\): Số lượng hạt năng lượng chiếu vào.
5. Thách Thức và Tiềm Năng
Việc kiểm soát và tối ưu hóa electron yield là một thách thức lớn trong nghiên cứu khoa học vật liệu, nhưng đồng thời cũng mở ra nhiều cơ hội cho sự phát triển của các công nghệ mới như màn hình phẳng, cảm biến và các thiết bị quang điện.
Qua các thông tin trên, có thể thấy rằng electron yield là một khái niệm quan trọng không chỉ trong nghiên cứu khoa học cơ bản mà còn có nhiều ứng dụng thực tiễn trong công nghiệp và công nghệ cao.

Mục lục
-
1. Định nghĩa và tầm quan trọng của Electron Yield
Giới thiệu về khái niệm Electron Yield, các yếu tố ảnh hưởng và vai trò quan trọng trong vật lý, hóa học và các ngành công nghiệp khác.
-
2. Nguyên lý và cơ chế hoạt động của Electron Yield
Phân tích chi tiết về nguyên lý hoạt động của Electron Yield, bao gồm các quy tắc và quy trình để đo lường hiệu suất electron trong các phản ứng khác nhau.
-
3. Các phương pháp đo Electron Yield
Danh sách và mô tả các phương pháp phổ biến để đo Electron Yield như sử dụng kính hiển vi điện tử, phổ quang học, và các thiết bị hiện đại khác.
-
4. Ứng dụng của Electron Yield trong nghiên cứu và công nghiệp
Khám phá các ứng dụng thực tế của Electron Yield trong nghiên cứu khoa học, công nghệ bán dẫn, y học và công nghiệp vật liệu.
-
5. Các thách thức và hướng nghiên cứu tương lai
Thảo luận về những thách thức hiện tại trong nghiên cứu Electron Yield và định hướng cho các nghiên cứu trong tương lai nhằm cải thiện và ứng dụng rộng rãi hơn.
-
6. Tài liệu tham khảo và nguồn học liệu
Cung cấp danh sách các tài liệu tham khảo, sách, bài báo khoa học và các nguồn học liệu hữu ích để tìm hiểu sâu hơn về Electron Yield.
1. Khái niệm Electron Yield
Electron Yield là một khái niệm quan trọng trong lĩnh vực vật lý và hóa học, đặc biệt liên quan đến các hiện tượng tương tác giữa electron và vật liệu. Nó biểu thị tỷ lệ của số lượng electron được phát ra từ bề mặt vật liệu so với số lượng electron chiếu vào. Khái niệm này được áp dụng rộng rãi trong các nghiên cứu về quang điện tử, quang phổ học và các công nghệ bề mặt.
Quá trình Electron Yield có thể được phân tích qua các bước như sau:
- Xác định electron phát ra: Số lượng electron phát ra từ bề mặt vật liệu thường được đo bằng các phương pháp như quang phổ học electron.
- Đo đạc electron chiếu vào: Sử dụng các nguồn phát electron hoặc các tia X để chiếu electron vào bề mặt và đo đạc số lượng electron này.
- Tính toán Electron Yield: Tỷ lệ giữa số electron phát ra và số electron chiếu vào được tính theo công thức: \[ \text{Electron Yield} = \frac{\text{Số lượng electron phát ra}}{\text{Số lượng electron chiếu vào}} \]
Ứng dụng của Electron Yield rất đa dạng, từ nghiên cứu cấu trúc bề mặt, phân tích hóa học cho đến việc phát triển các vật liệu mới. Nó giúp chúng ta hiểu rõ hơn về các đặc tính điện tử và hóa học của các vật liệu, góp phần vào sự phát triển của công nghệ và khoa học hiện đại.

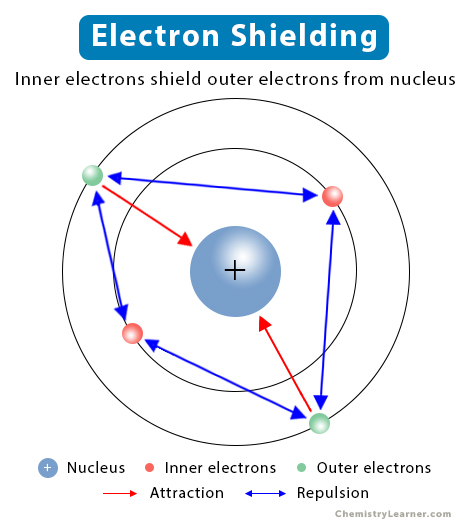
2. Cấu tạo và tính chất của Electron
Electron là một hạt hạ nguyên tử có điện tích âm, thường được ký hiệu là \( e^- \). Electron đóng vai trò quan trọng trong việc hình thành các liên kết hóa học và quyết định tính chất điện của các vật chất. Các electron được sắp xếp trong các lớp vỏ của nguyên tử, mỗi lớp vỏ có thể chứa một số electron nhất định tuân theo quy tắc \(2n^2\), trong đó \(n\) là số thứ tự của lớp.
- Cấu trúc lớp vỏ electron:
- Electron được phân bổ trong các lớp vỏ từ thấp đến cao, bắt đầu từ lớp K (n=1), L (n=2), M (n=3), và tiếp tục như vậy.
- Mỗi phân lớp có khả năng chứa một số electron nhất định: s có thể chứa tối đa 2 electron, p chứa 6, d chứa 10, và f chứa 14.
- Cấu hình electron xác định cách electron được phân bố trong các phân lớp, từ đó ảnh hưởng đến tính chất hóa học của nguyên tố.
- Thuộc tính của electron:
- Khối lượng của một electron rất nhỏ, chỉ khoảng \(9.109 \times 10^{-31}\) kg.
- Electron có điện tích âm và được xem là hạt cơ bản, không có cấu trúc nội tại phức tạp hơn.
- Các electron trong cùng một lớp vỏ có năng lượng tương tự nhau, nhưng mức năng lượng sẽ tăng dần từ lớp vỏ trong ra ngoài.
- Vai trò của electron trong tính chất hóa học:
- Electron ở lớp vỏ ngoài cùng (lớp electron hóa trị) quyết định khả năng phản ứng của nguyên tử, bao gồm việc nhường, nhận, hoặc chia sẻ electron để tạo liên kết hóa học.
- Nguyên tử có lớp vỏ ngoài cùng với ít hơn 4 electron có xu hướng nhường electron và thể hiện tính chất kim loại, trong khi nguyên tử có từ 5 đến 7 electron sẽ nhận thêm electron để trở nên ổn định, thường thể hiện tính chất phi kim.
3. Các công thức tính liên quan đến Electron Yield
Electron yield là một chỉ số quan trọng trong việc đo lường số lượng electron phát ra từ bề mặt một vật liệu khi bị chiếu sáng hoặc tác động bởi tia X hoặc các hạt tích điện. Dưới đây là các công thức và bước tính toán thường gặp:
- Công thức tổng quát:
- Công thức cơ bản để tính electron yield (\( \eta \)) là: \[ \eta = \frac{N_{e}}{N_{i}} \] Trong đó, \(N_{e}\) là số electron phát ra và \(N_{i}\) là số hạt tích điện hoặc photon tới.
- Ảnh hưởng của năng lượng bề mặt:
- Electron yield phụ thuộc vào năng lượng của các hạt tác động và tính chất bề mặt vật liệu. Công thức tính có thể được điều chỉnh dựa trên sự tương tác giữa hạt và vật liệu cụ thể.
- Phương pháp đo lường:
- Phép đo electron yield thường bao gồm việc chiếu tia X hoặc electron lên mẫu vật và đếm số electron phát ra bằng các thiết bị nhạy điện tử.
- Một số công thức khác có thể được sử dụng để điều chỉnh kết quả đo dựa trên điều kiện thí nghiệm và loại vật liệu.
- Các yếu tố ảnh hưởng:
- Các yếu tố như nhiệt độ, độ dày lớp vật liệu, và mức độ oxy hóa cũng có thể ảnh hưởng đến giá trị của electron yield.
Việc nắm rõ các công thức và yếu tố liên quan giúp tối ưu hóa việc sử dụng electron yield trong các ứng dụng thực tiễn như nghiên cứu vật liệu và phân tích bề mặt.

4. Ứng dụng của Electron Yield trong khoa học và công nghệ
Electron yield, với khả năng giải phóng và đo lường lượng electron từ bề mặt vật liệu, đóng vai trò quan trọng trong nhiều lĩnh vực khoa học và công nghệ. Những ứng dụng của nó không chỉ giới hạn trong nghiên cứu cơ bản mà còn mở rộng đến nhiều lĩnh vực công nghệ tiên tiến.
4.1. Ứng dụng trong nghiên cứu vật liệu
Electron yield được sử dụng để phân tích tính chất bề mặt của các vật liệu, đặc biệt là trong việc xác định thành phần và cấu trúc của lớp bề mặt. Kỹ thuật này giúp các nhà khoa học nghiên cứu về cách thức mà vật liệu tương tác với môi trường xung quanh, từ đó phát triển các vật liệu mới với tính năng vượt trội.
4.2. Ứng dụng trong phân tích hóa học
Trong phân tích hóa học, electron yield được áp dụng để xác định các phản ứng hóa học xảy ra trên bề mặt các chất xúc tác. Việc đo lường electron yield giúp xác định quá trình oxi hóa khử, giúp cải thiện hiệu suất của các phản ứng xúc tác trong công nghiệp hóa chất.
4.3. Ứng dụng trong công nghệ điện tử
Electron yield có vai trò quan trọng trong việc phát triển và tối ưu hóa các thiết bị điện tử, đặc biệt là trong việc chế tạo các linh kiện bán dẫn. Nhờ khả năng kiểm soát và đo lường electron, các kỹ sư có thể thiết kế các linh kiện với hiệu suất cao hơn, tiết kiệm năng lượng và kéo dài tuổi thọ thiết bị.
4.4. Ứng dụng trong công nghệ quang điện
Electron yield còn được sử dụng trong nghiên cứu các tế bào quang điện (solar cells). Việc tối ưu hóa electron yield giúp cải thiện hiệu suất chuyển đổi năng lượng ánh sáng thành điện năng, đóng góp vào sự phát triển của năng lượng tái tạo.
4.5. Ứng dụng trong công nghệ xử lý bề mặt
Trong công nghệ xử lý bề mặt, electron yield được dùng để kiểm tra và cải thiện chất lượng của các lớp phủ bảo vệ, giúp tăng cường độ bền và khả năng chống ăn mòn của vật liệu.
Như vậy, electron yield đã và đang đóng góp quan trọng vào nhiều lĩnh vực khoa học và công nghệ, từ nghiên cứu cơ bản đến các ứng dụng thực tiễn, giúp đẩy mạnh sự phát triển và tiến bộ của các ngành công nghiệp hiện đại.
XEM THÊM:
5. Thuyết Electron và Định luật Bảo toàn Điện tích
Thuyết electron là một lý thuyết cơ bản trong vật lý học, giải thích về bản chất của điện tích và các hiện tượng điện liên quan đến sự di chuyển của electron. Lý thuyết này giúp hiểu rõ cách thức các vật thể nhiễm điện và cách điện tích được bảo toàn trong một hệ kín.
Cấu tạo nguyên tử về phương diện điện:
- Nguyên tử gồm có một hạt nhân mang điện dương ở trung tâm, bao quanh bởi các electron mang điện âm.
- Hạt nhân chứa proton (mang điện dương) và neutron (không mang điện).
- Electron có điện tích \(-1,6 \times 10^{-19} \, C\) và proton có điện tích \(+1,6 \times 10^{-19} \, C\).
Nội dung thuyết electron:
- Electron có thể rời khỏi nguyên tử và di chuyển sang nơi khác. Khi nguyên tử mất electron, nó trở thành ion dương; khi nhận thêm electron, nó trở thành ion âm.
- Một vật nhiễm điện âm khi số electron nhiều hơn số proton, và nhiễm điện dương khi số electron ít hơn số proton.
Các hiện tượng điện liên quan:
- Sự nhiễm điện do hưởng ứng: Khi một vật mang điện được đưa lại gần một vật trung hòa, các electron trong vật trung hòa sẽ dịch chuyển, dẫn đến sự phân bố lại điện tích.
- Sự nhiễm điện do tiếp xúc: Khi một vật chưa nhiễm điện tiếp xúc với một vật đã mang điện, điện tích sẽ được chuyển từ vật mang điện sang vật chưa mang điện, làm cho cả hai vật cùng loại điện tích.
Định luật Bảo toàn Điện tích:
Định luật Bảo toàn Điện tích khẳng định rằng trong một hệ kín, tổng điện tích luôn được bảo toàn. Điều này có nghĩa là điện tích không thể tự sinh ra hoặc mất đi, mà chỉ có thể chuyển từ vật này sang vật khác. Ví dụ:
- Giả sử có một thanh kim loại nhiễm điện \(-2,5 \times 10^{-6} \, C\) và sau khi mất đi một số electron, thanh kim loại có điện tích \(5,5 \times 10^{-6} \, C\). Số điện tích mà thanh kim loại đã mất là \[ q_{\text{mất}} = 5,5 \times 10^{-6} - (-2,5 \times 10^{-6}) = 8 \times 10^{-6} \, \text{C} \]
- Hai quả cầu kim loại A và B có điện tích lần lượt là \( q_{1} = -3,2 \times 10^{-7} \, C \) và \( q_{2} = 2,4 \times 10^{-7} \, C \), sau khi tiếp xúc nhau, tổng điện tích của hệ sẽ được bảo toàn và phân phối đều.
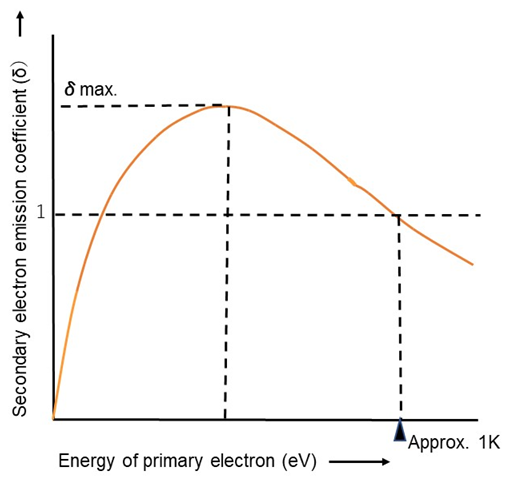
6. Các ví dụ minh họa và bài tập liên quan
Dưới đây là một số ví dụ minh họa và bài tập liên quan đến thuyết electron và định luật bảo toàn điện tích. Các bài tập này giúp hiểu rõ hơn về các khái niệm cũng như cách áp dụng vào thực tế.
Ví dụ 1: Tính toán số mol electron trong phản ứng oxi hóa-khử
Cho phản ứng sau:
\[
\text{MnO}_4^- + 8\text{H}^+ + 5\text{e}^- \rightarrow \text{Mn}^{2+} + 4\text{H}_2\text{O}
\]
Trong phản ứng này, một phân tử \(\text{MnO}_4^-\) nhường 5 mol electron. Dựa vào số mol các chất, có thể tính toán lượng electron tham gia trong phản ứng.
Ví dụ 2: Bài tập về bảo toàn electron trong phản ứng hóa học
Cho 15,8 gam \(\text{KMnO}_4\) tác dụng với dung dịch HCl đậm đặc. Tính thể tích khí \(\text{Cl}_2\) thoát ra (ở điều kiện tiêu chuẩn).
Giải:
- Viết phương trình phản ứng và cân bằng electron:
- Tính số mol \(\text{KMnO}_4\) và số mol electron nhường:
- Từ số mol electron, tính thể tích khí \(\text{Cl}_2\) thoát ra:
\[
\text{MnO}_4^- + 8\text{H}^+ + 5\text{e}^- \rightarrow \text{Mn}^{2+} + 4\text{H}_2\text{O}
\]
\[
n(\text{KMnO}_4) = \frac{15,8}{158} = 0,1 \text{ mol}
\]
Số mol electron nhường:
\[
n(\text{e}^-) = 5 \times 0,1 = 0,5 \text{ mol}
\]
\[
V(\text{Cl}_2) = 22,4 \times n(\text{e}^-) = 22,4 \times 0,5 = 11,2 \text{ lít}
\]
Bài tập tự luyện
- Bài 1: Hòa tan hoàn toàn 1,08 gam Al trong dung dịch HNO3. Tính thể tích khí thoát ra và xác định chất khử chính trong phản ứng.
- Bài 2: Tính số mol electron được nhường trong phản ứng giữa Fe và Cu với dung dịch HNO3.
- Bài 3: Xác định lượng kết tủa tạo thành khi cho một lượng xác định dung dịch BaCl2 vào dung dịch chứa ion sulfate.

7. Kết luận
Trong quá trình nghiên cứu về hiện tượng electron yield, chúng ta đã thấy rõ vai trò quan trọng của nó trong các ứng dụng liên quan đến quang điện và quang hóa. Hiện tượng này không chỉ phản ánh khả năng của một vật liệu trong việc phát ra electron dưới tác động của bức xạ mà còn liên quan mật thiết đến các yếu tố như năng lượng photon và công thoát electron.
Các ví dụ và bài tập đã thảo luận đã minh họa rõ ràng cách tính toán và xác định giá trị electron yield dựa trên các thông số vật lý như bước sóng, cường độ ánh sáng và bản chất vật liệu. Bằng cách áp dụng các công thức như:
Chúng ta có thể định lượng được khả năng phát xạ electron của một vật liệu khi bị chiếu xạ.
Từ đó, có thể kết luận rằng việc hiểu rõ và kiểm soát electron yield không chỉ giúp cải thiện hiệu suất trong các ứng dụng công nghệ cao mà còn mở ra cơ hội cho các nghiên cứu sâu hơn về vật lý lượng tử và công nghệ vật liệu tiên tiến.