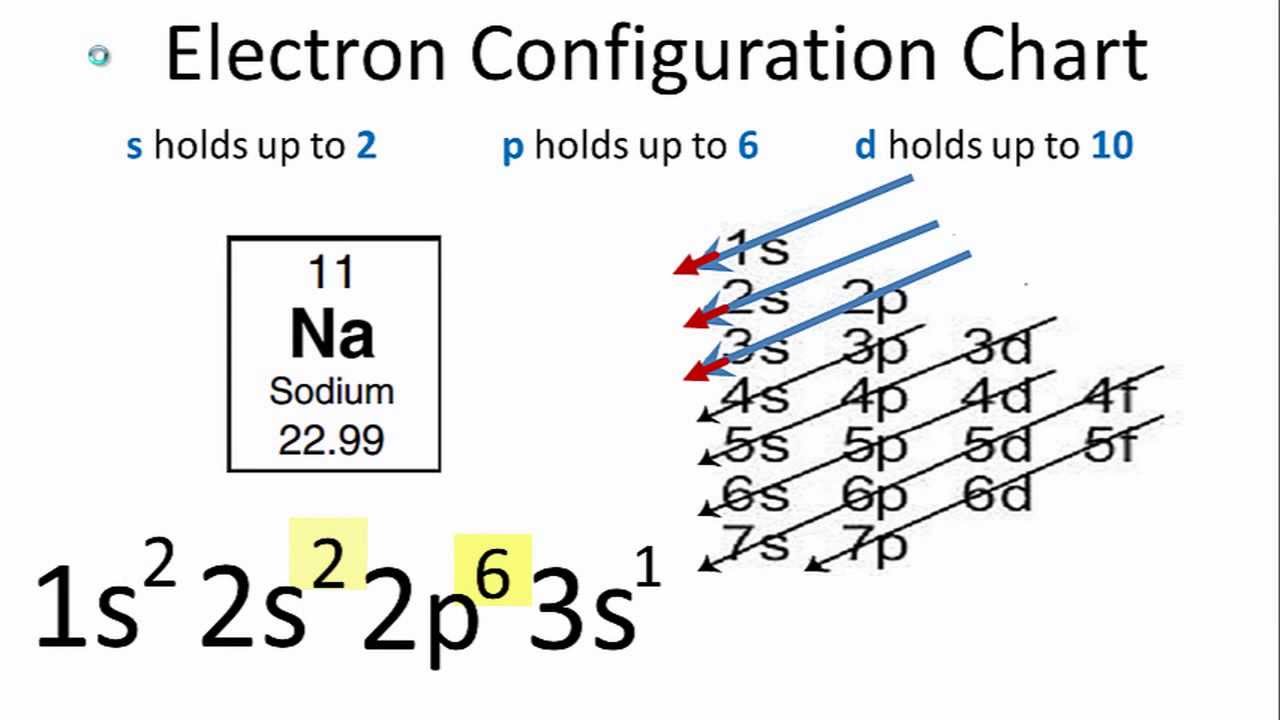
Chủ đề define electron affinity: Ái lực electron (electron affinity) là một khái niệm quan trọng trong hóa học và vật lý, mô tả khả năng của nguyên tử thu nhận electron. Bài viết này sẽ giải thích chi tiết về khái niệm này, các yếu tố ảnh hưởng và vai trò của nó trong các lĩnh vực nghiên cứu và ứng dụng thực tiễn. Tìm hiểu ngay để nắm vững kiến thức nền tảng và cách áp dụng ái lực electron vào các bài toán khoa học phức tạp.
Mục lục
- Định nghĩa "Electron Affinity"
- 1. Khái Niệm Ái Lực Electron
- 2. Đặc Điểm của Ái Lực Electron
- 3. Vai Trò của Ái Lực Electron trong Hóa Học
- 4. Vai Trò của Ái Lực Electron trong Vật Lý
- 5. So Sánh Ái Lực Electron Giữa Các Nguyên Tố
- 6. Các Phương Pháp Đo Lường Ái Lực Electron
- 7. Ứng Dụng Thực Tiễn của Ái Lực Electron
- 8. Kết Luận
Định nghĩa "Electron Affinity"
Ái lực electron (Electron Affinity) là một khái niệm quan trọng trong hóa học, mô tả khả năng của một nguyên tử hoặc phân tử để thu hút một electron và hình thành ion âm. Khi một nguyên tử trung hòa thu hút thêm một electron vào lớp vỏ điện tử của nó, năng lượng sẽ được giải phóng, và mức năng lượng này được gọi là ái lực electron.
Đặc điểm chính của ái lực electron
- Đơn vị đo: Ái lực electron được đo bằng đơn vị kilojoule trên mol (kJ/mol).
- Giá trị ái lực electron: Thường thì giá trị ái lực electron có thể là số âm, do năng lượng được giải phóng khi một nguyên tử thu hút một electron.
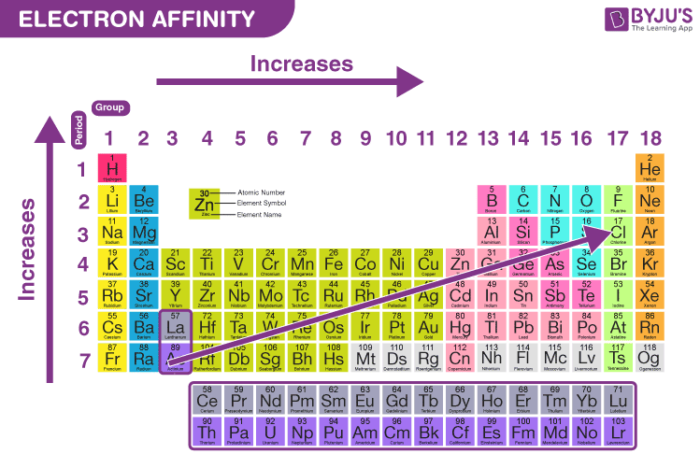
- Mối quan hệ với vị trí trong bảng tuần hoàn: Ái lực electron thường tăng khi đi từ trái sang phải trong một chu kỳ của bảng tuần hoàn và giảm khi đi xuống trong một nhóm. Điều này có nghĩa là các nguyên tử nhỏ hơn thường có ái lực electron cao hơn.
Ví dụ về ái lực electron
Nguyên tử clo (Cl) có ái lực electron cao vì khi nó nhận thêm một electron, nó sẽ đạt được cấu hình electron bền vững giống với khí hiếm gần nhất (argon). Vì lý do này, clo có xu hướng thu hút electron mạnh mẽ và có ái lực electron cao.
Ứng dụng của ái lực electron
Hiểu biết về ái lực electron giúp các nhà hóa học giải thích nhiều hiện tượng hóa học, như lý do tại sao một số nguyên tố có xu hướng nhận electron dễ dàng hơn và hình thành các ion âm mạnh. Nó cũng giúp trong việc dự đoán tính chất của các phản ứng hóa học và thiết kế các hợp chất hóa học mới.
Phương trình tính toán ái lực electron
Ái lực electron được định nghĩa thông qua phương trình:
\[
E_a = - \Delta H
\]
Trong đó:
- Ea là ái lực electron.
- \(\Delta H\) là sự thay đổi enthalpy (năng lượng) khi nguyên tử nhận thêm một electron.
Giá trị \(\Delta H\) âm biểu thị rằng năng lượng được giải phóng trong quá trình này.
1. Khái Niệm Ái Lực Electron
Ái lực electron (electron affinity) là đại lượng đặc trưng cho khả năng của một nguyên tử trung hòa khi thu nhận thêm một electron để trở thành ion âm. Quá trình này thường được miêu tả bởi phương trình:
\( X(g) + e^- \rightarrow X^-(g) \)
Trong đó:
- X(g) là nguyên tử ở trạng thái khí.
- e^- là electron tự do.
- X^-(g) là ion âm được tạo thành sau khi nguyên tử thu nhận electron.
Ái lực electron có thể được đo bằng năng lượng giải phóng trong quá trình này. Nếu năng lượng được giải phóng, ái lực electron mang giá trị dương; ngược lại, nếu cần cung cấp năng lượng để thêm electron, giá trị sẽ âm. Điều này phản ánh sự ổn định của ion âm so với nguyên tử trung hòa ban đầu.
Ái lực electron đóng vai trò quan trọng trong việc hiểu rõ tính chất hóa học của các nguyên tố, đặc biệt là trong dự đoán hành vi của nguyên tử trong các phản ứng hóa học.
2. Đặc Điểm của Ái Lực Electron
Ái lực electron là một đặc tính quan trọng của các nguyên tử, phản ánh khả năng thu hút và giữ chặt electron. Đặc điểm của ái lực electron có thể được hiểu rõ hơn qua các yếu tố sau:
- Độ lớn của ái lực electron: Đây là giá trị năng lượng được giải phóng khi một nguyên tử trung hòa nhận thêm một electron. Ái lực electron thường có giá trị âm, cho thấy năng lượng được giải phóng trong quá trình tạo thành ion âm.
- Xu hướng trong bảng tuần hoàn: Ái lực electron có xu hướng tăng dần từ trái sang phải trong một chu kỳ, do lực hút giữa hạt nhân và electron tăng lên khi số proton tăng. Ngược lại, ái lực electron giảm dần khi đi xuống một nhóm, do kích thước nguyên tử tăng làm giảm lực hút giữa hạt nhân và electron.
- Các yếu tố ảnh hưởng: Các yếu tố ảnh hưởng đến ái lực electron bao gồm kích thước nguyên tử, điện tích hạt nhân, cấu hình electron, và các hiệu ứng che chắn. Các nguyên tố với cấu hình electron bền vững thường có ái lực electron thấp.
Các nguyên tố phi kim thường có ái lực electron cao hơn kim loại, bởi vì chúng dễ dàng thu nhận thêm electron để đạt cấu hình electron ổn định. Ái lực electron là một khái niệm quan trọng trong việc dự đoán tính chất hóa học của các nguyên tố và cách chúng phản ứng trong các hợp chất.

3. Vai Trò của Ái Lực Electron trong Hóa Học
Ái lực electron đóng vai trò quan trọng trong hóa học, đặc biệt trong việc hiểu rõ tính chất hóa học của các nguyên tố và dự đoán các phản ứng hóa học. Dưới đây là một số vai trò cụ thể của ái lực electron:
- Dự đoán tính chất hóa học: Ái lực electron giúp xác định khả năng một nguyên tố sẽ thu nhận thêm electron để trở thành ion âm. Những nguyên tố có ái lực electron cao, như các halogen, có xu hướng nhận electron dễ dàng và tham gia vào các phản ứng hóa học mạnh mẽ.
- Hình thành liên kết hóa học: Ái lực electron ảnh hưởng đến khả năng hình thành liên kết ion giữa các nguyên tố. Ví dụ, nguyên tố có ái lực electron cao có xu hướng thu hút electron từ nguyên tố có ái lực electron thấp hơn, dẫn đến sự hình thành liên kết ion.
- Ổn định cấu trúc phân tử: Ái lực electron góp phần vào sự ổn định của cấu trúc phân tử. Khi một nguyên tử nhận thêm electron, cấu hình electron của nó trở nên bền vững hơn, điều này giúp ổn định cấu trúc của phân tử hoặc ion được hình thành.
- Ảnh hưởng đến năng lượng ion hóa: Ái lực electron cũng có mối quan hệ chặt chẽ với năng lượng ion hóa, khi cả hai đều phản ánh sự ổn định của nguyên tử và ion. Hiểu rõ ái lực electron giúp dự đoán được năng lượng cần thiết để loại bỏ electron khỏi nguyên tử hoặc ion.
Tổng kết, ái lực electron không chỉ là một khái niệm lý thuyết mà còn có ứng dụng thực tiễn trong việc hiểu và dự đoán tính chất hóa học, từ đó giúp tối ưu hóa các phản ứng và quá trình trong hóa học và công nghiệp.

4. Vai Trò của Ái Lực Electron trong Vật Lý
Ái lực electron không chỉ có ý nghĩa quan trọng trong hóa học, mà còn đóng vai trò thiết yếu trong nhiều lĩnh vực của vật lý. Dưới đây là một số vai trò cụ thể của ái lực electron trong vật lý:
- Liên quan đến năng lượng ion hóa: Ái lực electron có mối quan hệ mật thiết với năng lượng ion hóa, khi cả hai đại lượng này đều phản ánh sự tương tác giữa hạt nhân và electron. Hiểu rõ ái lực electron giúp dự đoán năng lượng cần thiết để loại bỏ một electron từ một nguyên tử hoặc ion, hỗ trợ trong việc nghiên cứu các hiện tượng ion hóa và quá trình kích thích trong vật lý nguyên tử.
- Ảnh hưởng đến cấu trúc năng lượng của vật liệu: Ái lực electron có thể ảnh hưởng đến cấu trúc băng của vật liệu bán dẫn và chất cách điện, từ đó quyết định tính chất dẫn điện và quang học của chúng. Trong nghiên cứu vật liệu, việc hiểu rõ ái lực electron giúp các nhà khoa học dự đoán và điều chỉnh các đặc tính vật lý của vật liệu để tối ưu hóa ứng dụng trong công nghệ điện tử và quang học.
- Đóng vai trò trong các thí nghiệm quang phổ: Ái lực electron ảnh hưởng đến phổ năng lượng của nguyên tử và ion, từ đó giúp xác định các mức năng lượng và cấu hình electron trong các thí nghiệm quang phổ. Điều này rất quan trọng trong việc nghiên cứu các hiện tượng liên quan đến phát xạ và hấp thụ năng lượng trong vật lý quang phổ.
- Tác động đến các hiện tượng từ tính: Ái lực electron có thể ảnh hưởng đến các đặc tính từ của vật liệu, đặc biệt là trong các hợp chất chứa nguyên tố có ái lực electron cao. Hiểu rõ mối liên hệ này giúp các nhà khoa học phát triển các vật liệu từ mới, có ứng dụng trong công nghệ lưu trữ và truyền tải thông tin.
Tóm lại, ái lực electron đóng góp quan trọng vào việc giải thích và dự đoán các hiện tượng vật lý, từ đó mở ra các hướng nghiên cứu và ứng dụng mới trong các lĩnh vực công nghệ cao.

5. So Sánh Ái Lực Electron Giữa Các Nguyên Tố
Ái lực electron giữa các nguyên tố có sự khác biệt rõ rệt, phản ánh đặc tính hóa học và cấu trúc nguyên tử của chúng. Dưới đây là một số yếu tố cần xem xét khi so sánh ái lực electron giữa các nguyên tố:
- Kim loại vs. Phi kim: Phi kim thường có ái lực electron cao hơn kim loại. Điều này do phi kim có xu hướng nhận thêm electron để đạt cấu hình electron ổn định, trong khi kim loại thường mất electron để tạo thành ion dương.
- Xu hướng trong bảng tuần hoàn:
- Theo chu kỳ: Ái lực electron có xu hướng tăng từ trái sang phải trong một chu kỳ, do số proton trong hạt nhân tăng làm tăng lực hút với electron thêm vào.
- Theo nhóm: Ái lực electron thường giảm khi đi xuống một nhóm, do kích thước nguyên tử tăng, làm giảm lực hút giữa hạt nhân và electron.
- Các ngoại lệ: Có một số ngoại lệ trong bảng tuần hoàn, ví dụ, các nguyên tố thuộc nhóm khí hiếm (như Neon, Argon) có ái lực electron rất thấp hoặc thậm chí là âm, do cấu hình electron bền vững của chúng.
Bảng so sánh dưới đây minh họa ái lực electron của một số nguyên tố điển hình:
| Nguyên Tố | Ái Lực Electron (kJ/mol) |
|---|---|
| Fluor (F) | -328 |
| Oxygen (O) | -141 |
| Sodium (Na) | -53 |
| Argon (Ar) | ~0 |
Sự khác biệt trong ái lực electron giúp giải thích tại sao các nguyên tố phản ứng khác nhau và tại sao chúng có xu hướng tạo thành các loại liên kết hóa học cụ thể.
XEM THÊM:
6. Các Phương Pháp Đo Lường Ái Lực Electron
Đo lường ái lực electron là một quá trình phức tạp, đòi hỏi các kỹ thuật chính xác để xác định năng lượng giải phóng khi một nguyên tử hoặc phân tử thu nhận thêm một electron. Dưới đây là một số phương pháp đo lường phổ biến:
- Phương pháp quang phổ khối (Mass Spectrometry):
Quang phổ khối là một trong những kỹ thuật quan trọng nhất để đo ái lực electron. Bằng cách ion hóa các nguyên tử hoặc phân tử và phân tích các ion thu được dựa trên tỷ số khối lượng trên điện tích, phương pháp này giúp xác định năng lượng liên quan đến quá trình thêm electron.
- Phương pháp phổ quang điện tử (Photoelectron Spectroscopy):
Trong phương pháp này, các electron bị kích thích bởi photon (ánh sáng) và được phát xạ từ nguyên tử. Năng lượng của các electron này được đo để xác định ái lực electron, dựa trên sự chênh lệch năng lượng giữa trạng thái ban đầu và trạng thái sau khi thêm electron.
- Phương pháp nhiệt hóa học (Thermochemical Method):
Phương pháp này dựa trên việc đo nhiệt lượng giải phóng hoặc hấp thụ trong quá trình phản ứng hóa học liên quan đến quá trình ion hóa và thêm electron. Thông qua cân bằng nhiệt động lực học, có thể tính toán được giá trị ái lực electron.
- Phương pháp lý thuyết (Theoretical Methods):
Các phương pháp tính toán lý thuyết như mô phỏng quantum mechanics và density functional theory (DFT) cũng được sử dụng để dự đoán ái lực electron. Các kỹ thuật này dựa trên các mô hình toán học phức tạp và cung cấp các kết quả khá chính xác, đặc biệt khi các phép đo thực nghiệm khó thực hiện.
Các phương pháp đo lường này đều có ưu nhược điểm riêng, và việc lựa chọn phương pháp phù hợp phụ thuộc vào yêu cầu chính xác, tính chất của mẫu vật, và điều kiện thực nghiệm.

7. Ứng Dụng Thực Tiễn của Ái Lực Electron
Ái lực electron là một khái niệm không chỉ có giá trị lý thuyết mà còn có nhiều ứng dụng thực tiễn trong các lĩnh vực khác nhau. Dưới đây là một số ứng dụng chính của ái lực electron:
- Trong công nghệ vật liệu:
Ái lực electron được sử dụng để thiết kế và tối ưu hóa các vật liệu bán dẫn, đặc biệt là trong ngành công nghiệp vi điện tử. Ái lực electron giúp xác định tính chất dẫn điện của vật liệu, ảnh hưởng đến hiệu suất của các thiết bị điện tử như diode, transistor, và các cảm biến.
- Trong hóa học tổng hợp:
Ái lực electron đóng vai trò quan trọng trong việc dự đoán tính chất phản ứng của các nguyên tố và hợp chất. Hiểu biết về ái lực electron giúp các nhà hóa học phát triển các phương pháp tổng hợp mới, cải thiện hiệu suất và độ chọn lọc trong các phản ứng hóa học.
- Trong kỹ thuật môi trường:
Các phản ứng oxy hóa-khử trong môi trường được ảnh hưởng mạnh bởi ái lực electron của các nguyên tố. Ví dụ, quá trình xử lý nước và các biện pháp giảm thiểu ô nhiễm đều dựa vào việc điều chỉnh các phản ứng oxy hóa khử, nơi mà ái lực electron là một yếu tố quan trọng.
- Trong nghiên cứu y sinh học:
Ái lực electron cũng được ứng dụng trong việc phát triển các loại thuốc và liệu pháp điều trị mới. Việc hiểu rõ ái lực electron của các nguyên tố và phân tử giúp dự đoán tương tác giữa thuốc và các phân tử sinh học, tối ưu hóa hiệu quả điều trị.
- Trong công nghệ năng lượng:
Ái lực electron được sử dụng trong việc nghiên cứu và phát triển các vật liệu mới cho pin, pin nhiên liệu và các hệ thống lưu trữ năng lượng khác. Hiểu rõ về ái lực electron giúp tối ưu hóa khả năng lưu trữ và giải phóng năng lượng trong các thiết bị này.
Những ứng dụng này cho thấy tầm quan trọng của ái lực electron trong việc thúc đẩy sự phát triển của khoa học và công nghệ hiện đại.

8. Kết Luận
Ái lực electron, một khái niệm quan trọng trong hóa học và vật lý, đã chứng minh tầm quan trọng của nó trong nhiều lĩnh vực nghiên cứu khoa học. Qua các nội dung đã thảo luận, chúng ta có thể thấy rõ ràng rằng ái lực electron không chỉ đóng vai trò quan trọng trong việc xác định các tính chất hóa học và vật lý của nguyên tử mà còn góp phần quan trọng trong việc phát triển các công nghệ mới và nghiên cứu khoa học hiện đại.
Trước hết, sự hiểu biết về ái lực electron giúp chúng ta có thể dự đoán và điều chỉnh các phản ứng hóa học một cách chính xác hơn, đặc biệt là trong quá trình tổng hợp các vật liệu mới. Điều này đã và đang đóng góp không nhỏ vào sự tiến bộ trong lĩnh vực công nghệ bán dẫn và các ngành công nghiệp liên quan.
Hơn nữa, ái lực electron còn giúp chúng ta hiểu sâu hơn về cấu trúc và năng lượng của nguyên tử, từ đó mở ra những cơ hội mới trong nghiên cứu và ứng dụng khoa học. Các phương pháp đo lường và tính toán ái lực electron đã cung cấp cho các nhà nghiên cứu những công cụ mạnh mẽ để khám phá và khai thác tiềm năng của các nguyên tố và hợp chất mới.
Nhìn chung, sự tiến bộ trong việc nghiên cứu và ứng dụng ái lực electron không chỉ mang lại những hiểu biết sâu sắc hơn về thế giới vi mô mà còn mở ra những khả năng ứng dụng trong thực tiễn, từ việc cải thiện hiệu suất các thiết bị điện tử đến phát triển các phương pháp sản xuất công nghiệp hiệu quả hơn.
Trong tương lai, các nghiên cứu về ái lực electron hứa hẹn sẽ tiếp tục mang lại những khám phá quan trọng, giúp mở rộng kiến thức của chúng ta về cấu trúc vật chất và tăng cường khả năng ứng dụng trong nhiều lĩnh vực khác nhau của khoa học và công nghệ.