Chủ đề valence electron meaning: Valence electron, hay còn gọi là điện tử hóa trị, đóng vai trò quan trọng trong việc xác định cách các nguyên tử phản ứng hóa học. Bài viết này sẽ giải thích rõ về khái niệm valence electron, tầm quan trọng của chúng trong các phản ứng hóa học và ứng dụng thực tế của điện tử hóa trị trong đời sống và nghiên cứu khoa học.
Mục lục
Valence Electron - Điện Tử Hóa Trị
Trong hóa học, điện tử hóa trị (valence electron) là các điện tử nằm ở lớp vỏ ngoài cùng của nguyên tử. Chúng đóng vai trò quan trọng trong việc hình thành liên kết hóa học, vì chúng là những điện tử tham gia vào các phản ứng hóa học.
Các Khái Niệm Liên Quan
- Lớp vỏ electron: Là các lớp mà các điện tử xoay quanh hạt nhân nguyên tử. Lớp vỏ ngoài cùng chứa các điện tử hóa trị.
- Cấu hình electron: Sắp xếp các điện tử trong các lớp vỏ và phân lớp của một nguyên tử.
- Liên kết hóa học: Là sự liên kết giữa các nguyên tử để tạo thành phân tử hoặc hợp chất. Liên kết có thể là liên kết cộng hóa trị, liên kết ion, hoặc liên kết kim loại.
Tầm Quan Trọng Của Điện Tử Hóa Trị
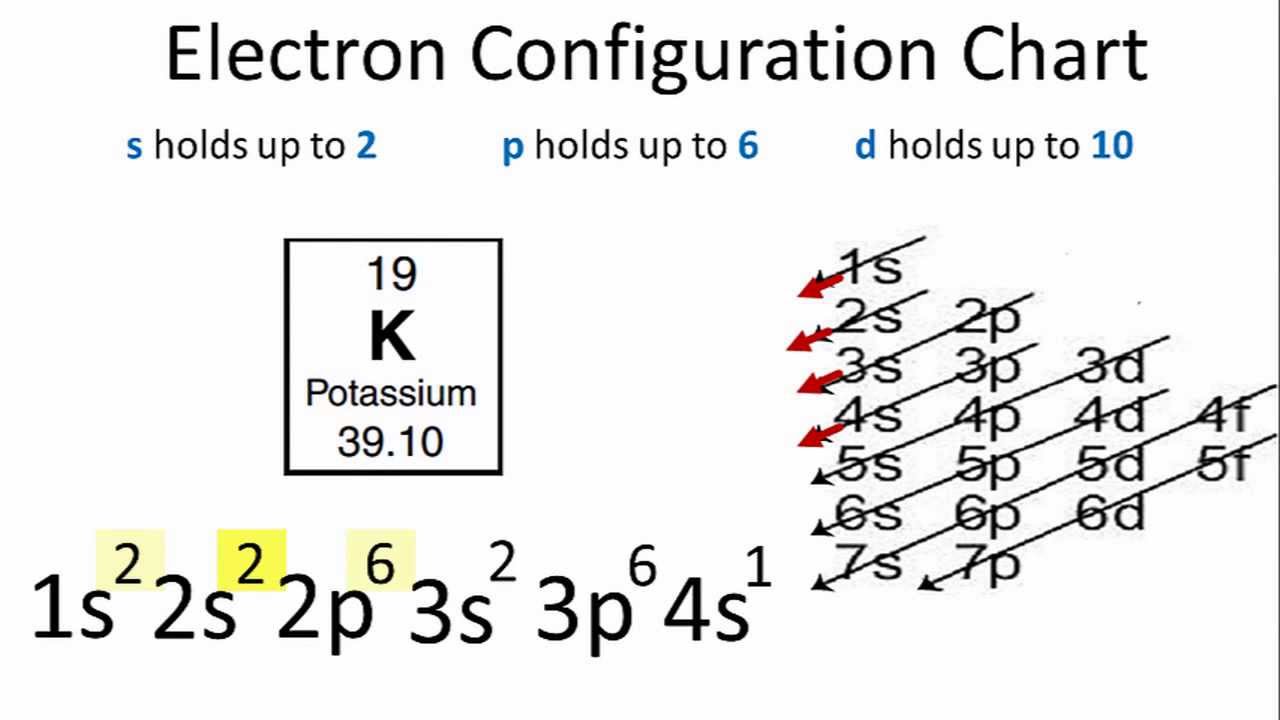
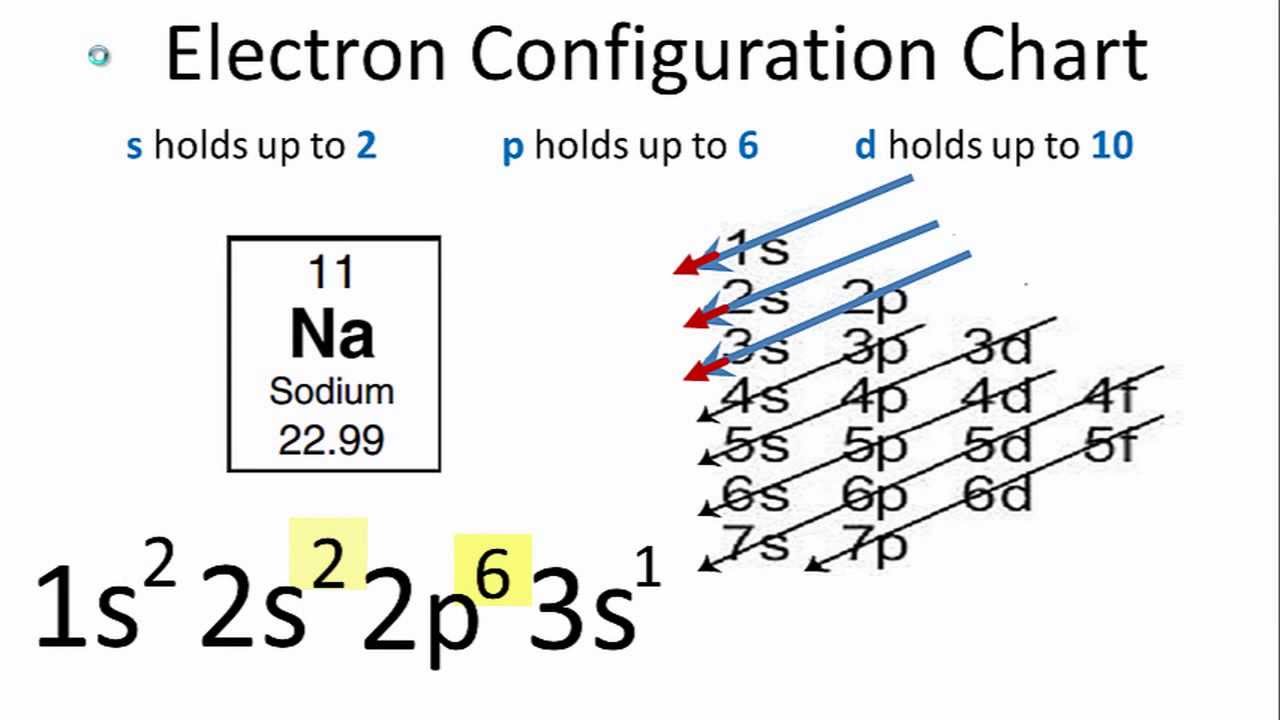
Điện tử hóa trị quyết định cách mà một nguyên tử phản ứng hóa học với các nguyên tử khác. Số lượng điện tử hóa trị cũng xác định hóa trị của nguyên tố, nghĩa là số lượng liên kết mà nguyên tử có thể hình thành. Ví dụ, nguyên tử natri có một điện tử hóa trị, do đó, nó thường tạo một liên kết hóa học.
Ứng Dụng Trong Hóa Học
- Hiểu về điện tử hóa trị giúp dự đoán cấu trúc phân tử và tính chất của hợp chất hóa học.
- Giúp giải thích hiện tượng ion hóa và năng lượng ion hóa trong các nguyên tử.
- Đóng vai trò quan trọng trong việc nghiên cứu phản ứng hóa học và cân bằng hóa học.
Bảng Một Số Nguyên Tố Và Số Điện Tử Hóa Trị
| Nguyên Tố | Số Điện Tử Hóa Trị |
| Hydro (H) | 1 |
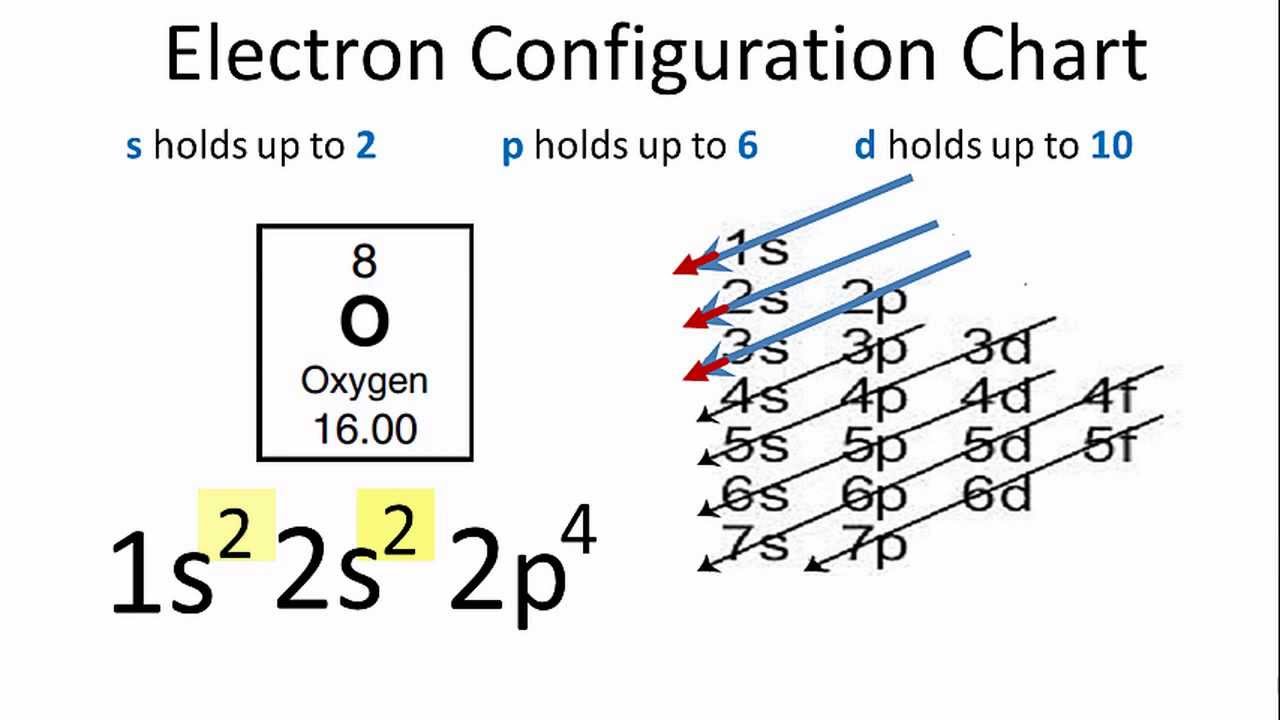
| Oxy (O) | 6 |
| Nitơ (N) | 5 |
| Clo (Cl) | 7 |
Qua đó, hiểu biết về điện tử hóa trị không chỉ quan trọng trong việc nghiên cứu hóa học lý thuyết mà còn ứng dụng rộng rãi trong các ngành công nghiệp và nghiên cứu khoa học.
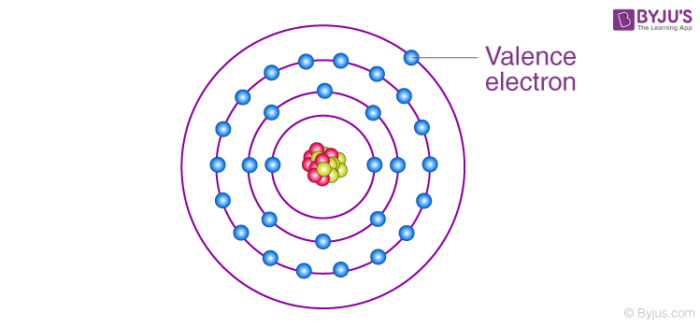
Khái Niệm Điện Tử Hóa Trị
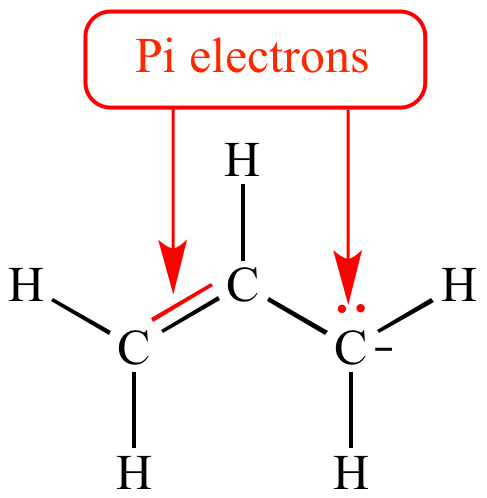
Điện tử hóa trị, hay còn gọi là valence electron, là các electron nằm ở lớp vỏ ngoài cùng của một nguyên tử. Những electron này chịu trách nhiệm cho các phản ứng hóa học vì chúng dễ dàng tương tác với các nguyên tử khác để hình thành liên kết.
- Lớp vỏ electron: Các electron trong nguyên tử được sắp xếp theo các lớp vỏ, và lớp ngoài cùng là nơi chứa các điện tử hóa trị.
- Liên kết hóa học: Điện tử hóa trị tham gia vào việc tạo ra liên kết hóa học, như liên kết cộng hóa trị và liên kết ion.
Việc xác định số lượng và cách sắp xếp của các điện tử hóa trị giúp giải thích tính chất hóa học của nguyên tố cũng như dự đoán được các phản ứng hóa học mà nguyên tố đó có thể tham gia.
Tầm Quan Trọng Của Điện Tử Hóa Trị Trong Hóa Học
Điện tử hóa trị đóng vai trò trung tâm trong việc xác định tính chất hóa học và khả năng phản ứng của các nguyên tố. Những electron này là yếu tố chính quyết định cách mà một nguyên tử tương tác với các nguyên tử khác, từ đó hình thành liên kết hóa học.
- Liên kết hóa học: Điện tử hóa trị tham gia trực tiếp vào việc hình thành các liên kết cộng hóa trị và ion, ảnh hưởng đến cấu trúc phân tử và tính chất của các hợp chất.
- Dự đoán phản ứng hóa học: Hiểu về điện tử hóa trị giúp nhà khoa học dự đoán các phản ứng có thể xảy ra, từ đó phát triển các hợp chất mới.
Vì vậy, kiến thức về điện tử hóa trị không chỉ là nền tảng của hóa học mà còn có ứng dụng rộng rãi trong nghiên cứu khoa học và công nghiệp.

Phân Bố Điện Tử Trong Nguyên Tử
Trong một nguyên tử, các electron được phân bố theo các lớp vỏ electron, mỗi lớp chứa một số lượng electron nhất định. Các lớp vỏ này được ký hiệu bằng các số nguyên từ 1 đến n, với lớp vỏ gần hạt nhân nhất có năng lượng thấp nhất.
- Lớp vỏ K: Lớp đầu tiên, chứa tối đa 2 electron.
- Lớp vỏ L: Lớp thứ hai, chứa tối đa 8 electron.
- Lớp vỏ M: Lớp thứ ba, chứa tối đa 18 electron.
- Lớp vỏ N: Lớp thứ tư, chứa tối đa 32 electron.
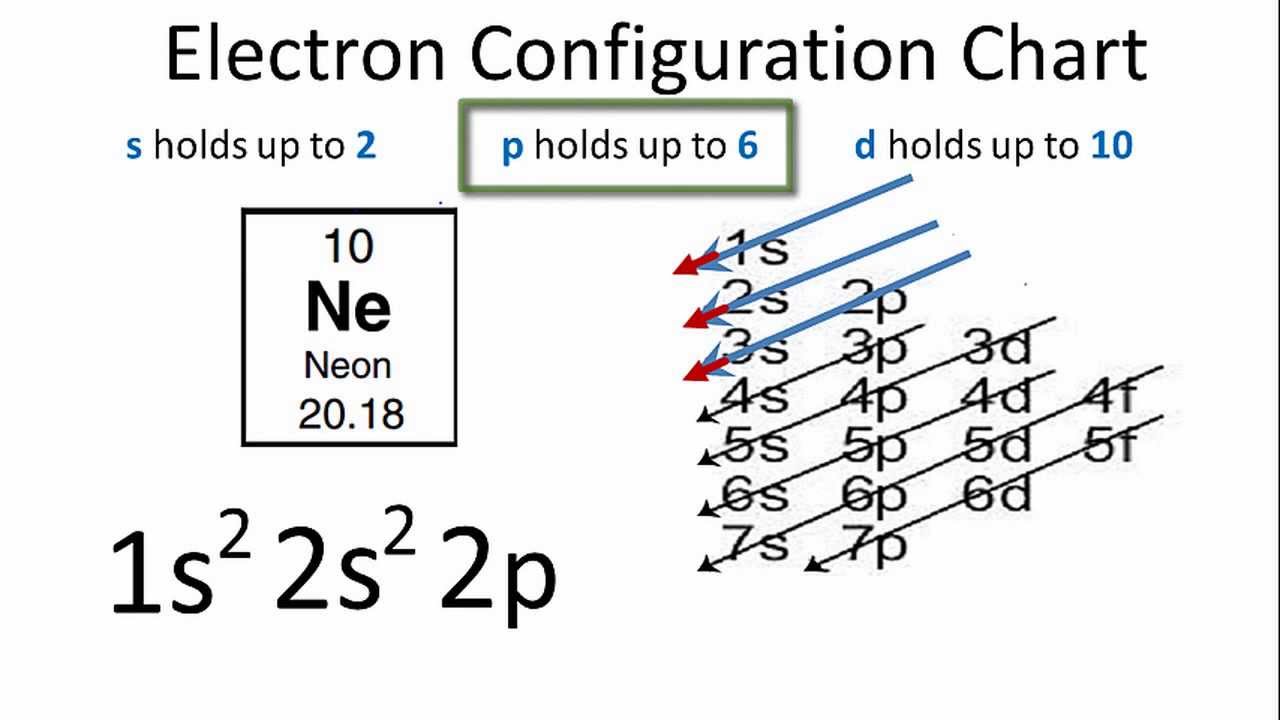
Các electron trong lớp vỏ ngoài cùng, được gọi là điện tử hóa trị, là những electron có năng lượng cao nhất và tham gia vào các phản ứng hóa học.

Ứng Dụng Thực Tiễn Của Điện Tử Hóa Trị
Điện tử hóa trị đóng vai trò quan trọng trong nhiều lĩnh vực khoa học và công nghiệp. Dưới đây là một số ứng dụng thực tiễn:
- Dự đoán phản ứng hóa học: Số lượng và cấu hình điện tử hóa trị giúp nhà hóa học dự đoán cách nguyên tử sẽ phản ứng trong các phản ứng hóa học.
- Thiết kế vật liệu mới: Hiểu về điện tử hóa trị cho phép các nhà khoa học thiết kế và phát triển các vật liệu mới với tính chất cụ thể, chẳng hạn như chất bán dẫn trong công nghệ điện tử.
- Phân tích hóa học: Phương pháp phân tích hóa học sử dụng kiến thức về điện tử hóa trị để xác định cấu trúc phân tử và thành phần của hợp chất.
- Nghiên cứu dược phẩm: Trong ngành dược phẩm, điện tử hóa trị được sử dụng để nghiên cứu tương tác giữa thuốc và cơ thể, từ đó phát triển các loại thuốc hiệu quả hơn.
Những ứng dụng này cho thấy vai trò thiết yếu của điện tử hóa trị trong việc thúc đẩy tiến bộ khoa học và công nghệ.

Ví Dụ Cụ Thể Về Điện Tử Hóa Trị
Điện tử hóa trị đóng vai trò quan trọng trong việc xác định tính chất hóa học của nguyên tố và cách chúng tham gia vào các phản ứng hóa học. Dưới đây là một số ví dụ cụ thể về cách điện tử hóa trị ảnh hưởng đến hành vi của các nguyên tố trong các tình huống thực tế:
1. Điện Tử Hóa Trị Trong Các Nguyên Tố Phổ Biến
- Natri (Na): Natri có số nguyên tử là 11, với cấu hình electron là \(2,8,1\). Điều này có nghĩa là Natri có một điện tử hóa trị trong lớp vỏ ngoài cùng. Để đạt được cấu hình bền vững giống như khí hiếm gần nhất (Neon), Natri dễ dàng mất đi một điện tử hóa trị, tạo ra ion Na+ với điện tích dương. Do đó, Natri rất dễ tham gia vào các phản ứng hóa học, đặc biệt là phản ứng tạo muối khi kết hợp với các halogen.
- Oxi (O): Oxi có số nguyên tử là 8 và cấu hình electron là \(2,6\). Với sáu điện tử hóa trị, Oxi cần thêm hai điện tử nữa để hoàn thành octet, khiến nó có xu hướng nhận thêm điện tử từ các nguyên tố khác. Điều này giải thích vì sao Oxi thường có số oxi hóa -2 trong các hợp chất, như trong nước (H2O) hoặc dioxide carbon (CO2).
- Cacbon (C): Cacbon có bốn điện tử hóa trị (cấu hình electron là \(2,4\)), cho phép nó tạo ra bốn liên kết cộng hóa trị với các nguyên tố khác. Điều này giải thích sự đa dạng trong hóa học hữu cơ, nơi cacbon tạo thành các mạch và vòng carbon phức tạp, như trong các hợp chất hữu cơ và polymer.
2. Bảng Số Điện Tử Hóa Trị Của Một Số Nguyên Tố
| Nguyên Tố | Số Nguyên Tử | Cấu Hình Electron | Số Điện Tử Hóa Trị | Valency (Hóa Trị) |
|---|---|---|---|---|
| Hydro (H) | 1 | 1 | 1 | 1 |
| Helium (He) | 2 | 2 | 2 | 0 |
| Carbon (C) | 6 | 2,4 | 4 | 4 |
| Nitơ (N) | 7 | 2,5 | 5 | 3 |
| Oxy (O) | 8 | 2,6 | 6 | 2 |
| Sodium (Na) | 11 | 2,8,1 | 1 | 1 |
| Magnesium (Mg) | 12 | 2,8,2 | 2 | 2 |
Những ví dụ và bảng số trên cho thấy rõ cách điện tử hóa trị ảnh hưởng đến khả năng tham gia phản ứng hóa học và tính chất của các nguyên tố. Hiểu biết về điện tử hóa trị giúp dự đoán và giải thích được nhiều hiện tượng hóa học quan trọng trong thực tiễn.