Chủ đề potassium electron configuration: Potassium electron configuration (cấu hình electron của Kali) đóng vai trò quan trọng trong hiểu biết về nguyên tố hóa học này. Bài viết sẽ cung cấp cái nhìn tổng quan từ cấu hình electron cơ bản đến ứng dụng thực tế của Kali trong đời sống, từ nông nghiệp, y học đến công nghiệp. Đừng bỏ lỡ nếu bạn muốn tìm hiểu chi tiết về một trong những kim loại kiềm phổ biến nhất.
Mục lục
Cấu Hình Electron Của Kali (K)
Kali (K) là một nguyên tố hóa học nằm trong nhóm kim loại kiềm của bảng tuần hoàn. Với số hiệu nguyên tử là 19, kali có cấu hình electron khá đơn giản, tuy nhiên lại rất quan trọng trong nhiều ứng dụng hóa học và sinh học.
Thông Tin Chung Về Kali
- Ký hiệu hóa học: K
- Số hiệu nguyên tử: 19
- Khối lượng nguyên tử: 39.10 u
- Vị trí trong bảng tuần hoàn: Nhóm 1 (Kim loại kiềm), Chu kỳ 4
- Trạng thái: Rắn ở điều kiện thường, màu trắng bạc
Cấu Hình Electron Của Nguyên Tử Kali
Cấu hình electron đầy đủ của nguyên tử kali được viết như sau:
Cấu hình này cho thấy kali có 19 electron phân bố trong các lớp vỏ và phân lớp electron khác nhau.
Cấu Hình Electron Thu Gọn
Để viết cấu hình electron một cách ngắn gọn hơn, ta có thể biểu diễn như sau:
Ký hiệu [Ar] đại diện cho cấu hình electron của nguyên tố argon (18 electron), sau đó thêm 1 electron ở phân lớp 4s.
Ứng Dụng Của Kali
Kali đóng vai trò quan trọng trong nhiều lĩnh vực khác nhau như:
- Sinh học: Kali là một ion thiết yếu trong cơ thể, đặc biệt là trong hoạt động của tế bào thần kinh và cơ.
- Nông nghiệp: Kali là một thành phần chính trong phân bón, giúp tăng cường sự phát triển của cây trồng.
- Công nghiệp: Kali được sử dụng trong sản xuất xà phòng, thủy tinh, và nhiều hợp chất hóa học khác.
Tính Chất Hóa Học
Với 1 electron lớp ngoài cùng (valence electron), kali dễ dàng mất đi electron này để tạo thành ion K+. Tính chất này giúp nó dễ dàng tạo ra các hợp chất như KCl (muối kali clorua) khi kết hợp với các anion.
Lịch Sử Phát Hiện
Kali được phát hiện bởi nhà hóa học người Anh, Humphry Davy, vào năm 1807 thông qua phương pháp điện phân kali hiđroxit (KOH). Từ đó, nguyên tố này đã trở thành một phần quan trọng trong hóa học hiện đại.
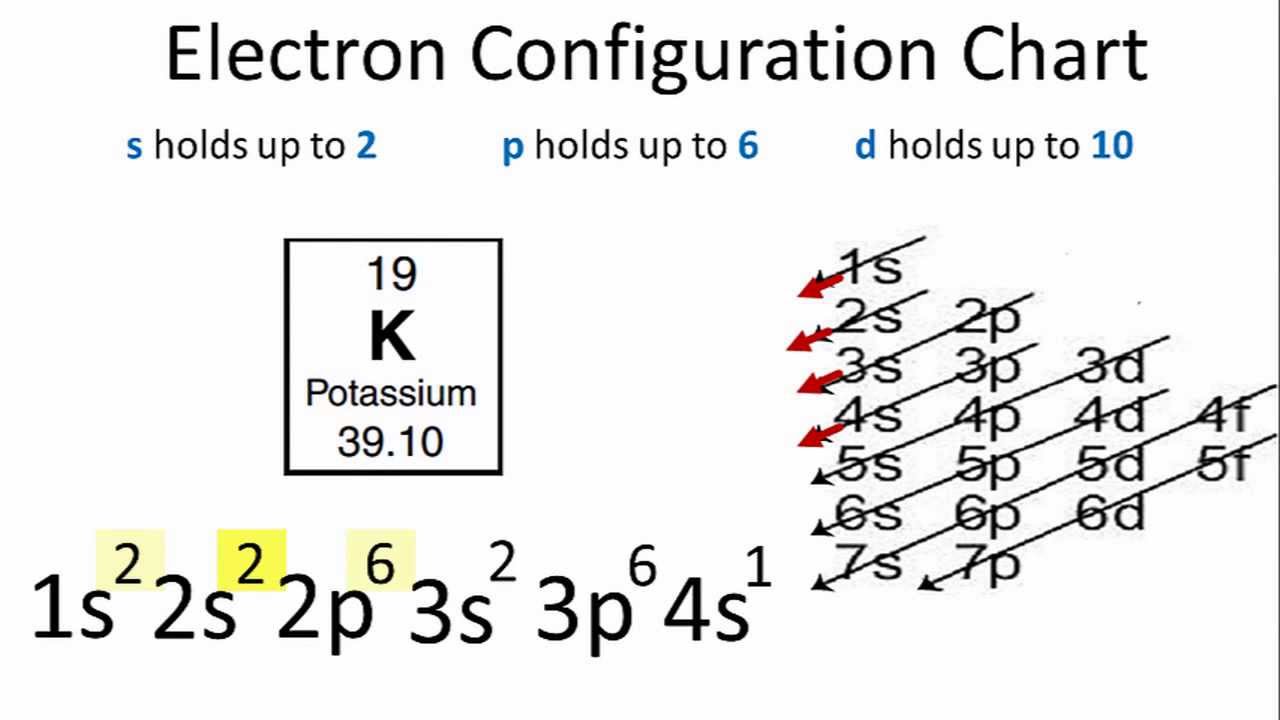
Tổng quan về Kali
Kali (K) là một nguyên tố hóa học thuộc nhóm kim loại kiềm với số nguyên tử là 19. Trong tự nhiên, Kali tồn tại dưới dạng muối ion và là một thành phần quan trọng trong nhiều hợp chất hóa học. Đặc tính nổi bật của Kali là phản ứng mạnh khi tiếp xúc với nước, tạo ra nhiệt lượng lớn đến mức đốt cháy khí hydro phát ra. Hơn nữa, Kali được biết đến là một kim loại mềm, dễ cắt, và bị oxy hóa nhanh khi tiếp xúc với không khí.
Trong bảng tuần hoàn, cấu hình electron của Kali ở trạng thái cơ bản là 1s22s22p63s23p64s1. Điều này cho thấy Kali có một electron đơn độc trong lớp vỏ ngoài cùng, dễ dàng bị mất đi để tạo thành ion K+ trong các phản ứng hóa học. Với đặc điểm này, Kali tham gia tích cực vào các phản ứng hình thành muối và các hợp chất ion khác, đóng vai trò thiết yếu trong nhiều lĩnh vực công nghiệp và sinh học.
- Kali là một trong những kim loại nhẹ nhất và có nhiệt độ nóng chảy thấp.
- Kali được lưu trữ dưới dạng lỏng không phản ứng như parafin để ngăn ngừa oxy hóa.
- Về mặt ứng dụng, Kali được sử dụng trong các tế bào quang điện và sản xuất phân bón.
Cấu hình electron chi tiết của Kali
Kali (K) có số nguyên tử là 19, do đó cấu hình electron của nó bao gồm 19 electron. Kali thuộc nhóm kim loại kiềm trong bảng tuần hoàn và có một electron duy nhất ở lớp vỏ ngoài cùng, điều này giúp Kali dễ dàng tạo thành ion K+ khi mất electron này.
Dưới đây là cấu hình electron chi tiết của Kali:
- Lớp thứ nhất: 1s2
- Lớp thứ hai: 2s22p6
- Lớp thứ ba: 3s23p6
- Lớp thứ tư: 4s1
Vì Kali chỉ có một electron ở lớp vỏ ngoài cùng (4s1), nó dễ dàng tham gia các phản ứng hóa học, đặc biệt là phản ứng với nước, tạo ra phản ứng mạnh và sinh ra khí hydro. Cấu hình electron này cũng có thể được viết gọn dưới dạng: [Ar]4s1, với [Ar] đại diện cho cấu hình của khí hiếm Argon.

Các đặc điểm của nguyên tố Kali
Kali (K) là một nguyên tố thuộc nhóm kim loại kiềm với số hiệu nguyên tử là 19 và nằm ở chu kỳ 4 trong bảng tuần hoàn. Nguyên tố này có đặc điểm là mềm, có màu xám bạc và có thể dễ dàng bị cắt bằng dao. Kali phản ứng mạnh với nước, tạo ra khí hydro và nhiệt lượng lớn, có thể gây cháy. Đặc tính này khiến nó phải được bảo quản trong dầu khoáng hoặc các môi trường không chứa oxy để tránh phản ứng với không khí.
Kali có độ âm điện thấp (khoảng 0.82 theo thang Pauling), điều này cho thấy nó có khả năng dễ dàng nhường electron, tạo thành cation K+. Trong tự nhiên, kali chủ yếu tồn tại dưới dạng hợp chất trong các khoáng chất và muối, được sử dụng nhiều trong công nghiệp phân bón nông nghiệp do vai trò quan trọng của nó đối với sự phát triển của cây trồng.
- Cấu trúc electron: Cấu hình electron của kali là [Ar] 4s1, với một electron ở lớp vỏ ngoài cùng.
- Tính chất vật lý: Nhiệt độ nóng chảy của kali là 63.5°C và nhiệt độ sôi là 759°C. Đây là một kim loại nhẹ với mật độ khoảng 0.86 g/cm3.
- Tính chất hóa học: Kali phản ứng mạnh với nước và các phi kim như oxy và clo, dễ dàng tạo thành các hợp chất như KOH (kali hydroxide) và KCl (kali chloride).
Nhờ các đặc tính này, kali không chỉ đóng vai trò quan trọng trong ngành công nghiệp mà còn rất cần thiết cho nhiều quá trình sinh học, đặc biệt trong hệ thống thần kinh và cơ bắp của sinh vật.

Thông tin liên quan đến Kali
Kali (Potassium) là một nguyên tố thuộc nhóm kim loại kiềm (alkali metals) trên bảng tuần hoàn với ký hiệu hóa học là K và số nguyên tử 19. Kali được phát hiện lần đầu bởi Humphry Davy vào năm 1807 thông qua phương pháp điện phân kali hydroxit. Kali tồn tại chủ yếu dưới dạng hợp chất, đóng vai trò quan trọng trong nhiều lĩnh vực từ nông nghiệp đến công nghiệp và sinh học. Nguyên tố này có tính chất đặc trưng là mềm, dễ cắt, và phản ứng mạnh với nước.
- Ký hiệu hóa học: K
- Số nguyên tử: 19
- Phân nhóm: Kim loại kiềm
- Nhiệt độ nóng chảy: 63,55°C
- Cấu hình electron: [Ar] 4s1
Trong cơ thể sinh vật, kali là một yếu tố thiết yếu giúp điều chỉnh áp suất thẩm thấu và hỗ trợ quá trình truyền xung thần kinh. Trong nông nghiệp, kali là thành phần quan trọng trong phân bón, đóng góp vào sự phát triển của cây trồng. Công nghiệp khai thác kali tập trung chủ yếu ở các quốc gia như Canada, Nga và Belarus.