Chủ đề na electron configuration: Cấu hình electron của Natri (Na) là một khái niệm quan trọng trong hóa học, giúp hiểu rõ hơn về tính chất và ứng dụng của nguyên tố này. Bài viết này sẽ cung cấp hướng dẫn chi tiết về cấu hình electron của Na, cùng với các ứng dụng thực tiễn trong công nghiệp và đời sống hàng ngày.
Mục lục
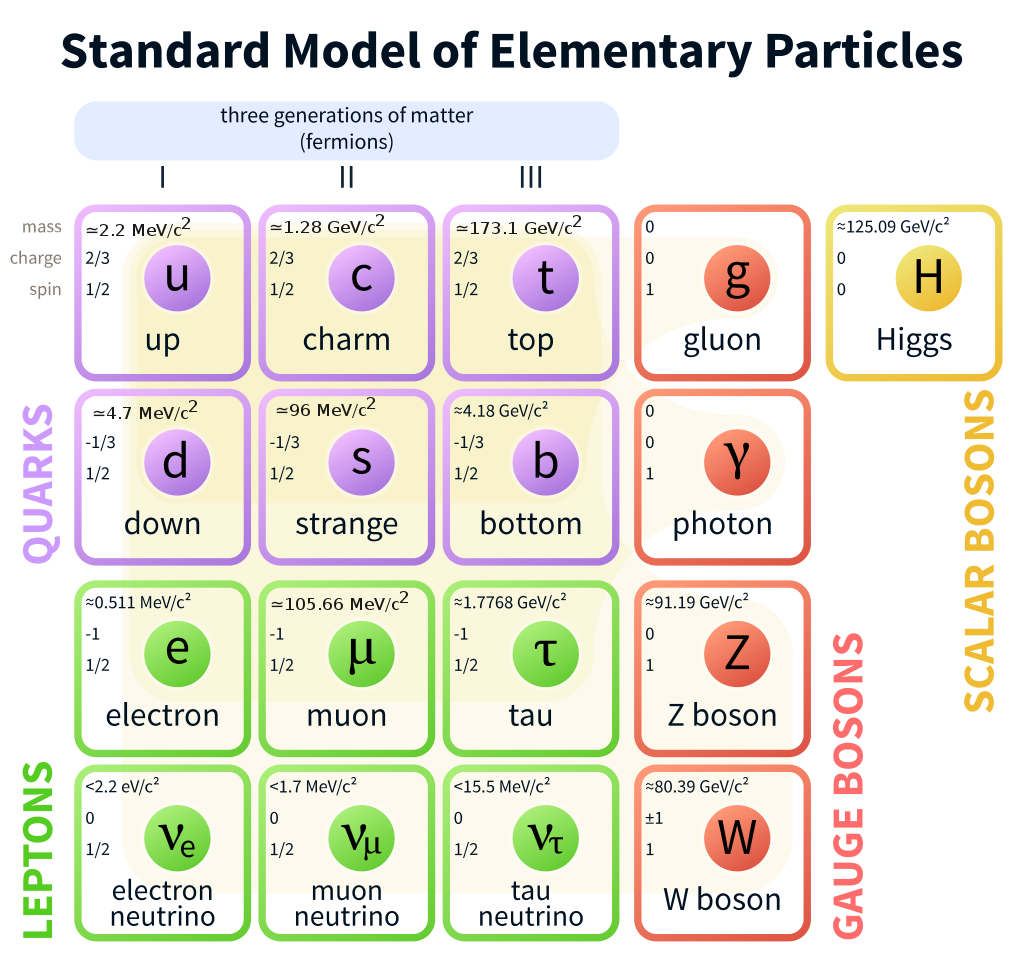
Cấu hình electron của Natri (Na)
Natri (Na) là nguyên tố hóa học có số hiệu nguyên tử là 11. Dưới đây là cấu hình electron chi tiết của Natri, cùng với các thông tin liên quan đến vị trí trong bảng tuần hoàn và tính chất hóa học của nguyên tố này.
1. Cấu hình electron của Natri
Cấu hình electron của Natri được viết đầy đủ như sau:
Viết gọn: [Ne] 3s1
2. Sơ đồ orbital của Natri
Sơ đồ orbital cho Natri như sau:
| 1s | ↑↓ |
| 2s | ↑↓ |
| 2p | ↑↓ ↑↓ ↑↓ |
| 3s | ↑ |
3. Vị trí của Natri trong bảng tuần hoàn
- Ô nguyên tố: 11
- Chu kỳ: 3
- Nhóm: IA
- Loại nguyên tố: Kim loại kiềm
4. Tính chất hóa học của Natri
Natri là một kim loại hoạt động mạnh do có 1 electron ở lớp ngoài cùng. Khi tham gia phản ứng hóa học, Natri có xu hướng nhường electron này để đạt cấu hình bền vững của neon (Ne), tạo thành ion Na+.
5. Công thức hóa học của hợp chất Natri
- Oxit cao nhất: Na2O (oxit bazơ)
- Hidroxit tương ứng: NaOH (bazơ mạnh)
6. Bài tập ví dụ
Nguyên tố M có cấu hình electron ở phân lớp ngoài cùng là 2p6. Vị trí của nguyên tố này trong bảng tuần hoàn là:
- Chu kỳ 2, nhóm VIA
- Chu kỳ 2, nhóm VIIIA
- Chu kỳ 3, nhóm VIIA
- Chu kỳ 3, nhóm IA
Đáp án: D (Chu kỳ 3, nhóm IA)
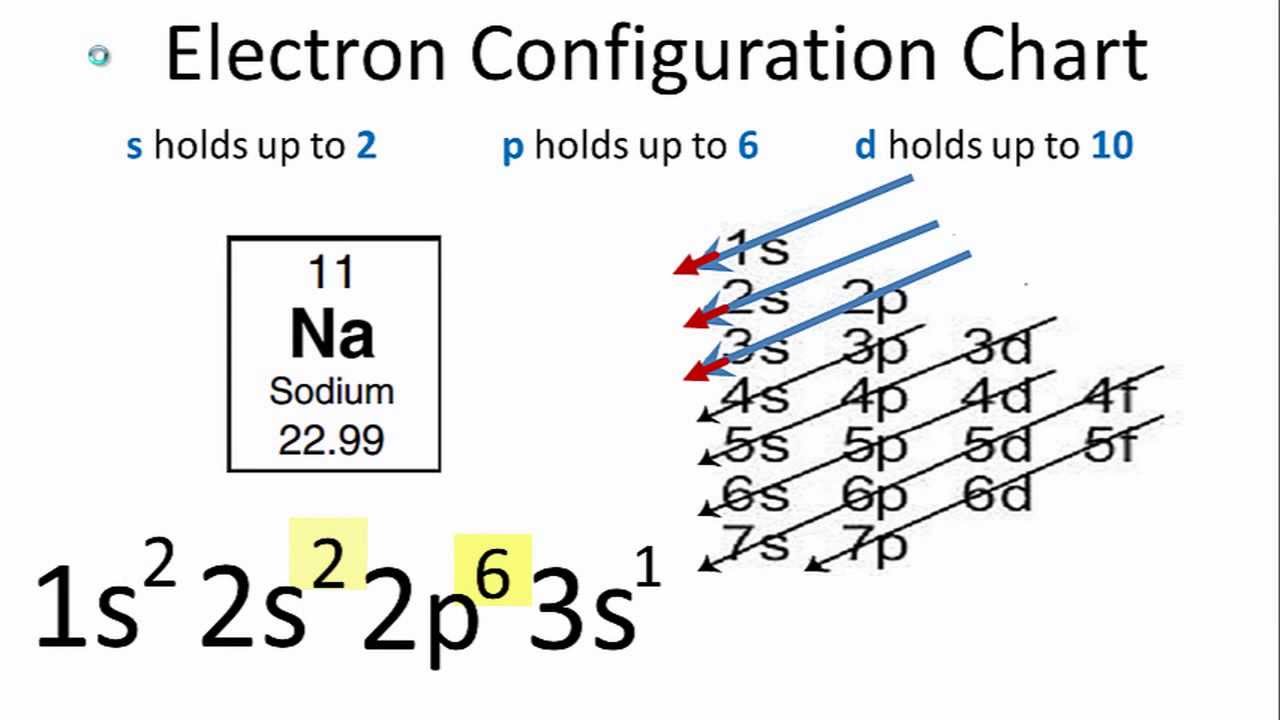
1. Giới thiệu về Natri (Na)
Natri (ký hiệu hóa học: Na) là một nguyên tố kim loại kiềm thuộc nhóm IA trong bảng tuần hoàn, có số hiệu nguyên tử là 11. Được phát hiện lần đầu tiên vào năm 1807 bởi nhà hóa học Humphry Davy, Natri là một trong những nguyên tố phổ biến và đóng vai trò quan trọng trong nhiều lĩnh vực, từ hóa học đến công nghiệp và đời sống hàng ngày.
- Ký hiệu hóa học: Na
- Số hiệu nguyên tử: 11
- Khối lượng nguyên tử: 22.98976928 u
- Nhóm: IA (Kim loại kiềm)
- Chu kỳ: 3
- Màu sắc: Kim loại mềm, có màu trắng bạc
Natri tồn tại nhiều trong tự nhiên, chủ yếu dưới dạng muối hòa tan trong nước biển và các khoáng chất. Nhờ tính phản ứng mạnh, Natri không tồn tại dưới dạng nguyên tố tự do trong tự nhiên mà thường kết hợp với các nguyên tố khác. Đặc biệt, Natri là thành phần chính của muối ăn (NaCl), một chất vô cùng quan trọng trong dinh dưỡng và y học.
Trong ngành công nghiệp, Natri được sử dụng rộng rãi trong sản xuất xà phòng, chất tẩy rửa, và một số loại hợp kim. Ngoài ra, hợp chất của Natri còn được sử dụng trong các quá trình chế tạo thủy tinh, giấy, và trong công nghệ thực phẩm.
Cấu hình electron của Natri đóng vai trò quan trọng trong việc xác định tính chất hóa học của nguyên tố này. Cấu hình electron đầy đủ của Natri là:
Cấu hình này cho thấy Natri có một electron độc thân ở lớp vỏ ngoài cùng, làm cho nó rất dễ mất electron này trong các phản ứng hóa học để đạt cấu hình bền vững của khí hiếm gần nhất, Neon (Ne).
2. Cấu hình electron của Natri
Cấu hình electron của một nguyên tử là sự phân bố các electron trong các lớp vỏ nguyên tử. Đối với Natri (Na), nguyên tố này có tổng cộng 11 electron, được sắp xếp vào các lớp vỏ theo thứ tự mức năng lượng từ thấp đến cao.
2.1. Cấu hình electron đầy đủ của Natri
Cấu hình electron đầy đủ của Natri được viết như sau:
Điều này có nghĩa là:
- Lớp thứ nhất (n=1) có 2 electron trong phân lớp 1s.
- Lớp thứ hai (n=2) có 8 electron, gồm 2 electron trong phân lớp 2s và 6 electron trong phân lớp 2p.
- Lớp thứ ba (n=3) chỉ có 1 electron trong phân lớp 3s.
2.2. Cấu hình electron rút gọn của Natri
Cấu hình electron của Natri cũng có thể được viết dưới dạng rút gọn sử dụng cấu hình của khí hiếm gần nhất, Neon (Ne):
Trong đó, [Ne] đại diện cho cấu hình electron của Neon, tương đương với 1s22s22p6.
2.3. Sơ đồ orbital của Natri
Sơ đồ orbital cho Natri giúp minh họa cách sắp xếp các electron trong các orbital:
| 1s | ↑↓ |
| 2s | ↑↓ |
| 2p | ↑↓ ↑↓ ↑↓ |
| 3s | ↑ |
Ở đây, mỗi mũi tên biểu thị một electron, và cặp mũi tên ↑↓ trong một ô orbital cho thấy rằng các electron đang ghép đôi.
2.4. Ý nghĩa của cấu hình electron của Natri
Cấu hình electron này cho thấy Natri có một electron độc thân ở lớp vỏ ngoài cùng, điều này giải thích tại sao Natri rất dễ mất đi electron này để tạo thành ion Na+. Điều này cũng làm cho Natri trở thành một kim loại hoạt động mạnh, đặc biệt là trong các phản ứng hóa học với nước và không khí.

5. Ứng dụng của Natri trong thực tế
Natri là một nguyên tố có nhiều ứng dụng quan trọng trong cuộc sống hàng ngày và trong công nghiệp. Từ các ngành sản xuất cho đến y học và khoa học, Natri đóng một vai trò thiết yếu. Dưới đây là một số ứng dụng chính của Natri trong thực tế:
5.1. Trong công nghiệp hóa chất
- Sản xuất hợp chất Natri: Natri được sử dụng để sản xuất nhiều hợp chất quan trọng như Natri hydroxide (NaOH), Natri clorua (NaCl), và Natri carbonate (Na2CO3).
- Chất khử: Natri kim loại được dùng làm chất khử trong quá trình chiết xuất một số kim loại từ các hợp chất của chúng, chẳng hạn như trong sản xuất titan và zirconium.
5.2. Trong y học và sinh học
- Điều chỉnh cân bằng điện giải: Natri là một ion quan trọng trong cơ thể, giúp duy trì cân bằng nước và áp suất thẩm thấu trong tế bào.
- Thuốc và dược phẩm: Một số hợp chất của Natri, như Natri bicarbonate (NaHCO3), được sử dụng trong các loại thuốc để điều trị các vấn đề về tiêu hóa và làm thuốc kháng axit.
5.3. Trong sản xuất năng lượng
- Pin Natri-Sulfur: Natri được sử dụng trong loại pin Natri-Sulfur (NaS), một loại pin hiệu suất cao được ứng dụng trong lưu trữ năng lượng quy mô lớn.
- Lò phản ứng hạt nhân: Natri lỏng được dùng làm chất làm mát trong một số lò phản ứng hạt nhân do khả năng dẫn nhiệt tốt và điểm sôi cao.
5.4. Trong đời sống hàng ngày
- Gia vị và bảo quản thực phẩm: Natri clorua (muối ăn) là gia vị phổ biến nhất, được dùng rộng rãi trong chế biến và bảo quản thực phẩm.
- Chất tẩy rửa: Natri hydroxide (xút) được sử dụng trong sản xuất xà phòng và các chất tẩy rửa khác.
Nhờ những tính chất hóa học đặc biệt, Natri đã trở thành một nguyên tố không thể thiếu trong nhiều lĩnh vực, góp phần quan trọng vào sự phát triển của công nghiệp, y học, và đời sống hàng ngày.

6. Các bài tập về cấu hình electron của Natri
Để giúp các bạn học sinh nắm vững kiến thức về cấu hình electron của Natri, dưới đây là một số bài tập từ cơ bản đến nâng cao. Các bài tập này được thiết kế để bạn có thể thực hành và hiểu rõ hơn về cách viết và phân tích cấu hình electron của nguyên tố Natri (Na).
6.1. Bài tập cơ bản
- Bài 1: Viết cấu hình electron đầy đủ và rút gọn của nguyên tử Natri (Z = 11).
- Giải:
- Cấu hình electron đầy đủ: \(1s^2 2s^2 2p^6 3s^1\)
- Cấu hình electron rút gọn: \([Ne] 3s^1\)
- Bài 2: Xác định số electron độc thân trong nguyên tử Natri.
- Giải: Natri có 1 electron độc thân ở phân lớp 3s.
- Bài 3: Hãy xác định vị trí của Natri trong bảng tuần hoàn dựa vào cấu hình electron của nó.
- Giải: Natri nằm ở chu kỳ 3, nhóm IA trong bảng tuần hoàn.
6.2. Bài tập nâng cao
- Bài 1: Một cation có cấu hình electron là \(1s^2 2s^2 2p^6\). Hãy xác định nguyên tử ban đầu và viết cấu hình electron của nó.
- Giải: Cation này có 10 electron, vậy nguyên tử ban đầu có 11 electron (Natri), cấu hình electron của nó là \(1s^2 2s^2 2p^6 3s^1\).
- Bài 2: Nguyên tử X có tổng số electron trong các phân lớp s là 5. Hãy xác định nguyên tố X và viết cấu hình electron của nó.
- Giải: Nguyên tố X là Natri (Z = 11), có cấu hình electron là \(1s^2 2s^2 2p^6 3s^1\).
- Bài 3: Trong các ion sau đây: \(Na^+, Mg^{2+}, Al^{3+}\), ion nào có cấu hình electron giống khí hiếm? Hãy viết cấu hình electron của các ion đó.
- Giải: Tất cả các ion \(Na^+, Mg^{2+}, Al^{3+}\) đều có cấu hình electron giống khí hiếm Ne (\(1s^2 2s^2 2p^6\)).
Qua các bài tập trên, hy vọng bạn đã có thể củng cố kiến thức về cấu hình electron của Natri và ứng dụng chúng trong việc giải các bài tập hóa học. Hãy tiếp tục luyện tập để nắm vững hơn phần kiến thức quan trọng này!

7. Kết luận
Qua bài viết này, chúng ta đã cùng tìm hiểu về cấu hình electron của nguyên tố Natri (Na), từ cấu hình đầy đủ, cấu hình rút gọn đến cách biểu diễn theo ô orbital. Natri với cấu hình electron 1s2 2s2 2p6 3s1 thể hiện tính chất hóa học của một kim loại kiềm đặc trưng, dễ dàng nhường electron để đạt cấu hình bền vững của neon.
Các kiến thức về cấu hình electron của Natri không chỉ giúp chúng ta hiểu rõ hơn về bản chất của nguyên tố này mà còn mở ra nhiều ứng dụng thực tiễn trong công nghiệp và đời sống, như sản xuất kim loại natri, ứng dụng trong y học, và nhiều lĩnh vực khác. Đồng thời, qua phần bài tập, chúng ta có cơ hội củng cố và áp dụng kiến thức đã học vào thực tế, giúp nắm vững hơn về chủ đề này.
Hy vọng rằng, với những kiến thức đã học và luyện tập, bạn đọc sẽ cảm thấy tự tin hơn khi đối mặt với các vấn đề liên quan đến cấu hình electron, đặc biệt là đối với Natri. Tiếp tục khám phá và mở rộng hiểu biết của bạn về hóa học để áp dụng hiệu quả vào thực tế!