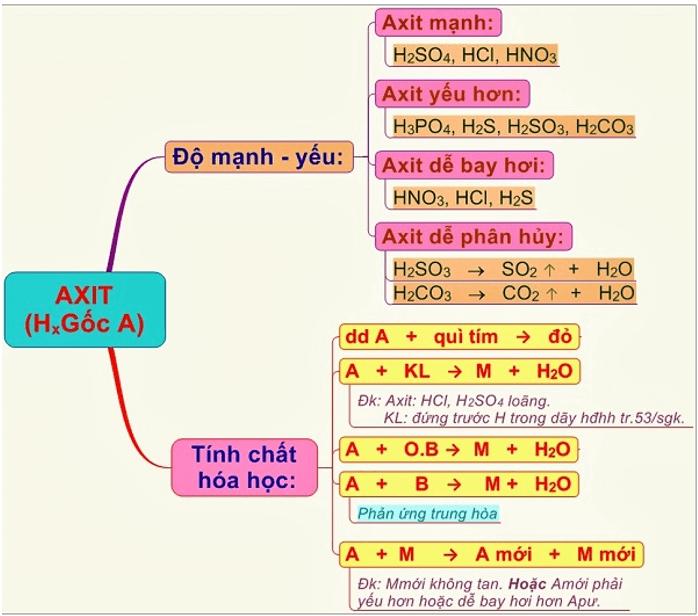
Sơ đồ tư duy tính chất hóa học của axit là một tài liệu hữu ích trong công tác giảng dạy và học tập của giáo viên và học sinh môn Hóa học lớp 9. Trong bài viết này, chúng ta sẽ tìm hiểu về axit, loại axit và tính chất của chúng.
Contents
1. Axit là gì?
- Axit là một hợp chất hóa học có công thức HxA, có vị chua và tan được trong nước để tạo ra dung dịch có nồng độ pH < 7. Độ pH càng lớn thì tính axit càng yếu và ngược lại.
- Axit cũng có thể được định nghĩa là các phân tử hoặc ion có khả năng nhường proton H+ cho bazo hoặc nhận các cặp electron không chia từ bazo.
2. Có những loại axit nào? Phân loại axit
Axit có thể được phân loại dựa vào một số tiêu chí như sau:
Bạn đang xem: Sơ đồ tư duy tính chất hóa học của axit
2.1. Dựa vào tính chất hóa học của axit
- Axit mạnh: Axit clohydric HCl, axit sulfuric H2SO4, axit nitric HNO3,…
- Axit yếu: Hydro sunfua H2S, axit cacbonic H2CO3,…
2.2. Dựa vào nguyên tử oxy
- Axit không có oxi: HCl, H2S, HBr, HI, HF…
- Axit có oxi: H2SO4, HNO3, H3PO4, H2CO3…
2.3. Phân loại khác
- Axit vô cơ: HCl, H2SO4, HNO3,…
- Axit hữu cơ – RCOOH: CH3COOH, HCOOH,…

3. Cách xác định độ mạnh, yếu của axit
- Độ mạnh, yếu của axit có thể xác định dựa vào sự linh động của nguyên tử Hydro trong axit đó. Nếu H càng linh động, tính axit càng mạnh và ngược lại.
- Với những axit có oxy trong cùng một nguyên tố, càng ít oxy, axit càng yếu.
- Với những axit của nguyên tố trong cùng chu kỳ, khi các nguyên tố ở hóa trị cao nhất, nguyên tố trung tâm có tính phi kim càng yếu thì axit đó càng yếu.
- Với axit của nguyên tố cùng nhóm A, tính axit có thể tăng dần hoặc giảm dần tùy vào có hay không có oxy.
- Với axit hữu cơ RCOOH, tính axit có thể giảm hoặc tăng tùy thuộc vào tính chất của gốc R.

4. Những tính chất của axit
4.1 Tính chất vật lý của axit
- Tan trong nước, có vị chua.
- Khi tiếp xúc với axit mạnh, có cảm giác đau nhói.
- Là chất điện li nên có thể dẫn điện.
4.2 Tính chất hóa học của axit
- Làm đổi màu chất chỉ thị (quỳ tím, giấy chỉ thị pH, dung dịch phenol phtalein).
- Tác dụng được với một số kim loại tạo thành muối và giải phóng hydro.
- Tác dụng với bazo tạo thành muối và nước.
- Tác dụng với oxit bazơ tạo thành muối + nước.
- Tác dụng với muối tạo muối mới và axit mới.
Axit axetic
- Công thức phân tử: C2H4O2
- Phân tử khối: 60
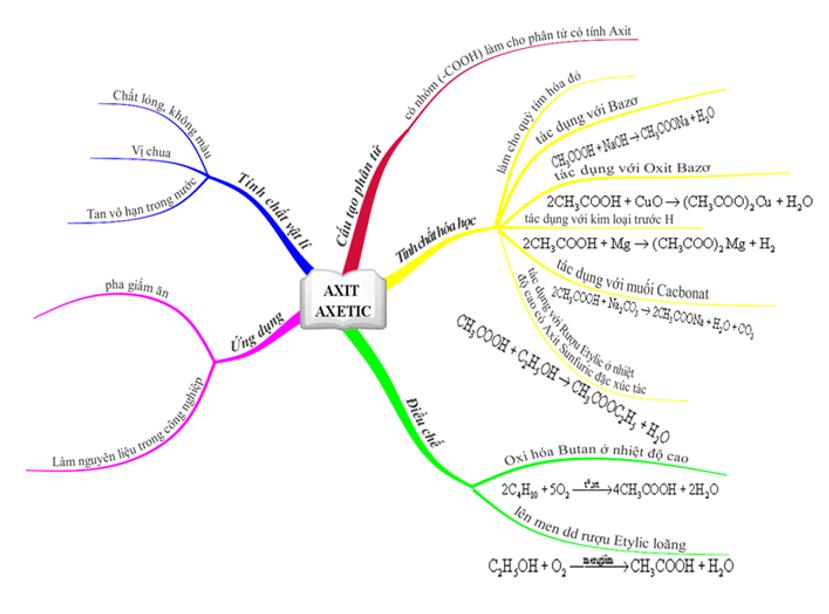
Tính chất vật lý của Axit axetic
- Axit axetic là chất lỏng, không màu, vị chua, tan vô hạn trong nước.
Cấu tạo phân tử của Axit axetic
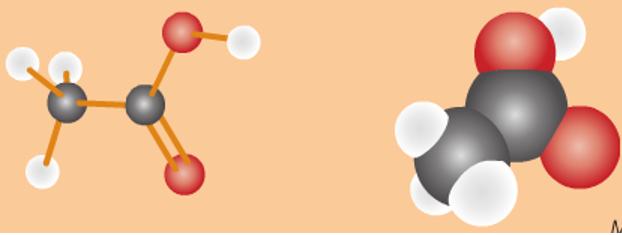
- Công thức rút gọn: CH3 – COOH
- Nhóm (-COOH) này làm cho phân tử có tính axit
Tính chất hóa học của Axit axetic
- Axit axetic là một axit hữu cơ mang tính chất của một axit. Tuy nhiên, axit axetic là một axit yếu.
- Làm hóa hồng quỳ tím.
- Tác dụng với kim loại: 2CH3COOH + Zn → (CH3COO)2Zn + H2↑ (có sủi bọt khí không màu).
- Tác dụng với bazơ: CH3COOH + NaOH → CH3COONa + H2O.
- Tác dụng với oxit bazơ: 2CH3COOH + CuO (bột, màu đen) → (CH3COO)2Cu + H2O (dung dịch Cu2+ màu xanh lam).
- Tác dụng với muối: 2CH3COOH + CaCO3 → (CH3COO)2Ca + CO2↑ + H2O.
Điều kiện xảy ra phản ứng
- Muối phản ứng là muối tan.
- Muối mới không tan trong axit mới.
- Sản phẩm có chứa một chất kết tủa hoặc bay hơi.

Bài tập minh họa
Xem thêm : Áp dụng sơ đồ tư duy vào học tập như nào cho hiệu quả?
Bài 1: Cho 180 gam axit axetic tác dụng với 138 gam rượu etylic (có xúc tác axit). Sau khi phản ứng hoàn toàn đã có 44% lượng axit chuyển thành este. Tính khối lượng các chất thu được sau phản ứng.
- Lượng axit axetic tham gia phản ứng là:
- Khối lượng axit axetic còn lại là: 180 – 79,2 = 108,8 (gam)
- Khối lượng rượu etylic còn lại là: 138 – 60,72 = 77,28 (gam)
- Khối lượng este thu được là: 116,16 (gam)
Ngoài Sơ đồ tư duy tính chất hóa học của axit đã được chúng tôi giới thiệu, mời các bạn cùng tham khảo thêm Chuyên đề Hóa học lớp 9, Trắc nghiệm Hóa học 9, Lý thuyết môn Hóa học lớp 9 để hoàn thành tốt chương trình học THCS.
Nguồn: https://ispacedanang.edu.vn
Danh mục: Học tư duy