Chủ đề cấu tạo nguyên tử của clo: Cấu tạo nguyên tử của Clo là một chủ đề quan trọng trong hóa học, đặc biệt là đối với học sinh và những người yêu thích môn khoa học này. Bài viết này sẽ giúp bạn khám phá sâu hơn về thành phần và tính chất của nguyên tử Clo, từ đó hiểu rõ hơn về vai trò của nó trong các phản ứng hóa học và ứng dụng thực tiễn.
Mục lục
- Cấu Tạo Nguyên Tử Của Clo
- Mục lục
- Cấu Trúc Của Nguyên Tử Clo
- Các Phản Ứng Hóa Học Của Clo
- Ứng Dụng Của Clo Trong Đời Sống Và Công Nghiệp
- Tác Động Của Clo Đến Sức Khỏe Và Môi Trường
- Các Phương Pháp Điều Chế Clo
- Cấu Trúc Của Nguyên Tử Clo
- Các Phản Ứng Hóa Học Của Clo
- Ứng Dụng Của Clo Trong Đời Sống Và Công Nghiệp
- Tác Động Của Clo Đến Sức Khỏe Và Môi Trường
- Các Phương Pháp Điều Chế Clo
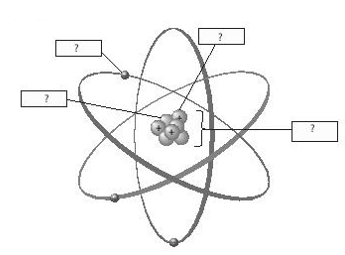
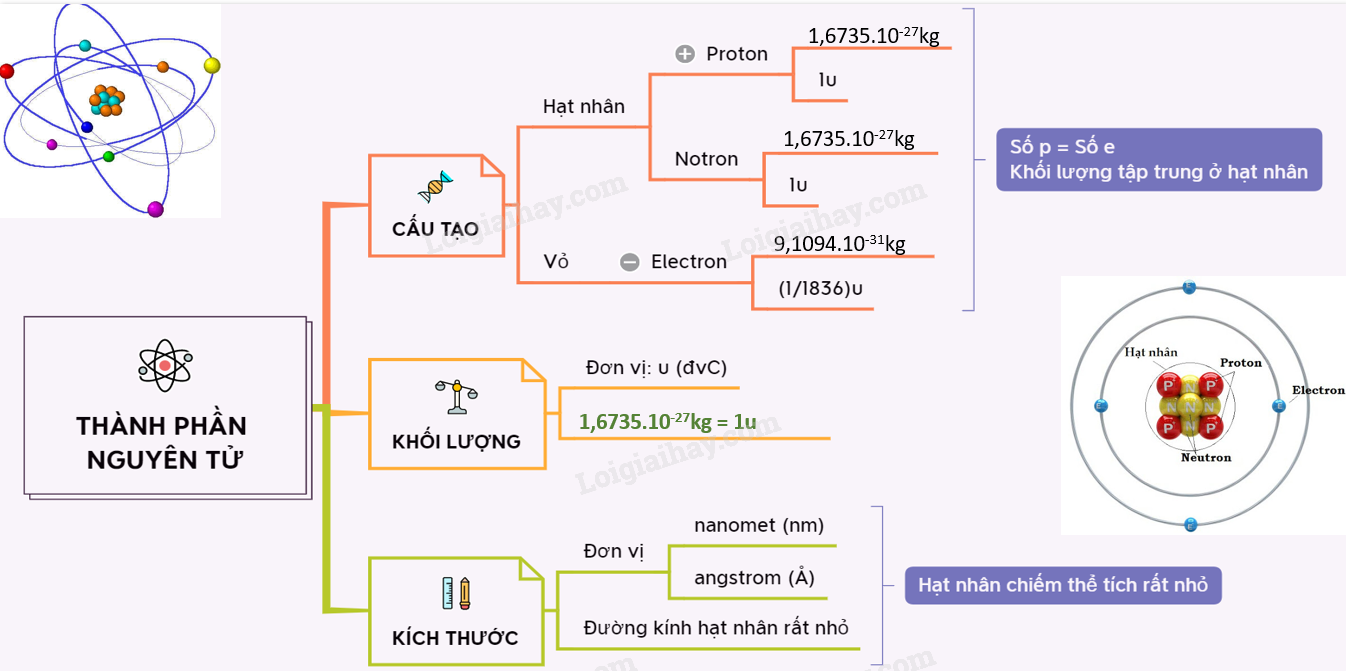
Cấu Tạo Nguyên Tử Của Clo
Nguyên tử của Clo là một trong những nguyên tử thuộc nhóm halogen, có cấu tạo tương đối đơn giản nhưng đóng vai trò quan trọng trong nhiều phản ứng hóa học. Dưới đây là một số thông tin chi tiết về cấu tạo của nguyên tử Clo.
1. Số Hiệu Nguyên Tử và Ký Hiệu Hóa Học
Nguyên tử Clo có số hiệu nguyên tử là 17 và được ký hiệu hóa học là Cl.
2. Cấu Hình Electron
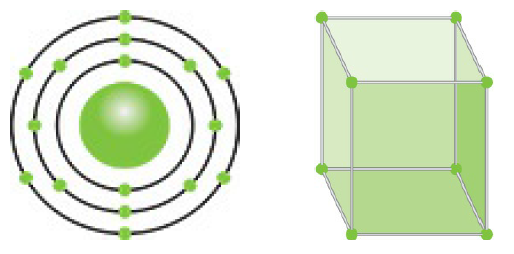
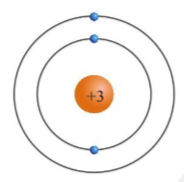
Nguyên tử Clo có tổng cộng 17 electron, được phân bố trên ba lớp vỏ electron theo cấu hình:
\[1s^2 2s^2 2p^6 3s^2 3p^5\]
Trong đó, lớp vỏ ngoài cùng (lớp thứ ba) chứa 7 electron, điều này làm cho Clo có xu hướng nhận thêm một electron để đạt cấu hình bền vững giống khí hiếm.
3. Số Proton và Neutron
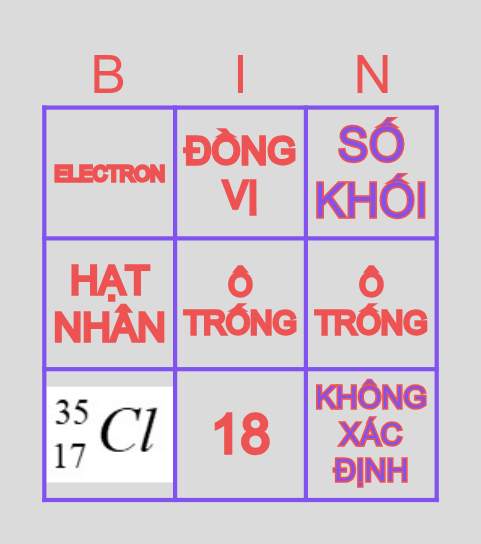
Nguyên tử Clo có 17 proton trong hạt nhân, tương ứng với số hiệu nguyên tử của nó. Số neutron trong Clo có thể khác nhau tùy thuộc vào đồng vị, nhưng đồng vị phổ biến nhất của Clo là \(\ce{^{35}Cl}\) có 18 neutron.
4. Đồng Vị của Clo
- \(\ce{^{35}Cl}\): Chiếm khoảng 75.77% tổng số Clo trong tự nhiên.
- \(\ce{^{37}Cl}\): Chiếm khoảng 24.23% còn lại.
Các đồng vị này có số neutron khác nhau nhưng đều có 17 proton.
5. Cấu Trúc Không Gian
Clo tồn tại ở trạng thái khí dưới dạng phân tử diatomic \(\ce{Cl2}\), với mỗi nguyên tử Clo chia sẻ một cặp electron với nguyên tử Clo còn lại, tạo thành liên kết cộng hóa trị đơn.
6. Ứng Dụng của Clo
Clo có nhiều ứng dụng quan trọng trong công nghiệp và đời sống, bao gồm:
- Tẩy trắng giấy, sợi và vải.
- Sát trùng trong xử lý nước thải và nước uống.
- Nguyên liệu trong sản xuất các hợp chất hữu cơ và vô cơ.
Nguyên tử Clo tuy nhỏ bé nhưng đóng góp lớn trong nhiều lĩnh vực khoa học và công nghiệp, là một yếu tố không thể thiếu trong đời sống hiện đại.
Mục lục
Cấu Trúc Của Nguyên Tử Clo
Thành phần của nguyên tử Clo
Sự phân bố electron trong các lớp vỏ
Tính chất hóa học của nguyên tử Clo
Nguyên tử Clo (Cl) có số hiệu nguyên tử là 17, bao gồm 17 proton, 17 electron và một số neutron thay đổi tùy vào đồng vị. Clo có hai đồng vị chính là \( \ce{Cl-35} \) và \( \ce{Cl-37} \).
Clo có cấu hình electron là \( 1s^2 2s^2 2p^6 3s^2 3p^5 \), nghĩa là có tổng cộng 7 electron ở lớp vỏ ngoài cùng, làm cho Clo có tính chất hóa học đặc trưng của một phi kim mạnh.
Clo có tính oxi hóa mạnh, dễ dàng nhận thêm 1 electron để đạt được cấu hình bền vững của khí hiếm. Clo tham gia vào nhiều phản ứng hóa học, đặc biệt là với kim loại, phi kim và nước.

Các Phản Ứng Hóa Học Của Clo
Phản ứng với kim loại
Phản ứng với phi kim
Phản ứng với nước
Clo phản ứng mạnh với kim loại để tạo thành muối halogenua, ví dụ như phản ứng với natri tạo ra natri clorua \( \ce{2Na + Cl2 → 2NaCl} \).
Clo có thể phản ứng với nhiều phi kim khác, chẳng hạn như hiđro \( \ce{H2 + Cl2 → 2HCl} \), hoặc với lưu huỳnh tạo thành lưu huỳnh clorua \( \ce{S + Cl2 → S2Cl2} \).
Khi sục khí Clo vào nước, Clo phản ứng tạo ra hỗn hợp axit clohidric (HCl) và axit hipoclorơ (HClO), có tính oxi hóa mạnh và khử khuẩn tốt.
Ứng Dụng Của Clo Trong Đời Sống Và Công Nghiệp
Công nghiệp hóa chất
Xử lý nước và môi trường
Sản xuất và bảo quản thực phẩm
Clo được sử dụng trong sản xuất nhiều hợp chất hóa học như PVC, clorua hữu cơ và vô cơ, dung môi công nghiệp như cacbon tetraclorua và dicloetan.
Clo là chất khử trùng quan trọng trong việc xử lý nước sinh hoạt và nước thải, giúp loại bỏ các vi khuẩn và tạp chất có hại.
Clo được dùng để tẩy trắng và sát trùng trong quá trình chế biến và bảo quản thực phẩm.

Tác Động Của Clo Đến Sức Khỏe Và Môi Trường
Tác động tích cực
Nguy cơ và tác động tiêu cực
Clo giúp bảo vệ sức khỏe con người thông qua việc khử khuẩn nước uống, nước sinh hoạt và làm sạch môi trường.
Khí Clo cực kỳ độc hại nếu hít phải, gây nguy cơ tổn thương hệ hô hấp. Ngoài ra, khi xả thải không kiểm soát, Clo có thể gây ô nhiễm môi trường.
XEM THÊM:
Các Phương Pháp Điều Chế Clo
Điều chế trong phòng thí nghiệm
Điều chế trong công nghiệp
Clo được điều chế trong phòng thí nghiệm bằng cách cho axit clohidric đặc tác dụng với các chất oxi hóa mạnh như mangan dioxit \( \ce{MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O} \).
Trong công nghiệp, Clo được điều chế thông qua quá trình điện phân dung dịch natri clorua \( \ce{2NaCl + 2H2O → 2NaOH + H2 + Cl2} \).
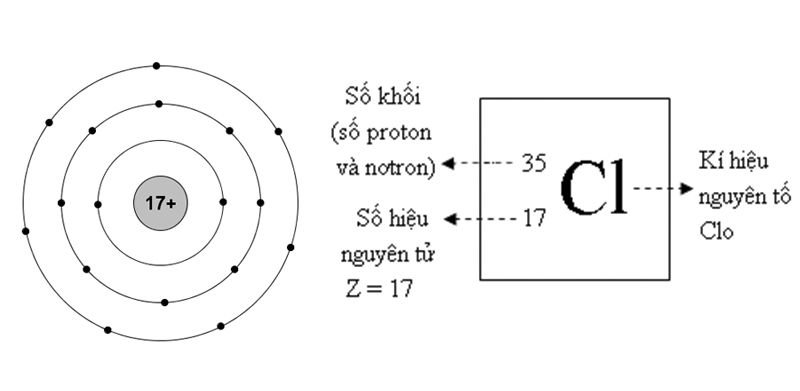
Cấu Trúc Của Nguyên Tử Clo
Nguyên tử Clo thuộc nhóm Halogen, có số hiệu nguyên tử là 17. Điều này có nghĩa là mỗi nguyên tử Clo có 17 proton trong hạt nhân. Clo có hai đồng vị chính là 35Cl và 37Cl, trong đó 35Cl chiếm khoảng 75% trong tự nhiên.
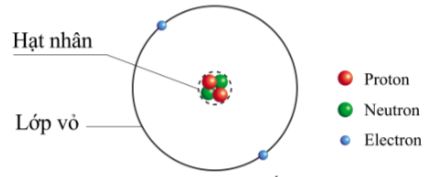
Cấu trúc của nguyên tử Clo bao gồm:
- Hạt nhân:
- Chứa 17 proton và số neutron tùy thuộc vào đồng vị. Đồng vị 35Cl có 18 neutron, trong khi đồng vị 37Cl có 20 neutron.
- Lớp vỏ electron:
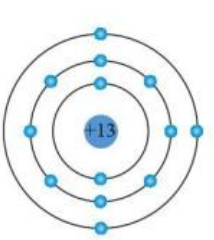
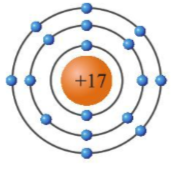
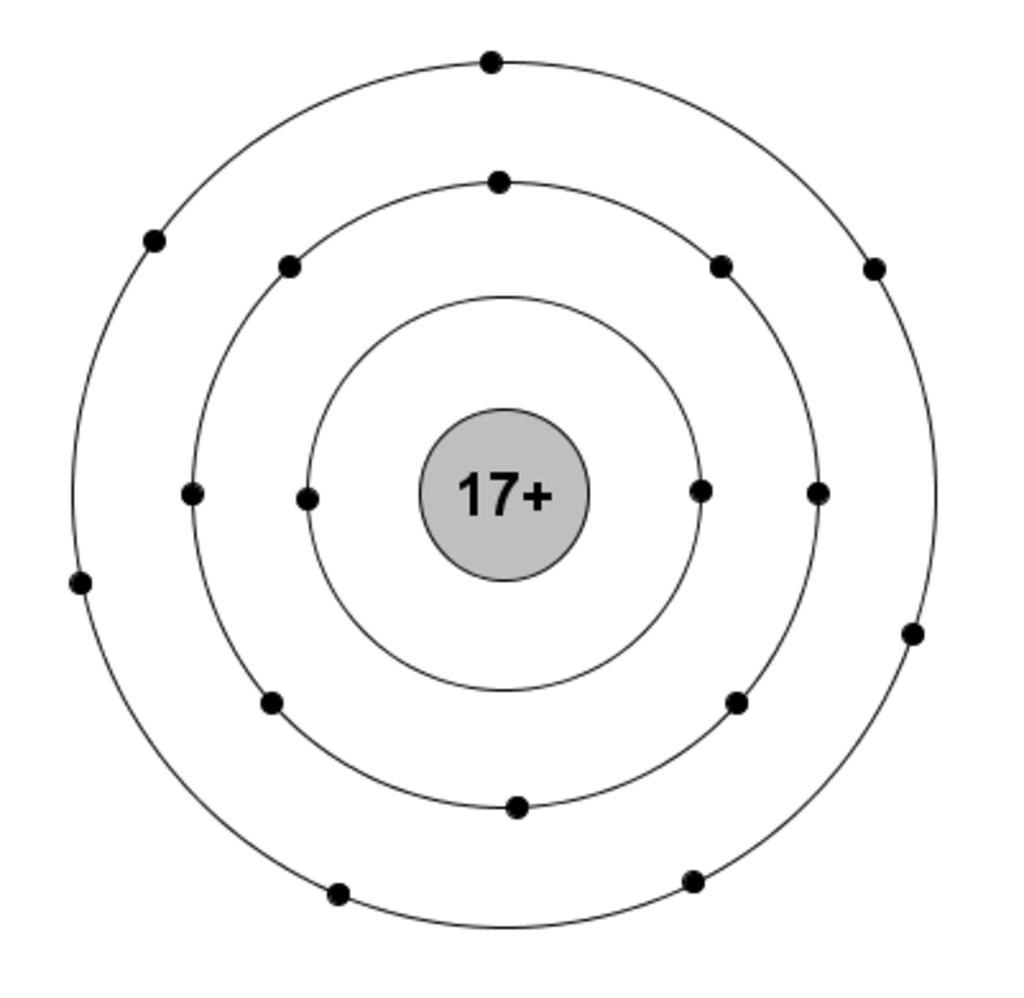
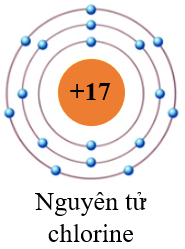
- Clo có 17 electron được phân bố trong 3 lớp vỏ:
- Lớp thứ nhất (K): 2 electron
- Lớp thứ hai (L): 8 electron
- Lớp thứ ba (M): 7 electron
Do có 7 electron ở lớp ngoài cùng, Clo có xu hướng nhận thêm 1 electron để đạt cấu hình bền vững của khí hiếm (tương tự như Argon), điều này làm cho Clo trở thành một phi kim có tính oxy hóa mạnh.
Một cách biểu diễn cấu trúc electron của Clo là:
\[ \text{Cl}: \, 1s^2 \, 2s^2 \, 2p^6 \, 3s^2 \, 3p^5 \]
Do tính chất hóa học mạnh, Clo thường tham gia vào nhiều phản ứng, đặc biệt là các phản ứng oxy hóa khử và phản ứng tạo liên kết với các nguyên tố khác để hình thành hợp chất.

Các Phản Ứng Hóa Học Của Clo
Clo (Cl2) là một phi kim hoạt động hóa học mạnh, tham gia nhiều phản ứng hóa học với các chất khác nhau. Dưới đây là một số phản ứng hóa học quan trọng của clo:
1. Phản ứng với Kim Loại
Clo phản ứng với hầu hết các kim loại để tạo thành muối clorua. Ví dụ:
- \[2Na + Cl_2 → 2NaCl\] (Clo phản ứng với natri tạo ra muối ăn).
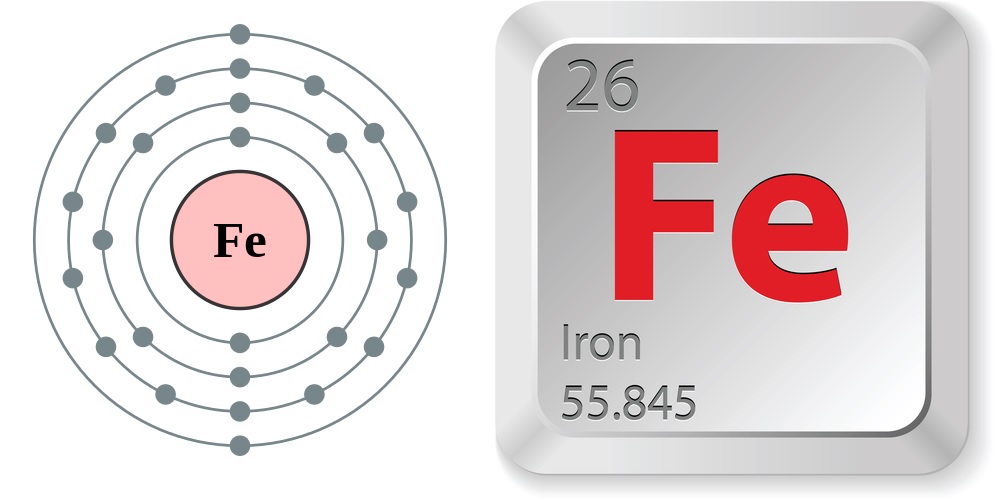
- \[Fe + Cl_2 → FeCl_3\] (Clo phản ứng với sắt tạo ra sắt(III) clorua).
2. Phản ứng với Phi Kim
Clo phản ứng với hydro để tạo thành axit hydrochloric:
- \[H_2 + Cl_2 → 2HCl\]
Khí HCl tan nhiều trong nước, tạo thành dung dịch axit clohidric mạnh.
3. Phản ứng với Nước
Khi hòa tan trong nước, clo tạo thành hỗn hợp gồm axit clohidric (HCl) và axit hipoclorơ (HClO):
- \[Cl_2 + H_2O ⇌ HCl + HClO\]
Axit hipoclorơ là một chất oxi hóa mạnh, làm cho nước clo có tính khử trùng và tẩy màu.
4. Phản ứng với Dung Dịch Kiềm
Clo phản ứng với dung dịch kiềm để tạo thành hỗn hợp muối clorua và hipoclorit. Ví dụ, khi phản ứng với natri hydroxit (NaOH):
- \[Cl_2 + 2NaOH → NaCl + NaClO + H_2O\]
Phản ứng này tạo ra dung dịch nước Gia-ven, có tính tẩy màu mạnh.
5. Phản ứng với Hợp Chất Khử
Clo có khả năng phản ứng với các chất khử mạnh, chẳng hạn như hydro sulfua (H2S):
- \[4Cl_2 + H_2S + 4H_2O → 8HCl + H_2SO_4\]
Ứng Dụng Của Clo Trong Đời Sống Và Công Nghiệp
Clo là một nguyên tố hóa học có rất nhiều ứng dụng trong đời sống và sản xuất công nghiệp, nhờ vào các tính chất hóa học nổi bật của nó. Dưới đây là những ứng dụng quan trọng của clo:
- Khử trùng nước: Clo được sử dụng rộng rãi trong việc khử trùng nước sinh hoạt và nước thải. Nó có khả năng tiêu diệt vi khuẩn, vi sinh vật gây bệnh và các tạp chất hữu cơ, giúp đảm bảo nước sạch và an toàn cho người dùng.
- Tẩy trắng và xử lý giấy: Trong ngành công nghiệp, clo được sử dụng để tẩy trắng vải sợi, bột giấy và nhiều sản phẩm công nghiệp khác nhờ tính oxi hóa mạnh.
- Sản xuất hóa chất: Clo là nguyên liệu quan trọng trong sản xuất nhiều loại hóa chất như PVC (polyvinyl chloride), axit hydrochloric (HCl), chloroform, và nhiều hợp chất hữu cơ khác. Đây là những nguyên liệu cơ bản cho nhiều ngành công nghiệp khác nhau.
- Xử lý thực phẩm: Clo được sử dụng trong quá trình sản xuất và bảo quản thực phẩm để tiêu diệt vi khuẩn và kéo dài thời gian bảo quản thực phẩm. Đây là một ứng dụng quan trọng giúp đảm bảo an toàn thực phẩm trong quá trình sản xuất.
- Hệ thống cấp thoát nước: Clo được sử dụng để khử trùng hệ thống cấp thoát nước, giúp loại bỏ các tác nhân gây bệnh trong nước, đảm bảo an toàn cho cộng đồng.
- Sản xuất nhựa và cao su: Clo là thành phần chính trong sản xuất nhựa PVC và các chất dẻo, cao su, được sử dụng rộng rãi trong các sản phẩm tiêu dùng và công nghiệp.
- Nước tẩy rửa: Clo cũng được dùng trong các sản phẩm tẩy rửa như nước tẩy clo, thường được sử dụng để tẩy trắng quần áo, vệ sinh bồn cầu, nhà cửa và các dụng cụ gia đình.
Tác Động Của Clo Đến Sức Khỏe Và Môi Trường
Clo là một hóa chất mạnh mẽ có cả tác động tích cực và tiêu cực đến sức khỏe con người và môi trường. Việc hiểu rõ các ảnh hưởng này là quan trọng để sử dụng clo một cách an toàn và hiệu quả.
Tác động tích cực
Xử lý nước sạch: Clo là chất khử trùng mạnh được sử dụng phổ biến để tiêu diệt vi khuẩn, virus, và các vi sinh vật gây bệnh trong nước uống, góp phần bảo vệ sức khỏe cộng đồng.
Ứng dụng trong y tế: Clo và các hợp chất của nó được sử dụng để sản xuất thuốc và các vật tư y tế, giúp ngăn ngừa nhiễm trùng và bảo vệ sức khỏe.
Nguy cơ và tác động tiêu cực
Ảnh hưởng đến hệ hô hấp: Khi tiếp xúc ở nồng độ cao, clo có thể gây kích ứng mạnh mẽ đến đường hô hấp, dẫn đến các triệu chứng như ho, khó thở, hoặc thậm chí là tổn thương phổi. Clo khí trong môi trường làm việc cũng có thể là nguy cơ nghiêm trọng cho những người tiếp xúc thường xuyên.
Ô nhiễm môi trường: Việc sử dụng clo trong công nghiệp, như sản xuất nhựa PVC, có thể gây ra sự phát thải các chất độc hại vào môi trường. Các chất thải này gây ô nhiễm không khí, đất, và nước, ảnh hưởng đến cả hệ sinh thái và sức khỏe con người.
Ảnh hưởng đến chất lượng nước: Dư lượng clo trong nước thải công nghiệp hoặc các sản phẩm khử trùng có thể gây ô nhiễm nguồn nước, ảnh hưởng đến động vật thủy sinh và hệ sinh thái nước ngọt.
Vì vậy, mặc dù clo đóng vai trò quan trọng trong nhiều lĩnh vực của đời sống và công nghiệp, việc sử dụng và quản lý đúng cách là vô cùng cần thiết để giảm thiểu các tác động tiêu cực lên sức khỏe và môi trường.
Các Phương Pháp Điều Chế Clo
Clo có thể được điều chế bằng các phương pháp khác nhau tùy thuộc vào quy mô và mục đích sử dụng. Có hai phương pháp chính là điều chế trong phòng thí nghiệm và trong công nghiệp.
1. Điều Chế Trong Phòng Thí Nghiệm
Trong phòng thí nghiệm, clo thường được điều chế bằng cách đun nóng nhẹ dung dịch axit hydrochloric (HCl) đậm đặc với chất oxy hóa mạnh như mangan (IV) oxit (MnO2) hoặc kali pemanganat (KMnO4).
Khí clo sinh ra có màu vàng lục, được thu thập bằng cách đẩy không khí ra ngoài và làm khô bằng axit sunfuric đặc.
2. Điều Chế Trong Công Nghiệp
Trong công nghiệp, clo được điều chế bằng phương pháp điện phân dung dịch natri clorua (NaCl) bão hòa có màng ngăn. Phương pháp này được áp dụng rộng rãi tại các nhà máy hóa chất và sản xuất clo quy mô lớn.
- (Điện phân dung dịch NaCl)
Khí clo thu được tại cực dương, trong khi khí hiđro được tạo ra tại cực âm và dung dịch NaOH được thu lại.
Ứng Dụng
Clo sau khi được điều chế có nhiều ứng dụng trong công nghiệp và đời sống, bao gồm xử lý nước, sản xuất hóa chất, và làm chất tẩy trắng.