Contents
Giới thiệu
Rượu Etylic C2H6O, một chất lỏng không màu, có tính chất hoá học đặc trưng và nhiều ứng dụng trong đời sống hàng ngày. Trong bài viết này, chúng ta sẽ tìm hiểu về tính chất vật lý và hoá học của rượu Etylic, công thức cấu tạo và cách điều chế. Chúng ta cũng sẽ khám phá các ứng dụng của rượu Etylic trong công nghiệp và đời sống.
Tính chất vật lý của rượu Etylic C2H6O
- Rượu Etylic là một chất lỏng không màu, có điểm sôi ở 78,3 độ C.
- Rượu Etylic nhẹ hơn nước và hoàn toàn hòa tan trong nước. Nó cũng có khả năng hòa tan nhiều chất khác nhau như iot và benzen.
- Độ rượu là lượng rượu Etylic tinh khiết trong 100ml hỗn hợp rượu Etylic và nước.
- Công thức tính độ rượu: Độ rượu = (số ml rượu Etylic / 100ml) x 100.
- Trong đó, V là thể tích được tính bằng ml hoặc lít.
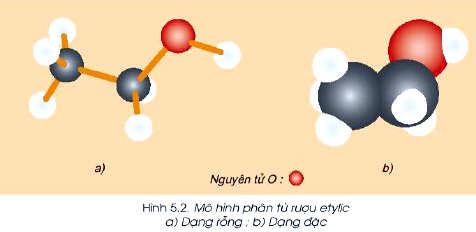
Cấu tạo phân tử của rượu Etylic C2H6O
Rượu Etylic có công thức cấu tạo CH3-CH2-OH. Trong phân tử, rượu Etylic có một nguyên tử hydro không liên kết với nguyên tử carbon mà liên kết với nguyên tử oxi tạo thành nhóm -OH. Đây chính là nhóm -OH gây nên tính chất hoá học đặc trưng của rượu.
Bạn đang xem: Rượu Etylic C2H6O tính chất hoá học, công thức cấu tạo rượu Etylic và bài tập – hoá 9 bài 44
Hình ảnh: Rượu Etylic C2H6O tính chất hoá học, công thức cấu tạo rượu Etylic và bài tập – hoá 9 bài 44

Tính chất hoá học của rượu Etylic C2H5OH
1. Tác dụng với oxi, phản ứng cháy
Rượu Etylic cháy với ngọn lửa màu xanh, toả nhiều nhiệt. Phản ứng cháy của rượu Etylic có thể được biểu diễn như sau:
C2H5OH + 3O2 → 2CO2 + 3H2O
2. Tác dụng với kim loại mạnh K, Na
Xem thêm : Có bao nhiêu quốc gia trên thế giới?
Khi thả mẩu Natri vào cốc chứa rượu Etylic, Natri sẽ tan dần và tạo bọt khí thoát ra. Phản ứng này có thể được biểu diễn như sau:
2C2H5OH + Na → 2C2H5ONa + H2↑
3. Phản ứng với axit axetic
Khi đổ rượu Etylic vào cốc chứa axit axetic với xúc tác H2SO4 đặc, ta tạo thành dung dịch đồng nhất. Đun nóng hỗn hợp một thời gian, trong ống nghiệm sẽ xuất hiện chất lỏng không màu, mùi thơm, không tan trong nước và nổi trên mặt nước. Phản ứng này có thể được biểu diễn như sau:
C2H5OH + CH3COOH → CH3COOC2H5 + H2O
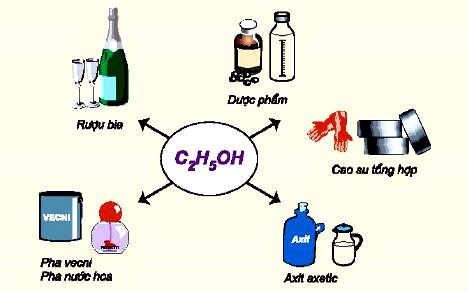
Ứng dụng của rượu Etylic C2H5OH
- Rượu Etylic được sử dụng làm nhiên liệu cho động cơ ô tô và đèn cồn trong phòng thí nghiệm.
- Nó cũng làm nguyên liệu để sản xuất axit axetic, dược phẩm và cao su tổng hợp.
- Rượu Etylic còn được sử dụng trong việc pha chế nhiều loại rượu uống.
Hình ảnh: Rượu Etylic C2H6O tính chất hoá học, công thức cấu tạo rượu Etylic và bài tập – hoá 9 bài 44

Điều chế rượu Etylic C2H5OH
Có hai phương pháp điều chế rượu Etylic:
Xem thêm : [Tự học SQL] Bài tập thực hành sql server nâng cao – Phần 1(full hướng dẫn)
Phương pháp 1: Điều chế rượu làm đồ uống
- Sử dụng tinh bột hoặc đường glucoz để điều chế rượu Etylic.
- Phản ứng hóa học: C6H12O6 → 2CO2 + 2C2H5OH
Phương pháp 2: Sản xuất rượu phục vụ ngành công nghiệp
- Cộng hợp etilen với nước và xúc tác axit.
- Phản ứng hóa học: C2H4 + H2O → C2H5OH
Bài tập về rượu Etylic C2H5OH
Bài 1 trang 139 sách giáo trình hoá 9:
Rượu Etylic phản ứng với natri vì:
A. Trong phân tử có nguyên tử oxi.
B. Trong phân tử có nguyên tử hydro và nguyên tử oxi.
C. Trong phân tử có nguyên tử cacbon, hydro và oxi.
D. Trong phân tử có nhóm – OH.
Lời giải bài 1 trang 139 sách giáo trình hoá 9:
Đáp án: D. Trong phân tử có nhóm – OH.
Câu A, B, C không chính xác.
Bài 2 trang 139 sách giáo trình hoá 9:
Trong số các chất sau: CH3-CH3, CH3-CH2OH, C6H6, CH3-O-CH3, chất nào tác dụng được với Na? Viết phương trình hóa học.
Lời giải bài 2 trang 139 sách giáo trình hoá 9:
- Chỉ có rượu Etylic tác dụng với Na theo phản ứng:
2C2H5OH + 2Na → 2C2H5ONa + H2↑
Bài 3 trang 139 sách giáo trình hoá 9:
Có ba ống nghiệm: Ống 1 đựng rượu Etylic, ống 2 đựng rượu 96o, ống 3 đựng nước. Cho Na dư vào các ống nghiệm trên, viết các phương trình hóa học.
Lời giải bài 3 trang 139 sách giáo trình hoá 9:
- Các phương trình hóa học:
- Ống 1: Rượu Etylic tác dụng với Na
2C2H5OH + 2Na → 2C2H5ONa + H2↑ - Ống 2: Rượu 96o tác dụng với Na (bao gồm C2H5OH và H2O)
2H2O + 2Na → 2NaOH + H2↑
2C2H5OH + 2Na → 2C2H5ONa + H2↑ - Ống 3: Nước tác dụng với Na
2H2O + 2Na → 2NaOH + H2↑
Bài 4 trang 139 sách giáo trình hoá 9:
Trên các chai rượu đều ghi các số như 45o, 18o, 12o.
a) Hãy giải thích ý nghĩa các số trên.
b) Tính số ml rượu Etylic có trong 500ml chai rượu 45o.
c) Có thể pha được bao nhiêu lít rượu 25o từ 500ml rượu 45o.
Lời giải bài 4 trang 139 sách giáo trình hoá 9:
a) Các con số 45o, 18o, 12o chỉ tỉ lệ rượu tinh khiết trong 100ml, lần lượt là 45ml, 18ml và 12ml.
b) Số ml rượu Etylic có trong 500ml chai rượu 45o là: 500 x (45/100) = 225ml.
c) Số lít rượu 25o có thể pha từ 500ml chai rượu 45o (hoặc 225ml rượu tinh khiết) là: 225 x (100/25) = 900ml.
Bài 5 trang 139 sách giáo trình hoá 9:
Đốt cháy hoàn toàn 9,2g rượu Etylic.
a) Tính thể tích khí CO2 tạo ra ở điều kiện tiêu chuẩn.
b) Tính thể tích không khí cần dùng cho phản ứng, biết oxi chiếm 20% thể tích của không khí.
Chúc các bạn thành công trong việc nghiên cứu về rượu Etylic C2H6O!
Nguồn: https://ispacedanang.edu.vn
Danh mục: Học tập