Chủ đề số electron của oxi: Số electron của oxi là một khái niệm quan trọng trong hóa học, giúp chúng ta hiểu rõ hơn về tính chất và ứng dụng của nguyên tố này. Bài viết này sẽ giải thích chi tiết về cấu hình electron của oxi và cách nó ảnh hưởng đến các phản ứng hóa học cũng như ứng dụng trong đời sống và công nghiệp.
Mục lục
Số Electron Của Nguyên Tử Oxi
Nguyên tử oxi, với ký hiệu hóa học là O, là một trong những nguyên tố cơ bản nhất trong bảng tuần hoàn, đóng vai trò quan trọng trong nhiều quá trình hóa học và sinh học. Để hiểu rõ hơn về tính chất của nguyên tố này, trước hết cần phải biết về cấu hình electron của nó.
Cấu Hình Electron Của Oxi
Oxi có số hiệu nguyên tử là 8, điều này có nghĩa rằng một nguyên tử oxi trung hòa sẽ có 8 electron. Các electron này được phân bố vào các lớp vỏ electron xung quanh hạt nhân theo quy luật nhất định:
- Lớp thứ nhất: 2 electron
- Lớp thứ hai: 6 electron
Như vậy, cấu hình electron của nguyên tử oxi được viết là:
\[1s^2 2s^2 2p^4\]
Tính Chất Hóa Học Liên Quan Đến Số Electron
Số electron ở lớp vỏ ngoài cùng (lớp 2) của oxi là 6. Điều này giải thích vì sao oxi có xu hướng nhận thêm 2 electron để đạt cấu hình bền vững giống như khí hiếm, tạo thành ion O2-. Đây là lý do tại sao oxi thường có hóa trị 2 trong các hợp chất.
Ứng Dụng Của Oxi Trong Đời Sống
Nhờ khả năng liên kết hóa học mạnh mẽ, oxi tham gia vào nhiều phản ứng hóa học quan trọng như quá trình cháy, hô hấp và oxi hóa khử. Một số ứng dụng của oxi bao gồm:
- Sản xuất thép và các kim loại khác.
- Sử dụng trong y học như một phần của liệu pháp oxy.
- Ứng dụng trong công nghệ xử lý nước thải và làm sạch môi trường.
Kết Luận
Với tổng số 8 electron và cấu hình electron đặc trưng, oxi là một nguyên tố có tính phản ứng cao, đóng vai trò thiết yếu trong nhiều quá trình tự nhiên và công nghiệp. Hiểu rõ cấu hình electron của oxi không chỉ giúp ta nắm bắt được tính chất hóa học của nó mà còn thấy rõ tầm quan trọng của oxi trong cuộc sống hàng ngày.

Cấu Hình Electron Của Nguyên Tử Oxi
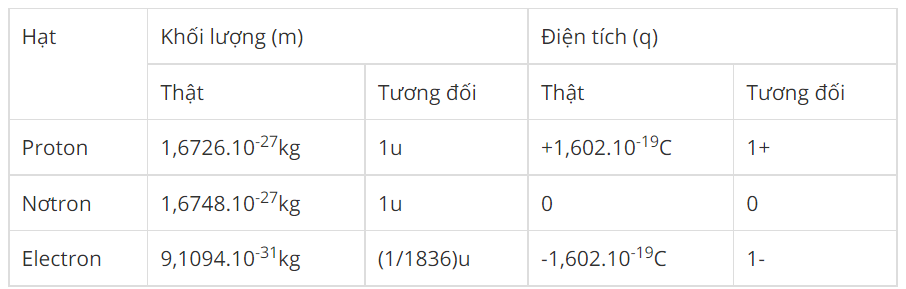
Nguyên tử oxi có số hiệu nguyên tử là 8, điều này có nghĩa là nó có 8 proton trong hạt nhân và, đối với nguyên tử trung hòa, sẽ có 8 electron bao quanh hạt nhân. Các electron này được sắp xếp theo các lớp vỏ electron với nguyên tắc điền electron theo thứ tự mức năng lượng từ thấp đến cao.
- Lớp thứ nhất: Lớp vỏ đầu tiên chỉ có thể chứa tối đa 2 electron. Vì vậy, 2 electron đầu tiên của oxi sẽ nằm trong lớp này. Cấu hình của lớp vỏ đầu tiên sẽ là \(1s^2\).
- Lớp thứ hai: Lớp vỏ thứ hai có thể chứa tối đa 8 electron. Trong trường hợp của oxi, lớp này chứa 6 electron còn lại. Các electron sẽ được phân bổ vào các obitan 2s và 2p. Cấu hình của lớp vỏ thứ hai sẽ là \(2s^2 2p^4\).
Như vậy, cấu hình electron của nguyên tử oxi đầy đủ sẽ là:
\[1s^2 2s^2 2p^4\]
Cấu hình này cho thấy rằng oxi có 6 electron ở lớp vỏ ngoài cùng, điều này làm cho nó có xu hướng nhận thêm 2 electron để đạt cấu hình bền vững giống như khí hiếm neon. Khả năng này giải thích tại sao oxi thường tồn tại dưới dạng ion O2- trong các hợp chất hóa học.
Tính Chất Hóa Học Liên Quan Đến Số Electron Của Oxi
Tính chất hóa học của nguyên tử oxi được quyết định bởi cấu hình electron của nó, đặc biệt là số lượng electron ở lớp vỏ ngoài cùng. Với 6 electron ở lớp ngoài cùng (\(2s^2 2p^4\)), oxi có xu hướng nhận thêm 2 electron để đạt cấu hình bền vững giống như khí hiếm. Điều này dẫn đến các tính chất hóa học đặc trưng sau:
- Khả năng tạo ion: Oxi dễ dàng nhận thêm 2 electron để trở thành ion O2-. Quá trình này giúp oxi đạt được cấu hình bền vững \([Ne]\), giống với cấu hình của khí hiếm neon. Đây là lý do vì sao oxi thường có hóa trị 2 trong các hợp chất ion.
- Phản ứng với kim loại: Oxi thường phản ứng với các kim loại để tạo ra oxit kim loại. Trong phản ứng này, oxi đóng vai trò là chất oxi hóa, nhận electron từ kim loại. Ví dụ, khi phản ứng với magie (Mg), oxi tạo ra magie oxit (\(MgO\)) theo phương trình: \[ 2Mg + O_2 \rightarrow 2MgO \]
- Phản ứng với phi kim: Khi phản ứng với các phi kim khác, oxi có thể tạo thành các oxit phi kim. Chẳng hạn, khi phản ứng với lưu huỳnh (S), oxi tạo ra lưu huỳnh dioxide (\(SO_2\)): \[ S + O_2 \rightarrow SO_2 \]
- Vai trò trong các phản ứng oxi hóa khử: Oxi thường tham gia vào các phản ứng oxi hóa khử, đóng vai trò là chất oxi hóa mạnh. Do có xu hướng nhận electron, oxi giúp khử các chất khác trong phản ứng. Ví dụ, trong quá trình hô hấp tế bào, oxi là tác nhân oxi hóa glucose để giải phóng năng lượng.
Như vậy, số electron ở lớp ngoài cùng quyết định mạnh mẽ đến tính chất hóa học của oxi, khiến nguyên tố này có vai trò quan trọng trong nhiều phản ứng hóa học và sinh học.

Ứng Dụng Của Oxi Trong Đời Sống Và Công Nghiệp
Oxi là một nguyên tố thiết yếu không chỉ đối với sự sống mà còn trong nhiều ngành công nghiệp. Nhờ các tính chất hóa học đặc trưng, oxi được ứng dụng rộng rãi trong nhiều lĩnh vực khác nhau. Dưới đây là một số ứng dụng quan trọng của oxi trong đời sống và công nghiệp:
- Ứng dụng trong y học: Oxi là một yếu tố quan trọng trong y học, đặc biệt trong liệu pháp oxy. Bệnh nhân gặp khó khăn về hô hấp thường được cung cấp oxy bổ sung để duy trì nồng độ oxy trong máu ổn định. Liệu pháp oxy cũng được sử dụng trong điều trị các bệnh như COPD, hen suyễn và trong các trường hợp cấp cứu.
- Ứng dụng trong công nghiệp sản xuất: Oxi được sử dụng rộng rãi trong ngành luyện kim để cắt và hàn kim loại. Trong quá trình sản xuất thép, oxi được thổi vào lò luyện để oxi hóa tạp chất, cải thiện chất lượng sản phẩm cuối cùng. Ngoài ra, oxi còn được sử dụng trong quá trình sản xuất hóa chất như axit sulfuric (\(H_2SO_4\)) và trong ngành công nghiệp giấy để tẩy trắng.
- Vai trò trong các quá trình đốt cháy: Oxi là một chất oxi hóa mạnh, đóng vai trò quan trọng trong các quá trình đốt cháy. Nó không chỉ giúp duy trì ngọn lửa mà còn làm tăng hiệu suất của quá trình đốt, chẳng hạn như trong các động cơ đốt trong và các hệ thống lò sưởi công nghiệp.
- Ứng dụng trong xử lý nước và môi trường: Oxi được sử dụng trong các quá trình xử lý nước thải để oxi hóa các chất ô nhiễm hữu cơ, giúp làm sạch nguồn nước. Ngoài ra, oxi còn được ứng dụng trong việc cải thiện chất lượng không khí và trong các hệ thống xử lý khí thải công nghiệp.
Nhờ các ứng dụng đa dạng trong đời sống và công nghiệp, oxi đóng vai trò quan trọng trong việc nâng cao chất lượng cuộc sống và thúc đẩy sự phát triển của các ngành công nghiệp hiện đại.

Tầm Quan Trọng Của Oxi Trong Hóa Học Và Sinh Học
Oxi là một trong những nguyên tố quan trọng nhất trong tự nhiên, đóng vai trò thiết yếu trong nhiều quá trình hóa học và sinh học. Dưới đây là những lý do tại sao oxi lại quan trọng đối với cả hóa học và sinh học:
- Vai trò trong quá trình hô hấp: Oxi là yếu tố cần thiết cho sự sống của hầu hết các sinh vật trên Trái Đất. Trong quá trình hô hấp, các tế bào sử dụng oxi để chuyển hóa glucose thành năng lượng, quá trình này được gọi là hô hấp tế bào. Phương trình hóa học của quá trình này như sau: \[ C_6H_{12}O_6 + 6O_2 \rightarrow 6CO_2 + 6H_2O + \text{Năng lượng} \] Không có oxi, các sinh vật sống sẽ không thể tạo ra đủ năng lượng để duy trì các chức năng sống cơ bản.
- Oxi trong các hợp chất hóa học quan trọng: Oxi là một phần của nhiều hợp chất hóa học quan trọng như nước (\(H_2O\)), carbon dioxide (\(CO_2\)), và nhiều axit khác. Những hợp chất này đóng vai trò quan trọng trong các quá trình sinh học và môi trường, chẳng hạn như quang hợp, nơi thực vật sử dụng \(CO_2\) và nước để tạo ra oxy và glucose: \[ 6CO_2 + 6H_2O + \text{Ánh sáng} \rightarrow C_6H_{12}O_6 + 6O_2 \]
- Vai trò trong phản ứng oxi hóa khử: Oxi là một chất oxi hóa mạnh, tham gia vào nhiều phản ứng oxi hóa khử quan trọng. Những phản ứng này không chỉ quan trọng trong các quá trình sinh học như hô hấp tế bào mà còn trong nhiều quá trình hóa học công nghiệp. Ví dụ, trong phản ứng đốt cháy nhiên liệu, oxi kết hợp với các hydrocarbon để tạo ra năng lượng, carbon dioxide, và nước.
- Tác động đến môi trường và sức khỏe: Nồng độ oxi trong không khí không chỉ cần thiết cho sự sống mà còn ảnh hưởng đến chất lượng không khí và sức khỏe con người. Thiếu oxi có thể dẫn đến các vấn đề về hô hấp, trong khi mức oxi quá cao có thể gây ra nguy cơ cháy nổ.
Như vậy, oxi không chỉ là một nguyên tố hóa học quan trọng mà còn là yếu tố sống còn trong nhiều quá trình sinh học. Hiểu rõ tầm quan trọng của oxi giúp chúng ta đánh giá cao vai trò của nó trong cuộc sống hàng ngày và trong sự phát triển của khoa học và công nghệ.