Chủ đề tính khối lượng của 1 mol electron: Tìm hiểu cách tính khối lượng của 1 mol electron qua các bước đơn giản, kết hợp với những ứng dụng thực tiễn trong khoa học và công nghệ. Bài viết sẽ cung cấp thông tin chi tiết, giúp bạn hiểu rõ hơn về vai trò của electron trong cấu trúc nguyên tử và các phản ứng hóa học.
Mục lục
Tính khối lượng của 1 mol electron
Để tính khối lượng của 1 mol electron, trước tiên cần biết khối lượng của một electron đơn lẻ và số Avogadro. Khối lượng của một electron là:
\[
m_e = 9.10938356 \times 10^{-31} \, \text{kg}
\]
Số Avogadro là số hạt có trong 1 mol của bất kỳ chất nào, được xác định là:
\[
N_A = 6.02214076 \times 10^{23} \, \text{mol}^{-1}
\]
Vì vậy, khối lượng của 1 mol electron sẽ được tính bằng cách nhân khối lượng của một electron với số Avogadro:
\[
M = m_e \times N_A = 9.10938356 \times 10^{-31} \, \text{kg} \times 6.02214076 \times 10^{23} \, \text{mol}^{-1}
\]
Thực hiện phép nhân trên, ta có khối lượng của 1 mol electron:
\[
M \approx 5.48579909070 \times 10^{-7} \, \text{kg/mol}
\]
Khối lượng này tương đương với:
\[
M \approx 0.548 \, \text{mg/mol}
\]
Ứng dụng của khối lượng 1 mol electron
- Trong hóa học, khối lượng của 1 mol electron được sử dụng để tính toán trong các phản ứng oxi hóa-khử, nơi mà electron được trao đổi giữa các chất.
- Trong vật lý, giá trị này giúp các nhà khoa học hiểu rõ hơn về cấu trúc nguyên tử và hành vi của electron trong các hiện tượng lượng tử.
- Khối lượng này cũng được dùng để thiết kế và tính toán các thiết bị điện tử, từ máy tính cho đến các cảm biến phức tạp.

1. Giới thiệu về electron và vai trò của chúng trong cấu trúc nguyên tử
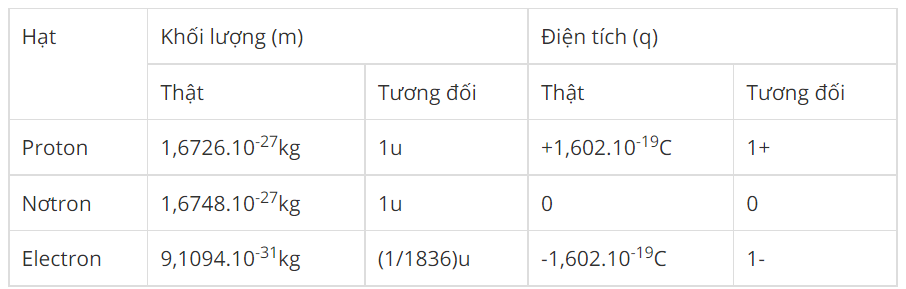
Electron là hạt cơ bản của vật chất, có điện tích âm và tồn tại trong vỏ nguyên tử. Chúng được nhà khoa học J.J. Thomson phát hiện vào năm 1897 và đóng vai trò quan trọng trong việc xác định tính chất của nguyên tử và phân tử. Electron có khối lượng rất nhỏ, khoảng \[9.10938356 \times 10^{-31}\] kg, nhỏ hơn rất nhiều so với proton và neutron.
Trong cấu trúc nguyên tử, electron di chuyển xung quanh hạt nhân theo các quỹ đạo nhất định, được mô tả bởi các mức năng lượng. Sự phân bố của electron trong các lớp vỏ nguyên tử quyết định các tính chất hóa học của nguyên tử, bao gồm cách nguyên tử liên kết với nhau để tạo thành phân tử.
- Electron giữ vai trò chính trong các phản ứng hóa học, đặc biệt là trong các phản ứng oxi hóa-khử, nơi chúng được chuyển từ chất này sang chất khác.
- Chúng cũng chịu trách nhiệm tạo ra lực hút tĩnh điện giữa các nguyên tử, từ đó hình thành các liên kết hóa học.
Hiểu biết về electron không chỉ giúp chúng ta giải thích được cấu trúc nguyên tử mà còn ứng dụng rộng rãi trong nhiều lĩnh vực, từ hóa học đến vật lý và công nghệ.
2. Khối lượng của một electron đơn lẻ
Electron là một trong những hạt cơ bản của vật chất, với khối lượng rất nhỏ so với các hạt khác như proton hay neutron. Khối lượng của một electron được xác định qua các thí nghiệm chính xác và được tính toán với giá trị:
\[
m_e = 9.10938356 \times 10^{-31} \, \text{kg}
\]
Giá trị này cho thấy electron có khối lượng cực kỳ nhỏ, nhỏ hơn proton khoảng 1836 lần. Đây là lý do tại sao electron được coi là hạt nhẹ nhất trong cấu trúc nguyên tử và đóng vai trò quan trọng trong nhiều quá trình vật lý và hóa học.
Việc xác định khối lượng của một electron không chỉ là thành tựu lớn trong lĩnh vực vật lý lượng tử mà còn mở ra những ứng dụng thực tế trong công nghệ, đặc biệt là trong các thiết bị điện tử hiện đại như vi xử lý và các cảm biến phức tạp.
Khối lượng của electron, mặc dù nhỏ bé, nhưng là yếu tố quyết định trong việc tính toán nhiều thông số khác nhau trong các quá trình vật lý và hóa học, bao gồm cả việc tính toán khối lượng của 1 mol electron, một trong những ứng dụng quan trọng trong hóa học và vật lý hiện đại.

3. Số Avogadro và ý nghĩa của nó
Số Avogadro, ký hiệu là \(N_A\), là một trong những hằng số cơ bản nhất trong hóa học và vật lý. Nó đại diện cho số hạt cơ bản (như nguyên tử, phân tử, electron) có trong 1 mol chất. Giá trị của số Avogadro là:
\[
N_A = 6.02214076 \times 10^{23} \, \text{mol}^{-1}
\]
Số Avogadro có ý nghĩa quan trọng trong việc kết nối các hiện tượng vi mô (ở cấp độ nguyên tử và phân tử) với các hiện tượng vĩ mô (ở cấp độ lượng chất có thể đo đạc được). Nó cho phép chúng ta chuyển đổi giữa khối lượng mol của một chất và số lượng hạt của chất đó.
- Trong hóa học: Số Avogadro giúp xác định lượng chất cần thiết để thực hiện các phản ứng hóa học. Ví dụ, khi biết khối lượng mol của một chất, ta có thể sử dụng số Avogadro để tính số lượng nguyên tử hoặc phân tử có trong một lượng nhất định của chất đó.
- Trong vật lý: Số Avogadro được sử dụng để xác định các tính chất vật lý ở cấp độ nguyên tử và phân tử, như mật độ, áp suất và nhiệt độ trong lý thuyết động học của chất khí.
- Trong công nghệ: Số Avogadro là cơ sở để thiết kế các thiết bị vi mô, như các cảm biến và linh kiện điện tử, giúp điều chỉnh chính xác các tính toán liên quan đến số lượng hạt trong các hệ thống nhỏ.
Sự hiểu biết về số Avogadro không chỉ giúp nắm rõ hơn về các quá trình hóa học và vật lý mà còn cung cấp công cụ quan trọng để nghiên cứu và phát triển các ứng dụng công nghệ hiện đại.

4. Tính khối lượng của 1 mol electron
Để tính khối lượng của 1 mol electron, chúng ta cần kết hợp giá trị khối lượng của một electron đơn lẻ và số Avogadro. Như đã đề cập trước đó, khối lượng của một electron là:
\[
m_e = 9.10938356 \times 10^{-31} \, \text{kg}
\]
Và số Avogadro là:
\[
N_A = 6.02214076 \times 10^{23} \, \text{mol}^{-1}
\]
Khối lượng của 1 mol electron, ký hiệu là \(M_e\), được tính bằng cách nhân khối lượng của một electron với số Avogadro:
\[
M_e = m_e \times N_A = 9.10938356 \times 10^{-31} \, \text{kg} \times 6.02214076 \times 10^{23} \, \text{mol}^{-1}
\]
Thực hiện phép nhân trên, ta có:
\[
M_e \approx 5.48579909070 \times 10^{-7} \, \text{kg/mol}
\]
Đơn vị của khối lượng này là kilogram trên mol (kg/mol), và nó thể hiện khối lượng của tất cả các electron có trong 1 mol electron. Để dễ hình dung hơn, giá trị này tương đương với:
\[
M_e \approx 0.548 \, \text{mg/mol}
\]
Việc tính toán khối lượng của 1 mol electron là cơ sở quan trọng trong các lĩnh vực hóa học và vật lý, đặc biệt trong các phản ứng oxi hóa-khử, nơi electron được chuyển từ chất này sang chất khác, và trong các quá trình vi mô khác.

5. Ứng dụng của khối lượng 1 mol electron
Khối lượng của 1 mol electron có nhiều ứng dụng quan trọng trong các lĩnh vực khác nhau, từ hóa học đến vật lý và công nghệ. Dưới đây là một số ứng dụng tiêu biểu:
- Trong hóa học: Khối lượng 1 mol electron được sử dụng để tính toán trong các phản ứng oxi hóa-khử, nơi mà số lượng electron chuyển giao giữa các chất được đo lường để xác định khối lượng sản phẩm hoặc chất phản ứng. Đây là cơ sở để hiểu và điều khiển các phản ứng hóa học phức tạp.
- Trong vật lý: Khối lượng 1 mol electron giúp trong việc nghiên cứu các tính chất của vật liệu và các hiện tượng vật lý vi mô. Ví dụ, trong lý thuyết động học của chất khí, electron đóng vai trò quan trọng trong việc xác định các tính chất nhiệt động học của hệ thống, như áp suất và nhiệt độ.
- Trong công nghệ: Với sự phát triển của công nghệ nano và vi điện tử, việc hiểu rõ khối lượng của 1 mol electron là rất quan trọng. Nó giúp tối ưu hóa các thiết bị điện tử như transistor, cảm biến, và vi xử lý, nơi các hiện tượng liên quan đến electron xảy ra ở mức vi mô. Các tính toán liên quan đến electron đóng vai trò quan trọng trong việc thiết kế và phát triển các thiết bị này.
- Trong nghiên cứu khoa học: Khối lượng của 1 mol electron còn được sử dụng trong các nghiên cứu về năng lượng, đặc biệt là trong các hệ thống chuyển đổi năng lượng như pin mặt trời và pin nhiên liệu, nơi mà electron tham gia vào quá trình chuyển đổi năng lượng từ dạng này sang dạng khác một cách hiệu quả.
Nhìn chung, hiểu biết về khối lượng của 1 mol electron không chỉ giúp trong các tính toán khoa học mà còn thúc đẩy những tiến bộ trong công nghệ và các ứng dụng thực tiễn khác.