Chủ đề số lượng electron trong một ao: Số lượng electron trong một Ångström là một chủ đề thú vị, mở ra cánh cửa khám phá về thế giới vi mô của các nguyên tử và phân tử. Bài viết này sẽ giúp bạn hiểu rõ hơn về cách tính toán và ý nghĩa của số lượng electron trong khoảng cách nhỏ bé này, từ đó làm sáng tỏ nhiều khía cạnh của khoa học vật liệu và hóa học.
Mục lục
Số Lượng Electron Trong Một Ångström
Ångström (\(\text{Å}\)) là một đơn vị đo chiều dài rất nhỏ, bằng \(10^{-10}\) mét, thường được sử dụng để đo kích thước nguyên tử và khoảng cách giữa các nguyên tử trong phân tử. Việc xác định số lượng electron trong một khoảng cách nhất định, chẳng hạn như trong một Ångström, phụ thuộc vào loại nguyên tử hoặc phân tử mà chúng ta đang xét đến.
Số lượng electron trong nguyên tử hydro
Nguyên tử hydro, là nguyên tử đơn giản nhất với chỉ một proton và một electron. Vì vậy, trong khoảng cách một Ångström, nếu ta chỉ xét một nguyên tử hydro, sẽ có:
\[ \text{Số lượng electron} = 1 \]
Số lượng electron trong nguyên tử lớn hơn
Đối với các nguyên tử lớn hơn, số lượng electron trong một Ångström sẽ khác nhau. Ví dụ, đối với nguyên tử oxy, với bán kính nguyên tử xấp xỉ 0,6 Ångström và có 8 electron:
Trong một khoảng cách 1 Ångström từ hạt nhân của nguyên tử oxy, số lượng electron sẽ không đơn giản là 1 hoặc 2 mà có thể là một tỷ lệ phần trăm nào đó trong tổng số 8 electron tùy thuộc vào vị trí cụ thể trong không gian.
Quá trình xác định số lượng electron
Để tính toán chính xác số lượng electron trong một khoảng cách nhất định, người ta thường sử dụng phương pháp toán học phức tạp, như tính phân bố xác suất của electron theo nguyên lý cơ học lượng tử. Công thức sóng của Schrödinger có thể được áp dụng để xác định phân bố này.
Công thức sóng Schrödinger được biểu diễn như sau:
\[ \hat{H} \Psi = E \Psi \]
Trong đó:
- \(\hat{H}\) là toán tử Hamilton mô tả tổng năng lượng của hệ thống.
- \(\Psi\) là hàm sóng mô tả trạng thái lượng tử của electron.
- \(E\) là năng lượng tương ứng với hàm sóng \(\Psi\).
Kết luận
Số lượng electron trong một Ångström phụ thuộc rất nhiều vào loại nguyên tử và vị trí không gian được xét đến. Đối với nguyên tử hydro, con số này đơn giản là 1. Tuy nhiên, đối với các nguyên tử phức tạp hơn, cần phải áp dụng các nguyên tắc cơ học lượng tử để xác định chính xác phân bố và số lượng electron trong một khoảng cách cụ thể.

Khái Niệm Về Ångström Và Electron
Ångström là một đơn vị đo chiều dài cực kỳ nhỏ, thường được sử dụng trong lĩnh vực khoa học để đo kích thước của các nguyên tử và phân tử. Được ký hiệu là \(\text{Å}\), một Ångström bằng \(10^{-10}\) mét, hay 0,1 nanomét. Đơn vị này rất hữu ích trong việc mô tả các khoảng cách giữa các nguyên tử trong một phân tử hoặc tinh thể.
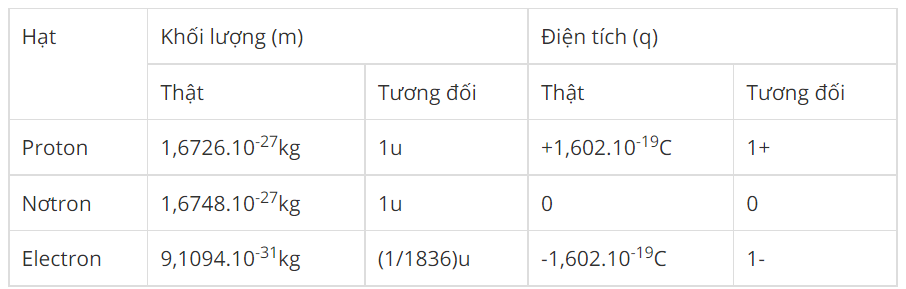
Electron là một trong những hạt cơ bản cấu thành nên nguyên tử, mang điện tích âm. Electron quay quanh hạt nhân nguyên tử và chịu ảnh hưởng bởi lực điện từ. Khối lượng của một electron rất nhỏ, chỉ khoảng \(9.109 \times 10^{-31}\) kg, và điện tích của nó là \(1.602 \times 10^{-19}\) coulombs.
Khi nói về số lượng electron trong một Ångström, chúng ta thường đề cập đến mật độ electron hoặc xác suất tìm thấy electron trong khoảng cách này. Đây là một khái niệm quan trọng trong vật lý nguyên tử và hóa học, nơi mà vị trí và mật độ của electron ảnh hưởng lớn đến tính chất và hành vi của nguyên tử hoặc phân tử.
Để hiểu rõ hơn về mối quan hệ giữa Ångström và electron, chúng ta có thể xem xét:
- Cách mà các electron được phân bố xung quanh hạt nhân trong nguyên tử.
- Khoảng cách trung bình giữa các electron và hạt nhân trong các nguyên tử khác nhau.
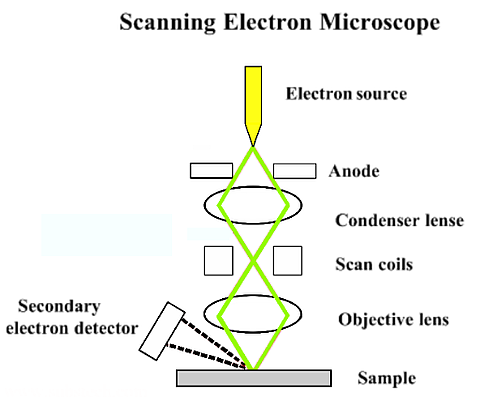
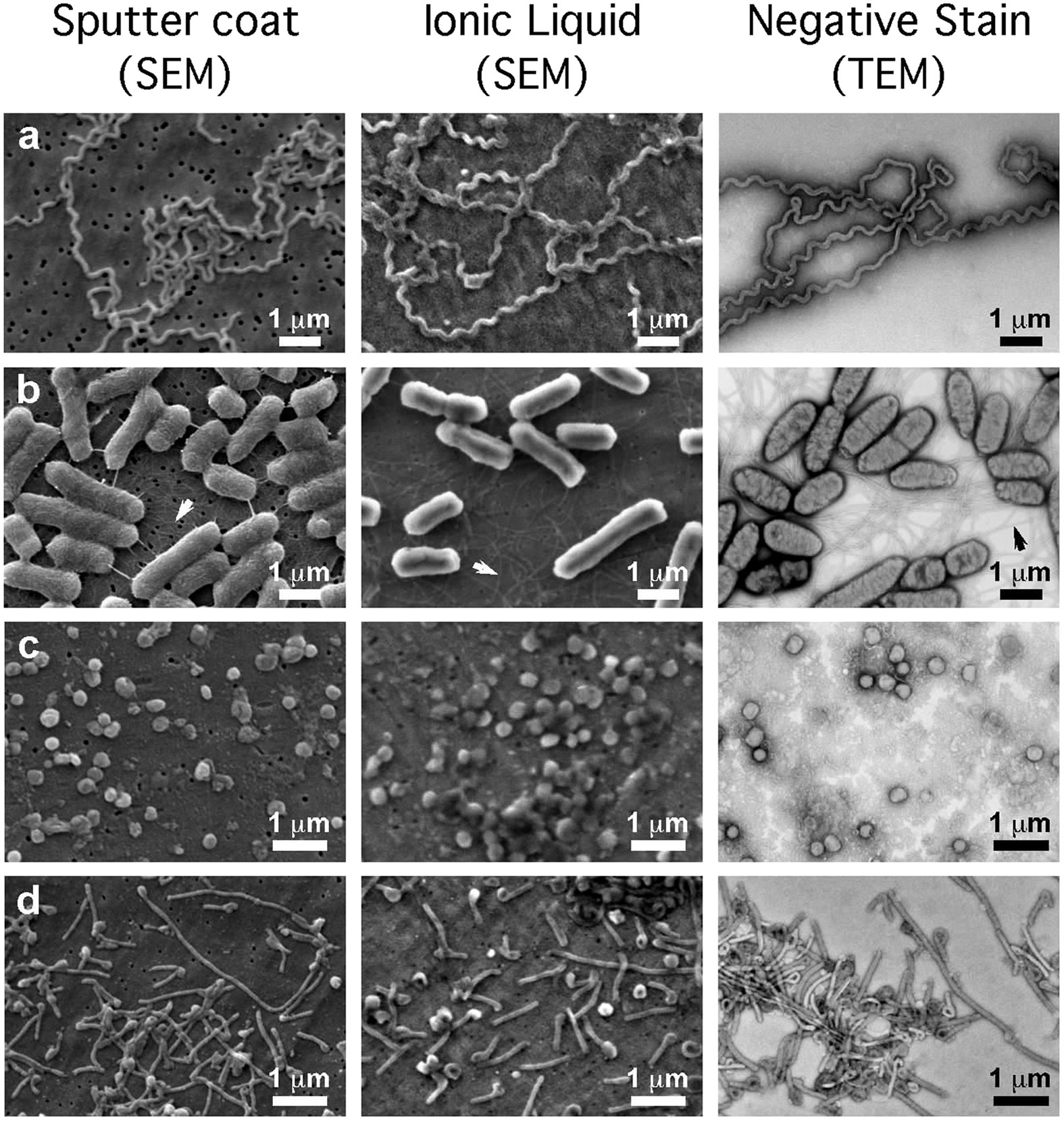
- Phương pháp đo lường khoảng cách này và các công cụ hỗ trợ như kính hiển vi điện tử.
Trong nhiều trường hợp, việc biết được số lượng electron trong một khoảng cách Ångström có thể giúp dự đoán và kiểm soát các phản ứng hóa học, cũng như các tính chất vật lý của vật liệu.
Số Lượng Electron Trong Các Nguyên Tử Khác Nhau
Số lượng electron trong một nguyên tử phụ thuộc vào số lượng proton trong hạt nhân của nguyên tử đó, vì trong trạng thái trung hòa, số lượng electron bằng với số lượng proton. Các nguyên tử khác nhau có số lượng proton khác nhau, do đó cũng có số lượng electron khác nhau. Dưới đây là một số ví dụ về số lượng electron trong một số nguyên tử phổ biến:
- Nguyên tử Hydro (H): Hydro là nguyên tố đơn giản nhất với chỉ một proton và một electron. Do đó, trong một nguyên tử hydro, số lượng electron là 1.
- Nguyên tử Helium (He): Helium có hai proton trong hạt nhân, do đó nó có hai electron quay quanh hạt nhân.
- Nguyên tử Carbon (C): Carbon có sáu proton, do đó số lượng electron trong một nguyên tử carbon là 6.
- Nguyên tử Oxy (O): Oxy có tám proton trong hạt nhân, nghĩa là nó có tám electron phân bố trong các lớp vỏ electron.
- Nguyên tử Sắt (Fe): Sắt có 26 proton, do đó trong một nguyên tử sắt, số lượng electron là 26.
Số lượng electron trong các nguyên tử này không chỉ quyết định tính chất hóa học của nguyên tố mà còn ảnh hưởng đến cách các nguyên tử tương tác với nhau để tạo thành phân tử và chất rắn.
Ví dụ, nguyên tử Carbon với 6 electron có thể tạo ra các liên kết mạnh mẽ trong hợp chất hữu cơ, trong khi nguyên tử Oxy với 8 electron thường tham gia vào các phản ứng oxy hóa khử.
Việc hiểu rõ số lượng electron trong mỗi nguyên tử là nền tảng quan trọng để giải thích các hiện tượng trong hóa học và vật lý, như sự hình thành liên kết hóa học, tính chất từ tính của vật liệu, và cấu trúc phân tử.
Trong trường hợp cụ thể của khoảng cách một Ångström, vị trí của các electron quanh hạt nhân có thể ảnh hưởng lớn đến mật độ electron tại vị trí đó. Điều này thường được nghiên cứu thông qua các mô hình lượng tử và các phép đo tiên tiến.

Các Phương Pháp Tính Toán Số Lượng Electron
Việc tính toán số lượng electron trong một nguyên tử hoặc một khoảng cách nhất định, như một Ångström, đòi hỏi sự hiểu biết sâu sắc về cơ học lượng tử và các phương pháp tính toán tiên tiến. Dưới đây là một số phương pháp phổ biến được sử dụng để xác định số lượng và phân bố electron:
- Phương Trình Sóng Schrödinger
- \(\hat{H}\) là toán tử Hamilton, mô tả tổng năng lượng của hệ thống (bao gồm cả động năng và thế năng).
- \(\Psi\) là hàm sóng, mô tả xác suất tìm thấy electron tại một vị trí nhất định.
- \(E\) là năng lượng tương ứng với trạng thái của electron.
- Phương Pháp Tích Phân Mật Độ Electron
- \(\rho(\mathbf{r})\) là mật độ electron tại vị trí \(\mathbf{r}\).
- \(V\) là thể tích không gian cần tính toán.
- \(n\) là tổng số electron trong thể tích \(V\).
- Phương Pháp Tính Toán Theo Mô Hình Lý Thuyết Hàm Mật Độ (DFT)
- Mô Phỏng Máy Tính Và Phân Tích Số
Phương trình sóng Schrödinger là công cụ nền tảng trong cơ học lượng tử để mô tả trạng thái lượng tử của electron. Phương trình này được viết dưới dạng:
\[
\hat{H} \Psi = E \Psi
\]
Trong đó:
Bằng cách giải phương trình này, ta có thể tìm ra hàm sóng \(\Psi\), từ đó xác định mật độ xác suất của electron trong không gian.
Để tính toán số lượng electron trong một vùng không gian cụ thể, chẳng hạn như trong một Ångström, ta có thể sử dụng phương pháp tích phân mật độ electron. Mật độ electron \(\rho(\mathbf{r})\) được tính toán dựa trên hàm sóng và tích phân qua toàn bộ không gian:
\[
n = \int_V \rho(\mathbf{r}) d\mathbf{r}
\]
Trong đó:
Mô hình lý thuyết hàm mật độ (Density Functional Theory - DFT) là một trong những phương pháp tính toán tiên tiến nhất hiện nay. Phương pháp này sử dụng hàm mật độ electron để xác định năng lượng của hệ thống mà không cần phải biết chi tiết hàm sóng. Phương pháp DFT cho phép tính toán với độ chính xác cao mà không cần phải xử lý quá nhiều biến phức tạp.
Các mô phỏng máy tính ngày nay được sử dụng rộng rãi để tính toán số lượng và phân bố electron. Bằng cách sử dụng các thuật toán phức tạp và sức mạnh tính toán cao, các nhà khoa học có thể mô phỏng chi tiết cấu trúc electron của nguyên tử, phân tử và chất rắn, từ đó suy ra các tính chất vật lý và hóa học của chúng.
Nhờ vào các phương pháp này, việc tính toán số lượng electron trong các vùng không gian nhỏ, chẳng hạn như một Ångström, đã trở nên khả thi và chính xác hơn, hỗ trợ mạnh mẽ cho các nghiên cứu và ứng dụng trong khoa học vật liệu, hóa học, và vật lý nguyên tử.

Ứng Dụng Thực Tiễn Của Ångström Trong Nghiên Cứu Electron
Đơn vị Ångström (\(\text{Å}\)) có ý nghĩa vô cùng quan trọng trong các nghiên cứu liên quan đến cấu trúc nguyên tử và phân tử. Với kích thước rất nhỏ bé, Ångström là đơn vị lý tưởng để đo đạc khoảng cách giữa các nguyên tử cũng như sự phân bố của electron. Dưới đây là một số ứng dụng thực tiễn của Ångström trong nghiên cứu electron:
- Phân Tích Cấu Trúc Tinh Thể
- Hiểu Rõ Về Liên Kết Hóa Học
- Quang Phổ Hấp Thụ X-Ray
- Thiết Kế Vật Liệu Nano
- Nghiên Cứu Màng Mỏng Và Bề Mặt
Trong lĩnh vực tinh thể học, Ångström được sử dụng để mô tả khoảng cách giữa các lớp nguyên tử trong một tinh thể. Các nhà khoa học sử dụng đơn vị này để xác định vị trí chính xác của electron trong mạng tinh thể, từ đó xác định tính chất vật lý của vật liệu. Ví dụ, khoảng cách giữa các nguyên tử cacbon trong kim cương khoảng 1,54 Å, điều này giúp giải thích độ cứng và tính dẫn điện của kim cương.
Trong hóa học, Ångström được dùng để đo khoảng cách giữa các nguyên tử trong một phân tử. Điều này giúp hiểu rõ hơn về liên kết hóa học giữa các nguyên tử, như liên kết đơn, đôi hoặc ba, tùy thuộc vào khoảng cách Ångström giữa chúng. Khoảng cách này quyết định độ mạnh và tính chất của liên kết.
Quang phổ hấp thụ X-ray (X-ray absorption spectroscopy) là một công cụ quan trọng để nghiên cứu cấu trúc electron ở mức độ Ångström. Bằng cách phân tích cách các electron hấp thụ và phát xạ tia X ở khoảng cách Ångström, các nhà khoa học có thể xác định chính xác cấu trúc electron của các nguyên tử và phân tử.
Ångström là đơn vị cơ bản trong việc nghiên cứu và phát triển các vật liệu nano. Việc kiểm soát cấu trúc vật liệu ở kích thước Ångström giúp các nhà khoa học tạo ra các vật liệu mới với tính chất cơ học, quang học, và điện từ được tối ưu hóa. Chẳng hạn, ống nano carbon có đường kính chỉ vài Ångström nhưng lại có độ bền và khả năng dẫn điện vượt trội.
Trong lĩnh vực nghiên cứu màng mỏng và bề mặt, Ångström được sử dụng để đo độ dày của các lớp nguyên tử cũng như sự phân bố của electron trên bề mặt. Điều này cực kỳ quan trọng trong việc phát triển các thiết bị điện tử hiện đại như màn hình OLED, pin mặt trời, và cảm biến siêu nhạy.
Nhờ vào việc sử dụng đơn vị Ångström, các nghiên cứu về electron đã đạt được những bước tiến vượt bậc, mở ra nhiều ứng dụng trong công nghệ và khoa học vật liệu. Việc hiểu rõ cấu trúc và phân bố electron ở mức độ Ångström không chỉ giúp chúng ta khám phá thế giới vi mô mà còn phát triển các công nghệ đột phá phục vụ đời sống.

Kết Luận Về Số Lượng Electron Trong Một Ångström
Số lượng electron trong một khoảng cách tương ứng với một Ångström (0,1 nanomet) phụ thuộc vào cấu trúc nguyên tử và cách các electron được phân bố trong không gian này. Mặc dù Ångström là đơn vị rất nhỏ, nhưng nó vẫn lớn hơn nhiều so với kích thước của một electron đơn lẻ. Tuy nhiên, khi xem xét các nguyên tử, đặc biệt là trong các nghiên cứu về cơ học lượng tử và cấu trúc phân tử, khoảng cách này có thể chứa nhiều electron tùy thuộc vào nguyên tử hoặc phân tử đang được nghiên cứu.
Ví dụ, trong một phân tử đơn giản như hydro (H₂), khoảng cách giữa hai hạt nhân của nguyên tử hydro thường vào khoảng 0,74 Ångström, và trong vùng không gian này, chúng ta có thể tính toán sự hiện diện của cặp electron liên kết giữa hai nguyên tử. Đối với các nguyên tử nặng hơn như oxy (O), số lượng electron trong không gian Ångström có thể lớn hơn do sự phân bố các electron trong các obitan nguyên tử và sự phức tạp của các liên kết hóa học.
Trong thực tế, số lượng electron trong một Ångström cũng phụ thuộc vào các yếu tố như điện tích hạt nhân, sự tương tác giữa các electron và mức năng lượng của chúng. Các phương pháp tính toán hiện đại như sử dụng hàm sóng Schrödinger hoặc các mô hình phân tử chi tiết cho phép xác định chính xác hơn về sự phân bố này. Những thông tin này không chỉ có ý nghĩa trong lý thuyết mà còn đóng vai trò quan trọng trong các ứng dụng thực tế như thiết kế vật liệu mới, nghiên cứu cấu trúc protein, và phát triển công nghệ nano.
Vì vậy, kết luận về số lượng electron trong một Ångström cho thấy rằng mặc dù chúng ta không thể xác định một con số cụ thể do tính phức tạp của các yếu tố liên quan, nhưng khoảng cách này là cơ sở để hiểu rõ hơn về cấu trúc vi mô của vật chất và các hiện tượng hóa học, vật lý xảy ra ở cấp độ nguyên tử.