
Chào bạn! Trong bài viết này, chúng ta sẽ khám phá về lý thuyết về hợp chất carbonyl trong môn hóa học 11. Hợp chất carbonyl là loại hợp chất hữu cơ có chứa nhóm chức carbonyl trong phân tử.
Bạn đang xem: Lý thuyết về hợp chất carbonyl – Hóa 11 chương trình mới
Contents
1. Khái niệm và danh pháp của hợp chất carbonyl
1.1 Khái niệm
Hợp chất carbonyl là những hợp chất hữu cơ mà trong phân tử có chứa nhóm chức carbonyl. Nhóm chức carbonyl tồn tại ở trong các aldehyde, ketone,…
-
Aldehyde là hợp chất hữu cơ có nhóm -CHO liên kết trực tiếp với nguyên tử carbon hoặc với nguyên tử hydrogen.
-
Dãy đồng đẳng của những aldehyde no, đơn chức và mạch hở có công thức chung như sau: CnH2n+1CHO (với n ≥ 1).
-
Ketone là hợp chất hữu cơ mà trong đó có chứa nhóm carbonyl liên kết với 2 gốc hydrocarbon.
1.2 Danh pháp
- Danh pháp thay thế:
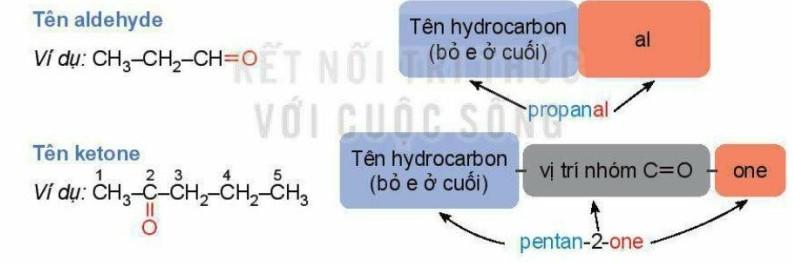
Chú ý: Đối với những hợp chất carbonyl mạch nhánh hoặc các chất có gốc hydrocarbon không no thì việc đánh số mạch chính cần được bắt đầu từ phía nào gần với nhóm carbonyl hơn.
- Tên gọi thông thường:
Một số các aldehyde và ketone đơn giản được gọi bằng tên thông thường và có nguồn gốc lịch sử nhất định. Tên thông thường của những aldehyde từ nguồn gốc tên của những acid tương ứng.
- Tên thông thường của aldehyde:
Với những aldehyde mà acid tương ứng của nó có tên thông thường thì gọi tên thông thường của aldehyde đó bằng cách thay đuôi “… ic acid” bằng đuôi “ …ic aldehyde” hoặc bằng “…aldehyde”.
Ví dụ như bảng dưới đây:

- Tên thông thường của ketone:
Một số ketone sẽ có tên thông thường. Ví dụ như:
CH3COCH3 có tên là Acetone
C6H5COCH3 có tên là Acetophenone.
1.3 Cấu tạo của hợp chất carbonyl
Đặc điểm cấu tạo nổi bật ở các hợp chất carbonyl là chúng có liên kết đôi C=O phân cực về hướng của nguyên tử oxygen.
2. Tính chất vật lý của hợp chất carbonyl
-
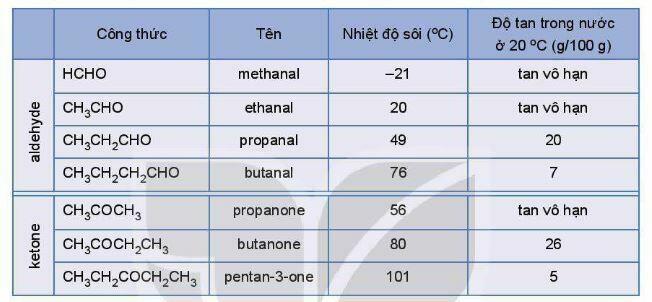
Những aldehyde và ketone sẽ có nhiệt độ sôi cao hơn khi so với những hydrocarbon mang khối lượng phân tử tương đương.
-
Ở nhiệt độ thường, các aldehyde tồn tại ở thể khí và có phân tử khối thường nhỏ, tan rất tốt ở trong nước. Khi số nguyên tử carbon tăng lên thì độ tan của hợp chất carbonyl sẽ bị giảm dần.
-
Hầu như các hợp chất carbonyl thơm đều không tan được trong nước.
3. Tính chất hóa học của hợp chất carbonyl
3.1 Phản ứng khử hợp chất carbonyl
Các hợp chất carbonyl bị khử bởi những tác nhân khử bao gồm NaBH4, LiAlH4,… hình thành những alcohol tương ứng. Aldehyde bị khử tạo ra alcohol bậc I tương ứng, còn ketone bị khử sẽ tạo ra alcohol bậc II.

3.2 Phản ứng oxy hóa aldehyde
- Oxi hóa aldehyde bằng nước bromine:
Aldehyde sẽ bị oxi hoá bằng nước bromine tạo ra carboxylic acid.
Ví dụ: CH3CHO + Br2 + H2O → CH3COOH + 2HBr
- Oxi hoá aldehyde bằng thuốc thử Tollens
Thuốc thử Tollens là một phức chất của ion Ag+ với nhóm ammonia, có công thức là [Ag(NH3)2]OH. Ion Ag+ có trong thuốc thử Tollens chính là chất oxi hoá.
- Thuốc thử Tollens chính là dung dịch AgNO3 ở trong NH3 dư:
AgNO3 + 3NH3 + H2O [Ag(NH3)2]OH + NH4NO3
- Phản ứng tổng quát của thuốc thử Tollens với aldehyde:
R-CH=O + 2[Ag(NH3)2]OH ⟶ R-COONH4 + 2Ag + 3NH3 + H2O
Phản ứng như trên gọi là phản ứng tráng bạc.
- Oxi hoá aldehyde bởi copper(II) hydroxide
Aldehyde có thể bị oxi hoá bằng copper(II) hydroxide Cu(OH)2 ở trong môi trường kiềm khi đun nóng sẽ tạo ra kết tủa copper(I) oxide (hay Cu2O) có màu đỏ gạch:
RCHO + 2 Cu(OH)2 + NaOH → RCOONa + Cu2O + 3H2O
Chú ý:
Ketone không tham gia phản ứng với thuốc thử Tollens hoặc Cu(OH)2 ở trong môi trường kiềm cho nên có thể sử dụng thuốc thử Tollens hoặc Cu(OH)2 ở trong môi trường kiềm nhằm phân biệt giữa aldehyde và ketone.
3.3 Phản ứng với hydrogen cyanide
Hợp chất carbonyl có thể tham gia phản ứng cộng với chất HCN, cộng vào liên kết đôi C=O.

3.4 Phản ứng tạo iodoform
Những hợp chất aldehyde và ketone có chứa nhóm methyl cạnh nhóm carbonyl có thể tham gia phản ứng với I2, ở trong môi trường kiềm. Phản ứng tạo ra sản phẩm kết tủa iodoform cho nên phản ứng như vậy được gọi là phản ứng lodoform và được sử dụng để nhận biết những aldehyde và ketone có chứa nhóm methyl cạnh nhóm carbonyl.

4. Ứng dụng và điều chế
4.1 Ứng dụng:
-
Formaldehyde chủ yếu được sử dụng trong việc sản xuất nhựa, phẩm nhuộm, dược phẩm và chất nổ. Dung dịch formaldehyde ở trong nước được gọi là dung dịch formalin giúp ngâm xác của động thực vật, tẩy uế hoặc tiệt trùng.
-
Acetaldehyde giúp sản xuất dược phẩm hoặc những chất có ứng dụng cao trong thực tiễn.
-
Acetone sử dụng làm dung môi trong quá trình sản xuất tơ nhân tạo hoặc thuốc súng không khói,… Ngoài ra, acetone còn được sử dụng nhiều trong quá trình tổng hợp Chloroform hoặc thuốc an thần.
4.2 Điều chế
Trong công nghiệp, một số hợp chất carbonyl được tổng hợp từ phương pháp oxi hoá những hydrocarbon, oxi hóa ethylene tạo ra acetaldehyde, oxi hoá cumene tạo ra acetone.
-
Phương trình điều chế acetaldehyde:
2CH2=CH2 + O2 ⟶ 2CH3-CH=O -
Phương trình điều chế acetone:
C6H5CH3 + O2 ⟶ C6H5COCH3
5. Bài tập về hợp chất carbonyl
Bài 1: Những aldehyde và ketone tạo ra mùi thơm đặc trưng cho các loài động vật và thực vật. Nhiều aldehyde và ketone cũng đóng vai trò quan trọng trong cơ thể như: tế bào võng mạc giúp cho mắt tiếp nhận được ánh sáng từ aldehyde, hormone giới tính nam và nữ có bản chất là các ketone. Hãy cho biết hợp chất carbonyl là gì và nó mang những tính chất nào?
Lời giải:
-
Hợp chất carbonyl là những hợp chất hữu cơ mà trong phân tử có chứa nhóm chức carbonyl. Nhóm chức carbonyl xuất hiện trong aldehyde, ketone …
-
Hợp chất carbonyl có khả năng tham gia vào các phản ứng:
- Phản ứng khử bằng những tác nhân khử bao gồm NaBH4; LiAlH4 …
- Phản ứng cộng với HCN, cộng vào liên kết đôi C=O.
- Những hợp chất aldehyde và ketone có chứa nhóm methyl cạnh nhóm carbonyl có khả năng tham gia phản ứng với I2 ở trong môi trường kiềm (hay còn gọi là phản ứng iodoform).
- Aldehyde dễ bị oxi hoá bằng những tác nhân oxi hoá thông thường bao gồm: Br2/H2O; [Ag(NH3)2]OH hoặc Cu(OH)2/OH−…
Bài 2: Cho biết những hợp chất cùng có khối lượng phân tử tương đương nhau và có nhiệt độ sôi như trong bảng dưới đây:
CH3CH2CH2CH3 CH3CH2CHO CH3CH2CH2OH
ts (oC) -0,5 49 97,1
Hãy so sánh nhiệt độ sôi giữa hợp chất carbonyl với alcohol và alkane mang khối lượng phân tử tương đương nhau. Dựa vào khả năng hình thành liên kết hydrogen và sự phân cực của các phân tử để có thể giải thích.
Lời giải:
-
Những hợp chất carbonyl sẽ có nhiệt độ sôi cao hơn so với những hydrocarbon mang khối lượng phân tử tương đương. Vì trong phân tử có chứa nhóm carbonyl phân cực nên phân tử hợp chất carbonyl cũng phân cực.
-
Xem thêm : Làm nhà hướng Đông Nam có tốt không?
Những hợp chất carbonyl sẽ có nhiệt độ sôi thấp hơn so với những alcohol mang khối lượng phân tử tương đương. Vì những hợp chất carbonyl không có liên kết hydrogen liên phân tử như ở những alcohol.
Bài 3: Phản ứng của hợp chất aldehyde với thuốc thử Tollens được thực hiện như sau:
Chuẩn bị: ống nghiệm, cốc nước nóng, dung dịch CH3CHO 5%, dung dịch NH3 5% và dung dịch AgNO3 1%
Tiến hành:
- Cho vào ống nghiệm khoảng 1 mL dung dịch AgNO3 1%.
- Thêm dần dung dịch NH3 5% vào trong ống nghiệm và lắc đều cho đến khi thấy kết tủa tan hoàn toàn.
- Nhỏ vài giọt của dung dịch CH3CHO 5% vào trong ống nghiệm và lắc đều lên.
- Đặt ống nghiệm vào trong một cốc có chứa nước nóng (khoảng tầm 70 – 80oC), để im trong vòng 5 phút.
Giải thích hiện tượng diễn ra có thể quan sát được và viết phương trình hoá học cho phản ứng diễn ra đó.
Lời giải:
Hiện tượng: Xuất hiện lớp bạc sáng bóng bám ở thành ống nghiệm. Vì aldehyde đã khử ion Ag+ có trong thuốc thử Tollens về tinh thể Ag.
Phương trình hoá học như sau:
CH3CHO + 2[Ag(NH3)2]OH ⟶ CH3COONH4 + 2Ag + 3NH3 + H2O
Bài 4: Thí nghiệm oxi hoá hợp chất CH3CHO bằng Cu(OH)2 được tiến hành như dưới đây:
- Cho 0,5 mL dung dịch CuSO4 5% cùng với tầm 1 mL dung dịch NaOH 10% vào trong ống nghiệm rồi lắc đều hỗn hợp lên.
- Thêm 1 mL hợp chất CH3CHO 5% vào trong ống nghiệm, rồi lại lắc đều ống nghiệm lên.
- Đun nóng nhẹ ống nghiệm đó ở trên ngọn lửa đèn cồn. Hỗn hợp phản ứng sẽ dần chuyển từ hỗn hợp màu xanh lam sang hỗn hợp màu đỏ gạch.
Trả lời các câu hỏi dưới đây:
a) Khi cho dung dịch CuSO4 vào với dung dịch NaOH, hỗn hợp sẽ tạo nên kết tủa có màu xanh lam, kết tủa ấy thực chất là chất gì?
b) Viết phương trình hoá học của những phản ứng đã xảy ra trong thí nghiệm nói trên.
Lời giải:
a) Khi cho dung dịch CuSO4 vào với dung dịch NaOH thì hỗn hợp sẽ tạo ra kết tủa có màu xanh lam, kết tủa ấy chính là copper(II) hydroxide (hay Cu(OH)2).
b) Phương trình hoá học của những phản ứng đã xảy ra:
CuSO4 + 2NaOH ⟶ Cu(OH)2 + Na2SO4
CH3CHO + 2Cu(OH)2 + NaOH ⟶ CH3COONa + Cu2O + 3H2O
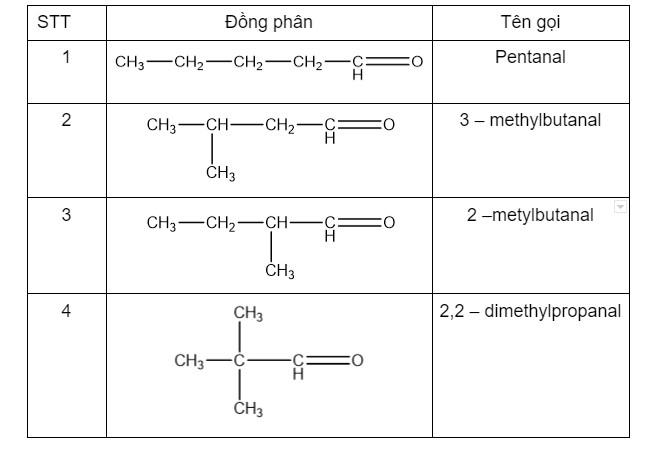
Bài 5: Viết công thức cấu tạo cũng như gọi tên thay thế của những aldehyde có chung công thức là C5H10O.
Lời giải:
Aldehyde C5H10O được thể hiện ở bảng dưới đây:

Bài 6: Em hãy tìm hiểu thêm bên ngoài và trình bày về những ứng dụng của một số aldehyde.
Lời giải:
Ứng dụng của một vài aldehyde đó là:
-
Formaldehyde được sử dụng chủ yếu nhằm sản xuất nhựa bao gồm poly(phenol – formaldehyde) hoặc urea formaldehyde. Formaldehyde cũng được dùng với mục đích sản xuất phẩm nhuộm, dược phẩm và chất nổ. Dung dịch chứa 37% – 40% formaldehyde ở trong nước, hay còn được gọi là formalin, được sử dụng nhằm ngâm xác những động thực vật hoặc tẩy uế và tiệt trùng.
-
Acetaldehyde (hay ethanal) được sử dụng nhiều trong quá trình tổng hợp hữu cơ để điều chế ra nhiều loại dược phẩm hoặc những chất có ứng dụng cao trong thực tiễn. Ví dụ từ acetaldehyde, người ta có thể điều chế được chất ethylidene diacetate sử dụng trong quá trình sản xuất poly(vinyl acetate).
-
Acetone có khả năng hoà tan tốt nhiều các chất hữu cơ khác nhau (bao gồm cả những polymer như cellulose trinitrate). Vì thế mà một lượng lớn acetone được sử dụng làm dung môi trong quá trình sản xuất tơ nhân tạo hoặc thuốc súng không khói … Ngoài ra, acetone còn được sử dụng nhiều trong quá trình tổng hợp hữu cơ như giúp tổng hợp nên bisphenol – A, chloroform hoặc thuốc an thần solfonal, …
Ngoài ra, nhiều hợp chất carbonyl có mùi thơm riêng biệt và được sử dụng với vai trò làm chất tạo hương ở trong công nghiệp thực phẩm hoặc mĩ phẩm: Benzaldehyde là chất có mùi và hương vị ở quả hạnh nhân, cinnamaldehyde có mùi thơm ở tinh dầu quế, vanillin là chất giúp tạo hương chính trong mùi thơm của kem vani, methone có mùi thơm đặc trưng của bạc hà và citral cho mùi thơm thoang thoảng của tinh dầu xả.
Bài 7: Trả lời những câu hỏi dưới đây:
- Vận dụng những kiến thức đã học về hợp chất carbonyl để giải thích về: những ứng dụng của các aldehyde và ketone ở trong cuộc sống bao gồm quá trình sản xuất gương hoặc làm dung môi,…
- Tìm hiểu về những ứng dụng của các hợp chất aldehyde và ketone có trong tự nhiên cùng với vai trò của một số aldehyde và ketone quan trọng đối với cơ thể con người.
Lời giải:
-
Phản ứng giữa aldehyde với thuốc thử Tollens tạo ra lớp bạc mỏng, sáng bóng bám ở thành bình nên phản ứng đó được ứng dụng vào quá trình sản xuất gương.
-
Một số hợp chất carbonyl có khả năng hoà tan tốt các chất hữu cơ khác nhau (bao gồm cả các polymer) nên được ứng dụng rất nhiều với vai trò dung môi.
-
Trong tự nhiên, những hợp chất có chứa nhóm chức của aldehyde và ketone tồn tại phổ biến ở trong tinh dầu của những loài cây cỏ được dùng làm chất tạo hương liệu trong công nghiệp mĩ phẩm hoặc thực phẩm.
-
Trong cơ thể người, một lượng rất ít acetone được hình thành qua quá trình chuyển hoá của chất béo không hoàn toàn. Ở người khoẻ mạnh bình thường, acetone được tạo ra ở gan và được chuyển hoá gần như hoàn toàn, chỉ còn một lượng rất nhỏ có mặt ở nước tiểu. Sự xuất hiện bất thường của acetone ở trong nước tiểu là một dấu hiệu của những bệnh nhân tiểu đường và được phát hiện thông qua quá trình xét nghiệm nước tiểu (chính là chỉ số KET).
Bài 8: Biết công thức cấu tạo của những chất carbonyl có công thức phân tử chung đều là C3H6O. Trình bày ít nhất hai phương pháp hoá học giúp phân biệt được các chất đó.
Lời giải:
Công thức có thể có của các hợp chất carbonyl là: CH3-CH2-CHO và CH3-CO-CH3.
Phương pháp hóa học như sau:
- Aldehyde khi phản ứng với thuốc thử Tollens sẽ tạo ra kết tủa màu xám bạc.
- Aldehyde khi phản ứng với Cu(OH)2 ở trong môi trường kiềm hình thành kết tủa có màu đỏ gạch (hay Cu2O).
- Hợp chất có chứa nhóm methyl ketone (hay CH3CO-R) khi phản ứng với iodine ở trong môi trường kiềm sẽ tạo ra kết tủa iodoform có màu vàng.

Kết luận
Sau bài viết này, chúng ta đã nắm được lý thuyết về hợp chất carbonyl và những tính chất và phản ứng của chúng. Đồng thời, cũng đã tìm hiểu về ứng dụng và điều chế của hợp chất carbonyl. Nếu bạn muốn tìm hiểu thêm các kiến thức khác thuộc môn hóa học 11 hoặc bất kỳ môn học nào khác, hãy truy cập vào website vuihoc.vn và đăng ký những khoá học phù hợp với bạn. Chúc bạn học tốt!
Nguồn: https://ispacedanang.edu.vn
Danh mục: Học tập









