Chủ đề độ phân cực: Độ phân cực là một yếu tố quan trọng ảnh hưởng đến tính chất và ứng dụng của các hợp chất trong hóa học và vật lý. Bài viết này sẽ giúp bạn hiểu rõ khái niệm độ phân cực, cách nó ảnh hưởng đến cấu trúc phân tử và các tính chất lý hóa, cùng với những ứng dụng thực tiễn trong đời sống và công nghiệp.
Mục lục
- Tổng Quan Về Độ Phân Cực
- Độ Phân Cực Trong Hóa Học
- Công Thức Tính Độ Phân Cực
- Kết Luận
- Độ Phân Cực Trong Hóa Học
- Công Thức Tính Độ Phân Cực
- Kết Luận
- Công Thức Tính Độ Phân Cực
- Kết Luận
- Kết Luận
- Mục Lục Tổng Hợp Về Độ Phân Cực
- 1. Định Nghĩa Và Khái Niệm Độ Phân Cực
- 2. Cấu Trúc Phân Tử Và Độ Phân Cực
- 3. Ảnh Hưởng Của Độ Phân Cực Đến Tính Chất Vật Lý
- 4. Độ Phân Cực Trong Các Hợp Chất Hóa Học Cụ Thể
- 5. Bài Tập Về Độ Phân Cực
- 6. Ứng Dụng Của Độ Phân Cực Trong Công Nghệ Và Y Học
Tổng Quan Về Độ Phân Cực
Độ phân cực là một khái niệm quan trọng trong lĩnh vực hóa học và vật lý, đề cập đến sự phân bố không đồng đều của các điện tích trong một phân tử. Điều này dẫn đến sự hình thành của các phân tử có một đầu dương và một đầu âm, tạo ra một lưỡng cực điện. Độ phân cực ảnh hưởng đến nhiều tính chất hóa học và vật lý của các chất, bao gồm độ tan, độ nhớt, và khả năng tương tác với các phân tử khác.

Độ Phân Cực Trong Hóa Học
Trong hóa học, độ phân cực của một phân tử phụ thuộc vào sự khác biệt độ âm điện giữa các nguyên tử. Khi có sự khác biệt lớn về độ âm điện, liên kết giữa các nguyên tử trở nên phân cực, với các electron bị hút về phía nguyên tử có độ âm điện cao hơn. Các liên kết phân cực thường gặp trong các hợp chất như nước (\(H_2O\)) và amoniac (\(NH_3\)).
- Liên kết cộng hóa trị phân cực: Xảy ra khi cặp electron liên kết không được chia sẻ đồng đều giữa hai nguyên tử, dẫn đến một phần của phân tử mang điện tích dương và phần còn lại mang điện tích âm.
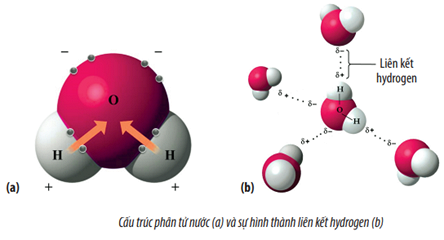
- Ví dụ về phân tử phân cực: Nước (\(H_2O\)) là một ví dụ điển hình, trong đó nguyên tử oxy có độ âm điện cao hơn nhiều so với hydro, tạo ra một phân tử với một đầu âm và một đầu dương.
Tác Động Của Độ Phân Cực
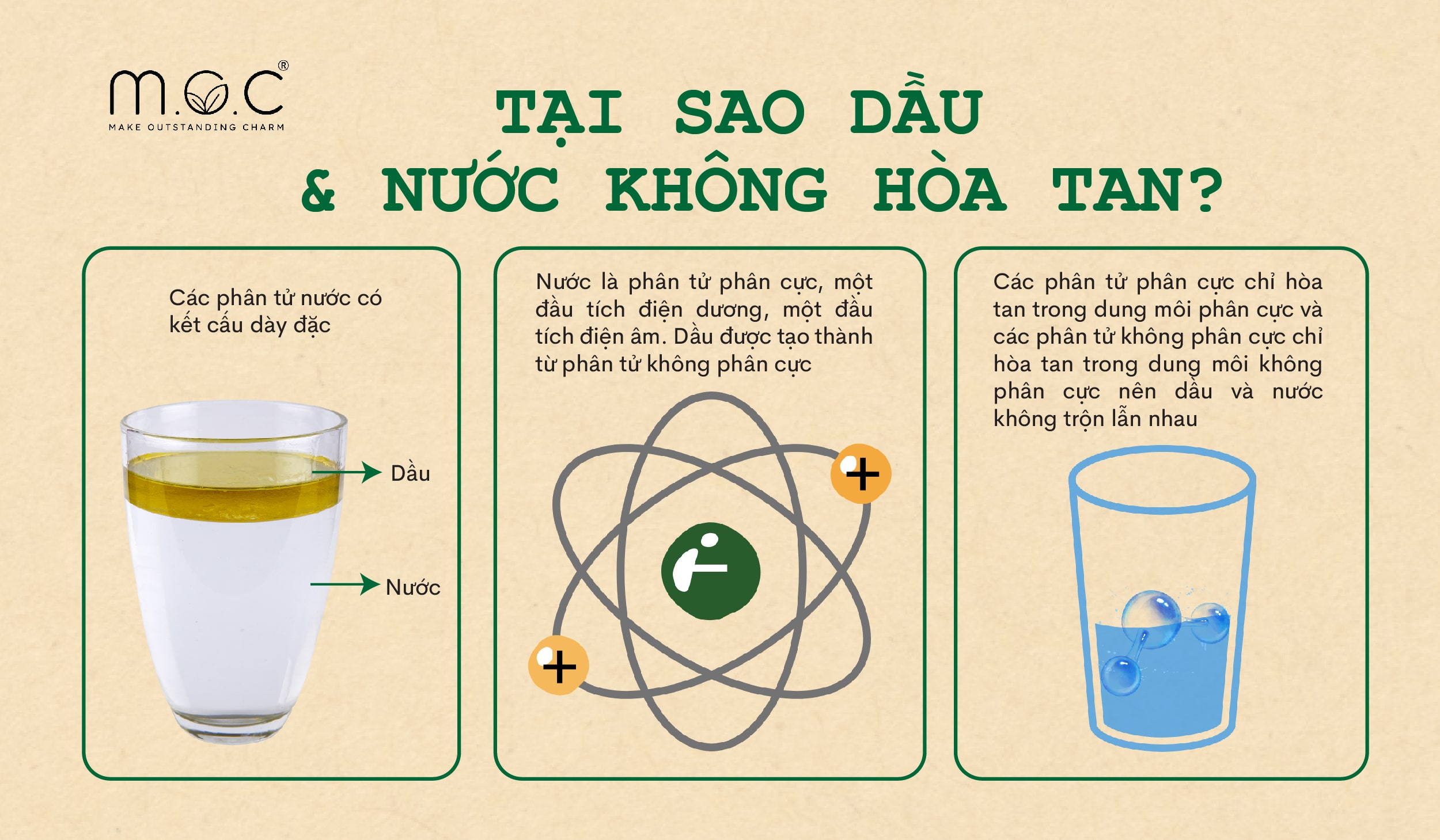
Độ phân cực ảnh hưởng mạnh mẽ đến tính chất vật lý và hóa học của chất. Ví dụ, các phân tử phân cực có xu hướng hòa tan tốt trong dung môi phân cực như nước, trong khi các phân tử không phân cực hòa tan tốt hơn trong các dung môi không phân cực như hexane.
Một số tính chất khác bị ảnh hưởng bởi độ phân cực bao gồm:
- Độ nhớt: Các chất có phân tử phân cực thường có độ nhớt cao hơn do các lực hút mạnh giữa các lưỡng cực.
- Điểm sôi: Các chất phân cực thường có điểm sôi cao hơn do lực hút giữa các phân tử mạnh hơn.
- Khả năng dẫn điện: Trong một số trường hợp, độ phân cực có thể ảnh hưởng đến khả năng dẫn điện của một chất, đặc biệt là trong các dung dịch.
Ứng Dụng Thực Tiễn
Độ phân cực có nhiều ứng dụng trong thực tiễn, từ việc thiết kế thuốc trong y học đến phát triển các vật liệu mới trong công nghiệp. Hiểu rõ về độ phân cực giúp các nhà khoa học tối ưu hóa các phản ứng hóa học, cải thiện hiệu suất của các quá trình công nghiệp và phát triển các sản phẩm có tính chất đặc biệt.
Công Thức Tính Độ Phân Cực
Độ phân cực của một phân tử thường được biểu thị qua mômen lưỡng cực (\(\mu\)), được tính theo công thức:
Trong đó:
- \(\mu\) là mômen lưỡng cực, đơn vị là Debye (D).
- \(q\) là điện tích, đơn vị là Coulomb (C).
- \(r\) là khoảng cách giữa hai điện tích, đơn vị là mét (m).

Kết Luận
Độ phân cực là một yếu tố quan trọng ảnh hưởng đến nhiều tính chất của các chất trong cả lĩnh vực hóa học và vật lý. Việc hiểu rõ khái niệm này không chỉ giúp chúng ta giải thích được các hiện tượng tự nhiên mà còn hỗ trợ trong việc phát triển các ứng dụng công nghệ mới.
Độ Phân Cực Trong Hóa Học
Trong hóa học, độ phân cực của một phân tử phụ thuộc vào sự khác biệt độ âm điện giữa các nguyên tử. Khi có sự khác biệt lớn về độ âm điện, liên kết giữa các nguyên tử trở nên phân cực, với các electron bị hút về phía nguyên tử có độ âm điện cao hơn. Các liên kết phân cực thường gặp trong các hợp chất như nước (\(H_2O\)) và amoniac (\(NH_3\)).
- Liên kết cộng hóa trị phân cực: Xảy ra khi cặp electron liên kết không được chia sẻ đồng đều giữa hai nguyên tử, dẫn đến một phần của phân tử mang điện tích dương và phần còn lại mang điện tích âm.
- Ví dụ về phân tử phân cực: Nước (\(H_2O\)) là một ví dụ điển hình, trong đó nguyên tử oxy có độ âm điện cao hơn nhiều so với hydro, tạo ra một phân tử với một đầu âm và một đầu dương.
Tác Động Của Độ Phân Cực
Độ phân cực ảnh hưởng mạnh mẽ đến tính chất vật lý và hóa học của chất. Ví dụ, các phân tử phân cực có xu hướng hòa tan tốt trong dung môi phân cực như nước, trong khi các phân tử không phân cực hòa tan tốt hơn trong các dung môi không phân cực như hexane.
Một số tính chất khác bị ảnh hưởng bởi độ phân cực bao gồm:
- Độ nhớt: Các chất có phân tử phân cực thường có độ nhớt cao hơn do các lực hút mạnh giữa các lưỡng cực.
- Điểm sôi: Các chất phân cực thường có điểm sôi cao hơn do lực hút giữa các phân tử mạnh hơn.
- Khả năng dẫn điện: Trong một số trường hợp, độ phân cực có thể ảnh hưởng đến khả năng dẫn điện của một chất, đặc biệt là trong các dung dịch.
Ứng Dụng Thực Tiễn
Độ phân cực có nhiều ứng dụng trong thực tiễn, từ việc thiết kế thuốc trong y học đến phát triển các vật liệu mới trong công nghiệp. Hiểu rõ về độ phân cực giúp các nhà khoa học tối ưu hóa các phản ứng hóa học, cải thiện hiệu suất của các quá trình công nghiệp và phát triển các sản phẩm có tính chất đặc biệt.

Công Thức Tính Độ Phân Cực
Độ phân cực của một phân tử thường được biểu thị qua mômen lưỡng cực (\(\mu\)), được tính theo công thức:
Trong đó:
- \(\mu\) là mômen lưỡng cực, đơn vị là Debye (D).
- \(q\) là điện tích, đơn vị là Coulomb (C).
- \(r\) là khoảng cách giữa hai điện tích, đơn vị là mét (m).
XEM THÊM:
Kết Luận
Độ phân cực là một yếu tố quan trọng ảnh hưởng đến nhiều tính chất của các chất trong cả lĩnh vực hóa học và vật lý. Việc hiểu rõ khái niệm này không chỉ giúp chúng ta giải thích được các hiện tượng tự nhiên mà còn hỗ trợ trong việc phát triển các ứng dụng công nghệ mới.

Công Thức Tính Độ Phân Cực
Độ phân cực của một phân tử thường được biểu thị qua mômen lưỡng cực (\(\mu\)), được tính theo công thức:
Trong đó:
- \(\mu\) là mômen lưỡng cực, đơn vị là Debye (D).
- \(q\) là điện tích, đơn vị là Coulomb (C).
- \(r\) là khoảng cách giữa hai điện tích, đơn vị là mét (m).

Kết Luận
Độ phân cực là một yếu tố quan trọng ảnh hưởng đến nhiều tính chất của các chất trong cả lĩnh vực hóa học và vật lý. Việc hiểu rõ khái niệm này không chỉ giúp chúng ta giải thích được các hiện tượng tự nhiên mà còn hỗ trợ trong việc phát triển các ứng dụng công nghệ mới.
Kết Luận
Độ phân cực là một yếu tố quan trọng ảnh hưởng đến nhiều tính chất của các chất trong cả lĩnh vực hóa học và vật lý. Việc hiểu rõ khái niệm này không chỉ giúp chúng ta giải thích được các hiện tượng tự nhiên mà còn hỗ trợ trong việc phát triển các ứng dụng công nghệ mới.

Mục Lục Tổng Hợp Về Độ Phân Cực
Độ phân cực là một khái niệm quan trọng trong cả hóa học và vật lý, ảnh hưởng lớn đến tính chất và ứng dụng của các hợp chất. Dưới đây là mục lục tổng hợp chi tiết về các khía cạnh liên quan đến độ phân cực:
- 1. Khái Niệm Độ Phân Cực
- 1.1. Định nghĩa cơ bản về độ phân cực
- 1.2. Độ phân cực trong hóa học
- 1.3. Độ phân cực trong vật lý
- 2. Độ Phân Cực Và Liên Kết Hóa Học
- 2.1. Liên kết cộng hóa trị và phân cực
- 2.2. Độ âm điện và sự phân cực
- 2.3. Ảnh hưởng của cấu trúc phân tử đến độ phân cực
- 3. Ảnh Hưởng Của Độ Phân Cực Đến Tính Chất Vật Lý
- 3.1. Tính chất điện và độ phân cực
- 3.2. Ảnh hưởng đến điểm sôi và nhiệt độ nóng chảy
- 3.3. Độ phân cực và khả năng hòa tan
- 4. Các Hợp Chất Cụ Thể Và Độ Phân Cực
- 4.1. Phân cực của phân tử nước \((H_2O)\)
- 4.2. Phân cực của phân tử amoniac \((NH_3)\)
- 4.3. Phân cực của phân tử carbon dioxide \((CO_2)\)
- 5. Ứng Dụng Của Độ Phân Cực
- 5.1. Ứng dụng trong thiết kế thuốc
- 5.2. Ứng dụng trong công nghệ vật liệu
- 5.3. Độ phân cực trong các thiết bị điện tử và cảm biến
Bằng cách hiểu rõ về độ phân cực, bạn có thể phân tích và dự đoán được nhiều tính chất quan trọng của các hợp chất hóa học và vật liệu, từ đó ứng dụng chúng vào các lĩnh vực khoa học và công nghệ khác nhau.
1. Định Nghĩa Và Khái Niệm Độ Phân Cực
Độ phân cực là một khái niệm quan trọng trong cả hóa học và vật lý, đề cập đến sự phân bố không đồng đều của điện tích trong một phân tử. Khi hai nguyên tử trong một phân tử có độ âm điện khác nhau, liên kết giữa chúng sẽ bị phân cực. Điều này có nghĩa là một phần của phân tử sẽ mang điện tích dương, trong khi phần kia mang điện tích âm, tạo ra một lưỡng cực điện.
Trong hóa học, độ phân cực được định nghĩa bằng sự khác biệt về độ âm điện giữa hai nguyên tử liên kết. Độ phân cực càng lớn, liên kết càng mang tính chất ion hơn. Ví dụ, trong phân tử nước \((H_2O)\), nguyên tử oxy có độ âm điện cao hơn so với nguyên tử hydro, dẫn đến phân tử nước có một lưỡng cực với oxy mang điện tích âm và hydro mang điện tích dương.
Công thức tính độ phân cực có thể được biểu diễn dưới dạng:
Trong đó:
- \(q\): Độ lớn của điện tích
- \(\vec{d}\): Khoảng cách giữa hai điện tích
Độ phân cực không chỉ ảnh hưởng đến cấu trúc phân tử mà còn tác động đến nhiều tính chất vật lý và hóa học khác nhau, như nhiệt độ nóng chảy, điểm sôi, và khả năng hòa tan của các chất.
2. Cấu Trúc Phân Tử Và Độ Phân Cực
Cấu trúc phân tử đóng vai trò quan trọng trong việc xác định độ phân cực của một phân tử. Độ phân cực không chỉ phụ thuộc vào sự khác biệt về độ âm điện giữa các nguyên tử mà còn chịu ảnh hưởng bởi hình dạng tổng thể của phân tử.
Một phân tử có thể có các liên kết phân cực nhưng không có độ phân cực nếu cấu trúc của nó đối xứng. Ví dụ, phân tử carbon dioxide \((CO_2)\) có hai liên kết \(\text{C=O}\) phân cực, nhưng do cấu trúc tuyến tính đối xứng, độ phân cực của hai liên kết này triệt tiêu lẫn nhau, khiến phân tử không có lưỡng cực điện tổng thể.
Ngược lại, phân tử nước \((H_2O)\) có hình dạng góc cạnh (góc liên kết khoảng 104.5 độ), dẫn đến một lưỡng cực điện rõ rệt do độ phân cực không bị triệt tiêu. Điều này làm cho nước có một đầu mang điện tích âm (ở phía nguyên tử oxy) và một đầu mang điện tích dương (ở phía các nguyên tử hydro).
Công thức tổng quát cho lưỡng cực điện của một phân tử có thể được viết là:
Trong đó:
- \(q_i\): Điện tích tại vị trí \(i\)
- \(\vec{r}_i\): Vectơ vị trí của điện tích so với một điểm tham chiếu
Sự phân bố không đều của các electron trong phân tử, kết hợp với cấu trúc hình học, tạo ra các tính chất vật lý đặc biệt như khả năng hòa tan trong nước, điểm sôi cao, và nhiệt độ nóng chảy khác biệt. Các yếu tố này đều xuất phát từ cấu trúc phân tử và độ phân cực tương ứng của chúng.

3. Ảnh Hưởng Của Độ Phân Cực Đến Tính Chất Vật Lý
Độ phân cực của các phân tử có ảnh hưởng đáng kể đến tính chất vật lý của các chất, bao gồm điểm sôi, độ hòa tan, và tính dẫn điện. Sự phân bố không đều của các điện tích trong phân tử tạo ra những lưỡng cực điện, dẫn đến các lực tương tác giữa các phân tử (liên kết hydro, lực Van der Waals) mạnh hơn hoặc yếu hơn, tùy thuộc vào mức độ phân cực.
Một trong những tác động quan trọng nhất của độ phân cực là khả năng hòa tan của các chất. Theo nguyên tắc "like dissolves like" (cùng loại hòa tan cùng loại), các phân tử phân cực thường hòa tan tốt trong dung môi phân cực như nước. Ví dụ, muối \((NaCl)\) hòa tan tốt trong nước vì cả hai đều có độ phân cực cao. Ngược lại, các phân tử không phân cực, như dầu, không hòa tan trong nước nhưng hòa tan trong các dung môi không phân cực như hexan.
Điểm sôi và điểm nóng chảy của các chất cũng chịu ảnh hưởng mạnh mẽ bởi độ phân cực. Các chất có độ phân cực cao thường có điểm sôi cao hơn do lực liên kết mạnh giữa các phân tử. Ví dụ, nước \((H_2O)\) có điểm sôi cao hơn nhiều so với hydro sulfide \((H_2S)\) mặc dù chúng có khối lượng phân tử tương tự, vì nước có liên kết hydro mạnh hơn do độ phân cực cao hơn.
Công thức tổng quát cho năng lượng liên kết giữa các phân tử có thể được biểu diễn như sau:
Trong đó:
- \(\mu_1\), \(\mu_2\): Độ lớn của các lưỡng cực điện của các phân tử
- \(r\): Khoảng cách giữa các phân tử
Độ phân cực cũng ảnh hưởng đến tính dẫn điện của các chất. Các chất phân cực thường có khả năng dẫn điện tốt hơn trong dung dịch, do sự phân tách các ion khi hòa tan, làm tăng tính dẫn điện của dung dịch.
4. Độ Phân Cực Trong Các Hợp Chất Hóa Học Cụ Thể
Độ phân cực trong các hợp chất hóa học là một yếu tố quyết định quan trọng đến tính chất và ứng dụng của chúng. Để hiểu rõ hơn về độ phân cực, chúng ta sẽ xem xét một số ví dụ cụ thể về các hợp chất phân cực và không phân cực, qua đó rút ra kết luận về cách thức độ phân cực ảnh hưởng đến các tính chất hóa học của chúng.
Một ví dụ điển hình là phân tử nước \((H_2O)\). Do sự chênh lệch độ âm điện giữa nguyên tử oxy và hai nguyên tử hydro, liên kết giữa chúng tạo ra một lưỡng cực điện. Kết quả là, phân tử nước có một đầu dương và một đầu âm, dẫn đến tính chất phân cực mạnh mẽ. Điều này giải thích tại sao nước có khả năng hòa tan nhiều chất khác nhau, đặc biệt là các hợp chất ion.
Ngược lại, các phân tử như carbon dioxide \((CO_2)\) lại không phân cực mặc dù có liên kết phân cực giữa carbon và oxy. Lý do là cấu trúc tuyến tính của \((CO_2)\) khiến các lưỡng cực điện của hai liên kết \(\text{C=O}\) triệt tiêu lẫn nhau, tạo ra một phân tử không phân cực.
Độ phân cực của một phân tử không chỉ phụ thuộc vào độ âm điện của các nguyên tử mà còn vào hình dạng hình học của phân tử đó. Ví dụ, trong phân tử methanol \((CH_3OH)\), liên kết \(\text{O-H}\) là phân cực, và do cấu trúc không đối xứng của phân tử, methanol là một chất phân cực.
Bảng dưới đây minh họa một số hợp chất hóa học cụ thể và độ phân cực của chúng:
| Hợp chất | Công thức | Độ phân cực |
|---|---|---|
| Nước | \(H_2O\) | Phân cực |
| Carbon dioxide | \(CO_2\) | Không phân cực |
| Methanol | \(CH_3OH\) | Phân cực |
| Ethan | \(C_2H_6\) | Không phân cực |
Kết luận, độ phân cực của các hợp chất hóa học cụ thể không chỉ ảnh hưởng đến tính chất vật lý mà còn đóng vai trò quan trọng trong các phản ứng hóa học và ứng dụng công nghiệp của chúng.
5. Bài Tập Về Độ Phân Cực
Dưới đây là một số bài tập liên quan đến độ phân cực của các phân tử và hợp chất hóa học. Các bài tập này giúp củng cố kiến thức về cách nhận biết độ phân cực và ảnh hưởng của nó đến tính chất vật lý và hóa học của các chất.
-
Xác định độ phân cực của các phân tử sau đây:
- Nước \((H_2O)\)
- Carbon dioxide \((CO_2)\)
- Ammonia \((NH_3)\)
- Methanol \((CH_3OH)\)
Giải thích lý do tại sao mỗi phân tử là phân cực hoặc không phân cực.
-
So sánh độ phân cực của các phân tử hydrogen fluoride \((HF)\) và hydrogen chloride \((HCl)\). Phân tử nào có độ phân cực lớn hơn và tại sao?
-
Cho biết mối quan hệ giữa độ phân cực của một phân tử và điểm sôi của nó. Giải thích tại sao nước có điểm sôi cao hơn so với các hợp chất có khối lượng phân tử tương đương như methane \((CH_4)\).
-
Lập bảng so sánh độ phân cực của các hợp chất sau: Ethanol \((C_2H_5OH)\), Dichloromethane \((CH_2Cl_2)\), và Ethene \((C_2H_4)\).
-
Vẽ cấu trúc Lewis của phân tử formaldehyde \((CH_2O)\) và xác định độ phân cực của nó. Dựa trên cấu trúc này, dự đoán tính chất vật lý của formaldehyde.
Những bài tập này không chỉ giúp làm rõ khái niệm về độ phân cực mà còn ứng dụng vào việc giải thích các hiện tượng trong thực tế liên quan đến tính chất của các chất.

6. Ứng Dụng Của Độ Phân Cực Trong Công Nghệ Và Y Học
Độ phân cực không chỉ là một khái niệm quan trọng trong hóa học và vật lý mà còn có nhiều ứng dụng thực tiễn trong công nghệ và y học. Sự phân cực ảnh hưởng đến tính chất của vật liệu, khả năng tương tác với môi trường, và hiệu quả trong các ứng dụng cụ thể. Dưới đây là một số ứng dụng tiêu biểu của độ phân cực:
6.1. Ứng Dụng Trong Phát Triển Vật Liệu Mới
- Thiết Kế Vật Liệu Chống Thấm: Độ phân cực của các phân tử được sử dụng để phát triển các vật liệu có tính chất chống thấm, giúp ngăn chặn sự thấm nước và dầu. Ví dụ, các lớp phủ phân cực có thể được áp dụng trên bề mặt kính hoặc vải để tăng cường tính chống thấm.
- Phát Triển Vật Liệu Nano: Độ phân cực được ứng dụng trong việc phát triển các vật liệu nano với các tính chất đặc biệt. Các vật liệu này có thể được sử dụng trong nhiều lĩnh vực khác nhau như y tế, điện tử, và môi trường.
- Công Nghệ Lọc Nước: Độ phân cực của các màng lọc được tối ưu hóa để tăng hiệu quả lọc, giúp loại bỏ các chất gây ô nhiễm trong nước và cải thiện chất lượng nước uống.
6.2. Ứng Dụng Trong Thiết Kế Thuốc
- Thiết Kế Phân Tử Thuốc: Độ phân cực của các phân tử thuốc ảnh hưởng đến khả năng xâm nhập vào tế bào và tương tác với các mục tiêu sinh học. Các nhà khoa học sử dụng độ phân cực để thiết kế các phân tử thuốc có khả năng tương tác chính xác và hiệu quả với các thụ thể trên bề mặt tế bào.
- Tối Ưu Hóa Dược Động Học: Độ phân cực ảnh hưởng đến quá trình hấp thu, phân bố, chuyển hóa và bài tiết của thuốc trong cơ thể. Điều này giúp tối ưu hóa liều lượng và cách thức sử dụng thuốc, đảm bảo hiệu quả điều trị và giảm thiểu tác dụng phụ.
- Ứng Dụng Trong Chẩn Đoán Y Khoa: Độ phân cực của các hợp chất hóa học được sử dụng trong các thiết bị chẩn đoán như máy MRI và siêu âm. Đặc tính phân cực của các phân tử tương tác với từ trường và sóng âm, cung cấp hình ảnh chi tiết về cấu trúc và chức năng của các mô và cơ quan trong cơ thể.
Nhìn chung, độ phân cực có vai trò quan trọng trong nhiều lĩnh vực khoa học và công nghệ, từ việc phát triển vật liệu mới đến cải tiến phương pháp chẩn đoán và điều trị y học. Những tiến bộ trong nghiên cứu về độ phân cực không chỉ nâng cao hiểu biết của chúng ta về thế giới tự nhiên mà còn mở ra những cơ hội mới cho các ứng dụng thực tiễn.