Chủ đề thế nào là số hiệu nguyên tử: Số hiệu nguyên tử là khái niệm quan trọng trong hóa học, giúp xác định vị trí của một nguyên tố trong bảng tuần hoàn và nhiều tính chất liên quan. Bài viết này sẽ giúp bạn hiểu rõ về số hiệu nguyên tử, cách xác định và vai trò quan trọng của nó trong khoa học cũng như trong cuộc sống hàng ngày.
Mục lục
- Số Hiệu Nguyên Tử Là Gì?
- 1. Khái Niệm Số Hiệu Nguyên Tử
- 2. Lịch Sử Phát Triển Của Khái Niệm Số Hiệu Nguyên Tử
- 3. Cách Xác Định Số Hiệu Nguyên Tử
- 4. Ứng Dụng Của Số Hiệu Nguyên Tử Trong Thực Tế
- 5. Vai Trò Của Số Hiệu Nguyên Tử Trong Bảng Tuần Hoàn
- 6. Các Nguyên Tố Đặc Biệt Và Số Hiệu Nguyên Tử
- 7. Số Hiệu Nguyên Tử Và Phản Ứng Hóa Học
- 8. Câu Hỏi Thường Gặp Về Số Hiệu Nguyên Tử
Số Hiệu Nguyên Tử Là Gì?
Số hiệu nguyên tử (\( Z \)) là một khái niệm cơ bản trong hóa học và vật lý, đại diện cho số lượng proton có trong hạt nhân của một nguyên tử. Số hiệu nguyên tử giúp xác định vị trí của nguyên tố trong bảng tuần hoàn và quyết định tính chất hóa học của nguyên tố đó.
Cách Xác Định Số Hiệu Nguyên Tử
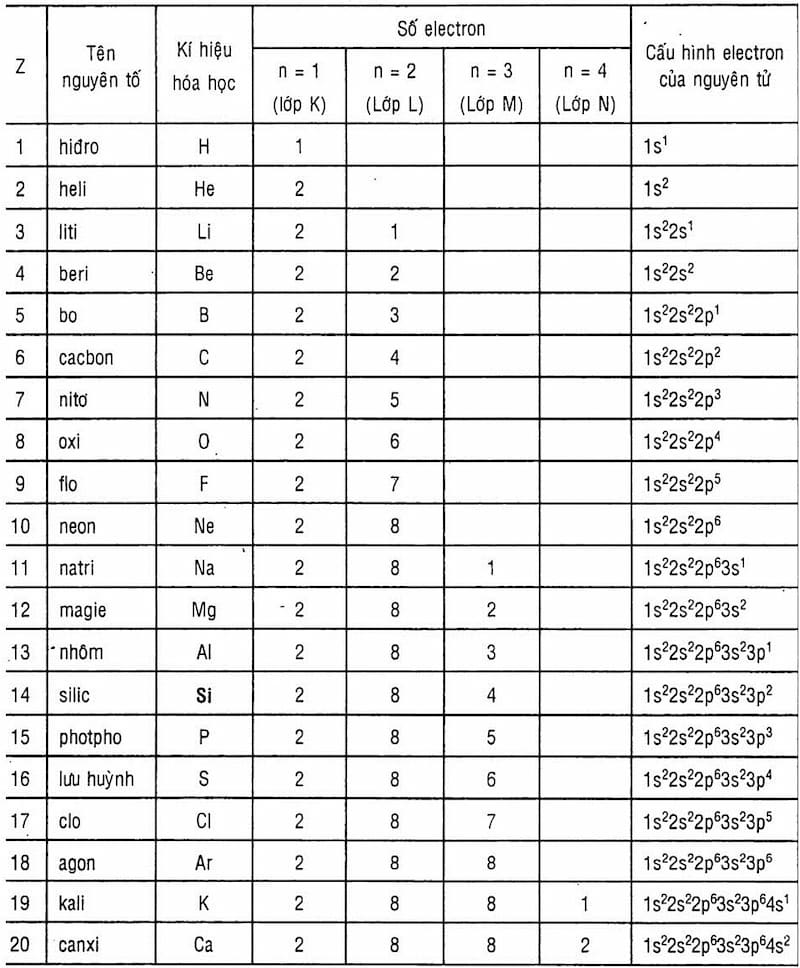
- Sử dụng bảng tuần hoàn: Số hiệu nguyên tử của một nguyên tố chính là số thứ tự của nguyên tố đó trong bảng tuần hoàn. Ví dụ, Hydrogen có số hiệu nguyên tử là 1.
- Đếm số lượng proton: Số lượng proton trong hạt nhân của nguyên tử tương ứng với số hiệu nguyên tử. Ví dụ, Carbon có 6 proton, vì vậy số hiệu nguyên tử của nó là 6.
- Phổ kế khối lượng: Kỹ thuật này sử dụng để xác định số proton trong hạt nhân bằng cách phân tích tỷ lệ khối lượng/điện tích (\( m/z \)) của các ion.
Phương Pháp Tiên Tiến Để Xác Định Số Hiệu Nguyên Tử
| Phương Pháp | Ưu Điểm | Nhược Điểm |
|---|---|---|
| Sử dụng bảng tuần hoàn | Đơn giản, trực quan | Không chính xác nếu không có bảng tuần hoàn |
| Đếm số lượng proton | Chính xác | Yêu cầu thiết bị phức tạp |
| Phổ kế khối lượng | Chính xác cao, phân tích được nhiều loại nguyên tử | Đắt tiền, yêu cầu kỹ thuật cao |
| Công nghệ tiên tiến (Hiển vi điện tử, Phổ phân tích tia X) | Chính xác, đa dạng phương pháp | Yêu cầu thiết bị và chuyên môn cao |
Lịch Sử Phát Triển Của Khái Niệm Số Hiệu Nguyên Tử
Khái niệm số hiệu nguyên tử đã trải qua nhiều giai đoạn phát triển quan trọng:
- John Dalton (1803): Đưa ra thuyết nguyên tử hiện đại đầu tiên.
- Dmitri Mendeleev (1869): Xây dựng bảng tuần hoàn dựa trên khối lượng nguyên tử và tính chất hóa học.
- Henry Moseley (1913): Chứng minh rằng số hiệu nguyên tử là số lượng proton trong hạt nhân bằng phương pháp phổ X-ray.
- Glenn T. Seaborg (1940s): Phát hiện các nguyên tố siêu urani và cải tiến cấu trúc bảng tuần hoàn.
Ứng Dụng Của Số Hiệu Nguyên Tử Trong Thực Tế
Số hiệu nguyên tử không chỉ là một con số mà còn là cơ sở để xác định và phân loại các nguyên tố trong tự nhiên. Nó đóng vai trò quan trọng trong:
- Nghiên cứu khoa học: Giúp xác định tính chất và phản ứng hóa học của các nguyên tố.
- Phát triển công nghệ: Ứng dụng trong việc chế tạo vật liệu mới, y học hạt nhân và công nghệ cao.
- Giáo dục: Là một phần quan trọng trong giảng dạy hóa học và vật lý tại các trường học.

1. Khái Niệm Số Hiệu Nguyên Tử
Số hiệu nguyên tử là một đại lượng quan trọng trong hóa học và vật lý hạt nhân, biểu thị số lượng proton trong hạt nhân của một nguyên tử. Nó xác định vị trí của nguyên tố trong bảng tuần hoàn và là đặc trưng cơ bản để phân biệt các nguyên tố với nhau. Cụ thể, số hiệu nguyên tử được ký hiệu là \(Z\).
- Số hiệu nguyên tử của hydro là 1 vì nó có 1 proton trong hạt nhân.
- Số hiệu nguyên tử của carbon là 6, có 6 proton trong hạt nhân.
- Điều này đồng nghĩa rằng, mỗi nguyên tố hóa học đều có một số hiệu nguyên tử duy nhất.
Số hiệu nguyên tử không chỉ xác định nguyên tố mà còn ảnh hưởng đến các tính chất hóa học của nguyên tố đó. Ví dụ, các nguyên tố có cùng số hiệu nguyên tử nhưng khác nhau về số neutron sẽ là các đồng vị của nhau.
| Nguyên Tố | Số Hiệu Nguyên Tử (\(Z\)) | Số Proton |
|---|---|---|
| Hydro (H) | 1 | 1 |
| Carbon (C) | 6 | 6 |
| Oxy (O) | 8 | 8 |
Số hiệu nguyên tử được xác định qua các thí nghiệm khoa học, như việc sử dụng phổ kế khối lượng, và có ý nghĩa quan trọng trong việc hiểu về cấu trúc nguyên tử và phản ứng hóa học. Nó là nền tảng cho việc sắp xếp các nguyên tố trong bảng tuần hoàn, giúp dễ dàng dự đoán tính chất hóa học của các nguyên tố.
2. Lịch Sử Phát Triển Của Khái Niệm Số Hiệu Nguyên Tử
Khái niệm số hiệu nguyên tử đã trải qua một quá trình phát triển lâu dài và đáng chú ý trong lịch sử khoa học, đặc biệt là trong lĩnh vực hóa học và vật lý. Dưới đây là một số mốc quan trọng đánh dấu sự tiến hóa của khái niệm này:
- John Dalton (1803): Dalton là một trong những người đầu tiên đề xuất thuyết nguyên tử hiện đại, cho rằng các nguyên tố hóa học được tạo thành từ các nguyên tử nhỏ không thể chia cắt.
- Dmitri Mendeleev (1869): Mendeleev đã xây dựng bảng tuần hoàn các nguyên tố dựa trên khối lượng nguyên tử và tính chất hóa học của chúng, tiên đoán sự tồn tại của các nguyên tố chưa được khám phá.
- Henry Moseley (1913): Moseley là người đầu tiên xác định rằng số hiệu nguyên tử tương ứng với số proton trong hạt nhân nguyên tử. Ông sử dụng phổ X-ray để xác định số proton và sắp xếp các nguyên tố trong bảng tuần hoàn theo số hiệu nguyên tử thay vì khối lượng nguyên tử.
- Glenn T. Seaborg (1940s): Seaborg đã phát hiện ra các nguyên tố siêu urani và đề xuất thay đổi cấu trúc của bảng tuần hoàn để bao gồm các nguyên tố mới này.
Trong những năm gần đây, các tiến bộ trong công nghệ như phổ kế khối lượng hiện đại đã giúp đo chính xác số lượng proton trong hạt nhân, góp phần quan trọng vào việc xác định số hiệu nguyên tử cho các nguyên tố mới.
| Phương pháp | Ưu điểm | Nhược điểm |
|---|---|---|
| Hiển vi điện tử truyền qua (TEM) | Quan sát cấu trúc nguyên tử và đếm số proton | Yêu cầu thiết bị phức tạp |
| Phổ phân tích tia X (XPS) | Phân tích năng lượng electron để suy ra số proton | Đòi hỏi kỹ thuật cao |
| Bảng tuần hoàn | Đơn giản, trực quan | Không chính xác nếu thiếu thông tin |
Khái niệm số hiệu nguyên tử không chỉ đơn thuần là một con số, mà nó còn đại diện cho sự phát triển của khoa học và công nghệ trong việc khám phá và hiểu rõ hơn về cấu trúc của nguyên tử.

3. Cách Xác Định Số Hiệu Nguyên Tử
Số hiệu nguyên tử là một con số quan trọng đại diện cho số proton trong hạt nhân của một nguyên tử, xác định đặc điểm của nguyên tố hóa học đó. Việc xác định số hiệu nguyên tử có thể được thực hiện thông qua các bước đơn giản sau:
- Sử dụng bảng tuần hoàn:
- Bảng tuần hoàn là công cụ hữu ích và phổ biến nhất để xác định số hiệu nguyên tử. Mỗi nguyên tố trên bảng có số hiệu nguyên tử riêng, thường được hiển thị ở góc trên bên trái của ô chứa nguyên tố.
- Xác định qua số proton:
- Số hiệu nguyên tử bằng đúng số lượng proton có trong hạt nhân nguyên tử. Ví dụ, hydro có 1 proton nên số hiệu nguyên tử là 1, carbon có 6 proton nên số hiệu nguyên tử là 6.
- Sử dụng phổ phân tích tia X (X-ray Spectroscopy):
- Kỹ thuật này phân tích năng lượng của các tia X phát ra từ nguyên tử để xác định số lượng proton, từ đó xác định số hiệu nguyên tử.
- Hiển vi điện tử truyền qua (TEM):
- Sử dụng hiển vi điện tử để quan sát cấu trúc nguyên tử và xác định số proton, giúp xác định số hiệu nguyên tử một cách trực tiếp và chính xác.
| Phương Pháp | Mô Tả | Độ Chính Xác |
|---|---|---|
| Bảng tuần hoàn | Xác định số hiệu nguyên tử từ vị trí của nguyên tố trên bảng tuần hoàn. | Cao |
| Số proton | Xác định số proton trong hạt nhân để tìm số hiệu nguyên tử. | Rất cao |
| Phổ phân tích tia X | Phân tích phổ tia X phát ra từ nguyên tử để xác định số proton. | Rất cao |
| Hiển vi điện tử truyền qua (TEM) | Quan sát trực tiếp cấu trúc nguyên tử để đếm số proton. | Rất cao |
Việc xác định số hiệu nguyên tử không chỉ giúp xác định nguyên tố mà còn cung cấp thông tin quan trọng về tính chất hóa học và vật lý của nó, đóng vai trò quan trọng trong nghiên cứu và ứng dụng khoa học hiện đại.

4. Ứng Dụng Của Số Hiệu Nguyên Tử Trong Thực Tế
Số hiệu nguyên tử không chỉ đơn thuần là một con số đại diện cho số proton trong hạt nhân, mà còn có nhiều ứng dụng quan trọng trong thực tế, từ nghiên cứu khoa học đến các ngành công nghiệp khác nhau. Dưới đây là một số ứng dụng nổi bật của số hiệu nguyên tử:
- Xác định và phân loại nguyên tố:
- Số hiệu nguyên tử giúp xác định rõ ràng nguyên tố nào đó thuộc loại gì, từ đó phân loại chúng trong bảng tuần hoàn. Điều này giúp các nhà khoa học và kỹ sư dễ dàng nhận biết và sử dụng nguyên tố phù hợp cho các ứng dụng cụ thể.
- Sử dụng trong y học:
- Các nguyên tố có số hiệu nguyên tử cụ thể được sử dụng trong các phương pháp điều trị và chẩn đoán y khoa, như sử dụng iodine (\(Z = 53\)) trong điều trị tuyến giáp, hoặc các nguyên tố phóng xạ trong xạ trị ung thư.
- Ứng dụng trong công nghệ vật liệu:
- Số hiệu nguyên tử giúp xác định đặc tính hóa học và vật lý của nguyên tố, từ đó chọn ra vật liệu phù hợp cho sản xuất công nghiệp, như sản xuất hợp kim, chất bán dẫn, hoặc vật liệu siêu dẫn.
- Phân tích môi trường:
- Sử dụng số hiệu nguyên tử để xác định và theo dõi các chất gây ô nhiễm trong môi trường, ví dụ như xác định các kim loại nặng trong nước và đất, từ đó đưa ra các biện pháp xử lý kịp thời.
- Nghiên cứu khoa học cơ bản:
- Số hiệu nguyên tử là cơ sở cho các nghiên cứu khoa học cơ bản về cấu trúc nguyên tử và phân tử, giúp mở rộng hiểu biết của con người về vật chất và vũ trụ.
| Ứng Dụng | Mô Tả | Ví Dụ |
|---|---|---|
| Y học | Chẩn đoán và điều trị bệnh lý thông qua các nguyên tố có số hiệu nguyên tử cụ thể. | Điều trị tuyến giáp bằng iodine (\(Z = 53\)). |
| Công nghệ vật liệu | Chọn vật liệu phù hợp dựa trên đặc tính nguyên tố. | Sản xuất hợp kim, chất bán dẫn. |
| Phân tích môi trường | Giám sát các chất gây ô nhiễm. | Xác định kim loại nặng trong nước. |
| Nghiên cứu khoa học | Khám phá cấu trúc và tính chất của vật chất. | Nghiên cứu cấu trúc phân tử. |
Như vậy, số hiệu nguyên tử không chỉ là công cụ định danh nguyên tố mà còn có vai trò quan trọng trong nhiều lĩnh vực khác nhau của cuộc sống, từ y tế, công nghệ đến nghiên cứu khoa học, góp phần nâng cao chất lượng cuộc sống và thúc đẩy sự phát triển của khoa học kỹ thuật.

5. Vai Trò Của Số Hiệu Nguyên Tử Trong Bảng Tuần Hoàn
Số hiệu nguyên tử (\( Z \)) đóng vai trò quan trọng trong việc xác định vị trí và tính chất của các nguyên tố trong bảng tuần hoàn. Đây là con số đại diện cho số lượng proton trong hạt nhân của một nguyên tử, giúp phân biệt mỗi nguyên tố với các nguyên tố khác.
- Định vị nguyên tố: Trong bảng tuần hoàn, các nguyên tố được sắp xếp theo số hiệu nguyên tử tăng dần từ trái sang phải, từ trên xuống dưới. Điều này giúp xác định vị trí chính xác của mỗi nguyên tố trong bảng.
- Quy định tính chất hóa học: Số hiệu nguyên tử ảnh hưởng trực tiếp đến cấu hình electron của nguyên tử, từ đó quyết định tính chất hóa học của nguyên tố. Ví dụ, các nguyên tố trong cùng một nhóm thường có tính chất hóa học tương tự do có cùng số electron hóa trị.
- Phân nhóm và chu kỳ: Số hiệu nguyên tử giúp phân chia các nguyên tố vào các nhóm và chu kỳ trong bảng tuần hoàn. Các nguyên tố trong cùng một nhóm có số electron ở lớp ngoài cùng giống nhau, trong khi các nguyên tố trong cùng một chu kỳ có cùng số lớp electron.
- Dự đoán tính chất: Bằng cách biết số hiệu nguyên tử, người ta có thể dự đoán được nhiều tính chất vật lý và hóa học của nguyên tố như bán kính nguyên tử, năng lượng ion hóa, ái lực electron, và độ âm điện.
Như vậy, số hiệu nguyên tử không chỉ là một con số định danh mà còn đóng vai trò nền tảng trong việc cấu trúc và hiểu biết về bảng tuần hoàn, giúp con người dễ dàng hơn trong việc học tập và nghiên cứu các nguyên tố hóa học.
XEM THÊM:
6. Các Nguyên Tố Đặc Biệt Và Số Hiệu Nguyên Tử
6.1 Các Nguyên Tố Hiếm Và Số Hiệu Nguyên Tử
Nguyên tố hiếm là những nguyên tố có số hiệu nguyên tử cao, thường xuất hiện với số lượng rất nhỏ trong tự nhiên. Những nguyên tố này đóng vai trò quan trọng trong nhiều lĩnh vực khoa học và công nghệ, từ vật liệu siêu dẫn đến công nghệ y học. Ví dụ, các nguyên tố thuộc nhóm Lanthanide và Actinide đều có số hiệu nguyên tử cao và được sử dụng trong các ứng dụng tiên tiến như sản xuất màn hình hiển thị, pin năng lượng, và nghiên cứu vật liệu.
- Lanthanum (La, Z=57): Được sử dụng trong gốm sứ, quang học và nam châm mạnh.
- Neodymium (Nd, Z=60): Thành phần chính trong nam châm vĩnh cửu và các thiết bị điện tử hiện đại.
- Uranium (U, Z=92): Nguyên tố hiếm có ứng dụng rộng rãi trong ngành năng lượng hạt nhân.
6.2 Các Đồng Vị Và Số Hiệu Nguyên Tử
Đồng vị là những nguyên tử của cùng một nguyên tố nhưng có số khối khác nhau do sự khác biệt về số neutron trong hạt nhân. Mặc dù số hiệu nguyên tử (Z) của các đồng vị của một nguyên tố là như nhau, nhưng sự khác biệt về số neutron tạo ra các đặc tính vật lý khác biệt. Điều này đặc biệt quan trọng trong các ứng dụng y học và khoa học, nơi các đồng vị được sử dụng để nghiên cứu sự phân rã phóng xạ, điều trị ung thư, và theo dõi các phản ứng hóa học.
- Carbon-12 (C-12): Đồng vị ổn định của carbon, chiếm phần lớn carbon trong tự nhiên.
- Carbon-14 (C-14): Đồng vị phóng xạ của carbon, được sử dụng trong phương pháp định tuổi bằng carbon.
- Iodine-131 (I-131): Đồng vị phóng xạ của iodine, được sử dụng trong điều trị bệnh lý tuyến giáp.

7. Số Hiệu Nguyên Tử Và Phản Ứng Hóa Học
Số hiệu nguyên tử không chỉ là một con số xác định vị trí của nguyên tố trong bảng tuần hoàn mà còn có vai trò quyết định đến tính chất hóa học của nguyên tố đó, từ đó ảnh hưởng trực tiếp đến các phản ứng hóa học mà nó tham gia. Dưới đây là những khía cạnh chính của số hiệu nguyên tử trong mối liên hệ với phản ứng hóa học:
7.1 Ảnh Hưởng Của Số Hiệu Nguyên Tử Đến Tính Phản Ứng
Số hiệu nguyên tử \(Z\) xác định số lượng proton trong hạt nhân của một nguyên tử và từ đó xác định số electron trong nguyên tử khi ở trạng thái trung hòa điện. Số lượng electron này quyết định cấu trúc electron của nguyên tử, và cấu trúc electron là yếu tố chính ảnh hưởng đến tính phản ứng của nguyên tử.
- Những nguyên tố có số hiệu nguyên tử nhỏ thường có xu hướng nhường hoặc nhận electron dễ dàng để đạt được cấu hình electron ổn định, từ đó thể hiện tính phản ứng mạnh mẽ.
- Nguyên tố có số hiệu nguyên tử lớn hơn thường có nhiều lớp electron, làm giảm lực hút của hạt nhân đối với electron ngoài cùng, dẫn đến tính phản ứng thay đổi tùy thuộc vào vị trí của nguyên tố trong bảng tuần hoàn.
7.2 Mối Liên Hệ Với Cấu Trúc Electron
Cấu trúc electron của một nguyên tử, vốn được quyết định bởi số hiệu nguyên tử, ảnh hưởng mạnh mẽ đến cách nguyên tử đó tương tác với các nguyên tử khác trong các phản ứng hóa học. Ví dụ:
- Nguyên tố có số hiệu nguyên tử nhỏ như hydrogen (Z = 1) chỉ có một electron và dễ dàng tham gia vào các phản ứng tạo liên kết đơn giản.
- Các nguyên tố thuộc nhóm Halogen như fluorine (Z = 9) có 7 electron ở lớp ngoài cùng, khiến chúng dễ dàng nhận thêm một electron để tạo liên kết ion với các kim loại.
- Các nguyên tố kim loại chuyển tiếp có số hiệu nguyên tử lớn hơn có cấu trúc electron phức tạp hơn, cho phép chúng tham gia vào các phản ứng đa dạng và tạo ra nhiều hợp chất với các mức oxi hóa khác nhau.
Nhìn chung, số hiệu nguyên tử là yếu tố then chốt trong việc dự đoán và giải thích tính chất hóa học của các nguyên tố, đồng thời đóng vai trò quan trọng trong việc hiểu biết các phản ứng hóa học.

8. Câu Hỏi Thường Gặp Về Số Hiệu Nguyên Tử
-
Số hiệu nguyên tử là gì?
Số hiệu nguyên tử, còn gọi là số nguyên tử, là số proton có trong hạt nhân của một nguyên tử. Ký hiệu của số hiệu nguyên tử là \(Z\). Số hiệu nguyên tử xác định duy nhất một nguyên tố hóa học, và trong một nguyên tử không tích điện, số proton bằng với số electron.
-
Làm thế nào để xác định số hiệu nguyên tử của một nguyên tố?
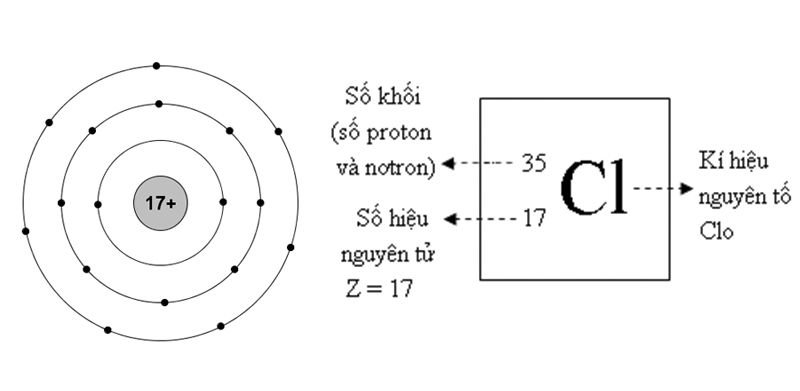
Để xác định số hiệu nguyên tử của một nguyên tố, bạn cần biết số proton trong hạt nhân của nguyên tử đó. Ví dụ, nguyên tử cacbon có 6 proton, do đó số hiệu nguyên tử của cacbon là \(Z = 6\).
-
Tại sao số hiệu nguyên tử lại quan trọng?
Số hiệu nguyên tử rất quan trọng vì nó quyết định tính chất hóa học của một nguyên tố. Vị trí của một nguyên tố trong bảng tuần hoàn cũng được xác định dựa trên số hiệu nguyên tử của nó. Các nguyên tố có cùng số hiệu nguyên tử sẽ có những đặc điểm hóa học tương tự nhau.
-
Số hiệu nguyên tử có thay đổi không?
Số hiệu nguyên tử không thay đổi cho một nguyên tố cụ thể. Tuy nhiên, các đồng vị của một nguyên tố có thể có số neutron khác nhau, dẫn đến khác biệt về khối lượng nguyên tử, nhưng số proton (tức là số hiệu nguyên tử) vẫn giữ nguyên.
-
Làm thế nào để số hiệu nguyên tử liên quan đến khối lượng nguyên tử?
Khối lượng nguyên tử \(A\) là tổng số proton (\(Z\)) và neutron (\(N\)) trong hạt nhân: \[A = Z + N\]. Tuy nhiên, số hiệu nguyên tử chỉ phản ánh số proton, do đó nó không trực tiếp xác định khối lượng nguyên tử mà chỉ quyết định danh tính của nguyên tố.