Chủ đề số hiệu nguyên tử 15: Số hiệu nguyên tử 15 tương ứng với nguyên tố Photpho, một nguyên tố quan trọng trong nhiều lĩnh vực khoa học và đời sống. Bài viết này sẽ giúp bạn khám phá mọi khía cạnh từ tính chất hóa học đến ứng dụng thực tiễn của Photpho, cùng với vai trò quan trọng của nó trong tự nhiên và công nghiệp.
Mục lục
Số Hiệu Nguyên Tử 15 - Nguyên Tố Photpho
Số hiệu nguyên tử của một nguyên tố hóa học được xác định bằng số proton có trong hạt nhân của nguyên tử đó. Với số hiệu nguyên tử 15, nguyên tố này là Photpho (ký hiệu hóa học P).
1. Đặc điểm của Nguyên Tố Photpho
- Số hiệu nguyên tử: \(Z = 15\)
- Số proton trong hạt nhân: 15
- Số electron: 15
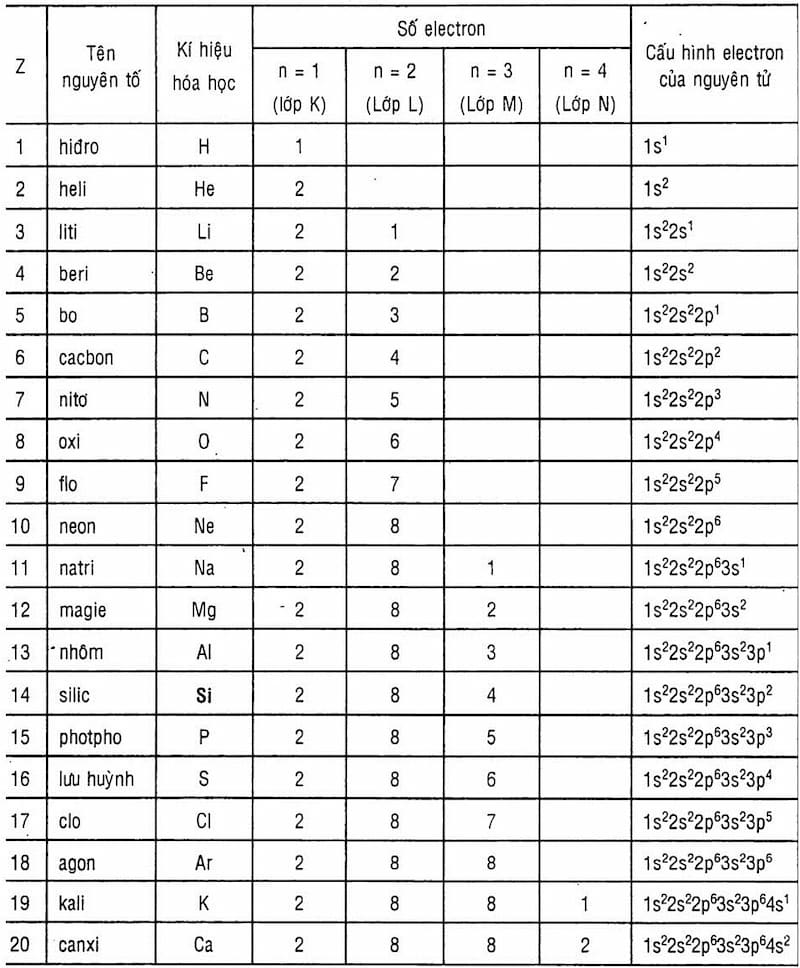
- Phân lớp electron: \(1s^2 2s^2 2p^6 3s^2 3p^3\)
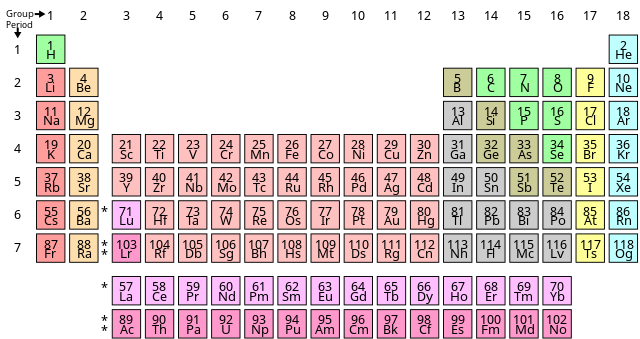
- Nhóm: VA, Chu kỳ 3 trong bảng tuần hoàn
- Photpho có nhiều dạng thù hình, bao gồm Photpho trắng và Photpho đỏ.
2. Ứng Dụng và Vai Trò
Photpho là một nguyên tố quan trọng trong tự nhiên và có nhiều ứng dụng thực tế:
- Trong công nghiệp phân bón, photpho được sử dụng dưới dạng các hợp chất photphat (P2O5) để cải thiện năng suất cây trồng.
- Photpho cũng tham gia vào quá trình tổng hợp DNA và ATP, các hợp chất cần thiết cho sự sống của tế bào.
- Trong lĩnh vực quân sự, Photpho trắng được sử dụng trong đạn và bom khói.
3. Tính Chất Hóa Học
Photpho có tính chất hóa học đặc trưng của phi kim:
- Phản ứng mạnh với oxy, tạo ra oxit photpho (P4O10).
- Hình thành nhiều hợp chất với các kim loại, như photphua kim loại.
- Photpho là thành phần chính trong các hợp chất hữu cơ phốt-phát, một phần quan trọng của sinh hóa học.
4. Cách Tính Số Hiệu Nguyên Tử
Số hiệu nguyên tử được xác định bằng số proton trong hạt nhân của nguyên tử. Đối với Photpho:
\[
Z = 15
\]
Do đó, Photpho có 15 proton trong hạt nhân và 15 electron bao quanh hạt nhân trong các phân lớp electron.
5. Đồng Vị của Photpho
Photpho có hai đồng vị tự nhiên chính:
- Photpho-31: Đồng vị ổn định và phổ biến nhất của photpho.
- Photpho-32: Đồng vị phóng xạ, được sử dụng trong nghiên cứu sinh học và y học.
6. Kết Luận
Photpho với số hiệu nguyên tử 15 là một nguyên tố rất quan trọng trong nhiều lĩnh vực, từ công nghiệp đến sinh học. Hiểu biết về số hiệu nguyên tử và đặc tính của Photpho giúp ta nắm bắt tốt hơn vai trò của nó trong tự nhiên và các ứng dụng thực tiễn.

1. Khái Niệm Số Hiệu Nguyên Tử 15 và Nguyên Tố Photpho
Số hiệu nguyên tử là một đại lượng đại diện cho số proton có trong hạt nhân của một nguyên tử. Đối với số hiệu nguyên tử 15, nguyên tố hóa học tương ứng là Photpho (ký hiệu hóa học là P). Nguyên tố này nằm ở vị trí nhóm VA và chu kỳ 3 trong bảng tuần hoàn các nguyên tố hóa học.
Photpho là một nguyên tố phi kim có vai trò quan trọng trong cả sinh học và công nghiệp. Trong tự nhiên, Photpho thường tồn tại dưới dạng hợp chất như photphat \(\left(PO_4^{3-}\right)\), chủ yếu trong các loại khoáng chất.
- Số hiệu nguyên tử: 15
- Ký hiệu hóa học: P
- Nhóm: VA
- Chu kỳ: 3
- Cấu hình electron: \[1s^2 2s^2 2p^6 3s^2 3p^3\]
Nguyên tố Photpho có nhiều dạng thù hình, phổ biến nhất là Photpho trắng và Photpho đỏ. Mỗi dạng thù hình có tính chất vật lý và hóa học khác nhau. Photpho trắng dễ cháy và có khả năng phát sáng trong bóng tối, trong khi Photpho đỏ ổn định hơn và được sử dụng nhiều trong sản xuất diêm.
Trong lĩnh vực sinh học, Photpho là thành phần chủ yếu của ADN, ARN và ATP, các phân tử thiết yếu cho sự sống. Nó cũng đóng vai trò quan trọng trong quá trình hình thành xương và răng ở con người.
2. Cấu Trúc Nguyên Tử của Photpho
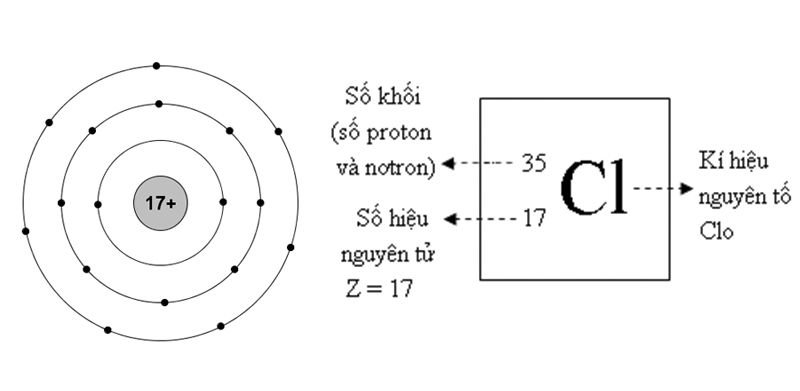
Nguyên tử Photpho có số hiệu nguyên tử 15, tức là trong hạt nhân của nguyên tử có 15 proton. Cấu trúc của một nguyên tử Photpho được xác định bởi số lượng proton, neutron, và electron. Dưới đây là chi tiết về cấu trúc nguyên tử của Photpho:
- Số proton: 15
- Số neutron: Trong đồng vị phổ biến nhất của Photpho, có 16 neutron, tạo thành tổng khối lượng nguyên tử là 31 (do 15 proton + 16 neutron).
- Số electron: 15, phân bố trong các lớp vỏ electron quanh hạt nhân.
Cấu hình electron của nguyên tử Photpho được sắp xếp theo các lớp vỏ và phân lớp như sau:
\[1s^2 2s^2 2p^6 3s^2 3p^3\]
Điều này có nghĩa là:
- Lớp thứ nhất chứa 2 electron trong phân lớp \(1s\).
- Lớp thứ hai chứa 8 electron, với 2 electron trong phân lớp \(2s\) và 6 electron trong phân lớp \(2p\).
- Lớp thứ ba chứa 5 electron, với 2 electron trong phân lớp \(3s\) và 3 electron trong phân lớp \(3p\).
Nhờ vào cấu hình electron này, Photpho có khả năng tạo ra nhiều loại hợp chất hóa học khác nhau. Đặc biệt, với 5 electron ở lớp vỏ ngoài cùng (valence shell), Photpho có xu hướng chia sẻ electron hoặc tạo liên kết cộng hóa trị trong các phản ứng hóa học, giúp nó dễ dàng kết hợp với các nguyên tố khác.
Trong tự nhiên, Photpho thường tồn tại dưới dạng ion photphat \(\left(PO_4^{3-}\right)\), đóng vai trò quan trọng trong cấu trúc ADN và ARN của sinh vật, cũng như trong nhiều phản ứng sinh hóa trong cơ thể sống.

3. Tính Chất Hóa Học của Photpho
Photpho là một nguyên tố phi kim với tính chất hóa học đặc trưng, thể hiện qua khả năng phản ứng mạnh với nhiều chất khác. Các tính chất hóa học của Photpho có thể được chia thành các dạng phản ứng và khả năng tạo hợp chất khác nhau, tùy thuộc vào trạng thái thù hình của nó.
- Phản ứng với Oxy: Photpho dễ dàng phản ứng với oxy, đặc biệt là Photpho trắng, để tạo thành điphotpho pentoxit \(\left(P_4O_{10}\right)\). Đây là một phản ứng tỏa nhiệt mạnh, với Photpho cháy sáng trong không khí.
- Phản ứng với Halogen: Photpho kết hợp với các halogen như clo, flo, brom để tạo ra các hợp chất halogenua photpho như \(\text{PCl}_3\) (trichlorua photpho) hoặc \(\text{PCl}_5\) (pentachlorua photpho).
- Phản ứng với Kim loại: Photpho cũng phản ứng với nhiều kim loại để tạo thành photphua kim loại, như photphua natri \(\text{Na}_3\text{P}\).
Một trong những tính chất nổi bật của Photpho là sự tồn tại ở các dạng thù hình khác nhau:
- Photpho Trắng: Dạng này có tính chất phản ứng mạnh, dễ cháy, và tự phát sáng trong bóng tối. Photpho trắng rất độc và phải được lưu trữ dưới nước để tránh phản ứng với oxy trong không khí.
- Photpho Đỏ: Ổn định hơn so với Photpho trắng, Photpho đỏ được sử dụng trong sản xuất diêm và pháo hoa. Nó không tự phát sáng và ít nguy hiểm hơn.
- Photpho Đen: Dạng này có cấu trúc tinh thể, ổn định hơn và ít phản ứng hơn, thường được nghiên cứu trong các ứng dụng vật liệu tiên tiến.
Photpho cũng có khả năng tạo ra nhiều hợp chất quan trọng trong cả hóa học vô cơ và hữu cơ, bao gồm các hợp chất photphat \(\left(PO_4^{3-}\right)\) quan trọng trong sinh học và công nghiệp phân bón.

4. Ứng Dụng Thực Tiễn của Photpho
Photpho là một nguyên tố có rất nhiều ứng dụng trong đời sống và công nghiệp. Các ứng dụng của Photpho bao trùm nhiều lĩnh vực khác nhau, từ nông nghiệp đến y học và công nghệ. Dưới đây là những ứng dụng chính của nguyên tố này:
- Công nghiệp phân bón: Photpho là thành phần chính trong các loại phân bón hóa học, đặc biệt là các loại phân superphotphat và photphat diamoni (DAP), giúp tăng cường năng suất cây trồng.
- Sản xuất diêm: Photpho đỏ là chất quan trọng trong sản xuất diêm. Nó giúp kích hoạt phản ứng cháy khi diêm được quẹt trên bề mặt thô.
- Y học và dược phẩm: Các hợp chất chứa Photpho, như Photpho-32, được sử dụng trong các ứng dụng y học, đặc biệt là trong điều trị và chẩn đoán bệnh ung thư thông qua phương pháp xạ trị.
- Công nghiệp hóa chất: Photpho tham gia vào việc sản xuất nhiều hóa chất quan trọng như axit photphoric, được sử dụng trong sản xuất thực phẩm, chất tẩy rửa và các chất phụ gia.
- Công nghiệp pháo hoa: Nhờ vào khả năng tạo ra lửa và phát sáng, Photpho đỏ được sử dụng trong pháo hoa và các loại thiết bị tạo hiệu ứng ánh sáng.
- Sinh học và năng lượng tế bào: Trong cơ thể sống, Photpho là thành phần cấu tạo chính của phân tử ATP (adenosine triphosphate), nguồn năng lượng chính cho các hoạt động sinh học.
Những ứng dụng của Photpho không chỉ giúp nâng cao chất lượng cuộc sống mà còn đóng vai trò thiết yếu trong phát triển các ngành công nghiệp quan trọng.

5. Các Đồng Vị của Photpho
Photpho có nhiều đồng vị, nhưng phổ biến nhất là đồng vị ổn định \(\text{P-31}\). Dưới đây là chi tiết về các đồng vị của nguyên tố này:
- \(\text{P-31}\): Đây là đồng vị ổn định duy nhất của Photpho, chiếm hầu hết lượng Photpho trong tự nhiên. Nó có 15 proton và 16 neutron, với khối lượng nguyên tử là 30.97376 amu.
- \(\text{P-32}\): Là một đồng vị phóng xạ của Photpho với chu kỳ bán rã khoảng 14,3 ngày. Đồng vị này được ứng dụng trong y học, đặc biệt trong điều trị ung thư và nghiên cứu sinh học phân tử.
- \(\text{P-33}\): Đây là một đồng vị phóng xạ khác của Photpho, có chu kỳ bán rã ngắn hơn (khoảng 25,4 ngày) và được sử dụng trong các nghiên cứu về sinh học và hóa sinh học, đặc biệt trong đánh dấu phân tử ADN và ARN.
Các đồng vị phóng xạ của Photpho, như \(\text{P-32}\) và \(\text{P-33}\), có vai trò quan trọng trong các nghiên cứu khoa học và y tế, đặc biệt trong việc theo dõi quá trình sinh học ở cấp độ phân tử.
XEM THÊM:
6. An Toàn và Xử Lý Photpho
Photpho là một nguyên tố hóa học có nhiều ứng dụng thực tiễn, tuy nhiên cũng tiềm ẩn những rủi ro an toàn nếu không được xử lý đúng cách. Việc hiểu rõ về các biện pháp an toàn và quy trình xử lý photpho là rất cần thiết trong các môi trường làm việc liên quan đến hóa chất này.
6.1. Biện pháp an toàn khi làm việc với Photpho
- Sử dụng trang bị bảo hộ cá nhân: Khi làm việc với photpho, cần trang bị đầy đủ các thiết bị bảo hộ như găng tay, kính bảo hộ, và áo choàng để tránh tiếp xúc trực tiếp với hóa chất.
- Phòng làm việc thoáng khí: Photpho, đặc biệt là photpho trắng, có thể dễ dàng cháy và gây độc nếu bị hít phải. Do đó, cần đảm bảo phòng làm việc có hệ thống thông gió tốt để giảm thiểu nguy cơ tích tụ khí độc.
- Lưu trữ trong môi trường thích hợp: Photpho cần được lưu trữ trong các bình chứa kín và đặt ở nơi mát mẻ, tránh ánh sáng trực tiếp và nhiệt độ cao.
6.2. Ảnh hưởng của Photpho đến sức khỏe và môi trường
Photpho có thể gây ra nhiều tác động tiêu cực đến sức khỏe con người và môi trường nếu không được quản lý cẩn thận:
- Sức khỏe: Tiếp xúc lâu dài với photpho có thể gây kích ứng da, mắt và hệ hô hấp. Đặc biệt, photpho trắng có thể gây bỏng da nghiêm trọng khi tiếp xúc trực tiếp.
- Môi trường: Photpho khi bị rò rỉ ra môi trường có thể gây ô nhiễm nước và đất, ảnh hưởng đến hệ sinh thái. Các hợp chất photpho trong nước có thể dẫn đến hiện tượng phú dưỡng hóa, làm suy giảm chất lượng nước và gây hại cho các loài sinh vật thủy sinh.
6.3. Quy trình xử lý và lưu trữ Photpho an toàn
- Xử lý photpho trắng: Photpho trắng cần được xử lý trong môi trường kín và dưới nước để tránh phản ứng với oxy không khí. Khi không sử dụng, cần lưu trữ photpho trắng trong các bình chứa đầy nước để ngăn chặn cháy nổ.
- Tiêu hủy photpho: Photpho thừa hoặc không sử dụng cần được tiêu hủy bằng cách đốt cháy trong lò chuyên dụng dưới điều kiện kiểm soát chặt chẽ nhằm tránh phát tán khí độc ra môi trường.
- Lưu trữ dài hạn: Photpho cần được lưu trữ trong các kho chứa chuyên dụng, đảm bảo cách ly khỏi nguồn nhiệt và các chất dễ cháy. Các kho này cần có hệ thống chữa cháy tự động và kiểm soát môi trường để đảm bảo an toàn.
7. Các Khái Niệm Liên Quan
Trong phần này, chúng ta sẽ tìm hiểu về một số khái niệm liên quan đến số hiệu nguyên tử 15, vốn là số hiệu nguyên tử của nguyên tố photpho (P). Những khái niệm này không chỉ giúp bạn hiểu rõ hơn về nguyên tố photpho mà còn cung cấp nền tảng vững chắc để nghiên cứu sâu hơn về các khái niệm hóa học khác.
- Số hiệu nguyên tử: Số hiệu nguyên tử là số lượng proton trong hạt nhân của một nguyên tử. Đối với nguyên tố photpho, số hiệu nguyên tử là \(15\), nghĩa là trong mỗi nguyên tử photpho có 15 proton. Số hiệu này quyết định vị trí của photpho trong bảng tuần hoàn các nguyên tố hóa học.
- Cấu hình electron: Photpho có cấu hình electron là \(1s^2 2s^2 2p^6 3s^2 3p^3\). Điều này có nghĩa là photpho có 5 electron ở lớp vỏ ngoài cùng (\(3s^2 3p^3\)), với 3 trong số đó nằm trong phân lớp \(p\), điều này làm cho nó có đặc tính của một phi kim mạnh.
- Photpho trong tự nhiên: Photpho là một phi kim tồn tại phổ biến trong tự nhiên dưới dạng hợp chất. Một trong những dạng phổ biến nhất là photphat (\(PO_4^{3-}\)), được tìm thấy trong đá photphat và là nguồn chính của photpho trong phân bón.
- Ứng dụng của photpho: Photpho đóng vai trò quan trọng trong nhiều quá trình sinh học, bao gồm việc tạo thành DNA, RNA, và ATP (adenosine triphosphate), nguồn năng lượng chính cho các tế bào. Ngoài ra, photpho còn được sử dụng rộng rãi trong sản xuất phân bón, thuốc trừ sâu, và các hợp chất hóa học khác.
- Khái niệm về ion photphat: Ion photphat \(PO_4^{3-}\) là một anion quan trọng trong nhiều quá trình hóa học và sinh học. Nó được hình thành khi photpho kết hợp với oxy, và đóng vai trò quan trọng trong việc truyền năng lượng trong các hệ thống sinh học.
- Phương pháp xác định số hiệu nguyên tử: Số hiệu nguyên tử có thể được xác định thông qua các phương pháp hiện đại như phổ kế khối lượng và hiển vi điện tử truyền qua (TEM), cho phép phân tích chính xác số lượng proton trong hạt nhân nguyên tử.
Những khái niệm này không chỉ giúp hiểu rõ hơn về nguyên tố photpho mà còn đóng vai trò quan trọng trong nghiên cứu khoa học và ứng dụng trong nhiều lĩnh vực khác nhau.

Kết Luận
Số hiệu nguyên tử 15 gắn liền với nguyên tố Photpho, một nguyên tố vô cùng quan trọng trong hóa học và sinh học. Photpho không chỉ có mặt trong bảng tuần hoàn mà còn đóng vai trò thiết yếu trong nhiều quá trình sinh học, đặc biệt là trong cấu trúc của DNA và ATP, hai thành phần cốt lõi của sự sống. Với các đặc tính hóa học độc đáo, Photpho đã trở thành một nguyên tố không thể thiếu trong các ngành công nghiệp, từ sản xuất phân bón đến y học.
Những hiểu biết về cấu trúc nguyên tử, các đồng vị và các ứng dụng thực tiễn của Photpho đã cung cấp cho chúng ta những cơ hội để phát triển các công nghệ mới, từ đó cải thiện chất lượng cuộc sống. Việc nghiên cứu Photpho cũng mở ra những triển vọng trong việc khám phá các phản ứng hóa học mới, cũng như ứng dụng của Photpho trong việc bảo vệ môi trường và sức khỏe con người.
Tuy nhiên, việc xử lý và lưu trữ Photpho cần phải tuân thủ các biện pháp an toàn nghiêm ngặt do tính phản ứng và độc tính của nó. Điều này đòi hỏi sự hiểu biết sâu sắc và kỹ năng chuyên môn cao từ các nhà khoa học và kỹ sư.
Nhìn chung, nguyên tố Photpho với số hiệu nguyên tử 15 không chỉ có tầm quan trọng trong học thuật mà còn trong nhiều khía cạnh thực tiễn của cuộc sống. Việc tiếp tục nghiên cứu và ứng dụng Photpho một cách an toàn và hiệu quả sẽ mang lại nhiều lợi ích cho tương lai.