Chủ đề ôn tập nguyên tử: Bài viết này sẽ cung cấp cho bạn một cái nhìn toàn diện về nguyên tử, từ các khái niệm cơ bản đến ứng dụng thực tiễn. Hãy khám phá các phương pháp ôn tập hiệu quả và những bài tập giúp bạn củng cố kiến thức một cách tốt nhất.
Mục lục
Ôn Tập Nguyên Tử
Ôn tập về nguyên tử là một phần quan trọng trong chương trình học Vật lý và Hóa học ở các cấp học phổ thông. Dưới đây là tổng hợp nội dung liên quan đến chủ đề nguyên tử, bao gồm các khái niệm cơ bản, bài tập vận dụng và những phương pháp học tập hiệu quả.
1. Cấu Tạo Nguyên Tử
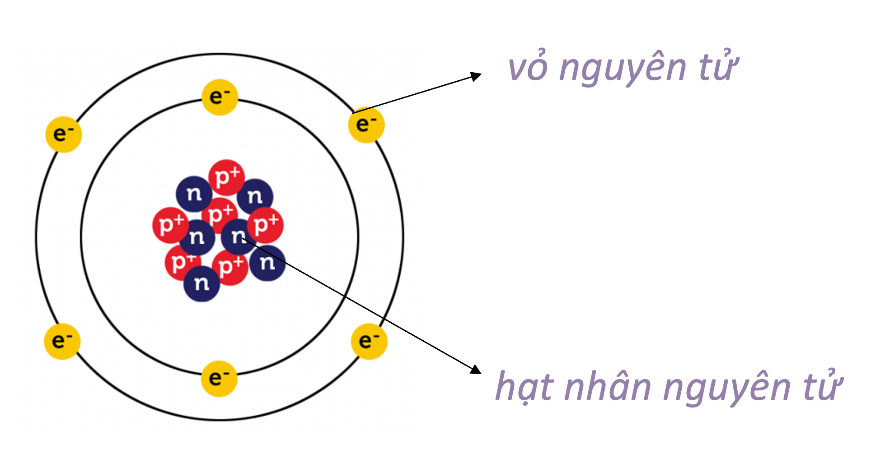
- Nguyên tử là đơn vị cơ bản của vật chất, bao gồm các thành phần chính: proton, neutron và electron.
- Proton mang điện tích dương (\(+\)) nằm ở hạt nhân, neutron không mang điện tích và electron mang điện tích âm (\(-\)) quay quanh hạt nhân.
- Số proton xác định số hiệu nguyên tử và vị trí của nguyên tố trong bảng tuần hoàn.
2. Các Dạng Bài Tập Về Nguyên Tử
Bài tập liên quan đến nguyên tử thường tập trung vào các dạng như:
- Tính toán khối lượng nguyên tử: Sử dụng các công thức liên quan đến số proton, neutron và electron.
- Tính số lượng hạt: Tính số lượng proton, neutron và electron trong một nguyên tử dựa trên các dữ liệu được cung cấp.
- Phân tích thành phần đồng vị: Sử dụng kiến thức về các đồng vị của nguyên tố để tính toán và giải quyết các bài toán liên quan.
3. Phương Pháp Học Tập Hiệu Quả
- Ghi nhớ các khái niệm cơ bản: Sử dụng sơ đồ tư duy để hệ thống hóa kiến thức về cấu tạo nguyên tử.
- Luyện tập bài tập thường xuyên: Thực hành nhiều dạng bài tập để nắm vững cách áp dụng công thức và lý thuyết vào thực tế.
- Tham khảo tài liệu học tập: Sử dụng sách giáo khoa và các nguồn tài liệu trực tuyến để mở rộng kiến thức và hiểu sâu hơn về chủ đề.
4. Ví Dụ Bài Tập Cụ Thể
Dưới đây là một ví dụ cụ thể về bài tập tính toán liên quan đến nguyên tử:
- Bài tập: Tính khối lượng tuyệt đối của một nguyên tử nhôm có 13 proton, 14 neutron và 13 electron.
- Lời giải: Sử dụng công thức: \[ m_{\text{Al}} = (13 \times m_{\text{proton}}) + (14 \times m_{\text{neutron}}) + (13 \times m_{\text{electron}}) \] với \(m_{\text{proton}} \approx 1.6726 \times 10^{-27} \, \text{kg}\), \(m_{\text{neutron}} \approx 1.6750 \times 10^{-27} \, \text{kg}\), và \(m_{\text{electron}} \approx 9.109 \times 10^{-31} \, \text{kg}\).
- Đáp số: \( m_{\text{Al}} \approx 4.4816 \times 10^{-26} \, \text{kg} \)
5. Các Tài Liệu Học Tập Liên Quan
- : Trang web cung cấp nhiều tài liệu và câu hỏi ôn tập cho học sinh.
- : Cung cấp nhiều bài tập và tài liệu ôn tập về nguyên tử.
Tổng Quan Về Nguyên Tử
Nguyên tử là đơn vị cơ bản của vật chất, cấu thành nên mọi vật thể và sinh vật. Mỗi nguyên tử bao gồm một hạt nhân chứa các proton và neutron, được bao quanh bởi một lớp vỏ electron. Các đặc tính của nguyên tử, như số hiệu nguyên tử và khối lượng nguyên tử, đóng vai trò quan trọng trong việc xác định tính chất hóa học của nguyên tố.
- Cấu trúc nguyên tử: Nguyên tử gồm có hạt nhân ở trung tâm và các electron quay quanh hạt nhân theo quỹ đạo xác định.
- Hạt nhân nguyên tử: Hạt nhân chứa các proton mang điện tích dương và neutron không mang điện. Số proton xác định số hiệu nguyên tử của nguyên tố.
- Electron và quỹ đạo: Các electron mang điện tích âm, sắp xếp theo các mức năng lượng hoặc quỹ đạo xung quanh hạt nhân. Số electron bằng số proton trong một nguyên tử trung hòa.
Nguyên tử không phải là đơn vị nhỏ nhất của vật chất, vì nó có thể được chia nhỏ hơn nữa thành các hạt cơ bản như quark và lepton. Tuy nhiên, trong hóa học và vật lý, nguyên tử là đơn vị nhỏ nhất có thể tham gia vào các phản ứng hóa học và giữ các đặc tính hóa học của nguyên tố.
Một trong những khía cạnh quan trọng của nguyên tử là liên kết hóa học, được tạo ra khi các nguyên tử chia sẻ hoặc trao đổi electron. Các loại liên kết chính bao gồm liên kết ion, liên kết cộng hóa trị và liên kết kim loại, mỗi loại có đặc trưng riêng và ảnh hưởng đến tính chất của chất tạo thành.
Để hiểu sâu hơn về nguyên tử và cấu trúc của chúng, chúng ta cần nghiên cứu về các mô hình nguyên tử khác nhau, như mô hình của Rutherford, mô hình Bohr, và mô hình cơ học lượng tử. Mỗi mô hình mang lại một cái nhìn khác nhau về cách mà các electron di chuyển xung quanh hạt nhân và cách mà các lực tương tác trong nguyên tử hoạt động.
Một công thức cơ bản trong việc tính toán khối lượng nguyên tử trung bình của một nguyên tố là:
Việc ôn tập và hiểu rõ các khái niệm liên quan đến nguyên tử sẽ giúp bạn nắm vững kiến thức nền tảng trong cả hóa học và vật lý, từ đó phát triển kỹ năng phân tích và giải quyết vấn đề trong các lĩnh vực khoa học tự nhiên.
Các Đặc Tính Của Nguyên Tử
Nguyên tử, mặc dù là đơn vị cơ bản của vật chất, nhưng lại có nhiều đặc tính phức tạp và đa dạng. Những đặc tính này không chỉ giúp phân biệt giữa các nguyên tố mà còn giải thích các hiện tượng vật lý và hóa học trong tự nhiên. Dưới đây là một số đặc tính quan trọng của nguyên tử:
- Số hiệu nguyên tử (Z): Số hiệu nguyên tử là số lượng proton trong hạt nhân của một nguyên tử. Đây là đặc tính quan trọng nhất vì nó xác định nguyên tố và vị trí của nguyên tố đó trong bảng tuần hoàn. Ví dụ, mọi nguyên tử có Z = 1 đều là nguyên tử của nguyên tố hydro.
- Khối lượng nguyên tử (A): Khối lượng nguyên tử là tổng số proton và neutron trong hạt nhân. Khối lượng này được biểu thị bằng đơn vị khối lượng nguyên tử (u), với \( 1u = \frac{1}{12} \) khối lượng của nguyên tử carbon-12. Công thức tính khối lượng nguyên tử là: \[ A = Z + N \] trong đó \( Z \) là số proton và \( N \) là số neutron.
- Kích thước nguyên tử: Kích thước nguyên tử được đo bằng bán kính nguyên tử, là khoảng cách từ hạt nhân đến electron ngoài cùng. Bán kính nguyên tử thường nằm trong khoảng 30 đến 300 picomet (pm).
- Cấu hình electron: Cấu hình electron là sự sắp xếp của các electron trong các lớp vỏ xung quanh hạt nhân. Cấu hình này quyết định tính chất hóa học và vật lý của nguyên tố. Ví dụ, các nguyên tố trong cùng một nhóm của bảng tuần hoàn có cấu hình electron tương tự nhau.
- Năng lượng ion hóa: Năng lượng ion hóa là năng lượng cần thiết để loại bỏ một electron khỏi nguyên tử trung hòa, tạo thành ion dương. Đặc tính này cho thấy mức độ khó khăn khi một nguyên tử mất đi một electron.
- Độ âm điện: Độ âm điện là thước đo khả năng của một nguyên tử trong việc thu hút electron về phía mình khi tạo liên kết hóa học. Nguyên tử có độ âm điện cao thường có khả năng mạnh mẽ trong việc tạo liên kết cộng hóa trị.
Những đặc tính trên không chỉ quan trọng trong việc phân loại nguyên tố mà còn trong việc hiểu rõ hơn về các phản ứng hóa học và các tính chất vật lý của vật chất. Việc nắm vững các đặc tính này sẽ giúp học sinh và người học khoa học có một nền tảng vững chắc để tiến xa hơn trong việc nghiên cứu và ứng dụng trong thực tiễn.

Ứng Dụng Và Vai Trò Của Nguyên Tử
Nguyên tử là thành phần cơ bản của mọi vật chất và đóng vai trò quan trọng trong nhiều lĩnh vực khoa học và công nghệ. Những ứng dụng của nguyên tử không chỉ giới hạn trong nghiên cứu cơ bản mà còn mở rộng ra nhiều lĩnh vực khác nhau, từ y học đến năng lượng và công nghiệp.
- Trong Y Học: Nguyên tử được ứng dụng rộng rãi trong y học, đặc biệt là trong lĩnh vực chẩn đoán và điều trị. Các đồng vị phóng xạ của nguyên tử được sử dụng trong y học hạt nhân để chụp cắt lớp và xạ trị. Ví dụ, \(^{131}I\) được dùng để điều trị bệnh cường giáp và ung thư tuyến giáp.
- Trong Năng Lượng: Nguyên tử là nguồn gốc của năng lượng hạt nhân, một nguồn năng lượng mạnh mẽ và sạch. Năng lượng này được khai thác từ sự phân rã của hạt nhân nguyên tử trong các lò phản ứng hạt nhân. Các nhà máy điện hạt nhân sử dụng phản ứng phân hạch của \(^{235}U\) để tạo ra điện năng.
- Trong Công Nghiệp: Nguyên tử cũng được sử dụng trong nhiều quy trình công nghiệp, chẳng hạn như việc kiểm tra và bảo dưỡng các vật liệu và cấu trúc. Kỹ thuật phóng xạ không phá hủy (NDT) sử dụng các tia phóng xạ để phát hiện khuyết tật trong kim loại và các vật liệu khác.
- Trong Nghiên Cứu Khoa Học: Nguyên tử là đối tượng nghiên cứu chủ yếu trong vật lý nguyên tử và hóa học. Các nhà khoa học nghiên cứu cấu trúc và tính chất của nguyên tử để hiểu rõ hơn về các quy luật tự nhiên, từ đó phát triển các công nghệ mới.
- Trong Môi Trường: Nguyên tử cũng đóng vai trò trong các nghiên cứu về môi trường, chẳng hạn như trong việc theo dõi và xử lý ô nhiễm. Các đồng vị phóng xạ được sử dụng để theo dõi sự di chuyển của các chất gây ô nhiễm trong môi trường.
Với những ứng dụng đa dạng và quan trọng, nguyên tử không chỉ là một khái niệm khoa học mà còn là yếu tố then chốt trong sự phát triển của nhiều ngành công nghiệp và công nghệ hiện đại. Việc nắm vững kiến thức về nguyên tử và các ứng dụng của nó sẽ mở ra nhiều cơ hội cho những tiến bộ trong khoa học và kỹ thuật.

Phương Pháp Ôn Tập Hiệu Quả Về Nguyên Tử
Để ôn tập hiệu quả về chủ đề nguyên tử, việc áp dụng các phương pháp học tập khoa học và có chiến lược là rất quan trọng. Dưới đây là một số phương pháp ôn tập giúp bạn nắm vững kiến thức về nguyên tử, từ cơ bản đến nâng cao.
- Phân Chia Nội Dung: Hãy chia nhỏ các nội dung liên quan đến nguyên tử thành các phần như cấu tạo nguyên tử, tính chất hạt nhân, và các hiện tượng liên quan. Việc này giúp bạn dễ dàng tập trung vào từng khía cạnh cụ thể.
- Sử Dụng Sơ Đồ Tư Duy: Sơ đồ tư duy là công cụ hữu ích giúp bạn hệ thống hóa kiến thức một cách trực quan. Vẽ sơ đồ liên kết giữa các khái niệm như proton, neutron, electron, và số hiệu nguyên tử sẽ giúp bạn ghi nhớ lâu hơn.
- Áp Dụng Công Thức Toán Học: Học cách sử dụng các công thức liên quan đến nguyên tử như khối lượng nguyên tử \[A = Z + N\], trong đó \(Z\) là số proton, \(N\) là số neutron. Việc thực hành các bài tập tính toán giúp bạn nắm chắc lý thuyết.
- Thực Hành Bài Tập Trắc Nghiệm: Để ôn tập hiệu quả, hãy thực hành nhiều bài tập trắc nghiệm. Điều này không chỉ giúp củng cố kiến thức mà còn tăng cường kỹ năng làm bài thi.
- Tự Đặt Câu Hỏi: Tự đặt ra các câu hỏi về nguyên tử và tìm cách giải thích chúng là một cách học hiệu quả. Việc này giúp bạn kiểm tra lại mức độ hiểu biết của mình và bổ sung các phần kiến thức còn thiếu.
- Ôn Tập Định Kỳ: Để tránh quên kiến thức, hãy lên kế hoạch ôn tập định kỳ. Ôn lại các khái niệm cơ bản thường xuyên sẽ giúp bạn nhớ lâu hơn và tự tin hơn khi đối diện với các bài kiểm tra.
Bằng cách áp dụng các phương pháp trên, bạn sẽ dễ dàng nắm vững kiến thức về nguyên tử và đạt kết quả tốt trong các kỳ thi.