Chủ đề nguyên tử 39x có cấu hình electron 1s22s22p63s23p64s1: Nguyên tử 39X với cấu hình electron 1s22s22p63s23p64s1 là một chủ đề hấp dẫn trong hóa học. Bài viết này sẽ giúp bạn hiểu rõ hơn về đặc điểm, tính chất hóa học và vật lý, cũng như các ứng dụng quan trọng của nguyên tố này trong cuộc sống và công nghiệp. Cùng khám phá những kiến thức hữu ích về nguyên tử 39X ngay dưới đây.
Mục lục
Nguyên tử 39X và cấu hình electron của nó
Nguyên tử 39X có cấu hình electron là:
\[1s^2 2s^2 2p^6 3s^2 3p^6 4s^1\]
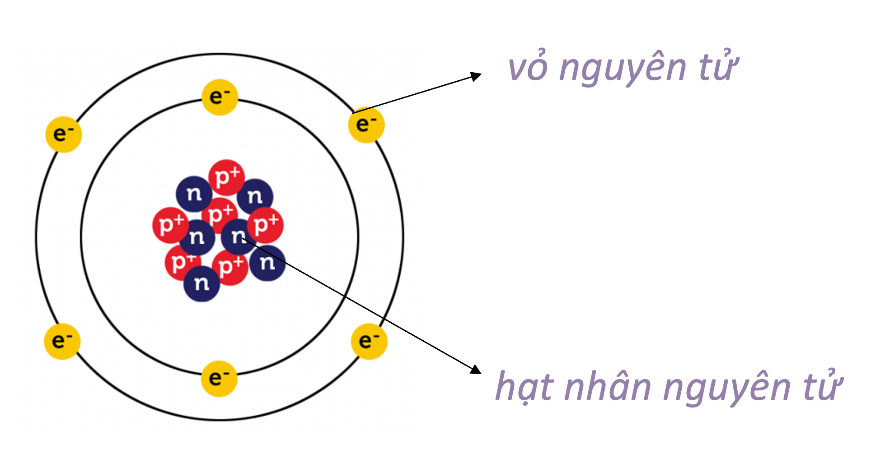
Nguyên tố này thuộc nhóm kim loại kiềm (nhóm IA) và nằm ở chu kỳ 4 trong bảng tuần hoàn. Với số hiệu nguyên tử là 19, nguyên tố này có 19 proton và 20 neutron trong hạt nhân, tương ứng với khối lượng nguyên tử là 39 đơn vị khối lượng nguyên tử (u).
Đặc điểm hóa học và vật lý
- Nguyên tử 39X là một kim loại mạnh, có khả năng dễ dàng mất đi một electron ở lớp vỏ ngoài cùng (4s) để tạo thành ion \(X^+\) với cấu hình electron bền vững của khí hiếm (cấu hình \(1s^2 2s^2 2p^6 3s^2 3p^6\)).
- Kim loại này phản ứng mạnh với nước, tạo ra dung dịch kiềm và giải phóng khí hydro. Đây là một tính chất đặc trưng của các kim loại thuộc nhóm IA.
- Ở trạng thái tự nhiên, kim loại này có màu trắng bạc, dễ bị oxy hóa trong không khí, vì vậy cần được bảo quản trong dầu hoặc môi trường không có oxy.
Ứng dụng và vai trò
Kim loại có cấu hình electron này được sử dụng trong nhiều lĩnh vực khác nhau, bao gồm:
- Sản xuất pin điện hóa.
- Sản xuất hợp kim có độ bền cao.
- Ứng dụng trong y tế và các thiết bị khoa học.
Kết luận
Nguyên tử 39X với cấu hình electron \(1s^2 2s^2 2p^6 3s^2 3p^6 4s^1\) là một nguyên tố kim loại quan trọng với nhiều ứng dụng trong cuộc sống. Cấu hình electron này giúp giải thích các tính chất hóa học và vật lý của nguyên tố, đồng thời mở ra các tiềm năng ứng dụng rộng rãi trong nhiều ngành công nghiệp.

1. Giới thiệu về nguyên tử 39X
Nguyên tử 39X có cấu hình electron \[1s^2 2s^2 2p^6 3s^2 3p^6 4s^1\], tương ứng với một nguyên tố thuộc nhóm kim loại kiềm (nhóm IA) trong bảng tuần hoàn. Nguyên tố này nằm ở chu kỳ 4 và có đặc điểm hóa học cũng như vật lý rất nổi bật.
Nguyên tử này có 19 proton, 20 neutron trong hạt nhân, dẫn đến khối lượng nguyên tử là 39 đơn vị khối lượng nguyên tử (u). Số electron của nó cũng là 19, phân bố trên bốn lớp vỏ electron. Electron ngoài cùng nằm ở phân lớp \(4s^1\), dễ bị mất đi trong các phản ứng hóa học, tạo thành ion \(X^+\) với cấu hình bền vững của khí hiếm \[1s^2 2s^2 2p^6 3s^2 3p^6\].
Nguyên tử 39X thuộc nhóm kim loại hoạt động mạnh. Kim loại này có khả năng phản ứng nhanh với nước và oxy, tạo ra dung dịch kiềm và khí hydro. Vì vậy, nó cần được bảo quản trong môi trường không có oxy để tránh quá trình oxy hóa.
Các đặc tính nổi bật của nguyên tử 39X bao gồm tính dẫn điện và dẫn nhiệt cao, đặc trưng của kim loại kiềm. Ngoài ra, với mật độ thấp, nguyên tố này thường tồn tại dưới dạng chất rắn mềm và có màu trắng bạc trong điều kiện tiêu chuẩn.
- Nhóm nguyên tố: IA (Kim loại kiềm)
- Chu kỳ: 4
- Số proton: 19
- Số neutron: 20
- Cấu hình electron: \[1s^2 2s^2 2p^6 3s^2 3p^6 4s^1\]
- Tính chất vật lý: Kim loại trắng bạc, mềm, mật độ thấp
2. Tính chất hóa học và vật lý của nguyên tố 39X
Nguyên tố 39X, với cấu hình electron \([1s^2 2s^2 2p^6 3s^2 3p^6 4s^1]\), có nhiều tính chất hóa học và vật lý đặc trưng liên quan đến cấu trúc electron của nó. Đặc biệt, lớp electron ngoài cùng của nguyên tử X chứa duy nhất một electron trong phân lớp 4s, đây là điểm quan trọng giúp xác định tính chất kim loại của nguyên tố này.
Tính chất hóa học
- Nguyên tố 39X là kim loại kiềm, có xu hướng mất electron ở lớp ngoài cùng để tạo thành ion dương \((X^+)\).
- Tính chất hóa học nổi bật là khả năng phản ứng mạnh với nước để tạo ra dung dịch bazơ và khí hydrogen.
- Do có tính khử mạnh, nguyên tố này dễ tham gia phản ứng với các phi kim như oxy, halogen để tạo thành các hợp chất ion.
Tính chất vật lý
- Nguyên tố 39X có màu trắng bạc và dẫn điện tốt, một đặc điểm chung của các kim loại kiềm.
- Điểm nóng chảy và điểm sôi tương đối thấp so với các kim loại khác, do lực liên kết giữa các nguyên tử yếu.
- Kim loại này có độ cứng thấp, dễ dàng bị cắt bởi dao và biến dạng dưới lực tác động nhẹ.

3. Ứng dụng và vai trò của nguyên tố 39X
Nguyên tố 39X, với cấu hình electron \[1s^22s^22p^63s^23p^64s^1\], là một nguyên tố hóa học quan trọng có nhiều ứng dụng trong đời sống và công nghiệp.
Dưới đây là một số ứng dụng và vai trò quan trọng của nguyên tố 39X:
- Sử dụng trong hợp kim: Nguyên tố này thường được sử dụng để tạo ra các hợp kim nhẹ và bền. Các hợp kim này được ứng dụng rộng rãi trong các ngành công nghiệp như hàng không, ô tô, và xây dựng nhờ vào tính chất bền vững và khả năng chống mài mòn của chúng.
- Vai trò trong điện tử và công nghệ: Do có đặc tính dẫn điện tốt, nguyên tố 39X được sử dụng trong các thiết bị điện tử và công nghệ cao như pin, chất bán dẫn, và thiết bị cảm biến.
- Y tế: Trong lĩnh vực y tế, nguyên tố này có thể được dùng trong các ứng dụng liên quan đến chẩn đoán hình ảnh và điều trị bệnh, nhờ vào khả năng tương tác với các thiết bị y tế tiên tiến.
- Công nghiệp hóa chất: 39X được sử dụng làm chất xúc tác trong nhiều quá trình sản xuất hóa chất, giúp tối ưu hóa và tăng hiệu suất của các phản ứng hóa học.
Nhờ vào những ứng dụng đa dạng và vai trò quan trọng trong các ngành công nghiệp, nguyên tố 39X đã góp phần cải thiện chất lượng cuộc sống và thúc đẩy sự phát triển của các công nghệ tiên tiến.

4. Các câu hỏi và bài tập liên quan đến nguyên tử 39X
Dưới đây là một số câu hỏi và bài tập phổ biến liên quan đến cấu hình electron của nguyên tử 39X. Các bài tập này nhằm giúp học sinh hiểu rõ hơn về cấu trúc nguyên tử, tính chất hóa học, và vai trò của nguyên tố trong các phản ứng.
- Câu 1: Viết cấu hình electron đầy đủ của nguyên tử 39X và xác định vị trí của nó trong bảng tuần hoàn.
- Câu 2: Nguyên tử 39X có bao nhiêu lớp electron? Hãy xác định số electron ở lớp ngoài cùng.
- Câu 3: Dựa vào cấu hình electron của nguyên tử 39X, hãy dự đoán tính chất hóa học cơ bản của nó (kim loại hay phi kim).
- Câu 4: Nguyên tử X có cấu hình electron \(1s^2 2s^2 2p^6 3s^2 3p^6 4s^1\). Hãy so sánh tính chất hóa học của nguyên tử X với các nguyên tử có cấu hình tương tự.
- Câu 5: Xác định số proton, neutron và electron trong nguyên tử 39X. Giải thích cách tính toán này.
Những câu hỏi và bài tập trên sẽ giúp củng cố kiến thức về cấu trúc nguyên tử, đồng thời nâng cao kỹ năng phân tích và dự đoán tính chất hóa học của các nguyên tố.

5. Kết luận
Nguyên tử 39X, với cấu hình electron \(1s^22s^22p^63s^23p^64s^1\), thể hiện rõ vai trò quan trọng của mình trong cả lĩnh vực hóa học lẫn các ứng dụng thực tiễn. Dựa trên những phân tích và thông tin đã trình bày, chúng ta có thể đưa ra các kết luận như sau:
5.1 Tổng hợp về đặc điểm và ứng dụng của nguyên tố 39X
Nguyên tố 39X mang nhiều đặc điểm và lợi thế:
- Cấu hình electron đơn giản với electron cuối cùng nằm ở phân lớp 4s giúp nguyên tố này dễ dàng tham gia vào các phản ứng hóa học, đặc biệt là với các chất oxy hóa mạnh.
- Vị trí trong nhóm kim loại kiềm xác định các tính chất vật lý như độ dẫn nhiệt, dẫn điện cao, cũng như tính mềm và khả năng tạo hợp kim dễ dàng.
- Với số proton, neutron cụ thể, nguyên tử 39X đóng vai trò nền tảng trong nhiều nghiên cứu khoa học và ứng dụng công nghệ, từ lĩnh vực vật liệu đến năng lượng.
5.2 Tầm quan trọng của nguyên tố 39X trong đời sống và công nghiệp
Nguyên tố 39X không chỉ dừng lại ở những ứng dụng cơ bản mà còn mở rộng ra nhiều lĩnh vực khác nhau:
- Trong đời sống hàng ngày, nguyên tố này góp phần vào việc sản xuất các sản phẩm điện tử, thiết bị gia dụng với tính năng vượt trội nhờ tính chất kim loại đặc trưng.
- Trong công nghiệp, 39X được sử dụng để tạo ra các hợp kim chịu nhiệt, chịu mài mòn, là yếu tố cốt lõi trong sản xuất các linh kiện máy móc và thiết bị công nghiệp.
- Trong nghiên cứu và phát triển, nguyên tố này là đối tượng của nhiều nghiên cứu nhằm phát triển công nghệ xanh, các giải pháp năng lượng mới và các vật liệu tiên tiến.
Với tất cả những ứng dụng và tiềm năng này, nguyên tử 39X chắc chắn sẽ tiếp tục đóng vai trò quan trọng trong nhiều lĩnh vực, từ công nghệ đến đời sống, thúc đẩy sự phát triển bền vững và sáng tạo.