Chủ đề độ phân cực dung môi: Độ phân cực dung môi đóng vai trò quan trọng trong nhiều lĩnh vực khoa học và công nghiệp. Bài viết này sẽ giúp bạn hiểu rõ hơn về khái niệm, cách tính toán, và những ứng dụng thực tiễn của độ phân cực dung môi trong hóa học cũng như các ngành công nghiệp liên quan.
Mục lục
Độ Phân Cực Dung Môi
Độ phân cực của dung môi là một khái niệm quan trọng trong hóa học, đặc biệt là trong việc lựa chọn dung môi cho các phản ứng hóa học và quá trình chiết xuất. Độ phân cực ảnh hưởng đến khả năng hòa tan của các chất trong dung môi và được xác định dựa trên hằng số điện môi (dielectric constant) của dung môi đó.
Phân Loại Dung Môi Theo Độ Phân Cực
Dung môi có thể được phân loại thành hai nhóm chính dựa trên độ phân cực của chúng:
- Dung môi phân cực: Đây là những dung môi có hằng số điện môi lớn hơn 15. Ví dụ điển hình là nước \(\text{H}_2\text{O}\), methanol \(\text{CH}_3\text{OH}\), ethanol \(\text{C}_2\text{H}_5\text{OH}\).
- Dung môi không phân cực: Đây là những dung môi có hằng số điện môi nhỏ hơn 15. Ví dụ như hexane \(\text{C}_6\text{H}_{14}\), toluene \(\text{C}_7\text{H}_8\), benzene \(\text{C}_6\text{H}_6\).
Hằng Số Điện Môi Và Độ Phân Cực
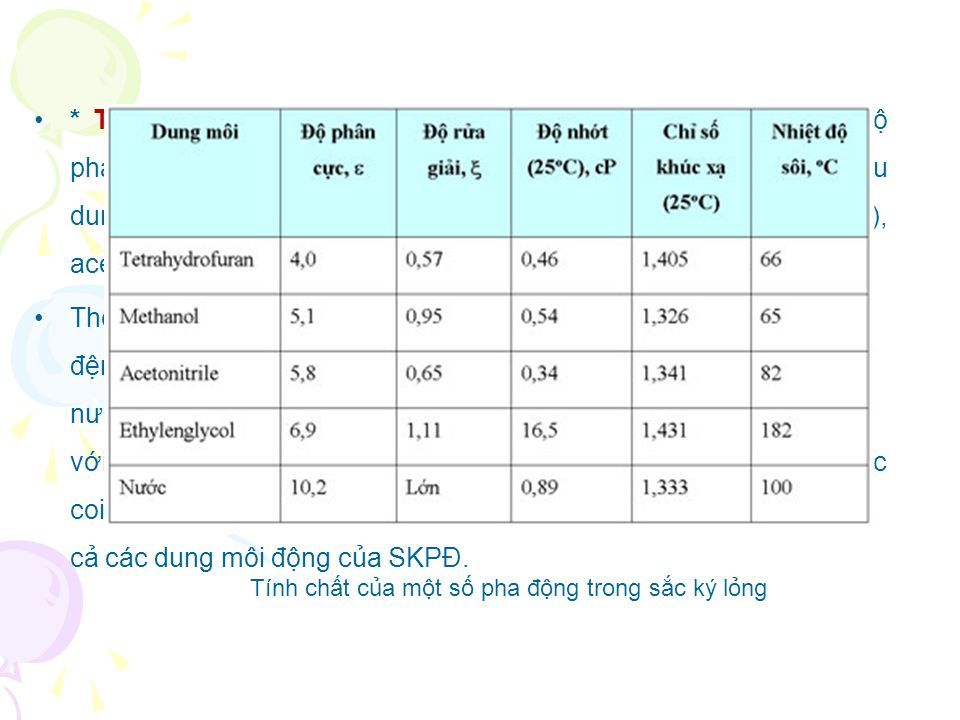
Hằng số điện môi là một thước đo quan trọng để xác định độ phân cực của dung môi. Ở nhiệt độ 20°C, hằng số điện môi của một số dung môi phổ biến là:
| Dung Môi | Hằng Số Điện Môi (\(\epsilon\)) |
| Nước (\(\text{H}_2\text{O}\)) | 80.10 |
| Methanol (\(\text{CH}_3\text{OH}\)) | 32.70 |
| Ethanol (\(\text{C}_2\text{H}_5\text{OH}\)) | 24.55 |
| Hexane (\(\text{C}_6\text{H}_{14}\)) | 1.88 |
| Benzene (\(\text{C}_6\text{H}_6\)) | 2.28 |
Ứng Dụng Của Độ Phân Cực Trong Thực Tiễn
Độ phân cực của dung môi ảnh hưởng đến nhiều ứng dụng thực tiễn trong các ngành công nghiệp và nghiên cứu:
- Trong sản xuất sơn: Dung môi phân cực và không phân cực được lựa chọn để điều chỉnh độ nhớt và khả năng hòa tan của các chất phụ gia trong sơn.
- Trong ngành dược phẩm: Độ phân cực của dung môi ảnh hưởng đến quá trình tách chiết và tinh chế các hợp chất hoạt tính trong thuốc.
- Trong phòng thí nghiệm: Dung môi phân cực như acetone thường được sử dụng để làm sạch và hòa tan các chất trong quá trình chuẩn bị mẫu và phản ứng hóa học.
- Trong công nghiệp hóa chất: Độ phân cực của dung môi là yếu tố quan trọng trong việc thiết kế các quy trình tổng hợp và chiết xuất các hợp chất hóa học.
Tổng Kết
Hiểu rõ về độ phân cực của dung môi không chỉ giúp lựa chọn dung môi phù hợp cho các ứng dụng cụ thể mà còn giúp tối ưu hóa quá trình sản xuất và nghiên cứu hóa học. Sự phân cực ảnh hưởng trực tiếp đến khả năng hòa tan, độ bay hơi, và tính chất hóa học của các chất khi hòa tan trong dung môi.

I. Giới Thiệu Về Độ Phân Cực Dung Môi
Độ phân cực dung môi là một trong những yếu tố quan trọng ảnh hưởng đến tính chất và ứng dụng của dung môi trong hóa học. Độ phân cực của một dung môi biểu thị khả năng của dung môi đó trong việc hòa tan các chất khác nhau dựa trên sự phân bố điện tích trong phân tử.
Một dung môi phân cực có các phân tử với phân bố điện tích không đều, dẫn đến việc hình thành các cực điện tích dương và âm. Ngược lại, dung môi không phân cực có sự phân bố điện tích đều đặn, không tạo ra các cực rõ rệt.
Độ phân cực được xác định dựa trên hằng số điện môi (\(\varepsilon\)), một giá trị thể hiện mức độ phân cực của phân tử dung môi. Dung môi có hằng số điện môi cao thường là dung môi phân cực mạnh, trong khi dung môi có hằng số điện môi thấp là dung môi không phân cực.
Vai trò của độ phân cực dung môi rất quan trọng trong việc xác định khả năng hòa tan của dung môi đối với các chất khác nhau. Ví dụ, dung môi phân cực như nước có khả năng hòa tan tốt các chất ion hoặc phân tử phân cực khác, trong khi dung môi không phân cực như hexan thường hòa tan tốt các chất không phân cực.
Việc lựa chọn dung môi dựa trên độ phân cực là một bước quan trọng trong các quy trình hóa học, bao gồm tổng hợp hữu cơ, chiết xuất, và các phản ứng hóa học khác. Hiểu rõ về độ phân cực dung môi giúp các nhà khoa học và kỹ sư tối ưu hóa hiệu quả của các quy trình này.
II. Phân Loại Dung Môi Theo Độ Phân Cực
Dung môi có thể được phân loại dựa trên độ phân cực của chúng, một yếu tố quan trọng quyết định khả năng hòa tan các chất khác nhau. Việc phân loại này giúp xác định dung môi phù hợp cho các quy trình hóa học cụ thể.
- Dung môi phân cực mạnh:
Các dung môi phân cực mạnh thường có hằng số điện môi (\(\varepsilon\)) cao, phản ánh sự phân bố điện tích không đồng đều trong phân tử. Những dung môi này có khả năng hòa tan tốt các chất ion và các hợp chất phân cực khác. Ví dụ:
- Nước (\(\text{H}_2\text{O}\)): Là dung môi phân cực mạnh nhất, có hằng số điện môi cao và khả năng hòa tan rộng rãi nhiều chất.
- Metanol (\(\text{CH}_3\text{OH}\)): Một dung môi phân cực mạnh khác, thường được sử dụng trong các phản ứng hóa học và các quy trình chiết xuất.
- Axeton (\(\text{CH}_3\text{COCH}_3\)): Dung môi hữu cơ phân cực mạnh, thường được sử dụng trong công nghiệp và nghiên cứu.
- Dung môi phân cực yếu:
Các dung môi phân cực yếu có hằng số điện môi trung bình và khả năng hòa tan hạn chế hơn so với các dung môi phân cực mạnh. Ví dụ:
- Clorofom (\(\text{CHCl}_3\)): Một dung môi phân cực yếu, thường được sử dụng trong các phản ứng hữu cơ.
- Dietyl ete (\(\text{(C}_2\text{H}_5)_2\text{O}\)): Dung môi này được sử dụng rộng rãi trong các quy trình chiết xuất và tách biệt các hợp chất hữu cơ.
- Dung môi không phân cực:
Dung môi không phân cực có hằng số điện môi thấp, với sự phân bố điện tích đồng đều trong phân tử. Chúng có khả năng hòa tan tốt các chất không phân cực hoặc ít phân cực. Ví dụ:
- Hexan (\(\text{C}_6\text{H}_{14}\)): Một dung môi không phân cực, thường được sử dụng trong các quy trình tách chiết dầu mỡ.
- Benzene (\(\text{C}_6\text{H}_6\)): Dung môi không phân cực, thường được sử dụng trong các phản ứng hữu cơ và các nghiên cứu hóa học.
- Carbon tetrachloride (\(\text{CCl}_4\)): Một dung môi không phân cực khác, chủ yếu được sử dụng trong ngành công nghiệp.
Việc hiểu rõ về phân loại dung môi theo độ phân cực giúp tối ưu hóa việc lựa chọn dung môi cho các phản ứng hóa học, đảm bảo hiệu quả cao nhất và giảm thiểu các rủi ro trong quá trình thực hiện.

III. Ứng Dụng Thực Tiễn Của Độ Phân Cực Dung Môi
Độ phân cực của dung môi là yếu tố quan trọng ảnh hưởng đến nhiều quy trình công nghiệp và nghiên cứu khoa học. Tùy thuộc vào mức độ phân cực, dung môi có thể được sử dụng trong nhiều ứng dụng thực tiễn khác nhau, từ ngành công nghiệp sơn, dược phẩm cho đến nghiên cứu hóa học và phân tích. Dưới đây là một số ứng dụng tiêu biểu của độ phân cực dung môi:
1. Ứng dụng trong ngành công nghiệp sơn
Trong ngành công nghiệp sơn, dung môi phân cực giúp cải thiện độ bám dính và độ bền của lớp sơn. Sự tương tác giữa các phân tử phân cực của dung môi và các thành phần khác trong sơn giúp tạo ra màng sơn đồng đều và bền vững.
Dung môi phân cực cũng giúp làm giảm thời gian bay hơi của sơn, từ đó cải thiện quá trình khô và giúp màng sơn trở nên bền màu hơn.
2. Ứng dụng trong ngành dược phẩm
Độ phân cực của dung môi là yếu tố quyết định trong việc lựa chọn dung môi cho các quy trình hòa tan và chiết xuất dược chất. Dung môi phân cực thường được sử dụng để chiết xuất các hợp chất có cực, đảm bảo rằng dược chất được tách ra một cách hiệu quả.
Việc kiểm soát độ phân cực của dung môi cũng giúp cải thiện độ tinh khiết của sản phẩm cuối cùng, tăng cường hiệu quả điều trị và an toàn cho người dùng.
3. Ứng dụng trong công nghiệp hóa chất
Trong ngành công nghiệp hóa chất, độ phân cực của dung môi đóng vai trò quan trọng trong việc tối ưu hóa các phản ứng hóa học. Dung môi phân cực giúp tăng cường sự tương tác giữa các phân tử phản ứng, từ đó tăng hiệu suất và tốc độ của phản ứng.
Hơn nữa, dung môi phân cực còn giúp ổn định các sản phẩm trung gian trong quá trình phản ứng, giảm thiểu rủi ro và tăng độ an toàn cho các quy trình công nghiệp.
4. Ứng dụng trong nghiên cứu và phân tích
Trong các nghiên cứu hóa học và phân tích, dung môi phân cực được sử dụng rộng rãi để tách chiết và phân tích các hợp chất hữu cơ. Độ phân cực của dung môi quyết định khả năng hòa tan của các chất cần phân tích, từ đó ảnh hưởng đến độ chính xác của kết quả phân tích.
Ứng dụng trong sắc ký lỏng hiệu năng cao (HPLC) là một ví dụ điển hình. Sự lựa chọn dung môi với độ phân cực phù hợp sẽ giúp tách chiết các hợp chất một cách hiệu quả và chính xác.
IV. Tính Toán Và Thực Hành
Trong phần này, chúng ta sẽ đi sâu vào các phương pháp tính toán độ phân cực của dung môi, đồng thời tìm hiểu cách xác định độ phân cực của hỗn hợp dung môi. Bằng việc nắm vững các công thức và quy trình, bạn sẽ có thể áp dụng hiệu quả trong thực tiễn nghiên cứu và sản xuất hóa học.
1. Tính toán độ phân cực từ hằng số điện môi
Độ phân cực của dung môi thường được xác định thông qua hằng số điện môi \(\varepsilon\). Công thức tính độ phân cực \(\mu\) của một phân tử trong dung môi dựa trên mô hình momen lưỡng cực được mô tả như sau:
\[
\mu = \sqrt{\frac{9kT \cdot (\varepsilon - 1)}{4\pi N_A \cdot (\varepsilon + 2)}}
\]
Trong đó:
- \(\mu\): Độ phân cực của phân tử (Debye)
- \(k\): Hằng số Boltzmann
- \(T\): Nhiệt độ tuyệt đối (Kelvin)
- \(\varepsilon\): Hằng số điện môi của dung môi
- \(N_A\): Số Avogadro
Bằng cách biết giá trị hằng số điện môi của dung môi, ta có thể dễ dàng tính toán được độ phân cực của nó.
2. Xác định độ phân cực của hỗn hợp dung môi
Đối với hỗn hợp dung môi, độ phân cực tổng hợp \(\mu_{mix}\) được tính dựa trên độ phân cực của từng thành phần dung môi trong hỗn hợp. Công thức được biểu diễn như sau:
\[
\mu_{mix} = \sum x_i \cdot \mu_i
\]
Trong đó:
- \(x_i\): Phân số mol của dung môi thành phần \(i\)
- \(\mu_i\): Độ phân cực của dung môi thành phần \(i\)
Bước tiếp theo là thực hiện tính toán độ phân cực của hỗn hợp dựa trên phân số mol của từng dung môi. Điều này rất quan trọng trong việc điều chỉnh tính chất của dung dịch trong các phản ứng hóa học và ứng dụng công nghiệp.

V. Bài Tập Về Độ Phân Cực Dung Môi
1. Bài tập tính toán độ phân cực của nước và ethanol
Giả sử hằng số điện môi của nước là \(\epsilon_r = 80.1\) và của ethanol là \(\epsilon_r = 24.3\). Hãy tính độ phân cực của hai dung môi này dựa trên hằng số điện môi.
- Bước 1: Xác định hằng số điện môi của nước và ethanol.
- Bước 2: Sử dụng công thức tính độ phân cực \(P = \epsilon_r - 1\).
- Bước 3: Tính độ phân cực của nước và ethanol.
2. Bài tập xác định dung môi phù hợp cho phản ứng hóa học
Giả sử bạn cần chọn dung môi cho phản ứng ester hóa giữa axit acetic và ethanol. Biết rằng phản ứng này cần một dung môi có độ phân cực trung bình. Hãy xác định dung môi thích hợp giữa các lựa chọn sau: nước, etanol, chloroform.
- Bước 1: Xác định độ phân cực của các dung môi.
- Bước 2: So sánh độ phân cực với yêu cầu của phản ứng.
- Bước 3: Chọn dung môi phù hợp nhất.
3. Bài tập so sánh độ phân cực của các dung môi hữu cơ
Hãy sắp xếp các dung môi sau theo thứ tự tăng dần về độ phân cực: hexane, toluene, methanol, acetonitrile.
- Bước 1: Tra cứu độ phân cực của từng dung môi.
- Bước 2: Sắp xếp chúng theo độ phân cực.
4. Bài tập ứng dụng độ phân cực trong chiết xuất
Cho rằng bạn muốn chiết xuất một hợp chất hữu cơ có tính phân cực cao từ dung dịch nước. Hãy xác định dung môi hữu cơ phù hợp nhất cho quá trình chiết xuất: ethyl acetate, hexane, chloroform.
- Bước 1: Xác định tính phân cực của hợp chất cần chiết xuất.
- Bước 2: So sánh độ phân cực của các dung môi.
- Bước 3: Lựa chọn dung môi phù hợp nhất.
5. Bài tập xác định hằng số điện môi của dung môi
Giả sử bạn có một hỗn hợp dung môi bao gồm 70% nước và 30% methanol. Hãy xác định hằng số điện môi tổng của hỗn hợp này.
- Bước 1: Xác định hằng số điện môi của từng dung môi.
- Bước 2: Tính hằng số điện môi trung bình của hỗn hợp.
6. Bài tập phân loại dung môi theo độ phân cực
Dựa trên hằng số điện môi, hãy phân loại các dung môi sau thành phân cực hoặc không phân cực: dichloromethane, acetonitrile, hexane, ethanol.
- Bước 1: Tra cứu hằng số điện môi của từng dung môi.
- Bước 2: Phân loại các dung môi vào hai nhóm: phân cực và không phân cực.
7. Bài tập tính toán năng lượng tương tác trong dung dịch
Sử dụng công thức \[ E = \frac{k q_1 q_2}{r \cdot \epsilon_r} \] để tính toán năng lượng tương tác giữa hai ion trong dung dịch nước (hằng số điện môi \(\epsilon_r = 80\)). Giả sử khoảng cách giữa hai ion là 2 nm và điện tích của chúng là \(q_1 = 1.6 \times 10^{-19} C\), \(q_2 = -1.6 \times 10^{-19} C\).
8. Bài tập về sự ảnh hưởng của độ phân cực đến tốc độ phản ứng
Hãy giải thích tại sao tốc độ phản ứng của các phản ứng trong dung môi phân cực thường nhanh hơn trong dung môi không phân cực. Sử dụng ví dụ minh họa.
9. Bài tập về sự bay hơi của dung môi dựa trên độ phân cực
Giả sử bạn có ba dung môi: nước, acetone và hexane. Hãy sắp xếp chúng theo thứ tự tốc độ bay hơi từ nhanh đến chậm và giải thích dựa trên độ phân cực của chúng.
- Bước 1: Xác định độ phân cực của các dung môi.
- Bước 2: Sắp xếp tốc độ bay hơi dựa trên độ phân cực.
10. Bài tập xác định dung môi cho phản ứng ester hóa
Giả sử bạn muốn thực hiện phản ứng ester hóa giữa axit benzoic và methanol. Hãy chọn một dung môi phân cực và giải thích lý do chọn lựa.
- Bước 1: Xác định yêu cầu về dung môi cho phản ứng ester hóa.
- Bước 2: Chọn dung môi phân cực phù hợp.
XEM THÊM:
VI. Tổng Kết
Độ phân cực của dung môi đóng vai trò quan trọng trong nhiều lĩnh vực nghiên cứu và ứng dụng thực tiễn. Việc hiểu rõ về độ phân cực giúp các nhà khoa học và kỹ sư lựa chọn dung môi phù hợp để tối ưu hóa các quá trình hóa học, từ đó nâng cao hiệu quả và chất lượng sản phẩm.
Trong nghiên cứu, độ phân cực dung môi có thể ảnh hưởng đến cấu trúc và tính chất của các hợp chất trong dung dịch, điều này dẫn đến sự thay đổi trong các kết quả thí nghiệm. Việc tính toán và đo lường độ phân cực chính xác là cơ sở để dự đoán và kiểm soát các phản ứng hóa học phức tạp.
Đối với các ngành công nghiệp như dược phẩm, hóa chất, và sơn, độ phân cực dung môi được áp dụng để cải thiện khả năng hòa tan, tốc độ phản ứng và sự ổn định của sản phẩm cuối cùng. Sự lựa chọn đúng loại dung môi không chỉ giúp tiết kiệm chi phí sản xuất mà còn giảm thiểu các tác động tiêu cực đến môi trường.
Về mặt ứng dụng trong tương lai, nghiên cứu về độ phân cực dung môi có thể mở ra những hướng đi mới trong việc phát triển các dung môi sinh học thân thiện với môi trường, đồng thời tạo ra các quy trình sản xuất hóa chất an toàn và hiệu quả hơn.
Nhìn chung, việc hiểu và vận dụng tốt độ phân cực của dung môi không chỉ nâng cao hiệu quả trong các quy trình công nghiệp và nghiên cứu mà còn đóng góp vào sự phát triển bền vững của khoa học và công nghệ. Điều này khẳng định tầm quan trọng của độ phân cực dung môi trong mọi khía cạnh của khoa học hóa học.