Chủ đề công thức đẳng tích: Công thức đẳng tích là một khái niệm quan trọng trong vật lý học, đặc biệt trong lĩnh vực nhiệt động lực học. Bài viết này sẽ giúp bạn khám phá sâu hơn về định luật Charles, công thức đẳng tích và những ứng dụng thực tiễn của nó trong đời sống hàng ngày.
Mục lục
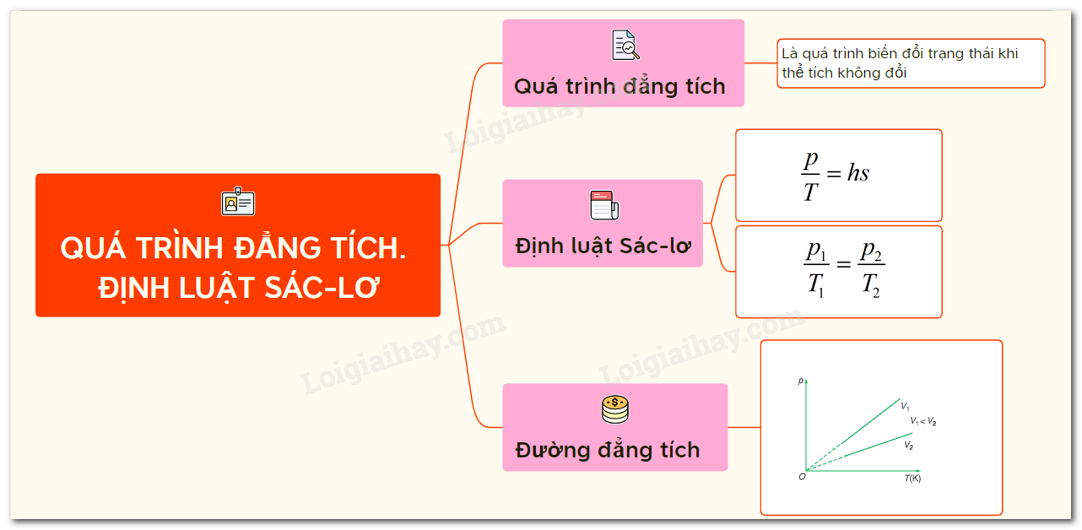
Quá Trình Đẳng Tích và Định Luật Charles
Quá trình đẳng tích là một khái niệm quan trọng trong vật lý học, đặc biệt trong lĩnh vực nhiệt động lực học. Quá trình này diễn ra khi thể tích của một hệ thống không thay đổi, trong khi các thông số khác như áp suất và nhiệt độ có thể biến đổi. Đây là một trong những quá trình cơ bản trong nghiên cứu các hệ thống khí lý tưởng.
Định Luật Charles
Định luật Charles, còn được gọi là định luật Sác-lơ, mô tả mối quan hệ giữa áp suất và nhiệt độ của một lượng khí cố định khi thể tích không đổi. Định luật này được phát biểu như sau:
"Trong quá trình đẳng tích của một lượng khí nhất định, áp suất tỉ lệ thuận với nhiệt độ tuyệt đối của khí đó."
- Công thức:
Giả sử ta có một lượng khí với áp suất p_1 ở nhiệt độ tuyệt đối T_1 trong trạng thái đầu, và áp suất p_2 ở nhiệt độ tuyệt đối T_2 trong trạng thái cuối. Định luật Charles có thể được biểu diễn bằng công thức:
\( \frac{p_1}{T_1} = \frac{p_2}{T_2} \)
Ở đây:
- p_1, p_2: Áp suất của khí ở trạng thái đầu và trạng thái cuối.
- T_1, T_2: Nhiệt độ tuyệt đối của khí ở trạng thái đầu và trạng thái cuối (đơn vị Kelvin).
Ứng Dụng của Quá Trình Đẳng Tích
Quá trình đẳng tích có nhiều ứng dụng trong cuộc sống và công nghiệp:
- Hệ thống làm lạnh và điều hòa không khí: Định luật Charles là nền tảng để hiểu cơ chế hoạt động của các hệ thống làm lạnh và điều hòa không khí. Khi khí nén và giãn nở, nhiệt độ của nó thay đổi, giúp làm mát không khí trong phòng.
- Đo nhiệt độ: Định luật này cũng áp dụng trong các thiết bị đo nhiệt độ, nơi sự thay đổi nhiệt độ được sử dụng để đo áp suất khí trong các cảm biến nhiệt độ.
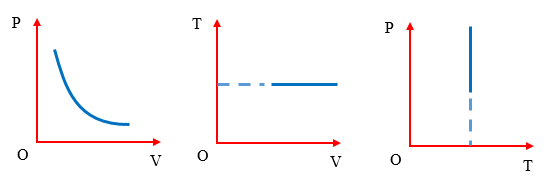
Đường Đẳng Tích
Đường đẳng tích là một biểu đồ biểu diễn sự biến thiên của áp suất theo nhiệt độ trong quá trình đẳng tích. Đường này thường có dạng đường thẳng trên hệ tọa độ (p, T) với độ dốc tỉ lệ thuận với hằng số của quá trình.
| Áp suất (Pa) | Nhiệt độ (K) | p/T (Pa/K) |
| 1,0 x 105 | 301 | 332,23 |
| 1,1 x 105 | 331 | 332,33 |
| 1,2 x 105 | 350 | 342,86 |
| 1,3 x 105 | 365 | 356,16 |
Đường đẳng tích cho thấy rằng khi nhiệt độ tăng, áp suất cũng tăng nếu thể tích không thay đổi, minh chứng cho tính đúng đắn của định luật Charles trong thực tế.
1. Quá Trình Đẳng Tích Là Gì?
Quá trình đẳng tích là một quá trình trong nhiệt động lực học, trong đó thể tích của hệ không thay đổi khi nhiệt độ và áp suất thay đổi. Đây là một quá trình quan trọng trong việc hiểu rõ mối quan hệ giữa các yếu tố như nhiệt độ, áp suất và thể tích trong các hệ thống kín.
Trong quá trình đẳng tích, định luật Charles được áp dụng, và công thức cơ bản của nó được viết dưới dạng:
$$\frac{P_1}{T_1} = \frac{P_2}{T_2}$$
Trong đó:
- \(P_1\) và \(P_2\) là áp suất ban đầu và áp suất sau khi thay đổi.
- \(T_1\) và \(T_2\) là nhiệt độ ban đầu và nhiệt độ sau khi thay đổi.
Quá trình đẳng tích thường được sử dụng trong các ứng dụng như máy nén khí, hệ thống điều hòa nhiệt độ và nhiều hệ thống nhiệt động khác. Hiểu biết về quá trình này giúp cải thiện hiệu suất và tối ưu hóa các hệ thống liên quan đến nhiệt động lực học.
2. Định Luật Charles và Công Thức Đẳng Tích
Định luật Charles là một định luật cơ bản trong nhiệt động lực học, phát biểu rằng thể tích của một lượng khí lý tưởng cố định tỷ lệ thuận với nhiệt độ tuyệt đối của nó khi áp suất không đổi. Đây là nền tảng cho công thức đẳng tích, giúp xác định mối quan hệ giữa áp suất và nhiệt độ trong quá trình đẳng tích.
Trong quá trình đẳng tích, thể tích (\(V\)) của hệ không thay đổi, do đó, định luật Charles có thể được áp dụng để thiết lập mối quan hệ giữa áp suất (\(P\)) và nhiệt độ (\(T\)) như sau:
$$\frac{P_1}{T_1} = \frac{P_2}{T_2}$$
Trong đó:
- \(P_1\) là áp suất ban đầu của khí khi ở nhiệt độ \(T_1\).
- \(P_2\) là áp suất của khí sau khi nhiệt độ thay đổi thành \(T_2\).
- \(T_1\) và \(T_2\) là nhiệt độ ban đầu và nhiệt độ sau khi thay đổi, tính bằng Kelvin (K).
Công thức đẳng tích này rất hữu ích trong các hệ thống nhiệt động lực học, nơi thể tích không thay đổi nhưng áp suất và nhiệt độ có thể biến đổi. Việc áp dụng định luật Charles và công thức đẳng tích giúp chúng ta dự đoán được sự thay đổi áp suất khi nhiệt độ thay đổi, một yếu tố quan trọng trong nhiều ứng dụng thực tiễn như thiết kế máy nén khí, hệ thống làm lạnh và điều hòa không khí.

3. Ứng Dụng của Định Luật Charles trong Thực Tiễn
Định luật Charles không chỉ là một lý thuyết cơ bản trong nhiệt động lực học, mà còn có nhiều ứng dụng thực tiễn trong đời sống hàng ngày và các ngành công nghiệp. Dưới đây là một số ví dụ nổi bật:
- Hệ thống điều hòa không khí và tủ lạnh: Định luật Charles được áp dụng để duy trì nhiệt độ ổn định bên trong các hệ thống làm lạnh. Khi nhiệt độ môi trường thay đổi, áp suất của chất làm lạnh cũng thay đổi theo để duy trì hiệu quả làm lạnh.
- Bong bóng khí cầu: Khi một khí cầu bay lên cao, nhiệt độ không khí giảm dần. Theo định luật Charles, áp suất bên trong khí cầu cũng giảm, làm cho khí cầu co lại. Điều này giải thích tại sao khí cầu cần phải được bơm phồng ở mặt đất trước khi bay.
- Động cơ đốt trong: Trong động cơ xe hơi, khi hỗn hợp không khí và nhiên liệu bị đốt cháy, nhiệt độ trong xi lanh tăng lên, dẫn đến sự tăng áp suất theo định luật Charles. Sự tăng áp suất này tạo ra lực đẩy piston, chuyển đổi năng lượng nhiệt thành công cơ học.
- Bình gas: Các bình gas trong gia đình hay sử dụng định luật Charles để đảm bảo áp suất bên trong ổn định khi nhiệt độ môi trường thay đổi. Điều này giúp đảm bảo an toàn và hiệu suất sử dụng cao.
Nhờ vào những ứng dụng này, định luật Charles đóng vai trò quan trọng trong nhiều lĩnh vực công nghiệp, góp phần nâng cao hiệu suất và độ an toàn của các hệ thống liên quan đến nhiệt động lực học.
4. Bài Tập và Lời Giải về Quá Trình Đẳng Tích
Quá trình đẳng tích là một phần quan trọng trong các bài tập nhiệt động lực học. Dưới đây là một số bài tập mẫu cùng với lời giải chi tiết để giúp bạn hiểu rõ hơn về quá trình này:
-
Bài tập 1: Một lượng khí lý tưởng có thể tích ban đầu là \( V_1 = 10 \, \text{lít} \) và nhiệt độ ban đầu là \( T_1 = 300 \, \text{K} \). Tính nhiệt độ cuối cùng \( T_2 \) khi thể tích không đổi và áp suất tăng gấp đôi.
Lời giải:
Áp dụng định luật Charles, ta có:
\[
\frac{P_1}{T_1} = \frac{P_2}{T_2}
\]Vì \( P_2 = 2P_1 \) và thể tích không đổi:
\[
T_2 = 2T_1 = 2 \times 300 = 600 \, \text{K}
\]Vậy nhiệt độ cuối cùng là \( T_2 = 600 \, \text{K} \).
-
Bài tập 2: Một lượng khí có thể tích \( 5 \, \text{lít} \) ở nhiệt độ \( 400 \, \text{K} \). Tính thể tích khi nhiệt độ giảm xuống \( 200 \, \text{K} \) và áp suất không đổi.
Lời giải:
Áp dụng định luật Charles, ta có:
\[
\frac{V_1}{T_1} = \frac{V_2}{T_2}
\]Thay giá trị vào:
\[
V_2 = \frac{V_1 \times T_2}{T_1} = \frac{5 \times 200}{400} = 2.5 \, \text{lít}
\]Vậy thể tích khi nhiệt độ giảm xuống là \( 2.5 \, \text{lít} \).
-
Bài tập 3: Một khí có thể tích không đổi với áp suất ban đầu \( P_1 = 1 \, \text{atm} \) và nhiệt độ ban đầu \( T_1 = 273 \, \text{K} \). Tính áp suất cuối cùng khi nhiệt độ tăng lên \( 546 \, \text{K} \).
Lời giải:
Áp dụng định luật Charles, ta có:
\[
\frac{P_1}{T_1} = \frac{P_2}{T_2}
\]Thay giá trị vào:
\[
P_2 = \frac{P_1 \times T_2}{T_1} = \frac{1 \times 546}{273} = 2 \, \text{atm}
\]Vậy áp suất cuối cùng là \( 2 \, \text{atm} \).
Những bài tập trên giúp làm rõ cách áp dụng định luật Charles và công thức đẳng tích trong các tình huống thực tiễn, qua đó giúp củng cố kiến thức về nhiệt động lực học.

5. Câu Hỏi Thường Gặp về Quá Trình Đẳng Tích
Quá trình đẳng tích là một chủ đề quan trọng trong nhiệt động lực học, và dưới đây là một số câu hỏi thường gặp liên quan đến chủ đề này:
-
Câu hỏi 1: Quá trình đẳng tích là gì?
Trả lời: Quá trình đẳng tích là quá trình trong đó thể tích của hệ không thay đổi. Điều này có nghĩa là mọi sự biến đổi trong hệ chỉ ảnh hưởng đến áp suất và nhiệt độ, trong khi thể tích vẫn giữ nguyên.
-
Câu hỏi 2: Định luật Charles có áp dụng cho quá trình đẳng tích không?
Trả lời: Có, định luật Charles áp dụng cho quá trình đẳng tích. Định luật này cho thấy mối quan hệ tỷ lệ thuận giữa áp suất và nhiệt độ của khí lý tưởng khi thể tích không đổi.
-
Câu hỏi 3: Công thức nào được sử dụng trong quá trình đẳng tích?
Trả lời: Công thức chính trong quá trình đẳng tích là \( \frac{P_1}{T_1} = \frac{P_2}{T_2} \), trong đó \( P \) là áp suất và \( T \) là nhiệt độ tuyệt đối, khi thể tích không đổi.
-
Câu hỏi 4: Có thể áp dụng quá trình đẳng tích trong thực tế không?
Trả lời: Quá trình đẳng tích thường được áp dụng trong các hệ thống kín, chẳng hạn như trong bình chứa hoặc các thiết bị có thể tích cố định, nơi sự thay đổi nhiệt độ dẫn đến sự thay đổi áp suất.
-
Câu hỏi 5: Điều gì xảy ra với năng lượng nội tại của khí trong quá trình đẳng tích?
Trả lời: Trong quá trình đẳng tích, năng lượng nội tại của khí thay đổi tỷ lệ thuận với nhiệt độ, vì thể tích không thay đổi, nên công thực hiện bởi hệ là không đáng kể.