Chủ đề bảng nguyên tử khối lớp 7: Bảng nguyên tử khối lớp 7 là một phần quan trọng trong chương trình Hóa học, giúp học sinh nắm vững khối lượng các nguyên tố. Bài viết này sẽ cung cấp một hướng dẫn chi tiết, dễ hiểu và các mẹo học thuộc nhanh chóng, giúp bạn đạt kết quả cao trong học tập.
Mục lục
Bảng Nguyên Tử Khối Lớp 7
Bảng nguyên tử khối là một phần quan trọng trong chương trình học Hóa học lớp 7, giúp học sinh hiểu và ghi nhớ khối lượng của các nguyên tố hóa học. Dưới đây là thông tin chi tiết về bảng nguyên tử khối và cách học thuộc nhanh chóng.
1. Bảng Nguyên Tử Khối Là Gì?
Nguyên tử khối là khối lượng của một nguyên tử tính theo đơn vị khối lượng nguyên tử (amu). Trong Hóa học lớp 7, bảng nguyên tử khối giúp học sinh xác định và so sánh khối lượng các nguyên tố khác nhau.
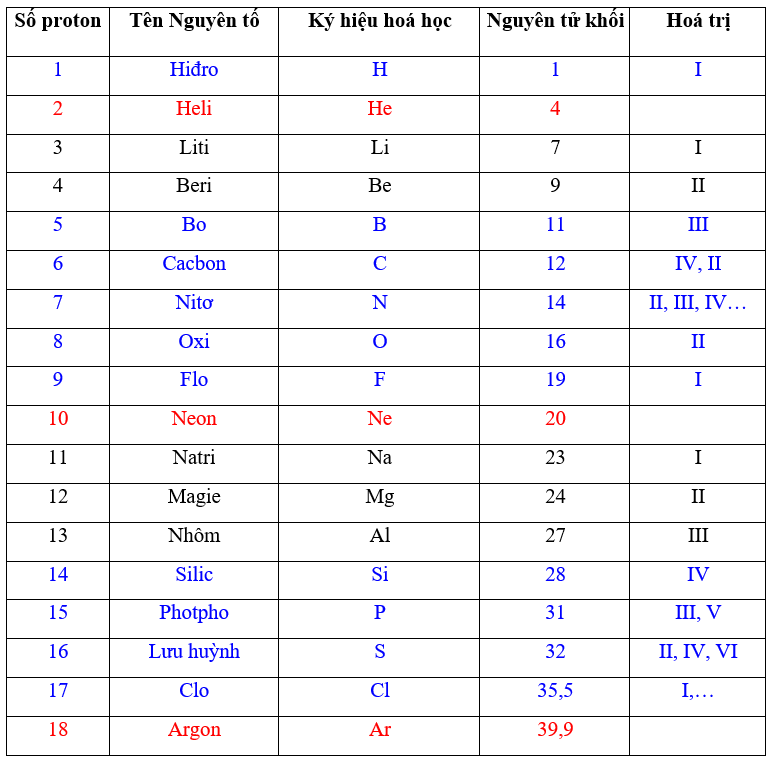
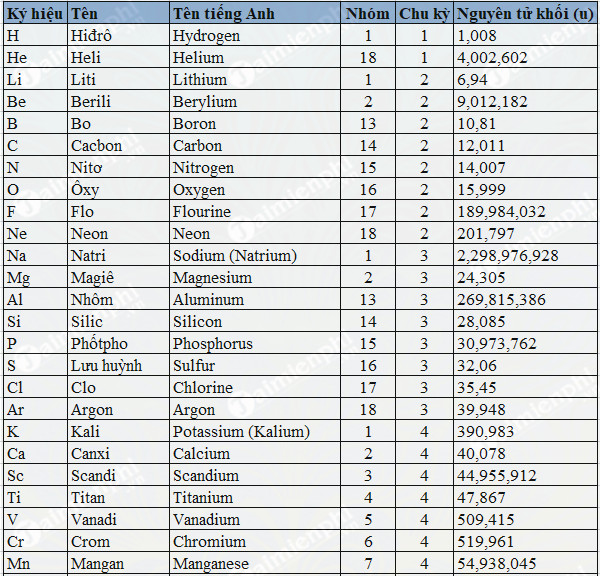
2. Bảng Nguyên Tử Khối Các Nguyên Tố Thường Gặp
| Nguyên Tố | Ký Hiệu Hóa Học | Nguyên Tử Khối (\(u\)) |
| Hydro | H | 1 |
| Carbon | C | 12 |
| Oxy | O | 16 |
| Natri | Na | 23 |
| Nhôm | Al | 27 |
3. Phương Pháp Học Thuộc Bảng Nguyên Tử Khối
- Thơ Học Thuộc: Học thuộc bảng nguyên tử khối thông qua các bài thơ vần điệu giúp học sinh dễ nhớ hơn.
- Bài Tập Thực Hành: Làm bài tập Hóa học thường xuyên sẽ giúp ghi nhớ nguyên tử khối một cách tự nhiên.
- Sử Dụng Flashcard: Flashcard là một công cụ hữu ích để ôn tập nhanh các nguyên tử khối khi cần thiết.
4. Ứng Dụng Của Bảng Nguyên Tử Khối Trong Hóa Học
Bảng nguyên tử khối được sử dụng rộng rãi trong các bài tập về tính khối lượng phân tử, tìm nguyên tố trong hợp chất và nhiều dạng bài tập khác. Việc nắm vững bảng nguyên tử khối giúp học sinh giải quyết các bài toán hóa học một cách dễ dàng và chính xác.
Ví dụ: Tính khối lượng phân tử của nước (H2O):
\[ M(H_2O) = 2 \times M(H) + 1 \times M(O) = 2 \times 1 + 16 = 18 \ (u) \]
5. Lời Khuyên Cho Học Sinh
Để ghi nhớ bảng nguyên tử khối một cách hiệu quả, học sinh nên kết hợp nhiều phương pháp học tập khác nhau, từ ghi nhớ truyền thống đến thực hành thường xuyên và sử dụng công nghệ hỗ trợ.

1. Giới Thiệu Chung Về Bảng Nguyên Tử Khối
Bảng nguyên tử khối là công cụ quan trọng trong Hóa học, giúp xác định khối lượng của các nguyên tử trong các nguyên tố khác nhau. Trong chương trình lớp 7, việc nắm vững bảng nguyên tử khối giúp học sinh dễ dàng tính toán và hiểu rõ hơn về thành phần và phản ứng hóa học.
Bảng nguyên tử khối cung cấp thông tin về khối lượng tương đối của từng nguyên tử, thường được tính theo đơn vị amu (atomic mass unit). Các nguyên tố hóa học được sắp xếp theo thứ tự tăng dần của số hiệu nguyên tử trong bảng tuần hoàn, với nguyên tử khối của mỗi nguyên tố được liệt kê ngay bên cạnh.
Dưới đây là một số điểm quan trọng khi học về bảng nguyên tử khối:
- Đơn vị đo lường: Khối lượng của một nguyên tử được đo bằng đơn vị khối lượng nguyên tử (amu), với 1 amu bằng \(\frac{1}{12}\) khối lượng của nguyên tử carbon-12.
- Khối lượng tương đối: Khối lượng của các nguyên tử được tính theo thang đo tương đối so với nguyên tử carbon-12.
- Sự chính xác: Bảng nguyên tử khối thường làm tròn đến một hoặc hai chữ số thập phân để thuận tiện trong tính toán và học tập.
Hiểu rõ và ghi nhớ bảng nguyên tử khối là bước cơ bản để học tốt môn Hóa học, đặc biệt là trong các bài tập liên quan đến tính toán khối lượng phân tử và phản ứng hóa học.
2. Cấu Trúc Bảng Nguyên Tử Khối
Bảng nguyên tử khối là một công cụ khoa học thiết yếu, được cấu trúc một cách logic và rõ ràng để giúp học sinh dễ dàng tra cứu và sử dụng. Dưới đây là các thành phần chính trong cấu trúc của bảng nguyên tử khối:
- Nguyên tố hóa học: Các nguyên tố được sắp xếp theo thứ tự tăng dần của số hiệu nguyên tử, từ 1 đến 118. Mỗi nguyên tố hóa học trong bảng tuần hoàn đều có một ký hiệu hóa học riêng (ví dụ: H cho Hydro, O cho Oxy).
- Khối lượng nguyên tử: Khối lượng nguyên tử được hiển thị dưới dạng số thập phân, thể hiện khối lượng trung bình của nguyên tử tính theo đơn vị khối lượng nguyên tử \((\text{amu})\). Giá trị này phản ánh sự phân bố của các đồng vị của nguyên tố đó trong tự nhiên.
- Số hiệu nguyên tử: Số hiệu nguyên tử của mỗi nguyên tố được hiển thị ở góc trên bên trái của ô nguyên tố, thể hiện số proton trong hạt nhân của nguyên tử.
- Các chu kỳ và nhóm: Các nguyên tố được xếp vào các chu kỳ (hàng ngang) và các nhóm (cột dọc) trong bảng tuần hoàn. Mỗi chu kỳ và nhóm cho biết các thuộc tính hóa học tương tự giữa các nguyên tố trong cùng một hàng hoặc cột.
Cấu trúc của bảng nguyên tử khối cho phép người dùng dễ dàng tra cứu thông tin cần thiết về các nguyên tố, đồng thời cung cấp một cái nhìn tổng quan về mối quan hệ giữa các nguyên tố dựa trên số hiệu nguyên tử và khối lượng của chúng.

4. Ứng Dụng Của Bảng Nguyên Tử Khối
Bảng nguyên tử khối không chỉ là công cụ học tập trong môn hóa học mà còn có nhiều ứng dụng thực tiễn trong nghiên cứu và đời sống hàng ngày. Dưới đây là một số ứng dụng phổ biến:
- Trong tính toán khối lượng phân tử: Bảng nguyên tử khối được sử dụng để tính toán khối lượng phân tử của các hợp chất hóa học. Ví dụ, khối lượng phân tử của nước \(\text{H}_2\text{O}\) có thể tính bằng cách cộng khối lượng của hai nguyên tử hydro và một nguyên tử oxy.
- Trong việc cân bằng phương trình hóa học: Để cân bằng các phương trình hóa học, việc biết được khối lượng của các nguyên tử giúp đảm bảo tính chính xác và đồng nhất về khối lượng giữa các chất phản ứng và sản phẩm.
- Trong nghiên cứu và phân tích: Khối lượng nguyên tử của các nguyên tố là cơ sở để thực hiện các phân tích hóa học định lượng, từ đó xác định thành phần và tỉ lệ của các nguyên tố trong một mẫu vật.
- Trong ngành công nghiệp: Bảng nguyên tử khối được ứng dụng trong quá trình sản xuất và kiểm soát chất lượng sản phẩm, đặc biệt trong ngành hóa dược, vật liệu và sản xuất kim loại.
- Giáo dục và đào tạo: Việc sử dụng bảng nguyên tử khối giúp học sinh nắm vững kiến thức cơ bản về hóa học, từ đó phát triển tư duy logic và kỹ năng giải quyết vấn đề.
Như vậy, bảng nguyên tử khối đóng vai trò quan trọng không chỉ trong việc học tập mà còn trong nhiều lĩnh vực khác, từ nghiên cứu đến ứng dụng thực tiễn.
5. Lời Khuyên Cho Học Sinh Khi Học Bảng Nguyên Tử Khối
Để học tốt bảng nguyên tử khối, học sinh cần có một phương pháp học tập khoa học và phù hợp với từng người. Dưới đây là một số lời khuyên giúp học sinh tiếp cận và ghi nhớ bảng nguyên tử khối hiệu quả:
- 5.1 Cách Tiếp Cận Hiệu Quả
- Hiểu rõ khái niệm: Trước tiên, hãy chắc chắn rằng bạn hiểu rõ khái niệm nguyên tử khối và vai trò của nó trong hóa học. Học thuộc lòng mà không hiểu rõ ý nghĩa chỉ khiến việc ghi nhớ trở nên khó khăn hơn.
- Sử dụng công cụ hỗ trợ học tập: Sử dụng flashcard, bài ca nguyên tử khối, hoặc các ứng dụng học tập để giúp ghi nhớ nguyên tử khối của các nguyên tố một cách hiệu quả. Ví dụ, bạn có thể dùng flashcard ghi tên nguyên tố ở một mặt và nguyên tử khối ở mặt kia để luyện tập nhớ.
- Tìm mối liên hệ giữa các nguyên tố: Học sinh nên tìm mối liên hệ giữa các nguyên tố gần nhau trong bảng tuần hoàn. Ví dụ, các nguyên tố thuộc cùng một nhóm trong bảng tuần hoàn thường có nguyên tử khối tăng dần từ trên xuống.
- 5.2 Tầm Quan Trọng Của Việc Ôn Luyện Thường Xuyên
- Ôn luyện theo phương pháp “lặp lại cách quãng”: Học sinh nên ôn luyện bảng nguyên tử khối theo phương pháp “lặp lại cách quãng”. Điều này giúp củng cố kiến thức và tránh tình trạng quên lãng theo thời gian. Ví dụ, học sinh có thể ôn luyện mỗi ngày 15 phút để đảm bảo kiến thức được lưu trữ trong trí nhớ dài hạn.
- Luyện tập thông qua bài tập: Sử dụng bài tập hóa học để vận dụng kiến thức về nguyên tử khối. Thường xuyên làm các bài tập tính khối lượng phân tử hoặc tìm nguyên tố trong hợp chất để giúp củng cố và ghi nhớ lâu hơn.
- Thảo luận nhóm: Học sinh có thể tổ chức các buổi học nhóm, cùng nhau thảo luận và giải bài tập liên quan đến nguyên tử khối. Việc trao đổi ý kiến và chia sẻ kiến thức sẽ giúp nâng cao khả năng ghi nhớ và hiểu sâu hơn về kiến thức.
Cuối cùng, quan trọng nhất là học sinh cần kiên trì và có thái độ tích cực trong quá trình học tập. Việc học bảng nguyên tử khối có thể khó khăn ban đầu, nhưng với phương pháp học tập phù hợp và sự nỗ lực không ngừng, việc nắm vững kiến thức sẽ trở nên dễ dàng hơn.

6. Các Bài Tập Vận Dụng Bảng Nguyên Tử Khối
Dưới đây là một số bài tập giúp bạn vận dụng bảng nguyên tử khối để tính toán và hiểu rõ hơn về khối lượng của các nguyên tố hóa học. Các bài tập này phù hợp cho học sinh lớp 7 và các bạn học sinh muốn ôn tập lại kiến thức cơ bản.
-
Bài tập 1: Tính khối lượng nguyên tử của một nguyên tố biết rằng nó có 8 proton và 8 neutron.
Hướng dẫn: Sử dụng công thức:
\[ \text{Khối lượng nguyên tử} = Z \times m_p + N \times m_n \]- Với \(Z = 8\), \(N = 8\), \(m_p \approx 1.007 \, u\), \(m_n \approx 1.008 \, u\).
Đáp án: Tính toán ra khối lượng nguyên tử.
-
Bài tập 2: Một nguyên tố Clo (Cl) có hai đồng vị phổ biến là \(^{35}Cl\) (75.77%) và \(^{37}Cl\) (24.23%). Tính khối lượng nguyên tử trung bình của Clo.
Hướng dẫn: Sử dụng công thức tính khối lượng nguyên tử trung bình:
\[ \text{Khối lượng nguyên tử trung bình} = (0.7577 \times 34.969) + (0.2423 \times 36.966) \]Đáp án: Khối lượng trung bình của Clo là khoảng \(35.45 \, u\).
-
Bài tập 3: Cho biết khối lượng nguyên tử của Hydro (H) là 1.008 u, của Carbon (C) là 12.011 u. Tính khối lượng phân tử của nước (H2O).
Hướng dẫn: Công thức tính khối lượng phân tử là tổng khối lượng nguyên tử của các nguyên tố trong phân tử:
\[ \text{Khối lượng phân tử H}_2\text{O} = 2 \times \text{khối lượng của H} + 1 \times \text{khối lượng của O} \] \[ = 2 \times 1.008 + 1 \times 15.999 = 18.015 \, u \]Đáp án: Khối lượng phân tử của nước là 18.015 u.
-
Bài tập 4: Tính khối lượng của một nguyên tử Natri (Na) biết khối lượng nguyên tử của Na là 22.990 u.
Hướng dẫn: Khối lượng của nguyên tử Na đã được cho trực tiếp từ bảng nguyên tử khối. Xác nhận giá trị từ bảng.
Đáp án: Khối lượng của một nguyên tử Natri là 22.990 u.
Các bài tập trên giúp học sinh hiểu rõ hơn về cách sử dụng bảng nguyên tử khối để tính toán khối lượng của các nguyên tố và phân tử. Bằng cách áp dụng các công thức cơ bản và thực hành nhiều bài tập, học sinh sẽ nắm vững kiến thức về nguyên tử và phân tử, từ đó có thể dễ dàng áp dụng trong các bài kiểm tra và bài thi.