Chủ đề tính điện tích hạt nhân: Tính điện tích hạt nhân là một khái niệm quan trọng trong hóa học và vật lý, giúp xác định đặc trưng của nguyên tử. Bài viết này sẽ hướng dẫn bạn cách tính điện tích hạt nhân, giải thích các ứng dụng quan trọng, và cung cấp ví dụ minh họa chi tiết để dễ dàng hiểu và áp dụng trong thực tế.
Mục lục
Tính Điện Tích Hạt Nhân
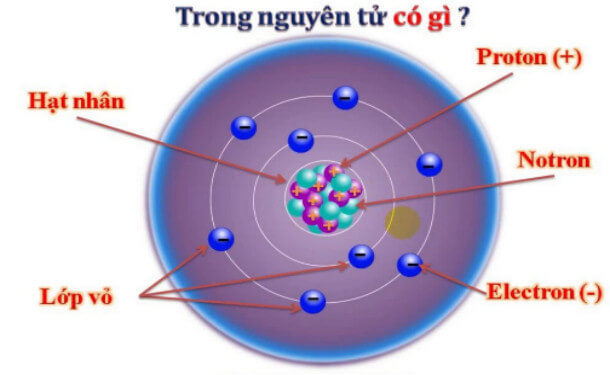
Điện tích hạt nhân là một khái niệm cơ bản trong hóa học và vật lý, liên quan đến số lượng proton có trong hạt nhân của một nguyên tử. Dưới đây là thông tin chi tiết về khái niệm này và cách tính toán liên quan:
1. Khái Niệm Điện Tích Hạt Nhân
Điện tích hạt nhân của một nguyên tử được xác định bởi số proton có trong hạt nhân. Số proton này cũng chính là số hiệu nguyên tử (Z) và quyết định tính chất hóa học của nguyên tố.
- Ví dụ: Nguyên tử Hydro có 1 proton, nên điện tích hạt nhân của nó là +1.
- Nguyên tử Nhôm (Al) có 13 proton, nên điện tích hạt nhân là +13.
2. Công Thức Tính Điện Tích Hạt Nhân
Điện tích hạt nhân của một nguyên tố được tính bằng số proton trong hạt nhân. Công thức tính như sau:
Trong đó, Z là số hiệu nguyên tử, đồng thời là điện tích hạt nhân của nguyên tử.
3. Ứng Dụng Của Điện Tích Hạt Nhân
Điện tích hạt nhân là một yếu tố quan trọng giúp xác định tính chất của các nguyên tố hóa học và vị trí của chúng trong bảng tuần hoàn. Các ứng dụng cụ thể bao gồm:
- Xác định nguyên tố: Số proton trong hạt nhân quyết định loại nguyên tố.
- Phân loại đồng vị: Điện tích hạt nhân kết hợp với số neutron giúp phân loại các đồng vị của cùng một nguyên tố.
- Cấu hình electron: Số proton xác định số electron và cấu hình electron, từ đó ảnh hưởng đến tính chất hóa học của nguyên tố.
4. Bài Tập Minh Họa
Dưới đây là một số bài tập giúp hiểu rõ hơn về cách tính điện tích hạt nhân:
- Xác định điện tích hạt nhân của nguyên tử có 20 proton.
- Viết cấu hình electron cho nguyên tử có điện tích hạt nhân là +11.
- Tính số khối của nguyên tử có 17 proton và 18 neutron.
5. Tổng Kết
Điện tích hạt nhân là một khái niệm then chốt trong việc hiểu rõ cấu trúc nguyên tử và tính chất của các nguyên tố. Việc nắm vững kiến thức về điện tích hạt nhân sẽ giúp ích trong nhiều lĩnh vực như hóa học, vật lý, và các ngành khoa học ứng dụng khác.
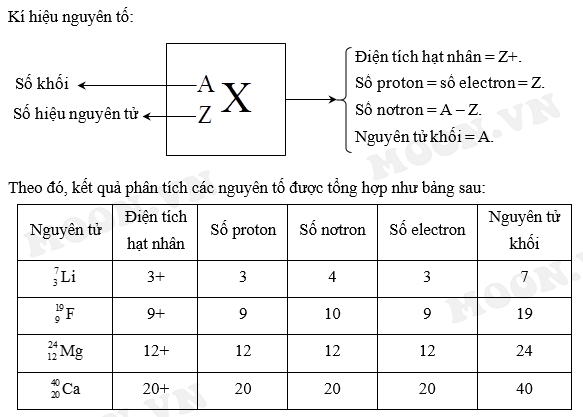
3. Ứng Dụng Của Điện Tích Hạt Nhân Trong Hóa Học
Điện tích hạt nhân không chỉ là một khái niệm lý thuyết mà còn có nhiều ứng dụng thực tiễn trong hóa học. Dưới đây là một số ứng dụng nổi bật:
- Xác định nguyên tố hóa học: Điện tích hạt nhân, hay số hiệu nguyên tử, xác định loại nguyên tố. Mỗi nguyên tố trong bảng tuần hoàn có một điện tích hạt nhân riêng biệt, giúp phân biệt chúng.
- Phân loại đồng vị: Đồng vị của một nguyên tố có cùng số proton nhưng khác số neutron. Tuy nhiên, điện tích hạt nhân vẫn không đổi, giúp xác định đồng vị của nguyên tố đó.
- Cấu hình electron: Điện tích hạt nhân quyết định số lượng electron trong một nguyên tử, từ đó ảnh hưởng đến cấu hình electron. Cấu hình này đóng vai trò quan trọng trong việc xác định tính chất hóa học và khả năng phản ứng của nguyên tố.
- Lực hút giữa hạt nhân và electron: Điện tích hạt nhân tạo ra lực hút giữa hạt nhân và các electron. Lực này càng mạnh thì các electron càng bị hút chặt vào hạt nhân, ảnh hưởng đến kích thước nguyên tử và năng lượng ion hóa.
- Vai trò trong phản ứng hóa học: Điện tích hạt nhân ảnh hưởng đến cách thức nguyên tử liên kết với nhau trong các phản ứng hóa học. Nguyên tử với điện tích hạt nhân lớn thường có xu hướng hút electron mạnh hơn, dẫn đến khả năng tạo ra các liên kết cộng hóa trị hoặc ion hóa.
Nhờ những ứng dụng trên, hiểu biết về điện tích hạt nhân giúp các nhà khoa học và học sinh có thể phân tích, dự đoán và giải thích các hiện tượng hóa học một cách chính xác hơn.
4. Cách Tính Số Khối Và Số Proton Trong Hạt Nhân
Số khối và số proton là hai đại lượng quan trọng trong việc xác định đặc tính của một nguyên tử. Dưới đây là cách tính số khối và số proton trong hạt nhân, trình bày theo từng bước cụ thể.
Cách Tính Số Proton
Số proton trong hạt nhân của một nguyên tử được xác định dựa trên số hiệu nguyên tử (Z) của nguyên tố đó. Số hiệu nguyên tử chính là số proton, và có thể tìm thấy trên bảng tuần hoàn.
Ví dụ, đối với nguyên tử Carbon (C), số hiệu nguyên tử là 6, nên số proton trong hạt nhân của nó là:
Cách Tính Số Khối
Số khối (A) của một nguyên tử là tổng số proton và neutron trong hạt nhân. Công thức tính số khối được thể hiện như sau:
Trong đó:
- A: Số khối
- Z: Số proton
- N: Số neutron
Ví dụ, nếu nguyên tử Carbon (C) có 6 proton và 6 neutron, số khối của nó sẽ là:
Việc tính toán số khối và số proton giúp chúng ta hiểu rõ hơn về cấu trúc của nguyên tử và vai trò của chúng trong các phản ứng hóa học.

5. Các Bài Tập Về Điện Tích Hạt Nhân
Dưới đây là một số bài tập giúp bạn hiểu rõ hơn về cách tính điện tích hạt nhân cũng như vận dụng vào các trường hợp cụ thể. Các bài tập này được thiết kế để củng cố kiến thức và rèn luyện kỹ năng tính toán trong hóa học.
Bài Tập 1: Tính Điện Tích Hạt Nhân
Cho các nguyên tố sau: Helium (He), Oxygen (O), và Sodium (Na). Hãy tính điện tích hạt nhân cho từng nguyên tố.
- Helium:
- Oxygen:
- Sodium:
Bài Tập 2: Xác Định Số Proton Và Số Neutron
Một nguyên tử có số khối là 23 và số hiệu nguyên tử là 11. Hãy xác định số proton và số neutron trong nguyên tử đó.
Hướng dẫn: Số proton chính là số hiệu nguyên tử (Z), còn số neutron được tính bằng hiệu giữa số khối (A) và số proton:
Bài Tập 3: Phân Loại Đồng Vị
Cho ba đồng vị của nguyên tố Carbon: C-12, C-13, và C-14. Xác định số proton, neutron và điện tích hạt nhân của từng đồng vị.
- C-12: 6 proton, 6 neutron, điện tích hạt nhân
- C-13: 6 proton, 7 neutron, điện tích hạt nhân
- C-14: 6 proton, 8 neutron, điện tích hạt nhân
Bài Tập 4: So Sánh Điện Tích Hạt Nhân
Hãy so sánh điện tích hạt nhân của các nguyên tử Lithium (Li), Beryllium (Be), và Boron (B) và sắp xếp chúng theo thứ tự tăng dần.
- Lithium:
- Beryllium:
- Boron:
Các bài tập trên được thiết kế nhằm giúp bạn hiểu rõ hơn về điện tích hạt nhân và cách tính toán trong các trường hợp khác nhau, từ cơ bản đến phức tạp.
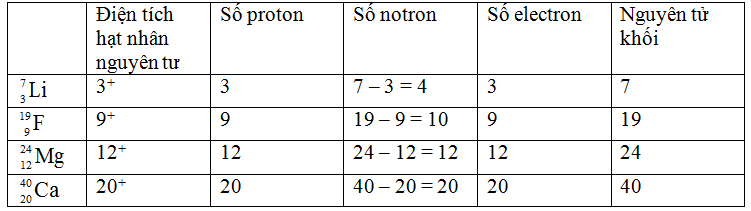
6. Tài Liệu Tham Khảo Và Học Tập
Việc nắm vững kiến thức về tính điện tích hạt nhân là cực kỳ quan trọng trong quá trình học tập và nghiên cứu hóa học. Dưới đây là một số tài liệu tham khảo hữu ích giúp bạn củng cố và mở rộng hiểu biết về chủ đề này.
6.1. Sách Giáo Khoa Hóa Học
- Sách giáo khoa lớp 10: Đây là tài liệu cơ bản cung cấp những kiến thức nền tảng về điện tích hạt nhân, cấu trúc nguyên tử và vai trò của các hạt cơ bản như proton, neutron.
- Sách giáo khoa lớp 11: Nâng cao kiến thức về các yếu tố ảnh hưởng đến điện tích hạt nhân và cách tính số proton trong hạt nhân của các nguyên tố hóa học khác nhau.
- Sách giáo khoa lớp 12: Đi sâu vào cấu hình electron, mối quan hệ giữa số proton và điện tích hạt nhân, đồng thời áp dụng vào phân tích và xác định tính chất hóa học của các nguyên tố.
6.2. Các Nguồn Tài Liệu Trực Tuyến
- Hóa Học Online: Website chuyên về các bài giảng hóa học từ cơ bản đến nâng cao. Tại đây, bạn có thể tìm thấy các bài tập và hướng dẫn tính điện tích hạt nhân cũng như giải thích về vai trò của điện tích trong hóa học.
- Thư viện VLOS: Cung cấp nhiều bài viết về hóa học, bao gồm cả các công thức tính điện tích hạt nhân và bài tập thực hành giúp bạn nắm chắc kiến thức lý thuyết.
- Web Hoctap365: Một nguồn tài liệu học tập phong phú với các đề thi, bài tập về điện tích hạt nhân, số khối, và các bài toán liên quan đến đồng vị. Đây là trang web hữu ích cho học sinh và sinh viên.
- Khan Academy: Đây là nền tảng học trực tuyến nổi tiếng với các video hướng dẫn cụ thể, chi tiết về cách tính toán và hiểu sâu hơn về các khái niệm hóa học cơ bản, bao gồm cả điện tích hạt nhân.
Bạn có thể truy cập các nguồn tài liệu này để tự học và thực hành các kiến thức về điện tích hạt nhân, từ đó nâng cao khả năng giải quyết các bài toán liên quan trong các kỳ thi hoặc nghiên cứu khoa học.