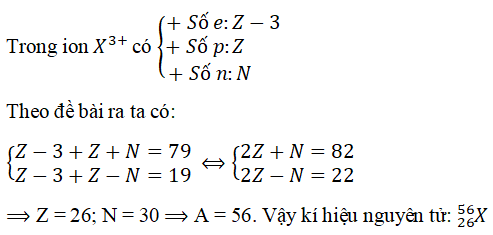Chủ đề số hiệu nguyên tử của các nguyên tố: Số hiệu nguyên tử của các nguyên tố là yếu tố quan trọng trong hóa học và vật lý. Bài viết này sẽ cung cấp cái nhìn toàn diện về số hiệu nguyên tử, từ khái niệm cơ bản đến các ứng dụng thực tiễn trong công nghiệp và nghiên cứu. Khám phá những thông tin chi tiết giúp bạn hiểu rõ hơn về các nguyên tố hóa học xung quanh chúng ta.
Mục lục
Số Hiệu Nguyên Tử Của Các Nguyên Tố Hóa Học
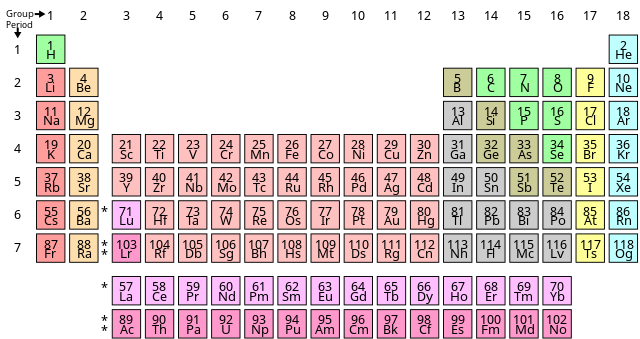
Số hiệu nguyên tử của một nguyên tố hóa học là một con số quan trọng thể hiện vị trí của nguyên tố đó trong bảng tuần hoàn, cũng như các đặc tính cơ bản của nguyên tử. Trong bài viết này, chúng ta sẽ khám phá các khía cạnh liên quan đến số hiệu nguyên tử, bao gồm cách đọc và ý nghĩa của nó.
1. Định Nghĩa Số Hiệu Nguyên Tử
Số hiệu nguyên tử, ký hiệu là \(Z\), là số lượng proton trong hạt nhân của một nguyên tử. Con số này cũng xác định số thứ tự của nguyên tố trong bảng tuần hoàn. Ví dụ, số hiệu nguyên tử của Hydro là 1, nghĩa là trong hạt nhân của nguyên tử Hydro có 1 proton.
2. Cách Đọc Số Hiệu Nguyên Tử Trong Bảng Tuần Hoàn
Mỗi nguyên tố trong bảng tuần hoàn được sắp xếp theo thứ tự tăng dần của số hiệu nguyên tử. Dựa vào vị trí này, ta có thể suy ra các đặc tính cơ bản của nguyên tố như:
- Số lượng proton: Bằng với số hiệu nguyên tử \(Z\).
- Số lượng electron: Trong nguyên tử trung hòa, số electron cũng bằng số hiệu nguyên tử \(Z\).
- Số lớp electron: Tăng dần khi đi từ trên xuống dưới trong một nhóm.
- Tính kim loại và phi kim: Tính kim loại tăng dần từ phải sang trái và từ trên xuống dưới trong bảng tuần hoàn, ngược lại với tính phi kim.
3. Ý Nghĩa Của Số Hiệu Nguyên Tử
Số hiệu nguyên tử không chỉ đơn thuần là một con số, mà còn mang ý nghĩa khoa học sâu sắc:
- Vị trí trong bảng tuần hoàn: Dựa vào số hiệu nguyên tử, ta có thể xác định vị trí của nguyên tố trong bảng tuần hoàn, từ đó suy ra các đặc tính hóa học cơ bản.
- Điện tích hạt nhân: Số hiệu nguyên tử bằng với điện tích hạt nhân, ảnh hưởng trực tiếp đến lực hút giữa hạt nhân và electron, từ đó quyết định các tính chất hóa học của nguyên tố.
- Sự sắp xếp electron: Số hiệu nguyên tử quyết định số lượng và cấu trúc lớp vỏ electron, ảnh hưởng đến cách nguyên tố tương tác với các nguyên tố khác.
4. Ví Dụ Về Số Hiệu Nguyên Tử
Hãy xem xét một vài ví dụ để hiểu rõ hơn về số hiệu nguyên tử và ý nghĩa của nó:
- Nguyên tố Natri (Na): Số hiệu nguyên tử của Na là 11. Điều này có nghĩa rằng Natri có 11 proton trong hạt nhân, và trong một nguyên tử trung hòa, nó cũng có 11 electron.
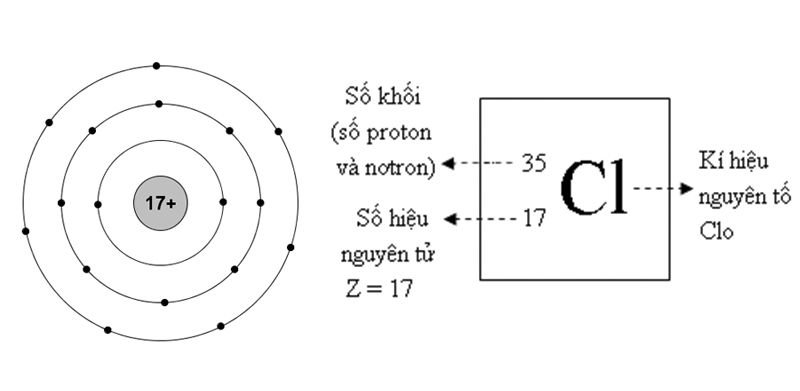
- Nguyên tố Clo (Cl): Số hiệu nguyên tử của Cl là 17, cho thấy Clo có 17 proton trong hạt nhân và cũng có 17 electron.
- Nguyên tố Uranium (U): Số hiệu nguyên tử của U là 92, điều này có nghĩa là Uranium có 92 proton và 92 electron trong một nguyên tử trung hòa.
5. Kết Luận
Số hiệu nguyên tử là một trong những khái niệm cơ bản nhất trong hóa học, cung cấp cái nhìn sâu sắc về cấu trúc và tính chất của các nguyên tố. Việc hiểu rõ số hiệu nguyên tử giúp chúng ta nắm bắt được các quy luật hoạt động hóa học và ứng dụng chúng trong nghiên cứu khoa học cũng như thực tiễn.
Để tìm hiểu thêm về bảng tuần hoàn và số hiệu nguyên tử của từng nguyên tố, bạn có thể tham khảo các nguồn tài liệu học tập hoặc công cụ tra cứu trực tuyến về hóa học.

1. Khái Niệm Về Số Hiệu Nguyên Tử
Số hiệu nguyên tử, hay còn gọi là số nguyên tử, là một đại lượng quan trọng trong hóa học và vật lý, biểu thị số proton có trong hạt nhân của một nguyên tử. Đây là một yếu tố cơ bản quyết định tính chất hóa học của nguyên tố đó.
Trong bảng tuần hoàn, các nguyên tố được sắp xếp theo thứ tự tăng dần của số hiệu nguyên tử. Ví dụ, nguyên tố Hydrogen có số hiệu nguyên tử là 1, trong khi Uranium có số hiệu nguyên tử là 92.
Công thức cơ bản để xác định số hiệu nguyên tử của một nguyên tố là:
Trong đó:
- \(Z\) là số hiệu nguyên tử
- \(p\) là số proton trong hạt nhân
Số hiệu nguyên tử không chỉ xác định vị trí của nguyên tố trong bảng tuần hoàn mà còn quyết định cấu trúc electron, ảnh hưởng đến khả năng phản ứng và liên kết hóa học của nguyên tố.
Ví dụ:
| Nguyên tố | Số hiệu nguyên tử |
| Hydrogen | 1 |
| Carbon | 6 |
| Oxygen | 8 |
Vì vậy, số hiệu nguyên tử là một khái niệm cơ bản giúp chúng ta hiểu rõ hơn về cấu trúc và tính chất của các nguyên tố trong tự nhiên.
2. Cách Tính Số Hiệu Nguyên Tử
Số hiệu nguyên tử, ký hiệu là \( Z \), là một đại lượng cơ bản trong hóa học và vật lý, đại diện cho số lượng proton có trong hạt nhân của một nguyên tử. Dưới đây là các bước chi tiết để tính số hiệu nguyên tử của một nguyên tố:
-
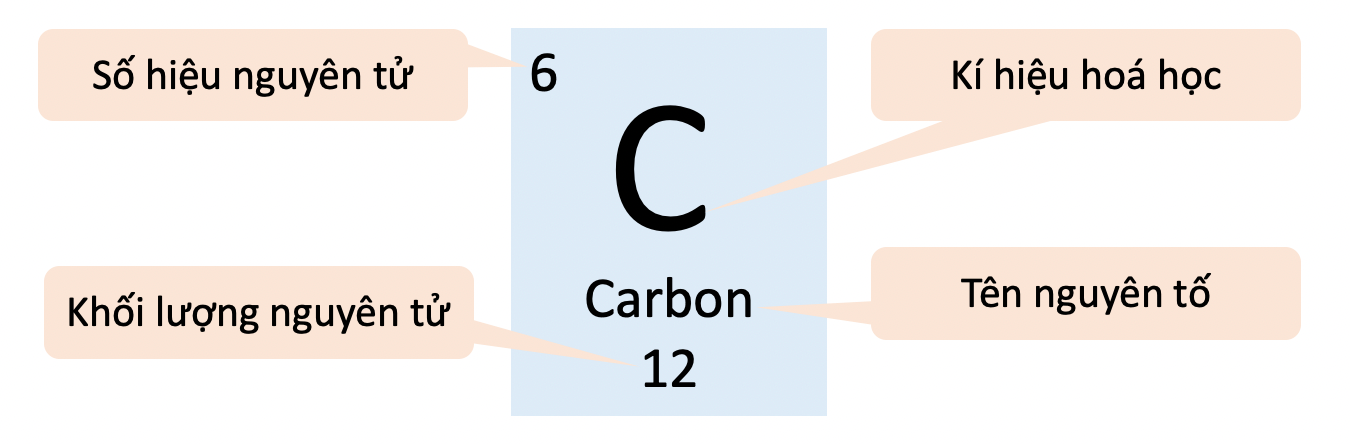
Xác định số proton: Số hiệu nguyên tử \( Z \) chính là số lượng proton trong hạt nhân của nguyên tử. Ví dụ, nguyên tố carbon có 6 proton, do đó số hiệu nguyên tử của carbon là \( Z = 6 \).
-
Tính số electron: Đối với một nguyên tử trung hòa về điện, số lượng electron cũng bằng số lượng proton, nghĩa là \( Z = \text{Số proton} = \text{Số electron} \).
-
Tính số neutron: Số neutron trong một nguyên tử có thể được xác định bằng công thức:
\[ N = A - Z \]
Trong đó \( A \) là số khối (tổng số proton và neutron), \( Z \) là số hiệu nguyên tử, và \( N \) là số neutron.
-
Xác định ion: Đối với ion, nếu nguyên tử mất hoặc nhận electron, số lượng electron sẽ thay đổi. Đối với ion dương (\( \text{cation} \)), số electron ít hơn số proton. Đối với ion âm (\( \text{anion} \)), số electron nhiều hơn số proton. Trong trường hợp này, số hiệu nguyên tử vẫn không thay đổi, nhưng tổng số hạt mang điện sẽ thay đổi.
Ví dụ minh họa:
| Nguyên tố | Số hiệu nguyên tử (Z) | Số khối (A) | Số neutron (N) |
|---|---|---|---|
| Carbon | 6 | 12 | 6 |
| Oxy | 8 | 16 | 8 |
| Uranium | 92 | 238 | 146 |

3. Các Phương Pháp Xác Định Số Hiệu Nguyên Tử
Số hiệu nguyên tử là một đại lượng cơ bản, đóng vai trò quan trọng trong việc xác định bản chất của nguyên tố hóa học. Có nhiều phương pháp khác nhau để xác định số hiệu nguyên tử \( Z \) của một nguyên tố, bao gồm các phương pháp thực nghiệm và lý thuyết. Dưới đây là các phương pháp phổ biến:
-
Phương pháp phổ khối lượng: Phổ khối lượng là một kỹ thuật phân tích sử dụng để đo khối lượng của các ion trong một mẫu. Dựa trên kết quả của phổ khối lượng, ta có thể xác định số proton, từ đó xác định số hiệu nguyên tử \( Z \).
-
Phương pháp X-quang: Sử dụng tia X chiếu qua một mẫu nguyên tử để phát hiện số proton trong hạt nhân. Mỗi nguyên tố có một đặc trưng phổ X-quang riêng, giúp xác định số hiệu nguyên tử của nguyên tố đó.
-
Phương pháp hóa học: Phản ứng hóa học của các nguyên tố có thể được sử dụng để xác định số proton thông qua các hợp chất và phản ứng tạo thành. Ví dụ, các tính chất hóa học như tính axit, bazơ, hoặc độ oxi hóa có thể liên quan trực tiếp đến số hiệu nguyên tử.
-
Phương pháp thực nghiệm trong phòng thí nghiệm: Xác định số hiệu nguyên tử qua thí nghiệm đo lường điện tích hạt nhân, hoặc sử dụng máy gia tốc hạt để xác định số proton trong hạt nhân.
Ví dụ, để xác định số hiệu nguyên tử của Carbon (\( Z = 6 \)) có thể sử dụng phổ khối lượng để đo khối lượng nguyên tử hoặc sử dụng phương pháp X-quang để xác định số proton trong hạt nhân.

4. Ứng Dụng Của Số Hiệu Nguyên Tử
Số hiệu nguyên tử là một đại lượng cơ bản quan trọng trong khoa học, có nhiều ứng dụng trong cả nghiên cứu và thực tiễn. Dưới đây là một số ứng dụng chính của số hiệu nguyên tử:
-
Xác định vị trí trong bảng tuần hoàn: Số hiệu nguyên tử \( Z \) của một nguyên tố giúp xác định vị trí của nó trong bảng tuần hoàn, từ đó suy ra các tính chất hóa học và vật lý của nguyên tố.
-
Ứng dụng trong y học: Một số đồng vị phóng xạ của các nguyên tố có số hiệu nguyên tử khác nhau được sử dụng trong chẩn đoán và điều trị bệnh. Ví dụ, \( ^{131}I \) được sử dụng trong điều trị bệnh tuyến giáp.
-
Nghiên cứu vật liệu: Số hiệu nguyên tử giúp các nhà khoa học hiểu rõ hơn về cấu trúc nguyên tử, liên kết hóa học, và tính chất vật liệu, từ đó phát triển các vật liệu mới với tính chất ưu việt.
-
Ứng dụng trong công nghiệp: Số hiệu nguyên tử của các nguyên tố được sử dụng để xác định thành phần nguyên liệu, chế tạo hợp kim, và trong các quy trình công nghiệp như sản xuất thép, nhôm.
-
Giáo dục và nghiên cứu: Hiểu biết về số hiệu nguyên tử là nền tảng trong giáo dục hóa học, vật lý, và các ngành khoa học liên quan, giúp học sinh và sinh viên tiếp cận kiến thức một cách hệ thống và khoa học.
Ví dụ, nhờ việc hiểu rõ số hiệu nguyên tử của Oxy (\( Z = 8 \)), các nhà khoa học đã có thể giải thích được vai trò quan trọng của nó trong các phản ứng hóa học và trong quá trình hô hấp của sinh vật.

5. Tổng Hợp Danh Sách Số Hiệu Nguyên Tử Các Nguyên Tố
Dưới đây là danh sách tổng hợp các nguyên tố hóa học cùng với số hiệu nguyên tử tương ứng của chúng. Danh sách này được sắp xếp theo thứ tự tăng dần của số hiệu nguyên tử, giúp bạn dễ dàng tra cứu và học tập.
| Nguyên Tố | Ký Hiệu Hóa Học | Số Hiệu Nguyên Tử |
|---|---|---|
| Hydro | H | \( Z = 1 \) |
| Helium | He | \( Z = 2 \) |
| Lithium | Li | \( Z = 3 \) |
| Berylium | Be | \( Z = 4 \) |
| Boron | B | \( Z = 5 \) |
| Carbon | C | \( Z = 6 \) |
| Nitrogen | N | \( Z = 7 \) |
| Oxygen | O | \( Z = 8 \) |
| Fluorine | F | \( Z = 9 \) |
| Neon | Ne | \( Z = 10 \) |
Danh sách trên chỉ là một phần trong toàn bộ bảng tuần hoàn các nguyên tố. Số hiệu nguyên tử không chỉ xác định vị trí của nguyên tố mà còn phản ánh tính chất hóa học đặc trưng của nó.
XEM THÊM:
6. Tổng Kết Và Dự Đoán Nghiên Cứu Tương Lai
Số hiệu nguyên tử là một yếu tố cơ bản, đóng vai trò quan trọng trong việc xác định các tính chất hóa học của nguyên tố. Qua việc hiểu rõ về số hiệu nguyên tử, chúng ta có thể dự đoán và khai thác nhiều khía cạnh khoa học mới, từ việc tạo ra các vật liệu mới cho đến khám phá các phản ứng hóa học tiên tiến.
Trong tương lai, các nhà nghiên cứu sẽ tiếp tục khám phá các nguyên tố mới và những tính chất chưa biết của các nguyên tố đã được xác định. Đặc biệt, các nghiên cứu về các nguyên tố siêu nặng và các nguyên tố ngoài bảng tuần hoàn hiện nay có thể mở ra nhiều ứng dụng mới trong công nghệ và y học.
- Phát triển vật liệu mới với tính năng vượt trội.
- Khám phá và tổng hợp các nguyên tố mới, mở rộng bảng tuần hoàn.
- Ứng dụng trong công nghệ nano và y học tiên tiến.
Những nghiên cứu này không chỉ góp phần làm rõ hơn về thế giới vi mô của các nguyên tử mà còn giúp chúng ta ứng dụng hiệu quả hơn trong các lĩnh vực đời sống và công nghiệp.