Chủ đề nhiệt dung riêng của sắt: Nhiệt dung riêng của sắt là một đại lượng vật lý quan trọng, giúp chúng ta hiểu rõ hơn về khả năng hấp thụ nhiệt của sắt. Trong bài viết này, chúng ta sẽ khám phá các đặc tính nổi bật và ứng dụng thực tiễn của sắt trong đời sống và công nghiệp, mang đến cái nhìn sâu sắc và toàn diện về kim loại này.
Mục lục
Nhiệt Dung Riêng Của Sắt
Nhiệt dung riêng là một đại lượng vật lý quan trọng, thể hiện khả năng hấp thụ nhiệt của một vật liệu. Đối với sắt, một kim loại phổ biến và quan trọng trong nhiều ngành công nghiệp, việc hiểu rõ về nhiệt dung riêng của nó là rất cần thiết.
Giá Trị Nhiệt Dung Riêng Của Sắt
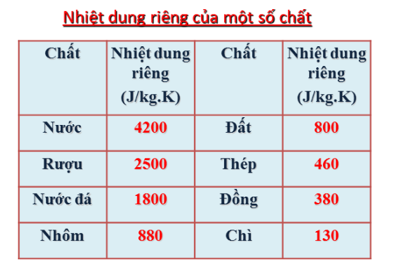
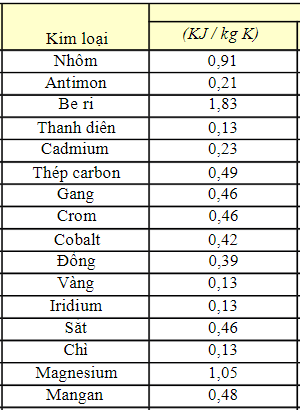
Sắt có nhiệt dung riêng là
Công Thức Tính Nhiệt Dung Riêng
Nhiệt dung riêng được tính theo công thức:
Q : Nhiệt lượng (J)m : Khối lượng vật (kg)c : Nhiệt dung riêng (J/kg.K)\Delta T : Độ tăng nhiệt độ (K hoặc °C)
Tầm Quan Trọng Của Nhiệt Dung Riêng Của Sắt
Nhiệt dung riêng của sắt có ý nghĩa quan trọng trong nhiều ứng dụng thực tế như:
- Trong công nghiệp, sắt được sử dụng để sản xuất các bộ phận máy móc, vì khả năng giữ nhiệt của nó thấp, giúp các bộ phận nhanh chóng đạt đến nhiệt độ làm việc mà không cần quá nhiều năng lượng.
- Trong xây dựng, các cấu trúc bằng sắt như cầu, nhà xưởng cần được thiết kế để chịu được sự thay đổi nhiệt độ, và nhiệt dung riêng của sắt đóng vai trò quan trọng trong các tính toán này.
- Trong lĩnh vực y học, sắt được sử dụng trong các thiết bị và dụng cụ y tế nhờ vào khả năng chống oxy hóa và độ bền cao, cùng với nhiệt dung riêng ổn định giúp các thiết bị không bị quá nhiệt khi sử dụng trong môi trường nhiệt độ cao.
Ứng Dụng Thực Tế Của Sắt
Sắt là một trong những kim loại được sử dụng nhiều nhất trong đời sống hàng ngày và công nghiệp, với ứng dụng từ sản xuất ô tô, máy bay, đến các công trình xây dựng và đồ dùng gia đình.
| Ứng Dụng | Ví Dụ |
| Sản xuất công nghiệp | Khung xe ô tô, tàu thuyền, máy bay |
| Xây dựng | Cầu, nhà xưởng, khung nhà |
| Đồ dùng gia đình | Dao, kéo, bếp |
| Y tế | Thiết bị phẫu thuật, giường bệnh |
Nhờ những đặc điểm vượt trội về mặt cơ học và nhiệt học, sắt đã trở thành một vật liệu không thể thiếu trong nhiều lĩnh vực, từ đời sống đến công nghiệp và y tế.
Tổng Quan Về Nhiệt Dung Riêng
Nhiệt dung riêng là một đại lượng vật lý quan trọng, được định nghĩa là lượng nhiệt cần thiết để làm tăng nhiệt độ của một đơn vị khối lượng của chất đó lên một đơn vị nhiệt độ. Nhiệt dung riêng thường được ký hiệu là c và đơn vị đo lường thường là J/kg·K.
Nhiệt dung riêng của một chất phụ thuộc vào cấu trúc vật lý và hóa học của chất đó, cũng như điều kiện môi trường như áp suất và nhiệt độ. Cụ thể:
- Cấu trúc nguyên tử: Các nguyên tử có cấu trúc khác nhau sẽ có nhiệt dung riêng khác nhau do khả năng rung động và quay của chúng.
- Liên kết hóa học: Các loại liên kết trong vật chất cũng ảnh hưởng đến lượng nhiệt cần thiết để tăng nhiệt độ.
- Trạng thái vật chất: Nhiệt dung riêng của chất rắn, lỏng và khí sẽ khác nhau đáng kể.
Nhiệt dung riêng không chỉ giúp ta hiểu rõ hơn về cách một vật liệu phản ứng với nhiệt mà còn có ứng dụng rộng rãi trong nhiều lĩnh vực như công nghệ vật liệu, cơ khí, và nhiệt động lực học. Đặc biệt, đối với sắt, một kim loại được sử dụng phổ biến trong công nghiệp, nhiệt dung riêng là thông số quan trọng trong thiết kế và vận hành các hệ thống nhiệt.
Công thức tính nhiệt dung riêng có dạng:
\[
c = \frac{Q}{m \Delta T}
\]
Trong đó:
- Q: Lượng nhiệt cần cung cấp (J)
- m: Khối lượng của vật liệu (kg)
- \Delta T: Độ thay đổi nhiệt độ (K)
Nhiệt Dung Riêng Của Sắt
Sắt là một kim loại phổ biến với nhiều ứng dụng trong công nghiệp và đời sống hàng ngày. Nhiệt dung riêng của sắt là một trong những đặc tính quan trọng, ảnh hưởng đến khả năng hấp thụ và truyền nhiệt của kim loại này.
Nhiệt dung riêng của sắt ở nhiệt độ phòng (25°C) thường có giá trị khoảng 450 J/kg·K. Điều này có nghĩa là để tăng nhiệt độ của 1 kg sắt lên 1°C, cần cung cấp 450 joules năng lượng.
Các yếu tố ảnh hưởng đến nhiệt dung riêng của sắt bao gồm:
- Nhiệt độ: Nhiệt dung riêng của sắt có thể thay đổi theo nhiệt độ. Khi nhiệt độ tăng, các phân tử trong sắt dao động mạnh hơn, dẫn đến thay đổi trong nhiệt dung riêng.
- Cấu trúc tinh thể: Sắt có thể tồn tại ở nhiều dạng thù hình (như α-Fe, γ-Fe), và mỗi dạng có nhiệt dung riêng khác nhau.
- Trạng thái vật lý: Sắt ở trạng thái rắn và trạng thái lỏng có nhiệt dung riêng khác nhau, với sắt lỏng có nhiệt dung riêng cao hơn do sự tự do di chuyển của các nguyên tử.
Ứng dụng của nhiệt dung riêng của sắt rất đa dạng, đặc biệt trong lĩnh vực luyện kim và cơ khí. Việc biết rõ nhiệt dung riêng của sắt giúp các kỹ sư thiết kế hệ thống nhiệt hiệu quả, từ đó tối ưu hóa quá trình sản xuất và tiết kiệm năng lượng.
Công thức liên quan đến nhiệt dung riêng của sắt có thể được biểu diễn như sau:
\[
Q = mc\Delta T
\]
Trong đó:
- Q: Lượng nhiệt cần cung cấp (J)
- m: Khối lượng của sắt (kg)
- c: Nhiệt dung riêng của sắt (J/kg·K)
- \Delta T: Độ thay đổi nhiệt độ (K)
Hiểu rõ nhiệt dung riêng của sắt là nền tảng để ứng dụng hiệu quả kim loại này trong nhiều lĩnh vực khác nhau, từ sản xuất công nghiệp đến đời sống hàng ngày.

Ứng Dụng Của Sắt Trong Đời Sống Và Công Nghiệp
Sắt là một kim loại thiết yếu với nhiều ứng dụng rộng rãi trong đời sống và công nghiệp, đóng vai trò quan trọng trong sự phát triển kinh tế và công nghệ của con người.
1. Ứng dụng trong xây dựng và cơ khí:
- Kết cấu xây dựng: Sắt và thép (hợp kim của sắt) được sử dụng làm khung kết cấu cho các tòa nhà, cầu, và các công trình hạ tầng khác. Với tính chất cứng và bền, sắt giúp tăng cường sự ổn định và an toàn cho các công trình.
- Gia công cơ khí: Sắt là nguyên liệu chính trong sản xuất máy móc, công cụ và thiết bị cơ khí. Tính dẻo và dễ dàng gia công của sắt giúp tạo ra các chi tiết máy có độ chính xác cao.
2. Ứng dụng trong giao thông vận tải:
- Sản xuất ô tô và phương tiện giao thông: Sắt là vật liệu chủ yếu trong sản xuất khung xe, động cơ, và các bộ phận khác của ô tô, tàu hỏa, tàu biển, và máy bay. Tính bền và khả năng chịu lực của sắt giúp phương tiện hoạt động an toàn và bền bỉ.
- Đường sắt: Sắt được sử dụng để chế tạo đường ray, tạo điều kiện cho các phương tiện di chuyển mượt mà và an toàn.
3. Ứng dụng trong đời sống hàng ngày:
- Dụng cụ nhà bếp: Sắt và thép không gỉ được sử dụng để chế tạo các dụng cụ nhà bếp như nồi, chảo, dao kéo, đảm bảo độ bền và vệ sinh an toàn thực phẩm.
- Nội thất và đồ gia dụng: Sắt cũng được sử dụng trong sản xuất nội thất như giường, bàn ghế, và các thiết bị gia dụng, mang lại sự chắc chắn và tuổi thọ cao cho sản phẩm.
4. Ứng dụng trong công nghiệp năng lượng:
- Đường ống dẫn dầu và khí: Sắt là nguyên liệu chính trong sản xuất các đường ống dẫn dầu và khí, chịu được áp lực và các điều kiện môi trường khắc nghiệt.
- Máy phát điện: Sắt được sử dụng trong lõi của các máy phát điện, giúp tạo ra từ trường mạnh mẽ để chuyển đổi năng lượng cơ học thành năng lượng điện.
Sắt không chỉ là một kim loại quan trọng trong sản xuất công nghiệp mà còn đóng vai trò thiết yếu trong việc cải thiện chất lượng cuộc sống của con người. Từ các công trình xây dựng cho đến các thiết bị gia dụng, sắt luôn hiện diện xung quanh chúng ta, góp phần vào sự phát triển bền vững và thịnh vượng.
Các Tính Chất Vật Lý Và Hóa Học Của Sắt
Sắt (Fe) là một trong những kim loại phổ biến và quan trọng nhất trong đời sống cũng như trong các ngành công nghiệp. Dưới đây là một số tính chất vật lý và hóa học đặc trưng của sắt:
Tính Chất Vật Lý
- Màu sắc: Sắt có màu trắng bạc, nhưng nhanh chóng bị oxy hóa khi tiếp xúc với không khí, tạo thành lớp màng oxit sắt màu nâu đỏ trên bề mặt.
- Khối lượng riêng: Sắt có khối lượng riêng khoảng 7.87 g/cm3.
- Độ cứng: Sắt có độ cứng trung bình trên thang Mohs, khoảng 4-5, đủ để làm các công cụ và thiết bị.
- Nhiệt độ nóng chảy: Sắt có nhiệt độ nóng chảy cao, khoảng 1538°C, khiến nó thích hợp cho các ứng dụng yêu cầu độ bền nhiệt.
- Tính dẫn điện và nhiệt: Sắt là chất dẫn điện và dẫn nhiệt tốt, thường được sử dụng trong các ứng dụng liên quan đến truyền tải điện và nhiệt.
Tính Chất Hóa Học
- Phản ứng với oxy: Khi tiếp xúc với không khí ẩm, sắt bị oxy hóa, tạo thành gỉ sắt (Fe2O3.nH2O). Quá trình này là một trong những nguyên nhân chính gây hư hỏng các cấu trúc bằng sắt.
- Phản ứng với axit: Sắt phản ứng mạnh với các axit như HCl để tạo ra muối sắt(II) và khí hydro (H2).
- Hợp kim hóa: Sắt có thể tạo hợp kim với nhiều kim loại khác như carbon (để tạo ra thép), crom, niken,... để tăng cường các tính chất cơ học và chống ăn mòn.
- Tác dụng với nước: Sắt ở nhiệt độ cao có thể phản ứng với nước để tạo ra sắt oxit (Fe3O4) và khí hydro.
Các tính chất vật lý và hóa học của sắt giúp nó trở thành một kim loại đa dụng, được ứng dụng rộng rãi trong nhiều lĩnh vực, từ xây dựng, sản xuất công cụ đến công nghệ cao.

Một Số Hợp Chất Quan Trọng Của Sắt
Sắt là một nguyên tố có khả năng tạo ra nhiều hợp chất quan trọng, có ứng dụng rộng rãi trong các lĩnh vực công nghiệp và đời sống hàng ngày. Dưới đây là một số hợp chất nổi bật của sắt:
- Oxit sắt (FeO, Fe2O3, Fe3O4): Các oxit sắt là những hợp chất phổ biến nhất của sắt, được sử dụng trong nhiều ứng dụng khác nhau như sản xuất thép, chất màu (pigment), và trong các ngành công nghiệp hóa chất. Fe2O3 là thành phần chính trong gỉ sét, trong khi Fe3O4 thường được sử dụng làm nguyên liệu cho nam châm.
- Sắt sunfat (FeSO4): Đây là một muối của sắt được sử dụng phổ biến trong điều trị thiếu máu do thiếu sắt. Ngoài ra, FeSO4 còn được sử dụng trong công nghiệp để xử lý nước, và làm chất keo tụ trong quá trình làm sạch nước.
- Sắt clorua (FeCl3): FeCl3 là một hợp chất có tính chất hút ẩm mạnh, thường được sử dụng trong công nghiệp xử lý nước, làm chất đông tụ để loại bỏ các tạp chất, và trong sản xuất bảng mạch điện tử.
- Ferrocyanide (K4Fe(CN)6): Đây là một hợp chất được sử dụng trong công nghiệp sản xuất thuốc nhuộm, trong ngành in ấn và làm chất chống đông cứng trong thực phẩm.
- Sắt oxalat (FeC2O4): Hợp chất này thường được sử dụng trong phòng thí nghiệm, đặc biệt là trong các thí nghiệm hóa học phân tích.
Các hợp chất của sắt đóng vai trò quan trọng không chỉ trong các ứng dụng công nghiệp mà còn trong các lĩnh vực như y tế, xử lý nước và sản xuất thực phẩm. Khả năng tạo ra nhiều loại hợp chất khác nhau giúp sắt trở thành một nguyên tố cực kỳ quan trọng và đa dụng trong cuộc sống.
XEM THÊM:
Các Phương Pháp Điều Chế Sắt
Điều chế sắt là quá trình quan trọng trong công nghiệp và cuộc sống hàng ngày. Dưới đây là các phương pháp chính để điều chế sắt:
1. Phương Pháp Nhiệt Luyện
Phương pháp nhiệt luyện là kỹ thuật cổ điển và phổ biến nhất để điều chế sắt từ quặng. Quá trình này bao gồm các bước sau:
- Khử quặng sắt: Quặng sắt (chủ yếu là Fe₂O₃ hoặc Fe₃O₄) được trộn với than cốc và đá vôi trong lò cao. Than cốc đốt cháy sinh ra nhiệt và khí CO, đóng vai trò là chất khử, biến oxit sắt thành sắt lỏng.
- Lọc xỉ: Đá vôi tác dụng với các tạp chất trong quặng để tạo thành xỉ, giúp tách sắt khỏi các tạp chất.
- Thu sắt lỏng: Sắt lỏng được thu thập tại đáy lò và có thể được đúc thành thỏi hoặc chuyển vào các quy trình xử lý tiếp theo.
2. Quy Trình Luyện Sắt Trong Công Nghiệp
Quá trình luyện sắt trong công nghiệp hiện đại đã được cải tiến để đạt hiệu suất cao và chất lượng sản phẩm tốt hơn. Các bước chính bao gồm:
- Luyện sắt bằng lò cao: Quặng sắt, than cốc và chất trợ dung (như đá vôi) được nạp vào lò cao, nơi quá trình khử oxit sắt diễn ra.
- Luyện sắt bằng lò hồ quang điện: Sử dụng điện năng để tạo ra nhiệt độ cao, khử quặng sắt thành sắt lỏng, phương pháp này giúp kiểm soát tốt hơn lượng tạp chất và tiết kiệm năng lượng.
- Luyện sắt bằng phương pháp hoàn nguyên trực tiếp: Quặng sắt được khử trực tiếp thành sắt rắn mà không cần qua giai đoạn nấu chảy, phương pháp này thường áp dụng trong các nhà máy nhỏ với sản lượng thấp.
Các phương pháp trên không chỉ giúp sản xuất sắt hiệu quả mà còn giảm thiểu tác động môi trường, góp phần phát triển bền vững trong ngành công nghiệp luyện kim.

Lợi Ích Và Ảnh Hưởng Của Sắt Đối Với Sức Khỏe
Sắt là một trong những khoáng chất quan trọng và thiết yếu cho cơ thể con người. Nó không chỉ đóng vai trò quan trọng trong quá trình hình thành hồng cầu mà còn tham gia vào nhiều chức năng sinh lý quan trọng khác. Dưới đây là những lợi ích và ảnh hưởng của sắt đối với sức khỏe:
Lợi Ích Của Sắt Đối Với Cơ Thể Người
- Tham gia vào quá trình tạo hồng cầu: Sắt là thành phần chính của hemoglobin, một loại protein trong hồng cầu có nhiệm vụ vận chuyển oxy từ phổi đến các tế bào trong cơ thể. Thiếu sắt có thể dẫn đến thiếu máu, khiến cơ thể mệt mỏi, suy nhược.
- Hỗ trợ chức năng hệ miễn dịch: Sắt giúp tăng cường hệ thống miễn dịch, giúp cơ thể chống lại các bệnh nhiễm trùng. Sắt cung cấp năng lượng cho các tế bào miễn dịch để thực hiện chức năng bảo vệ cơ thể.
- Tăng cường sự phát triển của cơ bắp: Myoglobin, một protein có trong cơ bắp, cũng chứa sắt và chịu trách nhiệm cho việc lưu trữ và sử dụng oxy trong cơ bắp. Điều này rất quan trọng đối với sự phát triển và chức năng của cơ bắp.
- Cải thiện chức năng não bộ: Sắt là yếu tố quan trọng trong việc duy trì chức năng nhận thức và sự tập trung. Thiếu sắt có thể gây ra các vấn đề về nhận thức và giảm hiệu suất làm việc.
Những Ảnh Hưởng Tiêu Cực Khi Thiếu Hoặc Thừa Sắt
- Thiếu sắt: Khi cơ thể thiếu sắt, tình trạng thiếu máu có thể xảy ra, gây ra các triệu chứng như mệt mỏi, da xanh xao, khó thở và đau đầu. Trẻ em thiếu sắt có thể bị chậm phát triển, suy giảm trí nhớ và khó tập trung.
- Thừa sắt: Dù sắt rất quan trọng, nhưng việc thừa sắt cũng có thể gây hại. Quá nhiều sắt trong cơ thể có thể dẫn đến tình trạng nhiễm độc sắt, gây tổn thương gan, tim và thậm chí là bệnh tiểu đường.
Như vậy, việc duy trì mức sắt cân đối trong cơ thể là rất quan trọng. Bạn nên bổ sung sắt thông qua chế độ ăn uống giàu sắt như thịt đỏ, rau xanh đậm và các loại đậu, đồng thời kiểm soát lượng sắt để tránh các vấn đề sức khỏe tiềm ẩn.