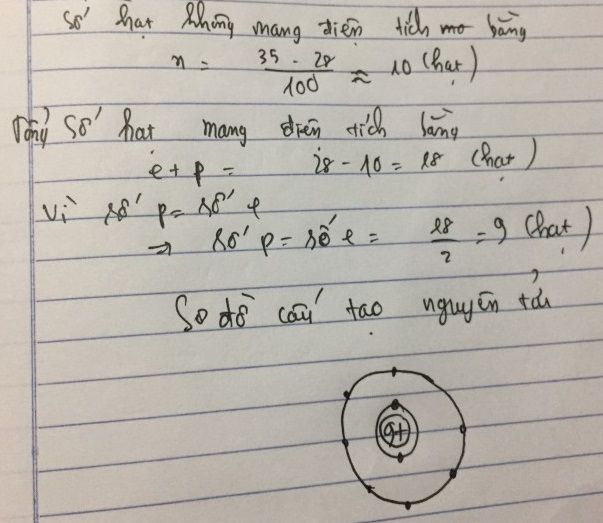Chủ đề nguyên tử z có tổng số hạt bằng 58: Nguyên tử Z có tổng số hạt bằng 58 là chủ đề quan trọng trong lĩnh vực hóa học, giúp ta hiểu rõ hơn về cấu trúc nguyên tử và vai trò của chúng trong các phản ứng hóa học. Bài viết này sẽ khám phá chi tiết về số lượng proton, neutron và electron, cũng như ứng dụng của nguyên tử Z trong đời sống.
Mục lục
Thông Tin Về Nguyên Tử Z Có Tổng Số Hạt Bằng 58
Trong lĩnh vực hóa học, việc xác định tổng số hạt trong nguyên tử Z có thể là một phần quan trọng trong việc hiểu cấu trúc nguyên tử. Dưới đây là các thông tin chi tiết về nguyên tử Z có tổng số hạt là 58.
1. Cấu Trúc Nguyên Tử Z
Nguyên tử Z có tổng số hạt bằng 58, bao gồm số proton (\(p\)), số neutron (\(n\)), và số electron (\(e\)). Ta có hệ phương trình:
\[
p + e + n = 58
\]
Vì số proton bằng số electron trong nguyên tử trung hòa điện, ta có:
\[
p = e
\]
Từ đó, ta có thể suy ra giá trị của các hạt:
\[
p + n + p = 58 \quad \Rightarrow \quad 2p + n = 58
\]
Giả sử \(p = 19\), ta sẽ tính được:
\[
n = 58 - 2p = 58 - 38 = 20
\]
Như vậy, nguyên tử Z có 19 proton, 19 electron và 20 neutron.
2. Ứng Dụng Trong Hóa Học
Nguyên tử Z với số proton là 19 tương ứng với nguyên tố Kali (K). Đây là một nguyên tố quan trọng trong bảng tuần hoàn, với vai trò thiết yếu trong nhiều phản ứng hóa học và ứng dụng trong công nghiệp, nông nghiệp.
3. Cấu Hình Electron
Cấu hình electron của nguyên tử Z (Kali) với \(Z = 19\) là:
\[
1s^2 2s^2 2p^6 3s^2 3p^6 4s^1
\]
Electron ngoài cùng của nguyên tử này nằm ở phân lớp \(4s\), điều này giải thích tính chất hóa học của Kali, bao gồm khả năng dễ dàng mất một electron để tạo thành ion \(K^+\).
4. Kết Luận
Thông qua việc phân tích cấu trúc của nguyên tử Z có tổng số hạt là 58, chúng ta hiểu rõ hơn về cấu tạo, tính chất và vai trò của nguyên tố này trong hóa học. Kali không chỉ quan trọng trong các phản ứng hóa học mà còn có nhiều ứng dụng thực tế trong đời sống và công nghiệp.
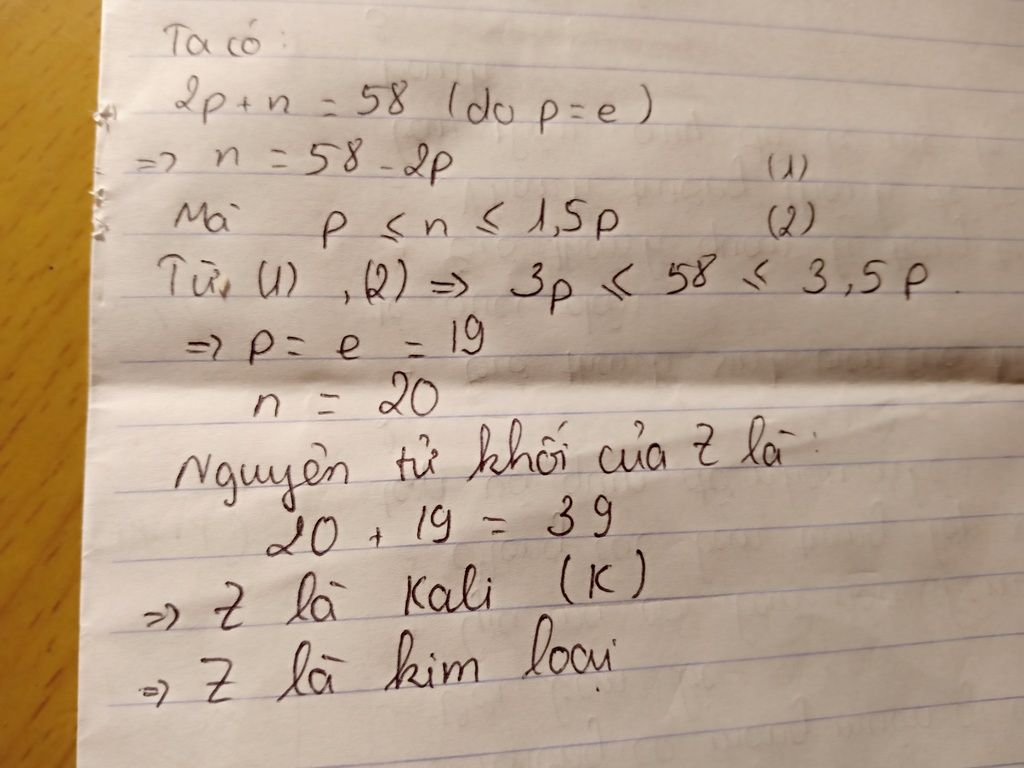
1. Tổng Quan Về Cấu Trúc Nguyên Tử Z
Nguyên tử Z là một thành phần cơ bản của vật chất, với tổng số hạt bằng 58. Để hiểu rõ cấu trúc của nguyên tử này, chúng ta cần phân tích các thành phần cơ bản của nó: proton, neutron và electron.
Trong nguyên tử, số hạt bao gồm:
- Proton (\(p\)): Các hạt mang điện tích dương, nằm trong hạt nhân nguyên tử.
- Neutron (\(n\)): Các hạt không mang điện, cũng nằm trong hạt nhân nguyên tử.
- Electron (\(e\)): Các hạt mang điện tích âm, chuyển động xung quanh hạt nhân trong các lớp vỏ electron.
Tổng số hạt trong nguyên tử Z được tính bằng công thức:
\[
Tổng \ số \ hạt \ = p + n + e
\]
Vì trong nguyên tử trung hòa, số proton bằng số electron (\(p = e\)), ta có thể viết lại phương trình trên như sau:
\[
Tổng \ số \ hạt = 2p + n = 58
\]
Điều này cho thấy, để xác định số lượng các hạt trong nguyên tử Z, chúng ta cần biết số proton và neutron.
Ví dụ, nếu số proton \(p\) là 19, thì số neutron \(n\) sẽ là:
\[
n = 58 - 2p = 58 - 38 = 20
\]
Do đó, nguyên tử Z sẽ có cấu trúc bao gồm 19 proton, 19 electron, và 20 neutron. Đây là cấu trúc của nguyên tử Kali (K), một nguyên tố quan trọng trong bảng tuần hoàn.
Cấu trúc này đóng vai trò quan trọng trong việc xác định tính chất hóa học và phản ứng của nguyên tố Z trong các ứng dụng thực tế và trong nghiên cứu khoa học.
2. Phân Tích Cấu Hình Electron Của Nguyên Tử Z
Cấu hình electron của nguyên tử Z, với tổng số hạt bằng 58, là một yếu tố quan trọng để xác định tính chất hóa học và khả năng phản ứng của nguyên tố này. Để phân tích cấu hình electron, chúng ta cần thực hiện các bước sau:
- Xác định số electron: Vì nguyên tử Z có tổng số hạt bằng 58, bao gồm proton, neutron và electron, và nguyên tử trung hòa về điện tích, số electron sẽ bằng số proton.
- Xác định số lớp vỏ electron: Số lớp vỏ electron được xác định dựa trên mức năng lượng chính (n). Mỗi lớp vỏ electron có thể chứa một số lượng tối đa electron theo công thức \(2n^2\).
- Xác định cấu hình electron: Cấu hình electron được viết theo thứ tự các mức năng lượng từ thấp đến cao, tuân theo quy tắc Hund và nguyên lý Pauli. Cấu hình electron thường được viết dưới dạng: \[ 1s^2 2s^2 2p^6 3s^2 3p^6 4s^2 3d^{10} 4p^6 5s^2 4d^{10} 5p^6 \]
Ví dụ, nếu nguyên tử Z có số proton bằng 30, cấu hình electron sẽ là:
\[
1s^2 2s^2 2p^6 3s^2 3p^6 4s^2 3d^{10}
\]
Cấu hình này cho thấy nguyên tử Z có 4 lớp vỏ electron, với các electron được sắp xếp sao cho năng lượng của hệ thống là thấp nhất. Sự sắp xếp này ảnh hưởng lớn đến tính chất hóa học của nguyên tử Z, như độ âm điện, năng lượng ion hóa, và bán kính nguyên tử.
Việc hiểu rõ cấu hình electron của nguyên tử giúp ta dự đoán được hành vi hóa học của nguyên tố trong các phản ứng hóa học, cũng như trong việc tạo liên kết hóa học với các nguyên tử khác.

3. Tầm Quan Trọng Của Nguyên Tử Z Trong Hóa Học
Nguyên tử Z, với tổng số hạt bằng 58, đóng vai trò quan trọng trong hóa học nhờ các đặc tính độc đáo của nó. Các nguyên tử này có cấu hình electron đặc biệt, ảnh hưởng đến tính chất hóa học và các phản ứng hóa học của chúng.
3.1. Vai Trò Của Nguyên Tử Z Trong Các Phản Ứng Hóa Học
Nguyên tử Z có thể tham gia vào nhiều phản ứng hóa học quan trọng nhờ vào cấu hình electron của nó. Cấu hình này cho phép nguyên tử Z:
- Dễ dàng mất hoặc nhận electron trong quá trình tạo liên kết hóa học.
- Tham gia vào các phản ứng oxi hóa - khử, nơi nguyên tử Z có thể đóng vai trò là chất khử hoặc chất oxi hóa.
- Hình thành các hợp chất có tính chất đặc biệt, chẳng hạn như hợp chất hữu cơ hoặc hợp chất vô cơ với những đặc tính đáng chú ý như độ bền, độ cứng, hoặc tính dẫn điện.
Điều này khiến cho nguyên tử Z trở thành một yếu tố không thể thiếu trong các nghiên cứu và ứng dụng hóa học hiện đại.
3.2. Ứng Dụng Của Nguyên Tử Z Trong Công Nghiệp và Nông Nghiệp
Nguyên tử Z không chỉ quan trọng trong lĩnh vực hóa học cơ bản mà còn có nhiều ứng dụng thực tiễn trong công nghiệp và nông nghiệp:
- Công nghiệp: Nguyên tử Z được sử dụng trong sản xuất các hợp kim đặc biệt có độ bền cao, chống ăn mòn, và chịu nhiệt tốt, phù hợp cho các ngành công nghiệp hàng không, ô tô, và xây dựng.
- Nông nghiệp: Một số hợp chất chứa nguyên tử Z được sử dụng làm phân bón hóa học hoặc thuốc bảo vệ thực vật, giúp tăng năng suất và chất lượng cây trồng.
- Nghiên cứu và phát triển: Nguyên tử Z được sử dụng trong các phòng thí nghiệm để nghiên cứu các tính chất hóa học cơ bản, góp phần vào sự phát triển của khoa học vật liệu và công nghệ nano.
Với những ứng dụng rộng rãi như vậy, nguyên tử Z đang góp phần quan trọng vào sự phát triển bền vững của nhiều ngành công nghiệp và nông nghiệp trên toàn thế giới.

4. Bài Tập Và Ứng Dụng Thực Tiễn
Trong phần này, chúng ta sẽ thực hiện một bài tập liên quan đến nguyên tử có tổng số hạt bằng 58. Bài tập này giúp củng cố kiến thức về cách xác định số lượng proton, neutron và electron trong nguyên tử, cũng như cách tính toán nguyên tử khối dựa trên các thông tin đã cho.
Bài tập:
- Một nguyên tử X có tổng số hạt proton (p), neutron (n), và electron (e) bằng 58. Biết rằng nguyên tử khối của X nhỏ hơn 40. Xác định số hạt mỗi loại trong nguyên tử X và tên của nguyên tố này.
Lời giải:
Để giải quyết bài tập này, ta sử dụng các thông tin đã cho:
- Tổng số hạt của nguyên tử X là 58, tức là \( p + n + e = 58 \).
- Trong một nguyên tử trung hòa, số proton bằng số electron, do đó \( p = e \). Gọi \( p = e = Z \), ta có: \[ Z + n + Z = 58 \implies 2Z + n = 58. \]
- Nguyên tử khối A của X nhỏ hơn 40, mà \( A = Z + n \), do đó: \[ Z + n < 40. \]
Kết hợp các phương trình trên, ta có hệ phương trình:
Giải hệ phương trình này, ta tìm được:
Thay vào phương trình \( Z + n < 40 \):
Mặt khác, do \( Z \leq n \leq 1.5Z \), ta có:
Giải bất phương trình, ta tìm được:
Do Z là số nguyên, ta có thể chọn \( Z = 19 \). Khi đó:
- \( Z = 19 \), vậy \( p = e = 19 \).
- \( n = 58 - 2 \times 19 = 20 \).
Suy ra, nguyên tố hóa học X là Kali (K) với số proton \( p = 19 \), số neutron \( n = 20 \), và nguyên tử khối \( A = 39 \).
Ứng dụng thực tiễn:
- Hiểu biết về cấu tạo nguyên tử giúp chúng ta xác định được tính chất hóa học của các nguyên tố.
- Biết cách tính toán số lượng hạt giúp dự đoán phản ứng hóa học và ứng dụng trong nghiên cứu khoa học.
Bài tập này là một ví dụ điển hình cho việc ứng dụng kiến thức hóa học cơ bản vào thực tế.

5. Kết Luận
Từ những phân tích trên, chúng ta có thể thấy rằng việc xác định nguyên tử Z với tổng số hạt bằng 58 và nguyên tử khối nhỏ hơn 40 yêu cầu một số phép tính hóa học cụ thể. Dựa vào các giả thiết và phương trình đã được đề xuất, chúng ta có thể tính toán để xác định nguyên tố hóa học mà Z đại diện.
Trong trường hợp này, chúng ta đã sử dụng các phương trình liên quan đến số hạt proton (\(p\)), neutron (\(n\)), và electron (\(e\)). Được biết:
- \(p + e + n = 58\)
- \(p + n < 40\)
Từ đó, ta có thể thiết lập phương trình:
Và bằng cách giải phương trình này, chúng ta tìm được khoảng giá trị của \(p\) và \(n\). Kết quả cho thấy:
- Nếu \(p = 17\), thì \(n = 24\) và số nguyên tử khối \(Z = 41\) (không thỏa mãn điều kiện nguyên tử khối nhỏ hơn 40).
- Nếu \(p = 18\), thì \(n = 22\) và số nguyên tử khối \(Z = 40\) (không thỏa mãn điều kiện nguyên tử khối nhỏ hơn 40).
- Nếu \(p = 19\), thì \(n = 20\) và số nguyên tử khối \(Z = 39\) (thỏa mãn điều kiện).
Do đó, nguyên tố Z là Kali (K), một kim loại kiềm nằm trong nhóm 1 của bảng tuần hoàn. Kali có nhiều ứng dụng trong công nghiệp và đời sống, đặc biệt là trong sản xuất phân bón và các phản ứng hóa học khác nhau.
Kết luận, việc phân tích các yếu tố và tính toán chi tiết giúp chúng ta xác định chính xác nguyên tố hóa học mà nguyên tử Z đại diện. Đây là một minh chứng cho tầm quan trọng của việc áp dụng các kiến thức hóa học cơ bản để giải quyết các vấn đề thực tiễn và nghiên cứu khoa học.