Chủ đề ion đơn nguyên tử là gì: Ion đơn nguyên tử là loại ion được hình thành từ một nguyên tử duy nhất khi mất hoặc nhận electron, trở thành phần tử mang điện tích. Ví dụ, ion natri (Na⁺) và ion clorua (Cl⁻) là những ion đơn nguyên tử phổ biến. Bài viết này sẽ giúp bạn hiểu rõ về khái niệm, cách hình thành và vai trò quan trọng của ion đơn nguyên tử trong đời sống và phản ứng hóa học.
Mục lục
- Ion Đơn Nguyên Tử Là Gì?
- Tính Chất Của Ion Đơn Nguyên Tử
- Tính Chất Của Ion Đơn Nguyên Tử
- 1. Khái Niệm Ion Đơn Nguyên Tử
- 2. Phân Loại Ion: Đơn Nguyên Tử và Đa Nguyên Tử
- 3. Ví Dụ Về Các Ion Đơn Nguyên Tử
- 4. Tính Chất Vật Lý và Hóa Học Của Ion Đơn Nguyên Tử
- 5. Ứng Dụng Ion Đơn Nguyên Tử Trong Hóa Học
- 6. Ion Đơn Nguyên Tử và Sự Phát Triển Công Nghệ
- 7. Những Điều Cần Lưu Ý Khi Nghiên Cứu Ion Đơn Nguyên Tử
- 8. Kết Luận
Ion Đơn Nguyên Tử Là Gì?
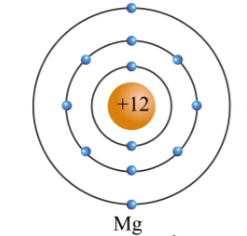
Ion đơn nguyên tử là một loại ion chỉ bao gồm một nguyên tử duy nhất. Khi một nguyên tử trung hòa về điện, tức là số proton mang điện dương bằng số electron mang điện âm, nếu nguyên tử này mất hoặc nhận thêm electron, nó sẽ trở thành một ion. Ion đơn nguyên tử có thể là ion dương (cation) hoặc ion âm (anion), tùy thuộc vào việc mất hay nhận electron.
Ví Dụ Về Ion Đơn Nguyên Tử
\[\text{Cl}^{-}\] : Ion clo, một anion do nhận thêm một electron.\[\text{Na}^{+}\] : Ion natri, một cation do mất đi một electron.\[\text{S}^{2-}\] : Ion lưu huỳnh, một anion do nhận thêm hai electron.\[\text{Ca}^{2+}\] : Ion canxi, một cation do mất đi hai electron.

Tính Chất Của Ion Đơn Nguyên Tử
Các ion đơn nguyên tử thường tồn tại trong các hợp chất ion và có các đặc điểm như sau:
- Tạo thành tinh thể ion có cấu trúc bền vững nhờ lực hút tĩnh điện giữa các ion trái dấu.
- Các hợp chất ion thường rắn, khó nóng chảy và khó bay hơi.
- Hợp chất ion tan nhiều trong nước, tạo thành dung dịch dẫn điện khi tan chảy hoặc khi hòa tan.
- Ở trạng thái rắn, tinh thể ion không dẫn điện nhưng khi ở dạng lỏng hoặc dung dịch, chúng dẫn điện tốt.
Tính Chất Của Ion Đơn Nguyên Tử
Các ion đơn nguyên tử thường tồn tại trong các hợp chất ion và có các đặc điểm như sau:
- Tạo thành tinh thể ion có cấu trúc bền vững nhờ lực hút tĩnh điện giữa các ion trái dấu.
- Các hợp chất ion thường rắn, khó nóng chảy và khó bay hơi.
- Hợp chất ion tan nhiều trong nước, tạo thành dung dịch dẫn điện khi tan chảy hoặc khi hòa tan.
- Ở trạng thái rắn, tinh thể ion không dẫn điện nhưng khi ở dạng lỏng hoặc dung dịch, chúng dẫn điện tốt.

1. Khái Niệm Ion Đơn Nguyên Tử
Ion đơn nguyên tử là ion được hình thành từ một nguyên tử duy nhất khi nguyên tử đó mất hoặc nhận electron. Sự thay đổi này khiến nguyên tử mang điện tích dương (cation) hoặc âm (anion). Các ion này đóng vai trò quan trọng trong nhiều phản ứng hóa học và quá trình sinh học.
- Cách tạo ion dương (cation): Khi một nguyên tử mất đi electron, nó sẽ trở thành ion dương. Ví dụ:
- Ion Natri (\( \text{Na}^+ \)): Hình thành khi nguyên tử natri mất 1 electron.
- Ion Canxi (\( \text{Ca}^{2+} \)): Hình thành khi nguyên tử canxi mất 2 electron.
- Cách tạo ion âm (anion): Khi một nguyên tử nhận thêm electron, nó sẽ trở thành ion âm. Ví dụ:
- Ion Clorua (\( \text{Cl}^- \)): Hình thành khi nguyên tử clo nhận thêm 1 electron.
- Ion Oxide (\( \text{O}^{2-} \)): Hình thành khi nguyên tử oxy nhận thêm 2 electron.
Ion đơn nguyên tử thường xuất hiện trong các phản ứng hóa học và đóng vai trò quan trọng trong nhiều quá trình tự nhiên và công nghiệp như xử lý nước, sản xuất năng lượng, và công nghệ vật liệu.

2. Phân Loại Ion: Đơn Nguyên Tử và Đa Nguyên Tử
Trong hóa học, ion được phân loại thành hai nhóm chính: ion đơn nguyên tử và ion đa nguyên tử. Sự phân loại này dựa trên số lượng nguyên tử tạo thành ion và vai trò của chúng trong các phản ứng hóa học.
- Ion Đơn Nguyên Tử: Là những ion được tạo thành từ một nguyên tử duy nhất mất hoặc nhận electron để trở thành ion. Các ion này có thể là ion dương (cation) hoặc ion âm (anion).
Ví dụ về Ion Đơn Nguyên Tử:
| Tên Ion | Công Thức | Cách Hình Thành |
|---|---|---|
| Ion Natri | \(\text{Na}^+\) | Na → \(\text{Na}^+\) + \(\text{e}^-\) |
| Ion Clorua | \(\text{Cl}^-\) | Cl + \(\text{e}^-\) → \(\text{Cl}^-\) |
| Ion Canxi | \(\text{Ca}^{2+}\) | Ca → \(\text{Ca}^{2+}\) + 2\(\text{e}^-\) |
| Ion Oxide | \(\text{O}^{2-}\) | O + 2\(\text{e}^-\) → \(\text{O}^{2-}\) |
- Ion Đa Nguyên Tử: Là những ion được tạo thành từ nhiều nguyên tử liên kết với nhau và mang một điện tích tổng hợp. Các ion này thường có vai trò quan trọng trong các phản ứng sinh hóa và công nghiệp.
Ví dụ về Ion Đa Nguyên Tử:
| Tên Ion | Công Thức | Cách Hình Thành |
|---|---|---|
| Ion Amonium | \(\text{NH}_4^+\) | \(\text{NH}_3\) + \(\text{H}^+\) → \(\text{NH}_4^+\) |
| Ion Sulfat | \(\text{SO}_4^{2-}\) | \(\text{H}_2\text{SO}_4\) - 2\(\text{H}^+\) → \(\text{SO}_4^{2-}\) |
| Ion Carbonat | \(\text{CO}_3^{2-}\) | \(\text{H}_2\text{CO}_3\) - 2\(\text{H}^+\) → \(\text{CO}_3^{2-}\) |
| Ion Nitrat | \(\text{NO}_3^-\) | \(\text{HNO}_3\) - \(\text{H}^+\) → \(\text{NO}_3^-\) |
Qua các ví dụ trên, chúng ta thấy rõ cách hình thành và vai trò quan trọng của các ion đơn nguyên tử và đa nguyên tử trong hóa học và đời sống hàng ngày. Ion đóng vai trò quan trọng trong các phản ứng hóa học, sinh hóa và nhiều ứng dụng công nghiệp.

3. Ví Dụ Về Các Ion Đơn Nguyên Tử
Ion đơn nguyên tử là những ion được tạo thành từ một nguyên tử duy nhất, có thể mang điện tích dương (cation) hoặc điện tích âm (anion) do mất hoặc nhận electron. Dưới đây là một số ví dụ cụ thể về các ion đơn nguyên tử phổ biến:
-
Ion Dương (Cation): Các ion này mang điện tích dương vì mất đi một hoặc nhiều electron.
-
Natri (\( \text{Na}^+ \)): Ion natri được tạo ra khi nguyên tử natri mất đi một electron.
Cách hình thành: \( \text{Na} \rightarrow \text{Na}^+ + \text{e}^- \)
-
Canxi (\( \text{Ca}^{2+} \)): Ion canxi được tạo ra khi nguyên tử canxi mất đi hai electron.
Cách hình thành: \( \text{Ca} \rightarrow \text{Ca}^{2+} + 2\text{e}^- \)
-
Nhôm (\( \text{Al}^{3+} \)): Ion nhôm được tạo ra khi nguyên tử nhôm mất đi ba electron.
Cách hình thành: \( \text{Al} \rightarrow \text{Al}^{3+} + 3\text{e}^- \)
-
-
Ion Âm (Anion): Các ion này mang điện tích âm vì nhận thêm một hoặc nhiều electron.
-
Clorua (\( \text{Cl}^- \)): Ion clorua được tạo ra khi nguyên tử clo nhận thêm một electron.
Cách hình thành: \( \text{Cl} + \text{e}^- \rightarrow \text{Cl}^- \)
-
Oxide (\( \text{O}^{2-} \)): Ion oxide được tạo ra khi nguyên tử oxy nhận thêm hai electron.
Cách hình thành: \( \text{O} + 2\text{e}^- \rightarrow \text{O}^{2-} \)
-
Nitride (\( \text{N}^{3-} \)): Ion nitride được tạo ra khi nguyên tử nitơ nhận thêm ba electron.
Cách hình thành: \( \text{N} + 3\text{e}^- \rightarrow \text{N}^{3-} \)
-
Những ví dụ trên giúp minh họa cách các ion đơn nguyên tử hình thành và vai trò của chúng trong hóa học, từ việc tham gia các phản ứng hóa học đến việc tạo ra các chất mới có tính chất khác biệt.
XEM THÊM:
4. Tính Chất Vật Lý và Hóa Học Của Ion Đơn Nguyên Tử
Ion đơn nguyên tử là những ion được tạo thành từ một nguyên tử duy nhất, mang điện tích dương hoặc âm do quá trình mất hoặc nhận electron. Các tính chất vật lý và hóa học của chúng có thể được chia thành hai nhóm chính: ion dương (cation) và ion âm (anion).
- Tính chất vật lý:
Cation và anion đơn nguyên tử thường tồn tại ở trạng thái rắn trong các hợp chất ion.
Ion đơn nguyên tử có kích thước nhỏ hơn hoặc lớn hơn nguyên tử ban đầu tùy thuộc vào việc mất hay nhận electron. Ví dụ, cation thường có bán kính nhỏ hơn so với nguyên tử do mất electron, trong khi anion có bán kính lớn hơn do nhận electron.
Các ion đơn nguyên tử thường có năng lượng ion hóa và ái lực electron khác nhau, ảnh hưởng đến tính bền của chúng trong phản ứng hóa học.
- Tính chất hóa học:
Các cation đơn nguyên tử như \( \text{Na}^+ \), \( \text{Ca}^{2+} \), và \( \text{Al}^{3+} \) thường hình thành do nguyên tử mất electron. Chúng có khả năng tham gia vào các phản ứng oxy hóa khử, làm chất oxy hóa hoặc chất khử trong các phản ứng hóa học.
Anion đơn nguyên tử như \( \text{Cl}^- \), \( \text{O}^{2-} \), và \( \text{N}^{3-} \) hình thành do nhận electron, đóng vai trò quan trọng trong việc tạo thành các hợp chất ion với các cation tương ứng.
Ion đơn nguyên tử có tính chất phản ứng cao, có khả năng tạo liên kết ion với các ion đối lập điện tích, dẫn đến sự hình thành các hợp chất ion như muối và oxit.
| Tên Ion | Công Thức | Phương Trình Hình Thành |
|---|---|---|
| Ion Natri | \( \text{Na}^+ \) | \( \text{Na} \rightarrow \text{Na}^+ + \text{e}^- \) |
| Ion Clorua | \( \text{Cl}^- \) | \( \text{Cl} + \text{e}^- \rightarrow \text{Cl}^- \) |
| Ion Canxi | \( \text{Ca}^{2+} \) | \( \text{Ca} \rightarrow \text{Ca}^{2+} + 2\text{e}^- \) |
| Ion Oxide | \( \text{O}^{2-} \) | \( \text{O} + 2\text{e}^- \rightarrow \text{O}^{2-} \) |
Các ví dụ trên minh họa rõ cách thức mà ion đơn nguyên tử được hình thành và vai trò quan trọng của chúng trong các phản ứng hóa học. Chúng đóng vai trò quan trọng trong sự hình thành các hợp chất và có tính chất hóa học đặc trưng, góp phần vào nhiều ứng dụng thực tế trong đời sống và công nghiệp.
5. Ứng Dụng Ion Đơn Nguyên Tử Trong Hóa Học
Ion đơn nguyên tử có vai trò quan trọng trong nhiều lĩnh vực hóa học, bao gồm các phản ứng hóa học cơ bản, quá trình sinh hóa, và nhiều ứng dụng thực tiễn khác. Dưới đây là một số ứng dụng cụ thể của các ion đơn nguyên tử:
- 1. Xác định phản ứng hóa học: Các ion đơn nguyên tử như \( \text{Na}^+ \), \( \text{Cl}^- \), và \( \text{Ca}^{2+} \) thường xuất hiện trong các phản ứng hóa học. Chúng giúp xác định tính chất của các phản ứng, chẳng hạn như phản ứng kết tủa, phản ứng trung hòa, và phản ứng oxy hóa-khử.
- 2. Cân bằng điện tích trong dung dịch: Ion đơn nguyên tử đóng vai trò quan trọng trong việc cân bằng điện tích trong các dung dịch nước. Ví dụ, \( \text{Na}^+ \) và \( \text{Cl}^- \) thường có mặt trong nước biển và giúp duy trì độ cân bằng điện tích của nước.
- 3. Ứng dụng trong sinh học: Các ion như \( \text{K}^+ \) (Kali) và \( \text{Na}^+ \) (Natri) rất quan trọng trong hoạt động của tế bào, đặc biệt trong việc duy trì áp suất thẩm thấu và truyền tín hiệu thần kinh trong cơ thể người.
- 4. Ứng dụng trong công nghiệp: Ion đơn nguyên tử như \( \text{Fe}^{2+} \) (sắt) và \( \text{Cu}^{2+} \) (đồng) được sử dụng trong nhiều quy trình công nghiệp như mạ điện, sản xuất pin và các quá trình xử lý kim loại.
- 5. Điều chỉnh pH: Các ion đơn nguyên tử như \( \text{H}^+ \) và \( \text{OH}^- \) đóng vai trò chính trong việc điều chỉnh độ pH của dung dịch. Điều này rất quan trọng trong nhiều ngành như sản xuất thực phẩm, dược phẩm, và xử lý nước thải.
Các ứng dụng trên cho thấy vai trò không thể thiếu của các ion đơn nguyên tử trong các quá trình hóa học và sinh học. Hiểu rõ về chúng giúp tối ưu hóa nhiều phản ứng và quá trình, từ nghiên cứu khoa học đến các ứng dụng trong đời sống hàng ngày.

6. Ion Đơn Nguyên Tử và Sự Phát Triển Công Nghệ
Ion đơn nguyên tử là những ion được hình thành từ một nguyên tử duy nhất, có thể mang điện tích dương (cation) hoặc âm (anion) tùy thuộc vào việc mất hay nhận thêm electron. Quá trình này đóng vai trò quan trọng trong nhiều ngành công nghệ và khoa học hiện đại, đặc biệt là trong các lĩnh vực hóa học, vật lý, và công nghệ nano.
- Công nghệ pin và lưu trữ năng lượng: Các ion đơn nguyên tử như Li+ được sử dụng rộng rãi trong công nghệ pin, đặc biệt là pin lithium-ion. Pin này có dung lượng cao và tuổi thọ dài, giúp cải thiện hiệu suất của thiết bị điện tử như điện thoại, máy tính xách tay và ô tô điện.
- Công nghệ xử lý nước và môi trường: Ion đơn nguyên tử đóng vai trò quan trọng trong các quá trình xử lý nước, bao gồm việc loại bỏ các kim loại nặng như Pb2+ và Hg2+. Công nghệ trao đổi ion sử dụng các hạt nhựa đặc biệt để hấp thụ các ion có hại và thay thế chúng bằng các ion vô hại, giúp cải thiện chất lượng nước.
- Kỹ thuật phân tích và y sinh: Các ion đơn nguyên tử cũng được sử dụng trong kỹ thuật phân tích như phổ khối (Mass Spectrometry) để xác định thành phần hóa học của mẫu. Trong y sinh, ion đơn nguyên tử giúp trong việc theo dõi các quá trình sinh học và phát hiện sớm bệnh tật.
Công nghệ ion đơn nguyên tử không chỉ dừng lại ở mức độ ứng dụng hiện tại mà còn tiếp tục được nghiên cứu và phát triển, mở ra các tiềm năng mới trong tương lai. Các nghiên cứu đang tập trung vào việc cải tiến hiệu suất, giảm chi phí và tìm kiếm các ứng dụng mới nhằm đáp ứng nhu cầu ngày càng cao của xã hội.
7. Những Điều Cần Lưu Ý Khi Nghiên Cứu Ion Đơn Nguyên Tử
Khi nghiên cứu về ion đơn nguyên tử, cần lưu ý một số khía cạnh quan trọng để đảm bảo tính chính xác và an toàn trong quá trình thực hiện.
7.1. Lưu Ý Về Tính An Toàn
- Bảo vệ cá nhân: Khi tiến hành các thí nghiệm với ion đơn nguyên tử, cần sử dụng đầy đủ trang bị bảo hộ như găng tay, kính bảo hộ, và áo choàng phòng thí nghiệm để tránh tiếp xúc trực tiếp với hóa chất.
- Xử lý hóa chất đúng cách: Các hóa chất liên quan đến ion đơn nguyên tử có thể có tính ăn mòn hoặc gây hại. Cần lưu trữ và xử lý hóa chất theo đúng quy định an toàn để tránh rủi ro.
7.2. Các Sai Lầm Thường Gặp Khi Xác Định Ion
- Xác định sai loại ion: Trong quá trình nghiên cứu, có thể dễ dàng nhầm lẫn giữa ion đơn nguyên tử và ion đa nguyên tử. Do đó, cần kiểm tra kỹ lưỡng các đặc điểm và cấu trúc hóa học của ion để đảm bảo xác định chính xác.
- Thiếu tính chính xác trong đo lường: Khi đo lường các tính chất vật lý hoặc hóa học của ion, cần sử dụng các thiết bị chính xác và hiệu chuẩn đúng cách để đảm bảo kết quả thu được là chính xác.
- Không xem xét điều kiện môi trường: Tính chất của ion có thể thay đổi dựa trên môi trường như nhiệt độ, pH, và nồng độ. Cần kiểm soát và ghi nhận các điều kiện này trong quá trình thí nghiệm.
Nghiên cứu về ion đơn nguyên tử đòi hỏi sự cẩn trọng và chính xác. Việc hiểu rõ các lưu ý trên sẽ giúp tối ưu hóa quá trình nghiên cứu và đảm bảo kết quả thu được là đáng tin cậy.

8. Kết Luận
Ion đơn nguyên tử đóng một vai trò quan trọng trong các phản ứng hóa học và trong các ứng dụng thực tiễn. Qua quá trình nghiên cứu và tìm hiểu, chúng ta có thể nhận thấy rằng các ion đơn nguyên tử không chỉ đơn thuần là các nguyên tử mang điện tích dương hoặc âm mà còn là nền tảng cho nhiều phản ứng và quá trình hóa học cơ bản.
Các ion đơn nguyên tử được hình thành khi nguyên tử mất hoặc nhận electron, từ đó tạo ra các ion có tính chất riêng biệt và đóng vai trò thiết yếu trong nhiều phản ứng hóa học. Ví dụ, ion natri \( \text{Na}^+ \) được tạo ra khi nguyên tử natri mất đi một electron, và ion clorua \( \text{Cl}^- \) hình thành khi nguyên tử clo nhận thêm một electron.
Hiểu rõ về ion đơn nguyên tử giúp chúng ta nắm bắt được bản chất của nhiều hiện tượng hóa học xung quanh, từ việc giải thích sự hòa tan của muối trong nước đến việc hiểu rõ cơ chế hoạt động của pin và các quá trình điện phân.
Với những kiến thức đã thu thập, hy vọng rằng bạn sẽ tiếp tục khám phá thêm về các loại ion khác, đặc biệt là ion đa nguyên tử, để mở rộng hiểu biết về thế giới vi mô kỳ diệu của hóa học.