Chủ đề nguyên tử magnesium: Nguyên tử magnesium là một nguyên tố quan trọng trong nhiều lĩnh vực từ hóa học, vật lý đến y học và công nghiệp. Bài viết này sẽ cung cấp cái nhìn sâu sắc về cấu trúc, tính chất hóa học và vật lý của magnesium, cùng với các ứng dụng thực tế trong đời sống. Đừng bỏ lỡ cơ hội hiểu rõ hơn về nguyên tố này và những ảnh hưởng tích cực của nó!
Mục lục
Thông Tin Về Nguyên Tử Magnesium
Magnesium (Mg) là một nguyên tố hóa học thuộc nhóm kim loại kiềm thổ, có số hiệu nguyên tử là 12. Nguyên tử magnesium gồm có 12 proton, 12 neutron và 12 electron, được sắp xếp theo cấu hình electron:
Cấu Trúc Nguyên Tử Magnesium
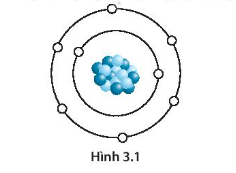
Nguyên tử magnesium có cấu trúc với 3 lớp vỏ electron, trong đó lớp vỏ ngoài cùng có 2 electron. Cấu trúc này mang lại cho Mg các tính chất hóa học đặc trưng của kim loại kiềm thổ. Magnesium có khối lượng mol là 24,305 g/mol.
- Số proton: 12
- Số neutron: 12
- Số electron: 12
Tính Chất Vật Lý
- Magnesium là kim loại màu trắng bạc, tương đối cứng và nhẹ, với khối lượng riêng 1,737 g/cm3.
- Nhiệt độ nóng chảy của magnesium là 648°C và nhiệt độ sôi là 1095°C.
- Trong điều kiện tự nhiên, magnesium thường bị oxi hóa chậm tạo thành một lớp oxit bảo vệ.
Tính Chất Hóa Học
- Phản ứng với phi kim: Magnesium phản ứng mạnh với oxi tạo thành oxit magnesium (MgO). Khi cháy, magnesium tạo ra ngọn lửa màu trắng rực rỡ.
- Phản ứng với axit: Magnesium dễ dàng phản ứng với các axit loãng như HCl, H2SO4 giải phóng khí hydro.
- Phản ứng với nước: Magnesium không phản ứng với nước lạnh, nhưng có thể phản ứng chậm với nước nóng để tạo thành Mg(OH)2.
Ứng Dụng Của Magnesium
Magnesium có nhiều ứng dụng trong thực tế, đặc biệt trong các ngành công nghiệp và y học:
- Công nghiệp hàng không vũ trụ: Magnesium được dùng để sản xuất hợp kim bền cho ngành công nghiệp này.
- Sản xuất pháo hoa: Nhờ khả năng cháy tạo ra ngọn lửa trắng, magnesium được sử dụng trong pháo hoa.
- Ngành xây dựng: Các hợp chất của magnesium được dùng trong sản xuất vật liệu chịu lửa và các công trình xây dựng.
- Y học: Magnesium được sử dụng trong sản xuất thuốc viên và các ứng dụng y tế khác.
1. Giới Thiệu Chung Về Nguyên Tử Magnesium
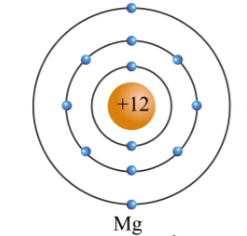
Magnesium, với ký hiệu hóa học \(\text{Mg}\) và số nguyên tử 12, là một nguyên tố kim loại thuộc nhóm kiềm thổ trong bảng tuần hoàn. Đây là một trong những nguyên tố phổ biến nhất trên Trái Đất, chiếm khoảng 2% khối lượng của lớp vỏ trái đất. Magnesium đóng vai trò quan trọng trong nhiều quá trình sinh học và công nghiệp.
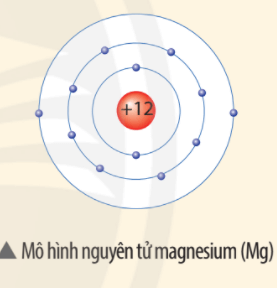
Nguyên tử magnesium có cấu trúc đơn giản với 12 proton trong hạt nhân và 12 electron sắp xếp trên ba lớp vỏ electron. Cấu hình electron của nó là \([ \text{Ne} ] 3s^2\), cho thấy hai electron hóa trị nằm ở lớp vỏ ngoài cùng. Điều này làm cho magnesium dễ dàng tham gia vào các phản ứng hóa học, đặc biệt là với phi kim để tạo thành các hợp chất ion.
Về mặt vật lý, magnesium là kim loại có màu trắng bạc, nhẹ và có độ dẫn điện tốt. Nó thường được sử dụng trong các hợp kim để tăng cường độ bền và giảm trọng lượng, đặc biệt trong ngành công nghiệp hàng không và chế tạo ô tô. Ngoài ra, magnesium còn đóng vai trò quan trọng trong y học, đặc biệt là trong việc duy trì hoạt động của hệ thần kinh và cơ bắp.
Magnesium có nguồn gốc phong phú trong tự nhiên, thường được tìm thấy dưới dạng hợp chất như \(\text{MgCO}_3\) (magnesit) và \(\text{MgSO}_4\) (epsomite). Quá trình khai thác và điều chế magnesium từ các nguồn tài nguyên này là một phần quan trọng trong công nghiệp hóa chất.
2. Tính Chất Vật Lý Của Magnesium
Magnesium là một kim loại kiềm thổ có màu trắng bạc, được biết đến với tính chất nhẹ và độ bền cao. Đây là những đặc điểm vật lý quan trọng của magnesium, làm cho nó trở thành một nguyên tố lý tưởng trong nhiều ứng dụng công nghiệp.
Dưới đây là một số tính chất vật lý quan trọng của magnesium:
- Màu sắc: Magnesium có màu trắng bạc sáng, dễ bị oxy hóa trong không khí, tạo thành một lớp mỏng oxide bảo vệ trên bề mặt.
- Khối lượng riêng: Magnesium có khối lượng riêng khoảng \[1.738 \, \text{g/cm}^3\], nhẹ hơn nhiều so với các kim loại khác như nhôm (\[2.7 \, \text{g/cm}^3\]).
- Nhiệt độ nóng chảy: Nhiệt độ nóng chảy của magnesium là \[650^\circ C\] (hoặc \[923 \, \text{K}\]), làm cho nó dễ dàng đúc và gia công.
- Nhiệt độ sôi: Magnesium có nhiệt độ sôi khoảng \[1091^\circ C\] (hoặc \[1364 \, \text{K}\]), cho thấy độ ổn định của nguyên tố này ở nhiệt độ cao.
- Tính dẫn điện và dẫn nhiệt: Magnesium có khả năng dẫn điện và dẫn nhiệt tốt, tuy nhiên không cao bằng nhôm hay đồng. Điều này làm cho nó phù hợp với các ứng dụng yêu cầu độ nhẹ và khả năng dẫn điện trung bình.
- Tính dẻo: Magnesium có độ dẻo tương đối, dễ dàng được kéo sợi và dát mỏng. Điều này làm cho magnesium có thể được sử dụng trong các hợp kim để tăng cường độ bền mà không làm tăng trọng lượng.
Nhờ vào những tính chất vật lý đặc biệt này, magnesium được ứng dụng rộng rãi trong các ngành công nghiệp như chế tạo máy bay, ô tô, và sản xuất các thiết bị điện tử nhẹ. Ngoài ra, magnesium còn được sử dụng trong các ứng dụng y học và khoa học vật liệu, nơi tính năng nhẹ và bền của nó đóng vai trò quan trọng.

3. Tính Chất Hóa Học Của Magnesium
Magnesium là một kim loại kiềm thổ với số hiệu nguyên tử 12 và ký hiệu hóa học là Mg. Đây là một nguyên tố hoạt động hóa học mạnh mẽ, dễ dàng tham gia vào các phản ứng hóa học với nhiều loại chất khác nhau.
Dưới đây là một số tính chất hóa học quan trọng của magnesium:
- Phản ứng với nước: Magnesium phản ứng chậm với nước lạnh để tạo ra magnesium hydroxide \(\text{Mg(OH)}_2\) và khí hydro \(\text{H}_2\). Tuy nhiên, trong nước nóng, phản ứng xảy ra nhanh hơn và tạo ra một lượng lớn khí hydro.
- Phản ứng với oxy: Khi đốt cháy trong không khí, magnesium phản ứng mạnh mẽ với oxy để tạo thành magnesium oxide \(\text{MgO}\), một chất rắn màu trắng. Phản ứng này tỏa ra một lượng lớn nhiệt và ánh sáng chói.
- Phản ứng với axit: Magnesium dễ dàng phản ứng với các axit mạnh như hydrochloric acid \(\text{HCl}\) để tạo ra muối magnesium chloride \(\text{MgCl}_2\) và khí hydro \(\text{H}_2\). Phản ứng này thường diễn ra rất mạnh mẽ với sự thoát ra của bọt khí hydro.
- Phản ứng với halogen: Magnesium phản ứng trực tiếp với các halogen như chlorine \(\text{Cl}_2\) để tạo ra muối halide như magnesium chloride \(\text{MgCl}_2\). Phản ứng này tỏa ra nhiệt và thường được sử dụng trong tổng hợp hóa học.
- Phản ứng với nitrogen: Ở nhiệt độ cao, magnesium có thể phản ứng với nitrogen \(\text{N}_2\) trong không khí để tạo ra magnesium nitride \(\text{Mg}_3\text{N}_2\), một hợp chất ion màu vàng nhạt.
Những tính chất hóa học này của magnesium làm cho nó trở thành một nguyên tố quan trọng trong nhiều quá trình công nghiệp và sản xuất, bao gồm chế tạo hợp kim, sản xuất kim loại, và tổng hợp các chất hóa học khác.
4. Ứng Dụng Của Magnesium Trong Thực Tiễn
Magnesium là một kim loại có nhiều ứng dụng thực tiễn quan trọng trong đời sống và công nghiệp, nhờ vào tính chất vật lý và hóa học đặc biệt của nó. Dưới đây là những ứng dụng chính của magnesium:
- Sản xuất hợp kim: Magnesium là một thành phần quan trọng trong các hợp kim nhôm-magnesium. Những hợp kim này có đặc tính nhẹ, bền, và chống ăn mòn, được sử dụng rộng rãi trong ngành công nghiệp hàng không, ô tô và các thiết bị điện tử.
- Công nghiệp hóa chất: Magnesium được sử dụng để sản xuất các hợp chất hóa học như magnesium oxide \(\text{MgO}\) và magnesium chloride \(\text{MgCl}_2\). \(\text{MgO}\) được sử dụng trong sản xuất gạch chịu lửa, trong khi \(\text{MgCl}_2\) được sử dụng trong sản xuất xi măng và hóa chất khác.
- Chế tạo thiết bị y tế: Magnesium được sử dụng trong sản xuất các thiết bị y tế nhờ tính biocompatible, tức là an toàn khi tiếp xúc với cơ thể người. Các hợp kim magnesium được sử dụng trong sản xuất nẹp xương và các thiết bị cấy ghép trong cơ thể.
- Năng lượng và công nghệ: Nhờ vào khả năng phản ứng mạnh mẽ, magnesium được sử dụng trong sản xuất các thiết bị đánh lửa, pháo hoa, và cả trong ngành năng lượng hạt nhân để sản xuất nhiên liệu phóng xạ.
- Ứng dụng trong nông nghiệp: Magnesium là một nguyên tố vi lượng cần thiết cho sự phát triển của cây trồng. Nó được sử dụng trong sản xuất phân bón magnesium sulfate (\(\text{MgSO}_4\)), giúp cải thiện sức khỏe và năng suất cây trồng.
- Ứng dụng trong thực phẩm và dược phẩm: Magnesium cũng được sử dụng như một chất bổ sung dinh dưỡng trong thực phẩm và thuốc. Magnesium carbonate \(\(\text{MgCO}_3\)\) được dùng làm chất tạo xốp trong bánh kẹo và là thành phần chính trong một số loại thuốc kháng axit.
Nhờ những ứng dụng đa dạng này, magnesium đã và đang đóng vai trò quan trọng trong nhiều lĩnh vực khác nhau của cuộc sống và ngành công nghiệp.

5. Phương Pháp Điều Chế Magnesium
Magnesium là một kim loại quan trọng và được điều chế chủ yếu thông qua hai phương pháp chính: phương pháp điện phân và phương pháp nhiệt kim.
- Phương pháp điện phân:
Đây là phương pháp phổ biến nhất để điều chế magnesium từ các muối chloride như \(\text{MgCl}_2\). Quá trình điện phân nóng chảy \(\text{MgCl}_2\) diễn ra trong các tế bào điện phân với các điện cực bằng carbon. Magnesium kim loại được thu tại cực âm, trong khi khí clo \(\text{Cl}_2\) được thu tại cực dương.
- Phương pháp nhiệt kim:
Trong phương pháp này, oxit magnesium \(\text{MgO}\) được khử bằng silic (\(\text{Si}\)) hoặc nhôm (\(\text{Al}\)) ở nhiệt độ cao. Quá trình này diễn ra trong lò hồ quang hoặc lò phản ứng nhiệt độ cao, nơi oxit magnesium bị khử để tạo ra magnesium kim loại và silic dioxide \(\text{SiO}_2\) hoặc nhôm oxide \(\text{Al}_2\text{O}_3\).
- Phương pháp nhiệt luyện:
Phương pháp này chủ yếu được sử dụng để điều chế magnesium từ dolomit \((\text{CaMg(CO}_3)_2)\) hoặc magnesite \((\text{MgCO}_3)\). Trong quá trình này, dolomit hoặc magnesite được nung nóng để tạo ra oxit magnesium, sau đó oxit này tiếp tục được khử bằng silicon hoặc nhôm để thu được magnesium kim loại.
Những phương pháp điều chế này đều đóng vai trò quan trọng trong sản xuất magnesium, phục vụ cho các nhu cầu công nghiệp và thương mại trên toàn cầu.
XEM THÊM:
6. Tác Động Của Magnesium Đối Với Sức Khỏe
Magnesium là một khoáng chất thiết yếu trong cơ thể con người, đóng vai trò quan trọng trong nhiều quá trình sinh học. Dưới đây là một số tác động chính của magnesium đối với sức khỏe:
6.1 Vai Trò Của Magnesium Trong Cơ Thể Người
Magnesium tham gia vào hơn 300 phản ứng enzyme trong cơ thể, bao gồm quá trình tổng hợp protein, chức năng cơ và thần kinh, điều hòa huyết áp, và kiểm soát lượng đường trong máu. Đặc biệt, magnesium còn giúp duy trì chức năng của hệ tim mạch và hệ thần kinh, đảm bảo hoạt động ổn định và hiệu quả của các cơ quan.
6.2 Lợi Ích Của Magnesium Trong Chăm Sóc Sức Khỏe
Việc bổ sung đầy đủ magnesium mang lại nhiều lợi ích sức khỏe, bao gồm:
- Hỗ trợ chức năng tim mạch: Magnesium giúp điều hòa nhịp tim, phòng ngừa các bệnh lý về tim mạch như tăng huyết áp, đột quỵ.
- Tăng cường hệ xương khớp: Magnesium kết hợp với canxi giúp tăng cường độ chắc khỏe của xương và phòng ngừa loãng xương.
- Cải thiện tâm trạng và giấc ngủ: Magnesium có tác dụng làm dịu thần kinh, giúp giảm căng thẳng, lo âu và cải thiện chất lượng giấc ngủ.
- Hỗ trợ kiểm soát đường huyết: Magnesium đóng vai trò quan trọng trong quá trình chuyển hóa glucose và cải thiện độ nhạy insulin, giúp phòng ngừa bệnh tiểu đường loại 2.
6.3 Nguy Cơ Thiếu Hụt Và Dư Thừa Magnesium
Thiếu hụt magnesium: Thiếu hụt magnesium có thể dẫn đến các triệu chứng như co thắt cơ, chuột rút, mệt mỏi, và rối loạn nhịp tim. Những người có chế độ ăn nghèo nàn hoặc mắc các bệnh lý mãn tính thường có nguy cơ thiếu hụt magnesium cao.
Dư thừa magnesium: Mặc dù hiếm gặp, nhưng dư thừa magnesium do sử dụng quá liều các loại thực phẩm bổ sung có thể gây ra các triệu chứng như tiêu chảy, buồn nôn, và thậm chí là ngộ độc magnesium trong các trường hợp nghiêm trọng.
Nhìn chung, việc duy trì lượng magnesium cân bằng là cần thiết để đảm bảo sức khỏe toàn diện và phòng ngừa các bệnh lý liên quan.