Chủ đề trong hạt nhân nguyên tử lưu huỳnh: Trong hạt nhân nguyên tử lưu huỳnh đóng vai trò quan trọng trong việc hiểu rõ hơn về cấu trúc và tính chất hóa học của nguyên tố này. Bài viết sẽ cung cấp thông tin chi tiết về các đồng vị, ứng dụng thực tiễn, cũng như những ảnh hưởng của lưu huỳnh đến môi trường và sức khỏe con người.
Mục lục
Tìm hiểu về hạt nhân nguyên tử lưu huỳnh
Trong nguyên tử lưu huỳnh (ký hiệu hóa học là S), hạt nhân bao gồm 16 proton. Các proton này mang điện tích dương và nằm ở trung tâm của nguyên tử. Số lượng proton trong hạt nhân quyết định tính chất hóa học của nguyên tố và vị trí của nó trong bảng tuần hoàn.
Cấu trúc của hạt nhân nguyên tử lưu huỳnh
- Số proton: 16
- Số neutron: Thông thường là 16 hoặc 18, tùy thuộc vào đồng vị cụ thể của lưu huỳnh.
- Số khối: Tổng số proton và neutron, ví dụ: đồng vị phổ biến nhất của lưu huỳnh là \( \text{^{32}S} \), có số khối là 32.
Như vậy, hạt nhân của lưu huỳnh có tổng cộng 16 proton và thường là 16 neutron, tạo nên sự ổn định của nguyên tử này. Các neutron không mang điện nhưng đóng vai trò quan trọng trong việc giữ các proton lại với nhau trong hạt nhân.
Các đồng vị của lưu huỳnh
Lưu huỳnh tồn tại ở nhiều đồng vị khác nhau, mỗi đồng vị có số neutron khác nhau:
- \( \text{^{32}S} \): Đồng vị phổ biến nhất với 16 neutron.
- \( \text{^{33}S} \): Đồng vị có 17 neutron.
- \( \text{^{34}S} \): Đồng vị có 18 neutron.
- \( \text{^{36}S} \): Đồng vị hiếm với 20 neutron.
Ứng dụng của lưu huỳnh
Lưu huỳnh có nhiều ứng dụng trong đời sống và công nghiệp:
- Trong công nghiệp: Sản xuất axit sulfuric \( H_2SO_4 \), lưu hóa cao su, và chế tạo thuốc nhuộm.
- Trong y học: Điều trị các bệnh về da như ghẻ, nấm, và các bệnh về đường hô hấp.
- Trong nông nghiệp: Sử dụng làm phân bón và thuốc trừ sâu.
Kết luận
Hạt nhân nguyên tử lưu huỳnh với 16 proton và một số neutron khác nhau tạo thành các đồng vị khác nhau, là yếu tố quan trọng trong việc định hình các tính chất vật lý và hóa học của nguyên tố này. Lưu huỳnh có vai trò quan trọng trong nhiều lĩnh vực, từ công nghiệp đến y học và nông nghiệp, góp phần vào sự phát triển của nhiều ngành kinh tế.

1. Giới thiệu về nguyên tử lưu huỳnh
Nguyên tử lưu huỳnh, có ký hiệu hóa học là S, là một phi kim thuộc nhóm 16 trong bảng tuần hoàn với số nguyên tử 16. Lưu huỳnh là một trong những nguyên tố phổ biến và cần thiết cho sự sống, tồn tại chủ yếu dưới dạng tinh thể màu vàng chanh ở nhiệt độ phòng.
Trong hạt nhân của một nguyên tử lưu huỳnh có 16 proton và thường là 16 neutron, tạo nên một khối lượng nguyên tử trung bình khoảng 32 đơn vị khối lượng nguyên tử (u). Các đồng vị phổ biến của lưu huỳnh bao gồm \(^{32}S\) (95,02%), \(^{33}S\) (0,75%), \(^{34}S\) (4,21%) và \(^{36}S\) (0,02%).
Lưu huỳnh không có mùi khi ở dạng đơn chất, nhưng khi kết hợp với hydro để tạo thành khí hydrogen sulfide (\(H_2S\)), nó sẽ tạo ra mùi trứng thối đặc trưng. Đây là một trong những tính chất nhận biết nổi bật của lưu huỳnh trong các phản ứng hóa học.
Về tính chất hóa học, lưu huỳnh có khả năng tạo thành các hợp chất với hầu hết các nguyên tố khác, ngoại trừ khí trơ. Các trạng thái oxy hóa phổ biến của lưu huỳnh là -2, +2, +4, và +6. Ví dụ, lưu huỳnh thường gặp trong các hợp chất như axit sulfuric (\(H_2SO_4\)), sulfur dioxide (\(SO_2\)), và hydrogen sulfide (\(H_2S\)).
Trong tự nhiên, lưu huỳnh thường được tìm thấy ở dạng đơn chất hoặc trong các khoáng chất như sulfide và sulfate. Nó cũng có mặt trong hai loại amino acid thiết yếu là cysteine và methionine, đóng vai trò quan trọng trong cấu trúc và chức năng của protein.
Lưu huỳnh là một nguyên tố đa dạng về cấu trúc và thù hình. Dạng phổ biến nhất của lưu huỳnh ở trạng thái rắn là các phân tử vòng tám nguyên tử (\(S_8\)), nhưng nó cũng có thể tồn tại dưới nhiều dạng vòng khác nhau như \(S_7\), \(S_{12}\) và \(S_{18}\).
Nguyên tử lưu huỳnh có một số tính chất đặc trưng khác như độ âm điện là 2,58 trên thang Pauling, năng lượng ion hóa thứ nhất là 999,6 kJ/mol, và bán kính cộng hóa trị khoảng 105 pm. Những đặc điểm này giúp lưu huỳnh tham gia vào nhiều phản ứng hóa học quan trọng, từ tổng hợp axit đến sản xuất phân bón và các ứng dụng trong ngành công nghiệp khác.
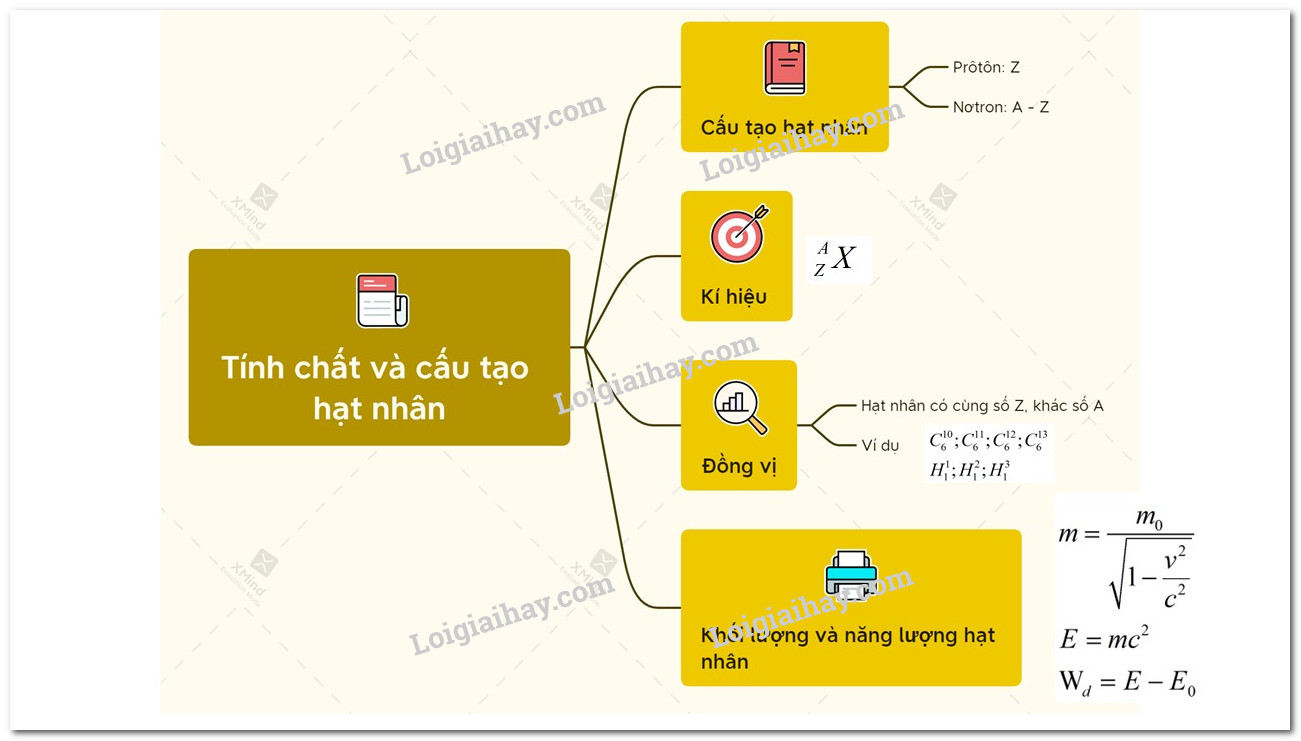
2. Cấu trúc hạt nhân nguyên tử lưu huỳnh
Nguyên tử lưu huỳnh có số hiệu nguyên tử là 16, tức là trong hạt nhân của nó chứa 16 proton. Số lượng proton này đồng thời xác định số electron trong nguyên tử, do đó, một nguyên tử lưu huỳnh trung hòa sẽ có 16 electron phân bố trong các lớp vỏ điện tử.
Bên cạnh 16 proton, hạt nhân của nguyên tử lưu huỳnh cũng chứa các nơtron. Số lượng nơtron trong nguyên tử lưu huỳnh phổ biến nhất, đồng vị 32S, là 16, do đó tổng số khối của nó là 32. Công thức tổng quát cho số khối \( A \) của một nguyên tử là:
\[ A = Z + N \]
Với:
- \( Z \) là số proton (số hiệu nguyên tử).
- \( N \) là số nơtron.
Như vậy, đối với đồng vị 32S:
\[ A = 16 + 16 = 32 \]
Các đồng vị khác của lưu huỳnh có thể có số nơtron khác nhau, chẳng hạn như 33S, 34S, và 36S, nhưng tất cả đều có 16 proton trong hạt nhân.
Hạt nhân nguyên tử lưu huỳnh có một cấu trúc bền vững nhờ sự cân bằng giữa lực đẩy điện tích dương của các proton và lực hạt nhân mạnh giữa các nucleon (proton và nơtron). Cấu trúc này giúp lưu huỳnh ổn định trong các phản ứng hóa học thông thường và duy trì vai trò quan trọng trong nhiều quá trình tự nhiên và công nghiệp.

3. Ứng dụng của lưu huỳnh trong đời sống và công nghiệp
Lưu huỳnh là một nguyên tố phi kim phổ biến và có nhiều ứng dụng quan trọng trong đời sống và công nghiệp. Dưới đây là một số ứng dụng tiêu biểu:
- Sản xuất axit sulfuric (H2SO4): Khoảng 90% lượng lưu huỳnh khai thác được sử dụng để sản xuất axit sulfuric. Đây là một trong những hóa chất quan trọng nhất trong ngành công nghiệp hóa chất, được dùng trong sản xuất phân bón, chế biến dầu mỏ, và nhiều ngành công nghiệp khác.
- Lưu hóa cao su: Lưu huỳnh được sử dụng để lưu hóa cao su, làm tăng độ bền, tính đàn hồi và khả năng chịu nhiệt của cao su. Quy trình này giúp cải thiện chất lượng sản phẩm cao su, như lốp xe và các sản phẩm cao su công nghiệp.
- Sản xuất diêm và pháo: Lưu huỳnh là thành phần chính trong sản xuất diêm và pháo. Nó kết hợp với các hóa chất khác như kali nitrat (KNO3) và than củi để tạo ra hỗn hợp cháy mạnh trong các sản phẩm này.
- Dược phẩm và hóa chất nông nghiệp: Lưu huỳnh được sử dụng trong sản xuất nhiều loại dược phẩm, chất diệt nấm và thuốc trừ sâu. Trong nông nghiệp, nó được sử dụng để kiểm soát các loại nấm bệnh trên cây trồng và bảo vệ mùa màng.
- Ứng dụng trong thực phẩm: Lưu huỳnh được dùng để làm trắng và bảo quản một số loại thực phẩm khô như trái cây sấy khô. Nó giúp ngăn ngừa sự oxi hóa và giữ màu sắc tươi sáng cho sản phẩm.
- Sản xuất thuốc súng: Lưu huỳnh cùng với than củi và kali nitrat được dùng để sản xuất thuốc súng đen, một loại thuốc nổ đơn giản nhưng hiệu quả.
- Phân bón: Lưu huỳnh là một nguyên tố vi lượng cần thiết cho sự phát triển của cây trồng. Nó được bổ sung vào đất dưới dạng phân bón để cải thiện năng suất cây trồng, đặc biệt là các cây cần lưu huỳnh như đậu tương và lúa mì.

4. Đồng vị và phản ứng hạt nhân của lưu huỳnh
4.1. Các đồng vị phổ biến của lưu huỳnh
Lưu huỳnh là một nguyên tố có nhiều đồng vị tự nhiên. Các đồng vị phổ biến của lưu huỳnh bao gồm: 32S, 33S, 34S, và 36S. Trong đó, 32S là đồng vị ổn định và phổ biến nhất, chiếm khoảng 95.02% tổng số lượng lưu huỳnh trong tự nhiên.
- 32S: Đồng vị ổn định nhất, chiếm phần lớn trong tự nhiên, không phóng xạ.
- 33S: Đồng vị ổn định, chiếm khoảng 0.75% trong tự nhiên.
- 34S: Đồng vị ổn định, chiếm khoảng 4.21% trong tự nhiên.
- 36S: Đồng vị ổn định, rất hiếm, chỉ chiếm khoảng 0.02% trong tự nhiên.
Các đồng vị này khác nhau về số neutron trong hạt nhân, dẫn đến sự khác biệt nhỏ trong tính chất vật lý nhưng không ảnh hưởng nhiều đến tính chất hóa học của lưu huỳnh. Đồng vị 32S được sử dụng nhiều trong nghiên cứu địa chất và khí tượng học để nghiên cứu các quá trình tự nhiên.
4.2. Phản ứng hạt nhân và vai trò trong nghiên cứu khoa học
Phản ứng hạt nhân liên quan đến các đồng vị của lưu huỳnh thường được nghiên cứu để hiểu rõ hơn về cấu trúc hạt nhân và các tương tác cơ bản trong vật lý hạt nhân. Các phản ứng phổ biến bao gồm phản ứng bắt neutron và phản ứng phân hạch.
- Phản ứng bắt neutron: Đồng vị 32S có thể bắt neutron để chuyển thành 33S trong phản ứng: \[ ^{32}S + n \rightarrow ^{33}S \] Phản ứng này rất quan trọng trong việc nghiên cứu các quá trình trong sao và sản xuất các đồng vị phóng xạ dùng trong y học.
- Phản ứng phân hạch: Dưới điều kiện năng lượng cao, các đồng vị lưu huỳnh có thể tham gia vào phản ứng phân hạch tạo ra các hạt nhân nhỏ hơn. Tuy nhiên, phản ứng này ít phổ biến và thường chỉ xảy ra trong điều kiện phòng thí nghiệm đặc biệt.
Các nghiên cứu về phản ứng hạt nhân của lưu huỳnh giúp mở rộng kiến thức về vật lý hạt nhân và hỗ trợ trong các ứng dụng như phát triển năng lượng hạt nhân, nghiên cứu thiên văn học, và các ứng dụng y tế.
| Đồng vị | Số Proton | Số Neutron | Tỷ lệ phần trăm trong tự nhiên |
|---|---|---|---|
| 32S | 16 | 16 | 95.02% |
| 33S | 16 | 17 | 0.75% |
| 34S | 16 | 18 | 4.21% |
| 36S | 16 | 20 | 0.02% |

5. Tác động của lưu huỳnh đến môi trường và sức khỏe
5.1. Ảnh hưởng của các hợp chất lưu huỳnh đến môi trường
Lưu huỳnh là một nguyên tố tự nhiên có thể ảnh hưởng đến môi trường thông qua các hợp chất của nó, đặc biệt là lưu huỳnh dioxide (SO2) và hydrogen sulfide (H2S). Khi được thải ra từ hoạt động công nghiệp như đốt cháy nhiên liệu hóa thạch và luyện kim, các hợp chất này có thể gây ra hiện tượng mưa axit, làm hỏng hệ sinh thái và tác động tiêu cực đến nước và đất.
- Mưa axit: SO2 trong không khí có thể phản ứng với nước để tạo thành axit sulfuric (H2SO4), gây mưa axit. Mưa axit có thể làm giảm độ pH của đất và nước, ảnh hưởng đến sự phát triển của thực vật và động vật.
- Ô nhiễm không khí: H2S là một khí độc có mùi trứng thối, có thể gây ô nhiễm không khí và làm giảm chất lượng không khí, ảnh hưởng đến sức khỏe con người và động vật.
5.2. Tác động đến sức khỏe con người
Lưu huỳnh và các hợp chất của nó có thể ảnh hưởng đến sức khỏe con người thông qua tiếp xúc trực tiếp hoặc gián tiếp. Các tác động này phụ thuộc vào dạng hóa học, nồng độ, và thời gian tiếp xúc.
- Tiếp xúc với SO2: Khí SO2 có thể gây kích ứng mắt, mũi, và cổ họng. Tiếp xúc lâu dài với SO2 ở nồng độ cao có thể dẫn đến các vấn đề về hô hấp như hen suyễn, viêm phế quản mãn tính.
- Tiếp xúc với H2S: H2S có thể gây ngộ độc cấp tính nếu hít phải ở nồng độ cao, dẫn đến các triệu chứng như chóng mặt, buồn nôn, và mất ý thức. Ở nồng độ thấp, H2S có thể gây kích ứng mắt và đường hô hấp.
Tuy nhiên, lưu huỳnh cũng có vai trò quan trọng trong y học. Một số hợp chất lưu huỳnh, như sulfur trong thuốc mỡ và thuốc kháng sinh, được sử dụng để điều trị các bệnh nhiễm trùng và da liễu.
5.3. Giải pháp và biện pháp xử lý tác động của lưu huỳnh
Để giảm thiểu tác động tiêu cực của lưu huỳnh đến môi trường và sức khỏe, các biện pháp sau đây có thể được áp dụng:
- Kiểm soát khí thải: Áp dụng các công nghệ lọc và xử lý khí thải trong công nghiệp để giảm lượng SO2 và H2S thải ra môi trường.
- Tái sử dụng và tái chế: Thu gom và tái chế lưu huỳnh từ các quá trình công nghiệp để giảm lượng chất thải.
- Trồng cây xanh: Phát triển các vùng cây xanh để hấp thụ SO2 và cải thiện chất lượng không khí.
- Giám sát chất lượng không khí: Sử dụng các hệ thống giám sát chất lượng không khí để phát hiện sớm các nồng độ cao của khí lưu huỳnh và thực hiện biện pháp phòng ngừa.
Những biện pháp này không chỉ giúp bảo vệ môi trường mà còn góp phần bảo vệ sức khỏe con người khỏi các tác động tiêu cực của lưu huỳnh và các hợp chất của nó.
XEM THÊM:
6. Kết luận
6.1. Tổng kết về vai trò của lưu huỳnh trong tự nhiên và đời sống
Lưu huỳnh là một nguyên tố hóa học quan trọng, không chỉ đóng vai trò thiết yếu trong cấu trúc của nhiều hợp chất tự nhiên mà còn có ứng dụng rộng rãi trong nhiều ngành công nghiệp. Từ vai trò trong quá trình sinh học đến ứng dụng trong sản xuất công nghiệp, lưu huỳnh đã chứng minh giá trị của mình trong cả tự nhiên và đời sống con người.
- Trong tự nhiên: Lưu huỳnh tồn tại dưới nhiều dạng hợp chất trong vỏ Trái Đất và đóng vai trò quan trọng trong chu trình sinh học, tham gia vào cấu trúc của axit amin và protein cần thiết cho sự sống.
- Trong đời sống: Lưu huỳnh được sử dụng rộng rãi trong sản xuất axit sulfuric, một hóa chất quan trọng trong công nghiệp hóa chất, phân bón, và chế biến dầu mỏ. Ngoài ra, lưu huỳnh còn có ứng dụng trong y học và mỹ phẩm, giúp điều trị các bệnh ngoài da và bảo vệ sức khỏe.
6.2. Hướng nghiên cứu tương lai liên quan đến lưu huỳnh
Những nghiên cứu tương lai về lưu huỳnh sẽ tập trung vào việc phát triển các phương pháp khai thác và sử dụng lưu huỳnh một cách bền vững và hiệu quả hơn. Điều này bao gồm:
- Nghiên cứu công nghệ mới: Phát triển các công nghệ tiên tiến nhằm giảm thiểu ô nhiễm từ các quá trình công nghiệp liên quan đến lưu huỳnh, đồng thời tối ưu hóa việc sử dụng tài nguyên lưu huỳnh.
- Khám phá các hợp chất lưu huỳnh mới: Tìm hiểu và phát triển các hợp chất lưu huỳnh mới có thể ứng dụng trong y học, nông nghiệp, và công nghiệp để nâng cao chất lượng cuộc sống và bảo vệ môi trường.
- Bảo vệ môi trường: Nghiên cứu tác động của lưu huỳnh và các hợp chất của nó đối với môi trường để phát triển các biện pháp bảo vệ môi trường hiệu quả hơn, giảm thiểu ảnh hưởng tiêu cực đến hệ sinh thái và sức khỏe con người.
Tóm lại, lưu huỳnh là một nguyên tố hóa học có vai trò quan trọng và đa dạng trong tự nhiên và đời sống. Việc tiếp tục nghiên cứu và phát triển các ứng dụng mới của lưu huỳnh sẽ góp phần vào sự phát triển bền vững và bảo vệ môi trường, cũng như nâng cao chất lượng cuộc sống của con người.