Chủ đề nguyên tử sắt: Nguyên tử sắt (Fe) là thành phần quan trọng trong tự nhiên và cuộc sống con người. Với số nguyên tử 26, sắt có vai trò chủ chốt trong cấu trúc của các hợp chất và vật liệu công nghiệp. Bài viết này sẽ đi sâu khám phá cấu trúc, tính chất hóa lý, và những ứng dụng thiết yếu của nguyên tử sắt, từ sinh học đến công nghiệp và công nghệ hiện đại, mang đến cái nhìn toàn diện về tầm quan trọng của nguyên tố này.
Mục lục
Nguyên Tử Sắt: Tính Chất, Cấu Trúc và Ứng Dụng
Nguyên tử sắt là một trong những kim loại quan trọng nhất trong ngành công nghiệp và khoa học. Với ký hiệu hóa học là Fe và số nguyên tử là 26, sắt là kim loại phổ biến với nhiều ứng dụng đa dạng từ xây dựng, sản xuất thép đến y học.
Tính Chất Vật Lý Của Sắt
- Màu sắc: Sắt có màu trắng xám và thường có ánh kim.
- Tính nhiễm từ: Sắt có tính nhiễm từ mạnh, làm cho nó bị hút bởi nam châm.
- Độ cứng: Sắt là kim loại có độ cứng vừa phải, dễ dàng được rèn thành các hình dạng khác nhau.
- Nhiệt độ nóng chảy: Sắt có nhiệt độ nóng chảy cao, khoảng \(1540^{\circ}C\).
- Tính dẫn điện: Sắt dẫn điện tốt, được sử dụng rộng rãi trong các ứng dụng điện.
Tính Chất Hóa Học Của Sắt
- Phản ứng với phi kim: Ở nhiệt độ cao, sắt phản ứng mạnh với các nguyên tố phi kim như oxy, lưu huỳnh và clo.
- Phản ứng với axit: Sắt phản ứng với axit loãng như HCl và H\(_2\)SO\(_4\) để tạo ra muối và khí hiđro.
- Phản ứng với nước: Ở nhiệt độ cao, sắt phản ứng với nước để tạo ra sắt oxit và khí hiđro.
Cấu Trúc Nguyên Tử Sắt
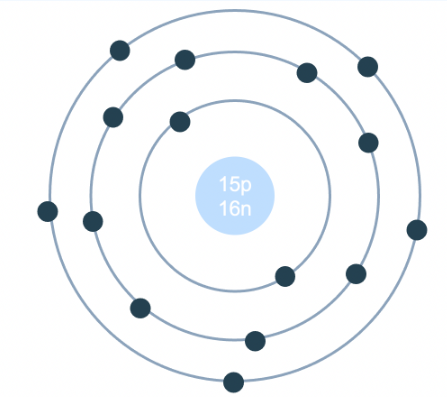
Sắt có cấu trúc nguyên tử gồm 26 proton, 30 neutron và 26 electron phân bố trên ba lớp vỏ. Cấu hình electron của sắt là \([Ar] 3d^6 4s^2\). Nguyên tử sắt có khả năng mất đi 2 hoặc 3 electron để tạo thành ion Fe\(^2+\) hoặc Fe\(^3+\), tùy vào môi trường phản ứng.
Ứng Dụng Của Sắt
| Ngành | Ứng dụng |
|---|---|
| Sản xuất thép | Sắt là nguyên liệu chính trong sản xuất thép, sử dụng trong xây dựng, sản xuất xe hơi, và nhiều lĩnh vực khác. |
| Y học | Sắt là thành phần quan trọng của hemoglobin, giúp vận chuyển oxy trong máu. |
| Công nghiệp điện | Sắt được dùng trong sản xuất các thiết bị điện và điện tử do tính dẫn điện tốt. |
| Ngành từ tính | Sắt và các hợp kim của nó được sử dụng để chế tạo nam châm và các thiết bị liên quan đến từ trường. |
Kết Luận
Sắt là một kim loại đa dụng với nhiều tính chất vật lý và hóa học độc đáo. Với vai trò quan trọng trong nhiều ngành công nghiệp, sắt đóng góp không nhỏ vào sự phát triển của khoa học và công nghệ hiện đại.
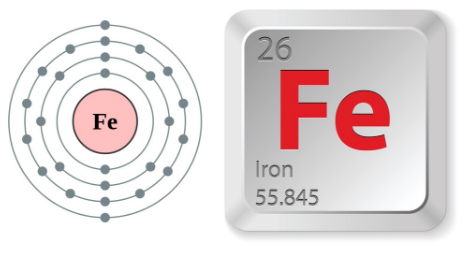
Tổng Quan về Nguyên Tử Sắt
Nguyên tử sắt (Fe) là một trong những nguyên tố quan trọng nhất trong bảng tuần hoàn, thuộc nhóm kim loại chuyển tiếp với số nguyên tử là 26. Sắt là một trong những nguyên tố phổ biến nhất trong vỏ Trái Đất và có nhiều ứng dụng rộng rãi trong công nghiệp và đời sống.
- Cấu trúc điện tử: Nguyên tử sắt có cấu trúc điện tử được biểu diễn dưới dạng \[ 1s^2 2s^2 2p^6 3s^2 3p^6 3d^6 4s^2 \]. Điều này cho thấy sắt có khả năng tham gia vào nhiều phản ứng hóa học phức tạp nhờ vào các electron lớp ngoài.
- Đồng vị: Sắt có bốn đồng vị tự nhiên là \( ^{54}Fe \), \( ^{56}Fe \), \( ^{57}Fe \) và \( ^{58}Fe \). Trong đó, \( ^{56}Fe \) là đồng vị phổ biến nhất, chiếm khoảng 91,75% tổng số nguyên tử sắt trong tự nhiên.
| Đồng vị | Tỷ lệ phần trăm (%) |
|---|---|
| \( ^{54}Fe \) | 5.8 |
| \( ^{56}Fe \) | 91.75 |
| \( ^{57}Fe \) | 2.1 |
| \( ^{58}Fe \) | 0.28 |
Cấu trúc tinh thể: Sắt có hai dạng cấu trúc tinh thể chính: lập phương tâm khối (BCC) ở nhiệt độ phòng và chuyển sang lập phương tâm diện (FCC) ở nhiệt độ cao hơn. Tính chất này giúp sắt có khả năng thay đổi độ bền và tính chất vật lý theo điều kiện nhiệt độ.
- Ứng dụng trong công nghiệp: Sắt là nguyên liệu chính trong sản xuất thép và các hợp kim, đóng vai trò quan trọng trong ngành xây dựng, sản xuất máy móc và ô tô.
- Vai trò trong sinh học: Sắt là thành phần quan trọng trong hemoglobin và myoglobin, giúp vận chuyển oxy trong máu và cơ bắp, là yếu tố không thể thiếu cho sự sống của con người và động vật.
- Ảnh hưởng đến môi trường: Sắt tham gia vào các chu trình sinh địa hóa, giúp duy trì sự cân bằng của các hệ sinh thái và có khả năng ứng dụng trong xử lý nước thải và ô nhiễm môi trường.
Với vai trò quan trọng trong nhiều lĩnh vực, sắt không chỉ là một nguyên tố hóa học đơn thuần mà còn là nền tảng cho sự phát triển của công nghệ và đời sống hiện đại.
Ứng Dụng Của Sắt Trong Đời Sống
Sắt là một trong những kim loại có ứng dụng rộng rãi nhất trong đời sống hàng ngày, từ công nghiệp đến y học và sinh học. Nhờ vào tính chất vật lý và hóa học đặc biệt, sắt đóng vai trò quan trọng trong nhiều lĩnh vực khác nhau.
- Công nghiệp sản xuất thép: Sắt là thành phần chính trong sản xuất thép, một trong những vật liệu cơ bản trong ngành xây dựng và sản xuất. Thép từ sắt có độ bền cao, khả năng chịu lực tốt và dễ dàng tạo hình, làm cho nó trở thành vật liệu không thể thiếu trong xây dựng cầu đường, nhà cửa và các công trình lớn.
- Sản xuất máy móc và thiết bị: Các hợp kim từ sắt, đặc biệt là thép không gỉ, được sử dụng rộng rãi trong sản xuất máy móc, thiết bị công nghiệp và gia dụng như ô tô, tủ lạnh, máy giặt và dụng cụ nhà bếp.
- Y học và sinh học: Sắt là thành phần quan trọng của hemoglobin, một protein trong máu có vai trò vận chuyển oxy từ phổi đến các tế bào trong cơ thể. Thiếu sắt có thể dẫn đến các vấn đề về sức khỏe như thiếu máu. Ngoài ra, sắt còn tham gia vào nhiều enzyme quan trọng trong cơ thể.
- Nông nghiệp: Sắt được sử dụng trong phân bón để bổ sung vi lượng cần thiết cho cây trồng, giúp cải thiện năng suất và chất lượng nông sản. Các hợp chất sắt cũng giúp cải thiện độ phì nhiêu của đất.
- Xử lý nước và môi trường: Các hợp chất của sắt, như sắt (III) sunfat, được sử dụng trong quá trình xử lý nước thải để loại bỏ các chất ô nhiễm. Sắt cũng giúp khử phèn trong nước ngầm, làm cho nước trở nên sạch và an toàn hơn cho sinh hoạt.
Với những ứng dụng đa dạng và quan trọng như vậy, sắt đóng vai trò không thể thiếu trong sự phát triển và tiến bộ của xã hội hiện đại.

Tính Chất Vật Lý của Sắt
Sắt là một kim loại chuyển tiếp có nhiều tính chất vật lý quan trọng, đóng vai trò quan trọng trong nhiều lĩnh vực công nghiệp và đời sống. Dưới đây là các tính chất vật lý nổi bật của sắt:
- Màu sắc và hình dạng: Sắt có màu xám bạc, bề mặt sáng bóng khi mới cắt hoặc đánh bóng, nhưng sẽ nhanh chóng bị oxi hóa và chuyển sang màu nâu đỏ khi tiếp xúc với không khí.
- Trạng thái: Ở điều kiện thường, sắt tồn tại ở trạng thái rắn với cấu trúc tinh thể lập phương tâm khối (BCC) ở nhiệt độ dưới 912°C và cấu trúc lập phương tâm diện (FCC) ở nhiệt độ từ 912°C đến 1394°C.
- Độ cứng và độ dẻo: Sắt có độ cứng tương đối cao nhưng vẫn giữ được độ dẻo, cho phép dễ dàng uốn cong và gia công thành nhiều dạng khác nhau. Điều này làm cho sắt trở thành một vật liệu lý tưởng cho xây dựng và chế tạo máy móc.
- Khối lượng riêng: Sắt có khối lượng riêng là \(\rho = 7.87 \, \text{g/cm}^3\), làm cho nó trở thành một trong những kim loại nặng nhưng lại dễ dàng xử lý và chế tạo.
- Nhiệt độ nóng chảy và nhiệt độ sôi: Sắt có nhiệt độ nóng chảy cao ở khoảng \[1538^\circ\text{C}\] và nhiệt độ sôi là \[2862^\circ\text{C}\], cho thấy sắt có khả năng chịu nhiệt tốt và phù hợp cho các ứng dụng yêu cầu tính chịu nhiệt cao.
- Tính dẫn điện và dẫn nhiệt: Sắt là kim loại dẫn điện và dẫn nhiệt tốt, với khả năng dẫn điện khoảng \(10 \, \text{MS/m}\). Điều này giúp sắt được sử dụng trong các ứng dụng như dây dẫn và các bộ phận truyền nhiệt.
- Từ tính: Một trong những tính chất vật lý nổi bật của sắt là tính từ tính. Sắt có thể trở thành nam châm hoặc bị hút mạnh bởi nam châm, làm cho nó hữu ích trong các ứng dụng như động cơ điện, máy phát điện và các thiết bị từ khác.
Những tính chất vật lý này làm cho sắt trở thành một kim loại không thể thiếu trong các ứng dụng công nghiệp và đời sống hàng ngày.
Tính Chất Hóa Học của Sắt
Sắt là một kim loại có tính hoạt động hóa học khá mạnh, đặc biệt khi gặp các điều kiện phù hợp. Dưới đây là các tính chất hóa học quan trọng của sắt:
- Phản ứng với oxi: Sắt dễ dàng phản ứng với oxi trong không khí để tạo ra oxit sắt. Phản ứng này có thể xảy ra ở điều kiện nhiệt độ thường, dẫn đến sự hình thành của gỉ sắt (\(\text{Fe}_2\text{O}_3\)): \[ 4\text{Fe} + 3\text{O}_2 \rightarrow 2\text{Fe}_2\text{O}_3 \]
- Phản ứng với nước: Sắt phản ứng chậm với nước lạnh nhưng phản ứng nhanh hơn khi ở nước nóng, tạo ra sắt oxit và hydro: \[ 3\text{Fe} + 4\text{H}_2\text{O} \rightarrow \text{Fe}_3\text{O}_4 + 4\text{H}_2 \]
- Phản ứng với axit: Sắt phản ứng mạnh với các axit như axit hydrochloric (\(\text{HCl}\)), tạo ra muối sắt và giải phóng khí hydro: \[ \text{Fe} + 2\text{HCl} \rightarrow \text{FeCl}_2 + \text{H}_2 \]
- Phản ứng với phi kim: Sắt có thể phản ứng với nhiều phi kim khác như lưu huỳnh để tạo ra các hợp chất như sắt(II) sunfua: \[ \text{Fe} + \text{S} \rightarrow \text{FeS} \]
- Khả năng tạo phức chất: Sắt có khả năng tạo ra nhiều phức chất với các ion và phân tử khác, đặc biệt là trong các dung dịch chứa amoniac, cyanide hoặc các chất tạo phức khác. Điều này làm sắt quan trọng trong hóa học phân tích và ứng dụng công nghiệp.
- Phản ứng oxi hóa-khử: Sắt có thể tồn tại ở nhiều trạng thái oxi hóa khác nhau, phổ biến là \(+2\) và \(+3\). Khả năng chuyển đổi giữa các trạng thái oxi hóa này làm cho sắt trở thành một chất khử mạnh trong nhiều phản ứng hóa học.
Nhờ những tính chất hóa học đặc trưng này, sắt không chỉ đóng vai trò quan trọng trong ngành công nghiệp chế tạo mà còn trong các phản ứng hóa học cơ bản và ứng dụng hàng ngày.

Sắt Trong Tự Nhiên và Công Nghiệp
Sắt là một trong những kim loại phổ biến nhất trên Trái Đất, đóng vai trò quan trọng trong tự nhiên và ngành công nghiệp. Dưới đây là chi tiết về sự phân bố và ứng dụng của sắt trong hai lĩnh vực này:
- Sắt Trong Tự Nhiên:
- Sắt tồn tại chủ yếu dưới dạng các hợp chất như hematit (\(\text{Fe}_2\text{O}_3\)), magnetit (\(\text{Fe}_3\text{O}_4\)), và siderit (\(\text{FeCO}_3\)).
- Sắt là thành phần chính của lớp vỏ Trái Đất, chiếm khoảng 5% tổng khối lượng.
- Sắt cũng có mặt trong các sinh vật sống, đóng vai trò thiết yếu trong cấu trúc của hemoglobin và myoglobin, hai protein quan trọng trong việc vận chuyển oxy.
- Trong tự nhiên, sắt thường được khai thác từ các mỏ quặng lớn và được chế biến để phục vụ cho các ngành công nghiệp khác nhau.
- Sắt Trong Công Nghiệp:
- Chế Tạo Thép: Sắt là thành phần chính trong sản xuất thép, một hợp kim quan trọng trong xây dựng và sản xuất. Thép được tạo ra bằng cách thêm các nguyên tố khác như carbon, mangan, và silic vào sắt để cải thiện các tính chất cơ học.
- Sản Xuất Máy Móc và Thiết Bị: Sắt được sử dụng rộng rãi trong chế tạo máy móc, dụng cụ, và thiết bị công nghiệp nhờ vào độ bền và tính linh hoạt.
- Công Nghiệp Ô Tô: Sắt và thép là các vật liệu chính trong chế tạo khung xe, động cơ, và các bộ phận khác của ô tô nhờ tính chịu lực cao và giá thành hợp lý.
- Ứng Dụng Trong Điện và Điện Tử: Sắt là một trong những vật liệu từ tính quan trọng, được dùng trong sản xuất nam châm, lõi biến áp, và các thiết bị điện tử.
- Gia Công Kim Loại: Sắt còn được sử dụng trong gia công kim loại để tạo ra các sản phẩm như dao, kéo, và các dụng cụ cắt gọt khác.
Sự phổ biến và đa dạng trong các ứng dụng của sắt trong tự nhiên và công nghiệp làm cho nó trở thành một kim loại không thể thiếu trong cuộc sống hàng ngày và trong sự phát triển của nhân loại.
XEM THÊM:
Vai Trò Của Sắt Trong Sinh Học
Sắt là một trong những nguyên tố vi lượng quan trọng trong cơ thể con người, đóng vai trò then chốt trong nhiều quá trình sinh học. Sắt không chỉ cần thiết cho quá trình sản xuất hemoglobin, mà còn có nhiều chức năng sinh học khác. Dưới đây là các vai trò quan trọng của sắt trong sinh học:
Sắt trong Hemoglobin
Hemoglobin là một loại protein trong hồng cầu có nhiệm vụ vận chuyển oxy từ phổi đến các tế bào trong cơ thể và mang carbon dioxide từ các tế bào trở lại phổi để thải ra ngoài. Mỗi phân tử hemoglobin chứa bốn nguyên tử sắt, và mỗi nguyên tử sắt có khả năng liên kết với một phân tử oxy, nhờ đó giúp quá trình hô hấp diễn ra hiệu quả.
- Hemoglobin giúp duy trì màu đỏ của máu và đảm bảo cơ thể nhận đủ lượng oxy cần thiết cho các hoạt động sống.
- Thiếu sắt có thể dẫn đến thiếu máu, khiến cơ thể bị mệt mỏi, suy nhược và giảm khả năng miễn dịch.
Sắt và Chức Năng Enzyme
Sắt là thành phần quan trọng của nhiều enzyme trong cơ thể, đóng vai trò xúc tác trong các phản ứng hóa học quan trọng. Các enzyme chứa sắt, như catalase và peroxidase, giúp phân giải các gốc tự do và bảo vệ tế bào khỏi tổn thương oxy hóa.
- Catalase: Một enzyme chứa sắt có khả năng phân hủy hydrogen peroxide thành nước và oxy, giúp bảo vệ tế bào khỏi các tổn thương do oxy hóa.
- Peroxidase: Một nhóm enzyme khác cũng chứa sắt, tham gia vào quá trình phân giải các chất độc hại trong tế bào.
Sắt và Chức Năng Miễn Dịch
Sắt đóng vai trò quan trọng trong hệ miễn dịch của cơ thể. Sắt cần thiết cho sự phát triển và hoạt động của các tế bào miễn dịch, như lymphocyte và macrophage, giúp cơ thể chống lại các tác nhân gây bệnh.
- Lymphocyte: Các tế bào bạch cầu cần sắt để phát triển và duy trì khả năng tấn công các vi khuẩn và virus.
- Macrophage: Sắt giúp các tế bào này tiêu diệt các tác nhân gây bệnh thông qua quá trình thực bào.
Sắt và Hệ Thần Kinh
Sắt cũng ảnh hưởng đến hệ thần kinh thông qua việc tham gia vào quá trình tổng hợp các chất dẫn truyền thần kinh như dopamine và serotonin. Thiếu sắt có thể ảnh hưởng đến chức năng não bộ, gây ra các vấn đề như mất tập trung, suy giảm trí nhớ và tâm trạng không ổn định.
- Dopamine: Một chất dẫn truyền thần kinh quan trọng trong việc kiểm soát cảm xúc và các chức năng vận động. Sắt là thành phần cần thiết để tổng hợp dopamine.
- Serotonin: Chất dẫn truyền thần kinh liên quan đến tâm trạng và cảm giác hạnh phúc. Sắt ảnh hưởng đến quá trình sản xuất serotonin trong não.
Tác dụng của Sắt đối với sức khỏe
Sắt là yếu tố không thể thiếu cho sức khỏe tổng thể. Việc duy trì mức độ sắt cân bằng trong cơ thể là cần thiết để đảm bảo các chức năng sinh học diễn ra bình thường. Tuy nhiên, thừa hay thiếu sắt đều có thể gây ra các vấn đề sức khỏe nghiêm trọng.
- Thiếu sắt: Dẫn đến thiếu máu do thiếu sắt, gây mệt mỏi, giảm sức đề kháng và ảnh hưởng đến chất lượng cuộc sống.
- Thừa sắt: Có thể gây ra tình trạng quá tải sắt, dẫn đến tổn thương các cơ quan như gan, tim, và tụy.
Do đó, việc bổ sung sắt qua chế độ ăn uống là cần thiết, đặc biệt đối với phụ nữ mang thai, trẻ em và người cao tuổi. Các thực phẩm giàu sắt bao gồm thịt đỏ, hải sản, các loại đậu và rau xanh.

Các Hợp Chất Quan Trọng Của Sắt
Sắt (Fe) là một kim loại chuyển tiếp quan trọng với nhiều ứng dụng rộng rãi trong công nghiệp và đời sống. Các hợp chất của sắt đóng vai trò thiết yếu trong nhiều quá trình hóa học và ứng dụng thực tế khác nhau. Dưới đây là một số hợp chất quan trọng của sắt và các ứng dụng của chúng.
- Hematit (Fe\(_{2}\)O\(_{3}\)): Hematit là một trong những quặng sắt phổ biến nhất, chủ yếu được sử dụng để sản xuất sắt thô và thép. Hematit có màu đỏ nâu đặc trưng và chứa khoảng 70% sắt.
- Magnetit (Fe\(_{3}\)O\(_{4}\)): Magnetit là một quặng sắt có từ tính mạnh, được sử dụng rộng rãi trong ngành sản xuất sắt thép và làm vật liệu từ. Quặng này chứa khoảng 72% sắt và thường có màu đen.
- Siderit (FeCO\(_{3}\)): Siderit là một loại quặng sắt ít phổ biến hơn nhưng vẫn được sử dụng trong sản xuất sắt và thép. Siderit chứa khoảng 48% sắt và thường được tìm thấy trong các mỏ quặng kết tinh.
- Pyrit (FeS\(_{2}\)): Mặc dù không phải là nguồn cung cấp sắt chính, pyrit (còn gọi là "vàng ngốc") thường được khai thác cho các ứng dụng trong công nghiệp hóa học và sản xuất axit sulfuric.
- Ferrit (Fe\(_{3}\)O\(_{4}\)): Ferrit là một dạng oxit sắt khác có tính từ mạnh và được sử dụng trong các ứng dụng từ tính như chế tạo lõi từ và vật liệu từ trong ngành điện tử.
Tính Chất Hóa Học và Ứng Dụng Của Sắt
Sắt có nhiều tính chất hóa học đặc biệt làm cho nó trở thành nguyên tố quan trọng trong nhiều lĩnh vực:
- Phản ứng với oxy: Sắt dễ dàng phản ứng với oxy trong không khí tạo ra oxit sắt, quá trình này là nguyên nhân chính của hiện tượng gỉ sét. Phản ứng có thể được mô tả như sau: \[4Fe + 3O_2 \rightarrow 2Fe_2O_3\]
- Khả năng tạo hợp kim: Sắt có thể kết hợp với các nguyên tố khác như carbon để tạo ra các hợp kim quan trọng như thép và gang, có tính ứng dụng cao trong xây dựng và công nghiệp chế tạo máy móc.
- Phản ứng với axit: Sắt phản ứng mạnh với các axit mạnh như axit clohydric (HCl) để tạo ra muối sắt và khí hydro: \[Fe + 2HCl \rightarrow FeCl_2 + H_2\]
Ứng Dụng Thực Tiễn Của Sắt Và Các Hợp Chất Của Nó
Sắt và các hợp chất của sắt được ứng dụng trong nhiều lĩnh vực khác nhau nhờ vào tính chất đa dạng của nó:
- Xây dựng: Sắt và thép được sử dụng làm vật liệu xây dựng chính cho cầu, tòa nhà và các công trình cơ sở hạ tầng khác.
- Công nghiệp ô tô: Sắt và thép là vật liệu quan trọng trong chế tạo khung xe và các bộ phận cơ khí.
- Điện tử: Nhờ vào tính dẫn điện và từ tính, sắt được sử dụng trong các thiết bị điện tử và linh kiện từ tính.
- Y học: Sắt là thành phần chính trong hemoglobin, một protein chịu trách nhiệm vận chuyển oxy trong máu.
Sắt là một nguyên tố quan trọng không chỉ trong công nghiệp mà còn trong đời sống hàng ngày. Với khả năng tái chế cao, việc sử dụng sắt góp phần bảo vệ môi trường và tiết kiệm tài nguyên thiên nhiên.

Những Lưu Ý Khi Sử Dụng Sắt
Sắt là một nguyên tố hóa học quan trọng trong cơ thể và có vai trò thiết yếu trong nhiều quá trình sinh học, nhưng việc sử dụng sắt không đúng cách có thể dẫn đến những tác dụng phụ nghiêm trọng. Dưới đây là một số lưu ý quan trọng khi sử dụng sắt để đảm bảo an toàn và hiệu quả:
- Không tự ý bổ sung sắt: Việc bổ sung sắt cần tuân thủ theo chỉ định của bác sĩ hoặc chuyên gia y tế, đặc biệt trong các trường hợp thiếu máu do thiếu sắt. Tự ý bổ sung có thể gây thừa sắt, dẫn đến tình trạng nhiễm độc sắt, ảnh hưởng đến gan và các cơ quan khác.
- Kết hợp với vitamin C: Sắt hấp thụ tốt hơn khi kết hợp với vitamin C. Do đó, nên sử dụng sắt cùng với các thực phẩm giàu vitamin C như cam, chanh, kiwi, hoặc bổ sung vitamin C theo hướng dẫn của bác sĩ.
- Tránh dùng cùng với các chất ức chế hấp thu sắt: Các thực phẩm chứa tanin (trà, cà phê), canxi (sữa, sản phẩm từ sữa) hoặc các loại thuốc kháng axit có thể giảm khả năng hấp thu sắt. Nên tránh dùng sắt cùng lúc với các loại thực phẩm và thuốc này.
- Chú ý liều lượng: Việc bổ sung sắt cần đúng liều lượng theo chỉ định để tránh tình trạng thừa sắt. Một lượng thừa sắt có thể gây ra các triệu chứng như buồn nôn, đau bụng, táo bón, hoặc nguy hiểm hơn là ngộ độc sắt.
- Thời điểm sử dụng: Sắt thường được khuyến cáo uống khi bụng đói để tăng khả năng hấp thu, tuy nhiên nếu gặp các vấn đề về dạ dày, có thể uống sau bữa ăn để giảm kích ứng dạ dày. Cần tham khảo ý kiến bác sĩ để xác định thời điểm sử dụng phù hợp.
- Theo dõi sức khỏe: Trong quá trình bổ sung sắt, cần theo dõi các dấu hiệu bất thường của cơ thể và đi khám định kỳ để kiểm tra mức độ sắt trong máu, đảm bảo sử dụng đúng liều lượng và an toàn.
Sắt là một vi chất dinh dưỡng cần thiết nhưng việc sử dụng phải cẩn trọng để tránh các nguy cơ tiềm ẩn. Hãy luôn tuân thủ hướng dẫn của bác sĩ và duy trì chế độ ăn uống cân bằng để đảm bảo sức khỏe tốt nhất.