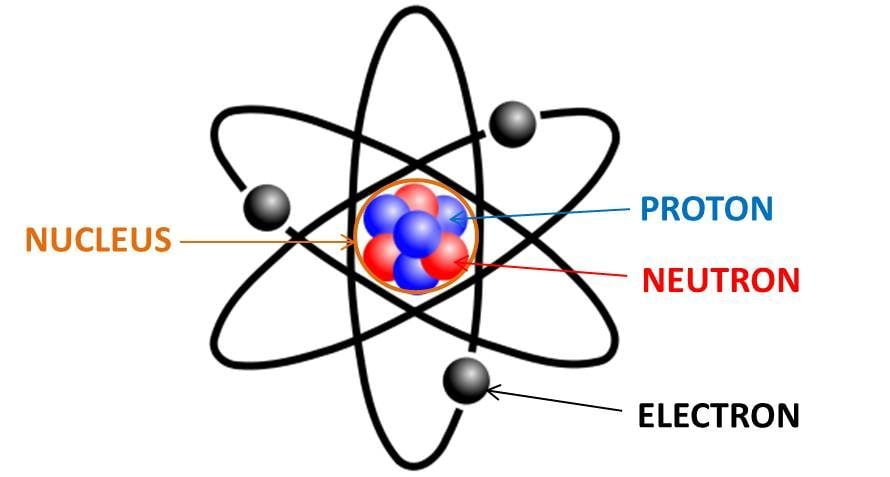
Chủ đề nguyên tử aluminium gồm 13 proton và 14 neutron: Nguyên tử aluminium gồm 13 proton và 14 neutron là nền tảng quan trọng giúp chúng ta hiểu rõ hơn về tính chất hóa học và vật lý của nhôm. Trong bài viết này, bạn sẽ khám phá cấu trúc của nguyên tử aluminium, các ứng dụng thực tiễn và vai trò quan trọng của nhôm trong nhiều lĩnh vực khác nhau.
Mục lục
Cấu Tạo Nguyên Tử Aluminium
Nguyên tử aluminium (nhôm) có cấu trúc hạt nhân bao gồm 13 proton và 14 neutron. Số proton quyết định số hiệu nguyên tử của aluminium, trong khi neutron giúp ổn định hạt nhân. Nhôm thuộc nhóm kim loại, là nguyên tố phổ biến thứ ba trong vỏ Trái Đất.
Hạt Nhân Nguyên Tử
Hạt nhân của nguyên tử aluminium chứa:
- \(13\) proton: Mang điện tích dương (+), quyết định số hiệu nguyên tử và tính chất hóa học của aluminium.
- \(14\) neutron: Các hạt không mang điện, đóng vai trò ổn định hạt nhân.
Cấu Hình Electron
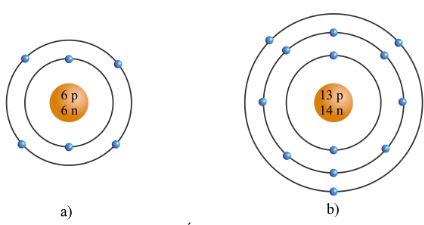
Nguyên tử aluminium có 13 electron được phân bổ theo các lớp vỏ năng lượng:
- Lớp \(K\) chứa \(2\) electron
- Lớp \(L\) chứa \(8\) electron
- Lớp \(M\) chứa \(3\) electron
Theo cấu hình electron: \(1s^2 2s^2 2p^6 3s^2 3p^1\).
Mô Hình Nguyên Tử
Mô hình Bohr của nguyên tử aluminium mô tả các electron chuyển động quanh hạt nhân theo quỹ đạo xác định:
- Các electron ở gần hạt nhân có năng lượng thấp, và năng lượng tăng dần khi electron ở xa hạt nhân.
- Nguyên tử aluminium có tổng cộng \(13\) electron, với 3 electron ở lớp vỏ ngoài cùng quyết định khả năng tham gia phản ứng hóa học.
Tính Chất Vật Lý Của Aluminium
Nhôm là một kim loại có các đặc tính vật lý nổi bật:
- Khối lượng riêng: \(2.7 \, \text{g/cm}^3\)
- Nhiệt độ nóng chảy: \(660^\circ \text{C}\)
- Nhiệt độ sôi: \(2519^\circ \text{C}\)
- Độ dẫn điện và nhiệt tốt
- Dễ tái chế và chống ăn mòn nhờ lớp oxit tự nhiên
Tính Chất Hóa Học Của Aluminium
Nhôm phản ứng mạnh với nhiều phi kim và axit:
- Phản ứng với clo: \(2Al + 3Cl_2 \rightarrow 2AlCl_3\)
- Phản ứng với axit HCl: \(2Al + 6HCl \rightarrow 2AlCl_3 + 3H_2\)
- Phản ứng với dung dịch bazơ: Nhôm tác dụng với dung dịch kiềm tạo thành \(\text{Al(OH)}_4^-\).
Ứng Dụng Thực Tế Của Aluminium
Với các tính chất hóa học và vật lý đặc biệt, nhôm được sử dụng rộng rãi trong các ngành:
- Xây dựng: Nhôm được dùng làm khung cửa, mái nhà và các kết cấu nhẹ.
- Hàng không: Nhôm có trọng lượng nhẹ, bền và chịu lực tốt, lý tưởng cho các cấu trúc máy bay.
- Công nghiệp điện: Độ dẫn điện cao giúp nhôm được sử dụng trong dây dẫn điện.
- Sản xuất bao bì: Nhôm có tính chống ăn mòn và dễ tái chế, thường được dùng làm vỏ hộp, lá nhôm bao gói thực phẩm.
Mô Hình Nguyên Tử Theo Mathjax
Công thức mô tả số proton, neutron và electron trong nguyên tử aluminium:
- Số proton: \(13 \, \text{proton}\)
- Số neutron: \(14 \, \text{neutron}\)
- Số electron: \(13 \, \text{electron}\)
Cấu hình electron có thể viết dưới dạng:
\[ 1s^2 2s^2 2p^6 3s^2 3p^1 \]
Kết Luận
Nguyên tử aluminium với \(13\) proton và \(14\) neutron có vai trò quan trọng trong đời sống và công nghiệp. Sự hiểu biết về cấu tạo và tính chất của nhôm giúp chúng ta ứng dụng hiệu quả kim loại này trong nhiều lĩnh vực khác nhau.

Mục Lục
-
Cấu Tạo Nguyên Tử Aluminium
- 13 Proton và 14 Neutron
- Vị Trí Của Aluminium Trong Bảng Tuần Hoàn
- Tương Quan Giữa Proton, Neutron và Electron
-
Tính Chất Hóa Học và Vật Lý Của Aluminium
- Tính Chất Hóa Học
- Tính Chất Vật Lý
- Khả Năng Phản Ứng
-
Ứng Dụng Của Aluminium Trong Thực Tiễn
- Ứng Dụng Trong Công Nghiệp
- Ứng Dụng Trong Đời Sống Hằng Ngày
-
Cách Tính Khối Lượng Của Nguyên Tử Aluminium
- Công Thức Tính Khối Lượng Proton, Neutron
- Ứng Dụng Công Thức Trong Thực Tế
-
Vai Trò Của Aluminium Trong Ngành Xây Dựng
- Nhôm Làm Vật Liệu Xây Dựng
- Độ Bền Và Tính Chịu Lực Của Nhôm
Cấu tạo của nguyên tử aluminium
Nguyên tử aluminium, còn được biết đến với ký hiệu hóa học là \( \text{Al} \), có số nguyên tử là 13. Cấu tạo của nguyên tử này gồm ba loại hạt cơ bản: proton, neutron và electron. Dưới đây là mô tả chi tiết về các hạt này trong nguyên tử aluminium:
- Proton: Nguyên tử aluminium có 13 proton, mang điện tích dương (\(+\)) và nằm ở hạt nhân của nguyên tử.
- Neutron: Số neutron trong nguyên tử aluminium là 14, chúng không mang điện tích và cũng nằm ở hạt nhân, cùng với proton.
- Electron: Nguyên tử aluminium có 13 electron, mang điện tích âm (\(-\)) và quay xung quanh hạt nhân theo các lớp vỏ electron.
Công thức cấu tạo của nguyên tử aluminium có thể được biểu diễn như sau:
Với cấu tạo này, aluminium là một nguyên tố kim loại nhẹ, có nhiều ứng dụng trong công nghiệp nhờ tính chất đặc trưng như độ bền cao và khả năng dẫn nhiệt, dẫn điện tốt.

Khối lượng của các hạt trong nguyên tử aluminium
Nguyên tử aluminium có cấu tạo từ ba loại hạt chính: proton, neutron và electron. Mỗi loại hạt này có khối lượng cụ thể và đóng vai trò quan trọng trong tính chất vật lý của nguyên tử. Dưới đây là chi tiết về khối lượng của từng hạt:
- Proton: Proton có khối lượng xấp xỉ \(1.6726 \times 10^{-27} \, \text{kg}\). Trong nguyên tử aluminium, có 13 proton tạo ra tổng khối lượng của phần này là:
- Neutron: Neutron có khối lượng xấp xỉ \(1.6749 \times 10^{-27} \, \text{kg}\). Aluminium có 14 neutron, do đó tổng khối lượng của neutron là:
- Electron: Khối lượng của electron rất nhỏ so với proton và neutron, xấp xỉ \(9.1094 \times 10^{-31} \, \text{kg}\). Với 13 electron, tổng khối lượng của phần này là:
\[
13 \times 1.6726 \times 10^{-27} \, \text{kg} \approx 2.17438 \times 10^{-26} \, \text{kg}
\]
\[
14 \times 1.6749 \times 10^{-27} \, \text{kg} \approx 2.34486 \times 10^{-26} \, \text{kg}
\]
\[
13 \times 9.1094 \times 10^{-31} \, \text{kg} \approx 1.18422 \times 10^{-29} \, \text{kg}
\]
Tổng khối lượng của nguyên tử aluminium chủ yếu đến từ proton và neutron, vì khối lượng của electron rất nhỏ. Khối lượng tổng cộng có thể được ước tính bằng cách cộng khối lượng của tất cả các hạt trong hạt nhân:
Khối lượng tổng của nguyên tử aluminium xấp xỉ \(4.519 \times 10^{-26} \, \text{kg}\).
Tính chất vật lý của nhôm
Nhôm (Aluminium) là một kim loại có nhiều đặc điểm vật lý nổi bật, nhờ đó nó được ứng dụng rộng rãi trong nhiều ngành công nghiệp. Dưới đây là các tính chất vật lý quan trọng của nhôm:
- Màu sắc: Nhôm có màu trắng bạc sáng bóng, mang lại vẻ ngoài sáng và thẩm mỹ cao.
- Tỉ trọng: Nhôm có khối lượng riêng là \[2.7 \, \text{g/cm}^3\], giúp nó trở thành một kim loại nhẹ so với các kim loại khác như sắt hay đồng.
- Điểm nóng chảy: Nhôm có nhiệt độ nóng chảy khoảng \[660.3^\circ C\] (933.5 K), thấp hơn nhiều so với các kim loại như sắt (\[1538^\circ C\]).
- Tính dẫn điện: Nhôm là chất dẫn điện tốt, có điện trở suất thấp, chỉ đứng sau đồng trong khả năng dẫn điện, giúp nó được sử dụng trong các ứng dụng liên quan đến dây dẫn.
- Tính dẫn nhiệt: Nhôm có khả năng dẫn nhiệt cao, làm cho nó trở thành vật liệu lý tưởng cho các sản phẩm liên quan đến tản nhiệt như tản nhiệt máy tính, bộ trao đổi nhiệt.
- Tính chất dẻo: Nhôm rất mềm và dẻo, có thể dễ dàng được gia công thành các hình dạng khác nhau qua các quá trình như cán, đúc, và rèn.
- Khả năng chống ăn mòn: Nhôm tạo ra một lớp oxide bề mặt tự nhiên (Al₂O₃), giúp bảo vệ nó khỏi quá trình oxi hóa và ăn mòn trong không khí hoặc nước.
Nhờ những tính chất vật lý này, nhôm là vật liệu quan trọng trong nhiều lĩnh vực như xây dựng, giao thông, điện tử và công nghiệp hàng không.

Ứng dụng và tính chất hóa học của aluminium
Nhôm (Aluminium) không chỉ nổi bật với các tính chất vật lý mà còn có những tính chất hóa học quan trọng, nhờ đó được ứng dụng rộng rãi trong nhiều lĩnh vực đời sống và công nghiệp.
Ứng dụng của aluminium
- Xây dựng: Nhôm là vật liệu phổ biến trong ngành xây dựng, được sử dụng trong các khung cửa sổ, mái che, và các kết cấu chịu lực nhờ vào tính nhẹ và bền.
- Công nghiệp ô tô và hàng không: Nhờ vào khối lượng nhẹ và độ bền cao, nhôm được sử dụng trong việc chế tạo thân xe, máy bay và các bộ phận chịu lực khác.
- Ngành điện tử: Nhôm có khả năng dẫn điện tốt, được sử dụng trong dây dẫn điện, linh kiện điện tử và các tấm tản nhiệt.
- Đồ gia dụng: Nhôm còn được sử dụng trong sản xuất đồ gia dụng như nồi, chảo, và các dụng cụ nấu ăn nhờ tính dẫn nhiệt cao và khả năng chống ăn mòn.
- Bao bì: Nhôm là nguyên liệu chính trong sản xuất lon nước giải khát và các sản phẩm bao bì khác nhờ đặc tính không thấm khí và nhẹ.
Tính chất hóa học của aluminium
- Tác dụng với phi kim: Nhôm phản ứng với oxy trong không khí, tạo ra lớp oxide nhôm \(\text{Al}_2\text{O}_3\), bảo vệ kim loại khỏi sự ăn mòn tiếp tục.
- Tác dụng với axit: Nhôm phản ứng mạnh với axit clohydric (HCl) để tạo ra khí hydro và muối nhôm: \[ 2Al + 6HCl \rightarrow 2AlCl_3 + 3H_2 \]
- Tác dụng với bazơ: Nhôm phản ứng với dung dịch kiềm mạnh như natri hydroxide (NaOH), tạo ra muối natri aluminat và khí hydro: \[ 2Al + 2NaOH + 6H_2O \rightarrow 2Na[Al(OH)_4] + 3H_2 \]
- Khả năng khử: Nhôm có tính khử mạnh, có thể khử các oxit kim loại khác thành kim loại nguyên chất trong quá trình nhiệt luyện, như phản ứng với oxit sắt: \[ 2Al + Fe_2O_3 \rightarrow 2Fe + Al_2O_3 \]
Nhờ vào tính chất hóa học đa dạng và khả năng phản ứng với nhiều hợp chất khác, nhôm có vai trò quan trọng trong công nghiệp hóa chất và sản xuất vật liệu tiên tiến.
XEM THÊM:
Vai trò của nhôm trong công nghiệp và đời sống
Nhôm là một kim loại nhẹ và có tính ứng dụng cao trong nhiều ngành công nghiệp và đời sống hàng ngày nhờ vào các tính chất vật lý và hóa học đặc biệt của nó. Dưới đây là các vai trò quan trọng của nhôm:
- Ngành công nghiệp xây dựng:
Nhôm được sử dụng phổ biến trong xây dựng do độ bền cao, khả năng chống ăn mòn, và trọng lượng nhẹ. Các cấu trúc như cửa sổ, cửa ra vào, tấm ốp tường, và khung nhà thường được làm từ nhôm, giúp giảm tải trọng và tăng tính thẩm mỹ cho công trình.
- Công nghiệp hàng không vũ trụ:
Nhôm là vật liệu lý tưởng cho ngành hàng không vũ trụ nhờ vào tỷ trọng thấp và khả năng chịu lực tốt. Nó được sử dụng để chế tạo các bộ phận máy bay như cánh, khung máy bay, và các thành phần khác giúp tối ưu hóa trọng lượng mà vẫn đảm bảo độ bền và an toàn.
- Ngành điện và điện tử:
Với khả năng dẫn điện tốt, nhôm thường được dùng để sản xuất dây điện, các thành phần của bảng mạch, và thiết bị điện tử. Khả năng dẫn điện chỉ đứng sau bạc và đồng nhưng nhôm có giá thành thấp hơn, nên được sử dụng rộng rãi trong sản xuất các thiết bị điện gia dụng và công nghiệp.
- Ngành bao bì:
Nhôm có khả năng chống thấm, chống oxy hóa tốt, và dễ dàng tái chế, nên được sử dụng rộng rãi trong sản xuất bao bì thực phẩm, đồ uống, và dược phẩm. Nhôm góp phần bảo quản sản phẩm tốt hơn, kéo dài thời gian sử dụng và đảm bảo an toàn vệ sinh thực phẩm.
- Sản phẩm gia dụng:
Nhôm được sử dụng trong nhiều sản phẩm gia dụng như nồi, chảo, và các vật dụng nhà bếp khác nhờ vào khả năng dẫn nhiệt tốt, nhẹ và bền. Ngoài ra, nhôm còn có khả năng chống gỉ sét, giúp các sản phẩm này duy trì tuổi thọ lâu dài.
- Tái chế và bảo vệ môi trường:
Nhôm là một trong những kim loại dễ tái chế nhất mà không mất đi các tính chất vật lý và hóa học ban đầu. Việc tái chế nhôm giúp tiết kiệm năng lượng và tài nguyên thiên nhiên, đồng thời giảm thiểu tác động đến môi trường.