Chủ đề khối lượng nguyên tử oxi: Khối lượng nguyên tử oxi đóng vai trò quan trọng trong nhiều lĩnh vực khoa học và công nghiệp. Bài viết này sẽ cung cấp cái nhìn tổng quan và chi tiết về khối lượng nguyên tử của oxi, ứng dụng của nó trong hóa học, sinh học, và công nghiệp, cùng với các công thức tính toán và nghiên cứu mới nhất. Hãy cùng khám phá những thông tin hữu ích và cập nhật nhất về chủ đề này.
Mục lục
Khối lượng nguyên tử oxi
Khối lượng nguyên tử oxi là một thông số quan trọng trong hóa học và vật lý học. Dưới đây là thông tin chi tiết về khối lượng nguyên tử oxi và ứng dụng của nó trong các lĩnh vực khác nhau.
1. Định nghĩa
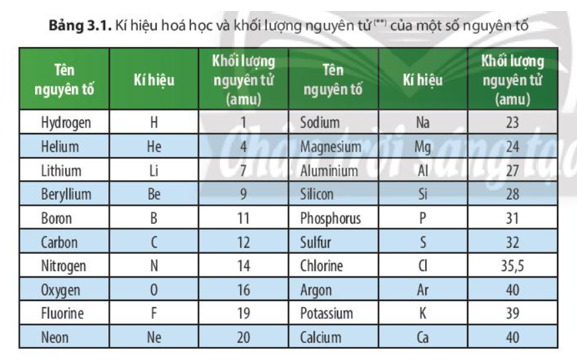
Khối lượng nguyên tử của oxi là khối lượng của một nguyên tử oxi, được tính bằng đơn vị khối lượng nguyên tử (amu). Đối với oxi, khối lượng nguyên tử là khoảng 15.999 amu.
2. Công thức hóa học và ứng dụng
Oxi là một nguyên tố hóa học thiết yếu, có công thức hóa học là O. Nó là thành phần chính trong không khí và có vai trò quan trọng trong quá trình hô hấp và quá trình cháy.
3. Khối lượng nguyên tử trong các hợp chất
Trong các hợp chất, khối lượng nguyên tử của oxi ảnh hưởng đến khối lượng phân tử của các hợp chất. Ví dụ:
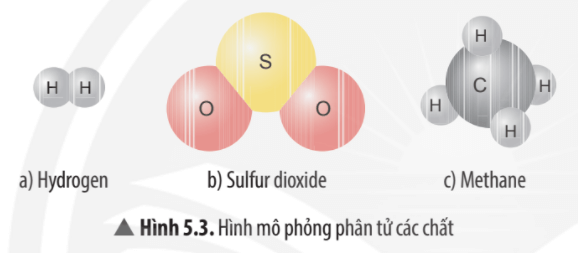
- Trong nước (H2O), oxi chiếm một phần quan trọng trong khối lượng phân tử.
- Trong carbon dioxide (CO2), oxi cũng đóng góp vào khối lượng phân tử của hợp chất này.
4. Bảng tổng hợp
| Nguyên tố | Khối lượng nguyên tử (amu) |
|---|---|
| Oxi | 15.999 |
5. Công thức và tính toán
Khối lượng nguyên tử của oxi có thể được sử dụng trong các tính toán hóa học. Công thức tính toán khối lượng phân tử của một hợp chất có chứa oxi là:
\[ M = \sum (n_i \times m_i) \]
Trong đó, \( M \) là khối lượng phân tử, \( n_i \) là số lượng nguyên tử của nguyên tố i, và \( m_i \) là khối lượng nguyên tử của nguyên tố i.

1. Giới thiệu về Khối lượng Nguyên tử Oxi
Khối lượng nguyên tử oxi là một chỉ số quan trọng trong hóa học và vật lý, cho biết khối lượng của một nguyên tử oxi so với khối lượng của nguyên tử carbon. Đây là một thông số cơ bản để hiểu về sự tương tác của oxi trong các phản ứng hóa học và các quá trình sinh học.
1.1. Định nghĩa và Giá trị Khối lượng Nguyên tử Oxi
Khối lượng nguyên tử của oxi được định nghĩa là khối lượng của một nguyên tử oxi so với khối lượng của nguyên tử carbon. Đơn vị của khối lượng nguyên tử là amu (atomic mass unit). Giá trị của khối lượng nguyên tử oxi là khoảng 15.999 amu.
1.2. Ý nghĩa của Khối lượng Nguyên tử Oxi
- Trong Hóa học: Khối lượng nguyên tử oxi là cơ sở để tính toán khối lượng phân tử của các hợp chất chứa oxi, như nước (H2O) và carbon dioxide (CO2).
- Trong Sinh học: Oxi đóng vai trò quan trọng trong quá trình hô hấp của sinh vật, và khối lượng nguyên tử của nó ảnh hưởng đến các phản ứng sinh hóa trong cơ thể.
- Trong Công nghiệp: Các ứng dụng công nghiệp như sản xuất thép và các phản ứng hóa học khác đều dựa vào giá trị khối lượng nguyên tử để tính toán và điều chỉnh quy trình.
1.3. Công thức và Tính toán
Để tính khối lượng phân tử của các hợp chất chứa oxi, ta có thể sử dụng công thức:
\[ M = \sum (n_i \times m_i) \]
Trong đó:
- \( M \) là khối lượng phân tử của hợp chất.
- \( n_i \) là số lượng nguyên tử của nguyên tố i trong hợp chất.
- \( m_i \) là khối lượng nguyên tử của nguyên tố i.
1.4. Bảng Tổng hợp
| Nguyên tố | Khối lượng Nguyên tử (amu) |
|---|---|
| Oxi | 15.999 |
2. Các Thông số Khoa học về Oxi
Oxi là một nguyên tố hóa học quan trọng với nhiều thông số khoa học cần được hiểu rõ. Dưới đây là các thông số chính liên quan đến oxi, từ khối lượng nguyên tử đến các đặc tính vật lý và hóa học của nó.
2.1. Khối lượng Nguyên tử và Khối lượng Phân tử
Khối lượng nguyên tử của oxi là khoảng 15.999 amu. Khối lượng phân tử của các hợp chất chứa oxi được tính bằng tổng khối lượng nguyên tử của tất cả các nguyên tử trong phân tử đó.
Công thức tính khối lượng phân tử là:
\[ M = \sum (n_i \times m_i) \]
2.2. Tính Chất Vật Lý của Oxi
- Điểm nóng chảy: -218.79°C
- Điểm sôi: -182.96°C
- Khối lượng riêng: 0.00143 g/cm³ (ở điều kiện tiêu chuẩn)
- Trạng thái: Ở điều kiện thường, oxi là khí không màu, không mùi và không vị.
2.3. Tính Chất Hóa Học của Oxi
Oxi là một nguyên tố hóa học rất phản ứng và đóng vai trò quan trọng trong nhiều phản ứng hóa học, bao gồm:
- Phản ứng oxy hóa: Oxi phản ứng với hầu hết các nguyên tố để tạo thành oxit.
- Phản ứng với nước: Oxi phản ứng với nước để tạo ra các oxit axit, như H2O trong trường hợp với hydrogen.
- Quá trình hô hấp: Oxi là thành phần chính trong quá trình hô hấp của các sinh vật sống.
2.4. Bảng Thông số Khoa học
| Thông số | Giá trị |
|---|---|
| Khối lượng Nguyên tử | 15.999 amu |
| Điểm nóng chảy | -218.79°C |
| Điểm sôi | -182.96°C |
| Khối lượng riêng | 0.00143 g/cm³ |

3. Ứng dụng của Khối lượng Nguyên tử Oxi
Khối lượng nguyên tử oxi không chỉ là một thông số khoa học quan trọng mà còn có nhiều ứng dụng thiết thực trong đời sống và các lĩnh vực công nghiệp. Dưới đây là các ứng dụng chính của khối lượng nguyên tử oxi.
3.1. Trong Hóa học
Khối lượng nguyên tử oxi được sử dụng để tính toán khối lượng phân tử của các hợp chất chứa oxi. Điều này là cần thiết trong các phản ứng hóa học để xác định tỷ lệ và lượng chất phản ứng cần thiết.
- Chế tạo hợp chất: Tính toán chính xác khối lượng nguyên tử giúp trong việc chế tạo các hợp chất hóa học như nước (H2O), axit sulfuric (H2SO4), và nhiều hợp chất khác.
- Phản ứng oxy hóa: Sử dụng trong các phản ứng oxy hóa để hiểu và dự đoán sự hình thành của các oxit và phản ứng hóa học liên quan.
3.2. Trong Sinh học
Oxi là yếu tố quan trọng trong quá trình sinh học và khối lượng nguyên tử của nó ảnh hưởng đến các quá trình này.
- Quá trình hô hấp: Oxi tham gia vào quá trình hô hấp của các sinh vật, trong đó khối lượng nguyên tử của oxi ảnh hưởng đến việc sản xuất năng lượng từ glucose.
- Chuyển hóa tế bào: Oxi đóng vai trò quan trọng trong các phản ứng chuyển hóa tế bào, ảnh hưởng đến sự sống của các tế bào và cơ thể sinh vật.
3.3. Trong Công nghiệp
Khối lượng nguyên tử oxi cũng có các ứng dụng quan trọng trong ngành công nghiệp, bao gồm:
- Quá trình sản xuất thép: Oxi được sử dụng trong các lò luyện để loại bỏ các tạp chất và cải thiện chất lượng thép.
- Sản xuất hóa chất: Khối lượng nguyên tử của oxi là cơ sở để tính toán và kiểm soát các phản ứng hóa học trong quá trình sản xuất các hóa chất như axit nitric và oxy già.
- Công nghệ y tế: Oxi được sử dụng trong các thiết bị hỗ trợ hô hấp và điều trị các bệnh lý liên quan đến hô hấp.
3.4. Bảng Tổng hợp Ứng dụng
| Lĩnh vực | Ứng dụng |
|---|---|
| Hóa học | Tính toán khối lượng phân tử, phản ứng oxy hóa |
| Sinh học | Quá trình hô hấp, chuyển hóa tế bào |
| Công nghiệp | Sản xuất thép, hóa chất, công nghệ y tế |

4. Công thức và Phương pháp Tính toán
Việc tính toán khối lượng nguyên tử oxi và các liên quan đến nó là rất quan trọng trong hóa học và vật lý học. Dưới đây là các công thức và phương pháp cơ bản để thực hiện các tính toán này.
4.1. Công thức Tính khối lượng nguyên tử
Khối lượng nguyên tử của oxi được xác định bằng cách sử dụng các phương pháp phân tích quang phổ hoặc khối phổ. Đơn vị khối lượng nguyên tử là amu (atomic mass unit), và giá trị của khối lượng nguyên tử oxi là khoảng 15.999 amu.
4.2. Tính khối lượng phân tử
Khối lượng phân tử của một hợp chất chứa oxi được tính bằng tổng khối lượng nguyên tử của tất cả các nguyên tử trong phân tử đó. Công thức tính khối lượng phân tử là:
\[ M = \sum (n_i \times m_i) \]
Trong đó:
- \( M \) là khối lượng phân tử của hợp chất.
- \( n_i \) là số lượng nguyên tử của nguyên tố i trong hợp chất.
- \( m_i \) là khối lượng nguyên tử của nguyên tố i.
4.3. Ví dụ Tính toán
Dưới đây là ví dụ tính toán khối lượng phân tử của nước (H2O):
- Khối lượng nguyên tử của H là 1.008 amu.
- Khối lượng nguyên tử của O là 15.999 amu.
Công thức tính khối lượng phân tử của nước là:
\[ M_{\text{H}_2\text{O}} = (2 \times 1.008) + (1 \times 15.999) = 18.015 \text{ amu} \]
4.4. Tính khối lượng của một lượng chất cụ thể
Để tính khối lượng của một lượng chất cụ thể chứa oxi, bạn có thể sử dụng công thức sau:
\[ m = n \times M \]
Trong đó:
- \( m \) là khối lượng của lượng chất.
- \( n \) là số mol của chất.
- \( M \) là khối lượng molar của chất.
4.5. Bảng Tổng hợp Công thức
| Công thức | Giải thích |
|---|---|
| \[ M = \sum (n_i \times m_i) \] | Tính khối lượng phân tử |
| \[ m = n \times M \] | Tính khối lượng của lượng chất cụ thể |

5. Nghiên cứu và Phân tích Nâng cao
Khối lượng nguyên tử oxi là một lĩnh vực nghiên cứu quan trọng trong hóa học và vật lý học. Nghiên cứu và phân tích nâng cao không chỉ giúp hiểu rõ hơn về các tính chất cơ bản mà còn khám phá các ứng dụng và ảnh hưởng của oxi trong các lĩnh vực khác nhau.
5.1. Nghiên cứu về Định lượng Khối lượng Nguyên tử
Các nghiên cứu về khối lượng nguyên tử oxi thường sử dụng các phương pháp phân tích chính xác như:
- Khối phổ (Mass Spectrometry): Phương pháp này giúp xác định khối lượng của các nguyên tử và phân tử với độ chính xác cao.
- Quang phổ hấp thụ nguyên tử (Atomic Absorption Spectroscopy): Dùng để đo lường sự hấp thụ ánh sáng của nguyên tử trong mẫu để xác định nồng độ của oxi.
5.2. Phân tích Isotop của Oxi
Oxi có ba đồng vị ổn định chính: O-16, O-17 và O-18. Phân tích isotop của oxi giúp hiểu rõ hơn về các quá trình sinh học và địa chất:
- O-16: Là đồng vị phổ biến nhất, chiếm khoảng 99.76% tổng số nguyên tử oxi trong tự nhiên.
- O-17: Chiếm khoảng 0.04%, đóng vai trò quan trọng trong nghiên cứu khí quyển và các quá trình sinh học.
- O-18: Chiếm khoảng 0.20%, được sử dụng trong nghiên cứu khí hậu và địa chất để xác định lịch sử khí hậu.
5.3. Ứng dụng trong Nghiên cứu Khoa học Mới
Khối lượng nguyên tử oxi và các đồng vị của nó có ứng dụng trong các nghiên cứu khoa học mới:
- Nghiên cứu sinh học: Phân tích các quá trình sinh học và sự chuyển hóa trong cơ thể sống, bao gồm nghiên cứu về hô hấp và sự trao đổi chất.
- Khoa học môi trường: Theo dõi sự biến đổi khí quyển và môi trường bằng cách phân tích đồng vị của oxi trong các mẫu khí và nước.
- Vật lý học: Nghiên cứu các tính chất vật lý của oxi dưới các điều kiện khác nhau, như trong các thí nghiệm vật lý hạt nhân.
5.4. Bảng Tổng hợp Nghiên cứu
| Lĩnh vực | Chi tiết |
|---|---|
| Khối phổ | Xác định khối lượng nguyên tử và phân tử với độ chính xác cao |
| Quang phổ hấp thụ nguyên tử | Đo lường sự hấp thụ ánh sáng để xác định nồng độ oxi |
| Đồng vị | Phân tích O-16, O-17, và O-18 trong các nghiên cứu sinh học và môi trường |
| Nghiên cứu khoa học mới | Ứng dụng trong nghiên cứu sinh học, môi trường, và vật lý học |
XEM THÊM:
6. Tài liệu Tham khảo và Nguồn thông tin
Để nghiên cứu và hiểu rõ hơn về khối lượng nguyên tử oxi, bạn có thể tham khảo các tài liệu và nguồn thông tin sau:
-
6.1. Sách và Tài liệu Khoa học
- Sách: "Hóa học đại cương" - Tác giả: Nguyễn Văn Bảy
Sách cung cấp các kiến thức cơ bản về hóa học, bao gồm khối lượng nguyên tử của các nguyên tố và ứng dụng của chúng trong hóa học.
- Sách: "Vật lý hóa học" - Tác giả: Lê Thị Hòa
Tài liệu chi tiết về các nguyên tố hóa học, bao gồm khối lượng nguyên tử của oxi và các phương pháp tính toán liên quan.
- Sách: "Hóa học đại cương" - Tác giả: Nguyễn Văn Bảy
-
6.2. Các Nghiên cứu và Bài báo
- Bài báo: "Khối lượng nguyên tử và ứng dụng trong phân tích hóa học" - Tạp chí Hóa học Việt Nam, 2023
Bài báo này tập trung vào việc phân tích và tính toán khối lượng nguyên tử của oxi, cùng với các ứng dụng trong phân tích hóa học.
- Nghiên cứu: "Ảnh hưởng của khối lượng nguyên tử đến phản ứng hóa học" - Tạp chí Nghiên cứu Khoa học, 2024
Nghiên cứu này đề cập đến sự ảnh hưởng của khối lượng nguyên tử của oxi trong các phản ứng hóa học và cách nó có thể ảnh hưởng đến kết quả của các thí nghiệm.
- Bài báo: "Khối lượng nguyên tử và ứng dụng trong phân tích hóa học" - Tạp chí Hóa học Việt Nam, 2023