Chủ đề bảng khối lượng nguyên tử lớp 8: Bảng khối lượng nguyên tử lớp 8 là công cụ học tập quan trọng, giúp học sinh nắm vững khái niệm cơ bản về khối lượng các nguyên tố hóa học. Khám phá bảng khối lượng nguyên tử để hiểu rõ hơn về các nguyên tố, ứng dụng trong tính toán hóa học, và cách thức giảng dạy hiệu quả. Bài viết cung cấp thông tin chi tiết và hướng dẫn thực hành hữu ích cho học tập và nghiên cứu.
Mục lục
- Thông Tin Về Bảng Khối Lượng Nguyên Tử Lớp 8
- Tổng Quan Về Bảng Khối Lượng Nguyên Tử
- Chi Tiết Các Nguyên Tố Hóa Học
- Các Thành Phần Của Bảng Khối Lượng Nguyên Tử
- Danh Sách Các Nguyên Tố Phổ Biến
- Ứng Dụng Trong Hóa Học
- Hướng Dẫn Sử Dụng Bảng Khối Lượng Nguyên Tử
- Tài Nguyên Tham Khảo
- Ứng Dụng Của Bảng Khối Lượng Nguyên Tử
- Phương Pháp Giảng Dạy Về Bảng Khối Lượng Nguyên Tử
- Ôn Tập Và Kiểm Tra
Thông Tin Về Bảng Khối Lượng Nguyên Tử Lớp 8
Bảng khối lượng nguyên tử lớp 8 là một tài liệu quan trọng trong chương trình học hóa học lớp 8, cung cấp thông tin về khối lượng của các nguyên tố hóa học. Dưới đây là tổng hợp chi tiết về nội dung của bảng khối lượng nguyên tử:
Các Thành Phần Chính
- Tên Nguyên Tố: Tên của từng nguyên tố hóa học.
- Ký Hiệu Nguyên Tố: Ký hiệu hóa học đại diện cho nguyên tố.
- Khối Lượng Nguyên Tử: Khối lượng của nguyên tử được đo bằng đơn vị amu (atomic mass unit).
Bảng Khối Lượng Nguyên Tử
| Tên Nguyên Tố | Ký Hiệu | Khối Lượng Nguyên Tử (amu) |
|---|---|---|
| Hydrogen | H | 1.008 |
| Carbon | C | 12.01 |
| Oxygen | O | 16.00 |
| Nitrogen | N | 14.01 |
Ứng Dụng
Bảng khối lượng nguyên tử được sử dụng để:
- Hỗ trợ tính toán khối lượng phân tử trong các phản ứng hóa học.
- Xác định tỷ lệ phần trăm của các nguyên tố trong hợp chất hóa học.
- Giúp học sinh hiểu rõ hơn về các yếu tố ảnh hưởng đến tính chất của vật liệu.
Việc nắm vững thông tin từ bảng khối lượng nguyên tử là rất quan trọng trong việc học và ứng dụng hóa học.

Tổng Quan Về Bảng Khối Lượng Nguyên Tử
Bảng khối lượng nguyên tử là một công cụ quan trọng trong hóa học, cung cấp thông tin về khối lượng của các nguyên tử trong các nguyên tố hóa học. Dưới đây là một cái nhìn tổng quan về bảng khối lượng nguyên tử lớp 8:
Khái Niệm Cơ Bản
Khối lượng nguyên tử là khối lượng của một nguyên tử của một nguyên tố hóa học, được đo bằng đơn vị khối lượng nguyên tử (amu). Nó phản ánh số lượng proton và neutron trong hạt nhân của nguyên tử.
Cấu Trúc Của Bảng Khối Lượng Nguyên Tử
Bảng khối lượng nguyên tử thường bao gồm các thông tin sau:
- Tên Nguyên Tố: Tên của nguyên tố hóa học.
- Ký Hiệu Nguyên Tố: Ký hiệu hóa học đại diện cho nguyên tố.
- Khối Lượng Nguyên Tử: Khối lượng của nguyên tử, tính bằng đơn vị amu.
Danh Sách Các Nguyên Tố Trong Bảng
Dưới đây là bảng khối lượng nguyên tử cho một số nguyên tố cơ bản:
| Tên Nguyên Tố | Ký Hiệu | Khối Lượng Nguyên Tử (amu) |
|---|---|---|
| Hydrogen | H | 1.008 |
| Carbon | C | 12.01 |
| Oxygen | O | 16.00 |
| Nitrogen | N | 14.01 |
Ý Nghĩa Của Khối Lượng Nguyên Tử
Khối lượng nguyên tử giúp chúng ta hiểu được tỉ lệ và khối lượng của các nguyên tố trong hợp chất hóa học, hỗ trợ trong việc tính toán và dự đoán tính chất của các phản ứng hóa học.
Đơn Vị Đo Lường
Khối lượng nguyên tử được đo bằng đơn vị khối lượng nguyên tử (amu), trong đó 1 amu được định nghĩa là 1/12 khối lượng của một nguyên tử carbon-12. Đơn vị này giúp so sánh khối lượng của các nguyên tử khác nhau một cách chính xác.
Chi Tiết Các Nguyên Tố Hóa Học
Tầm Quan Trọng Của Bảng Khối Lượng Nguyên Tử
Mục Đích Sử Dụng Trong Học Tập

Các Thành Phần Của Bảng Khối Lượng Nguyên Tử
Tên Nguyên Tố
Ký Hiệu Nguyên Tố
Khối Lượng Nguyên Tử
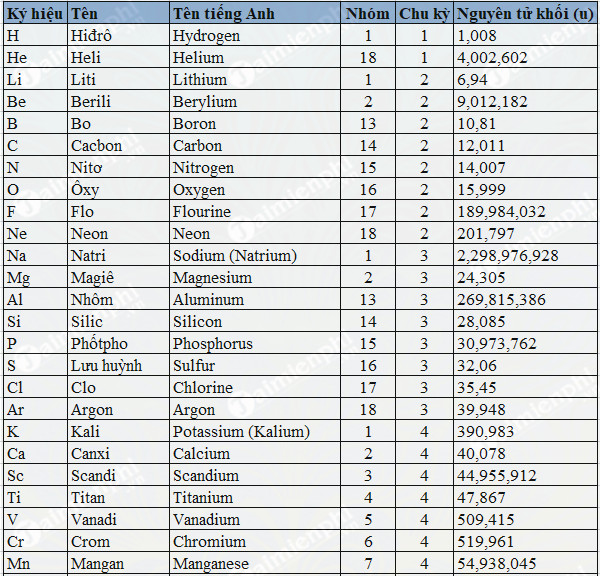
Danh Sách Các Nguyên Tố Phổ Biến
Nguyên Tố Thường Gặp Trong Lớp 8
Khối Lượng Nguyên Tử Của Các Nguyên Tố Chính

Ứng Dụng Trong Hóa Học
Cách Tính Khối Lượng Phân Tử
Xác Định Thành Phần Hóa Học
Ảnh Hưởng Đến Tính Chất Vật Liệu
XEM THÊM:
Hướng Dẫn Sử Dụng Bảng Khối Lượng Nguyên Tử
Các Bước Sử Dụng Trong Bài Tập
Phương Pháp Tính Toán Chính Xác

Tài Nguyên Tham Khảo
Sách Giáo Khoa
Các Trang Web Giáo Dục
Tài Liệu Hỗ Trợ Thêm

Ứng Dụng Của Bảng Khối Lượng Nguyên Tử
Bảng khối lượng nguyên tử lớp 8 có nhiều ứng dụng quan trọng trong hóa học và các lĩnh vực liên quan. Dưới đây là một số ứng dụng chính:
Tính Toán Khối Lượng Phân Tử
Khối lượng phân tử của một hợp chất hóa học có thể được tính bằng cách cộng tổng khối lượng nguyên tử của các nguyên tố cấu thành nó. Ví dụ:
| Hợp Chất | Khối Lượng Nguyên Tử | Khối Lượng Phân Tử |
|---|---|---|
| H2O (Nước) | H: 1.008 amu, O: 16.00 amu | 2 × 1.008 + 16.00 = 18.016 amu |
| CO2 (Carbon Dioxide) | C: 12.01 amu, O: 16.00 amu | 12.01 + 2 × 16.00 = 44.01 amu |
Xác Định Thành Phần Hóa Học
Bằng cách biết khối lượng nguyên tử của các nguyên tố, bạn có thể xác định tỷ lệ phần trăm của mỗi nguyên tố trong một hợp chất. Quy trình bao gồm:
- Tính khối lượng phân tử của hợp chất.
- Tính khối lượng tổng của từng nguyên tố trong hợp chất.
- Chia khối lượng của nguyên tố cho khối lượng phân tử của hợp chất và nhân với 100 để có tỷ lệ phần trăm.
Ứng Dụng Trong Phân Tích Chất
Trong phân tích hóa học, khối lượng nguyên tử giúp xác định thành phần và hàm lượng của các chất trong mẫu. Ví dụ, trong phân tích hóa học định lượng, thông tin về khối lượng nguyên tử là cần thiết để xác định hàm lượng các nguyên tố trong một hợp chất hoặc vật liệu.
Ảnh Hưởng Đến Tính Chất Vật Liệu
Khối lượng nguyên tử của nguyên tố ảnh hưởng đến các tính chất vật lý và hóa học của vật liệu. Ví dụ:
- Khối lượng nguyên tử cao thường dẫn đến mật độ vật liệu cao hơn.
- Nguyên tố với khối lượng nguyên tử lớn có thể có điểm nóng chảy và sôi cao hơn.
Phương Pháp Giảng Dạy Về Bảng Khối Lượng Nguyên Tử

Ôn Tập Và Kiểm Tra
Để giúp học sinh ôn tập và kiểm tra kiến thức về bảng khối lượng nguyên tử lớp 8, chúng ta có thể áp dụng các phương pháp và tài liệu dưới đây:
Câu Hỏi Ôn Tập
- Câu hỏi 1: Khối lượng nguyên tử của nguyên tố cacbon là bao nhiêu? Tại sao nó lại có giá trị như vậy?
- Câu hỏi 2: So sánh khối lượng nguyên tử của oxy và nito. Nguyên tố nào có khối lượng nguyên tử lớn hơn?
- Câu hỏi 3: Định nghĩa khối lượng nguyên tử và giải thích ý nghĩa của nó trong hóa học.
Bài Tập Thực Hành
Hãy thực hiện các bài tập sau để củng cố kiến thức:
- Tính khối lượng nguyên tử trung bình của một nguyên tố, dựa trên tỷ lệ phần trăm của các đồng vị của nó.
- Hoàn thành bảng khối lượng nguyên tử cho các nguyên tố trong danh sách được cung cấp.
- Vẽ sơ đồ và phân tích sự khác biệt về khối lượng nguyên tử giữa các nguyên tố kim loại và phi kim.
Đề Thi Và Đáp Án Mẫu
| Câu Hỏi | Đáp Án Mẫu |
|---|---|
| Câu hỏi 1: Khối lượng nguyên tử của nguyên tố magie là bao nhiêu? | Đáp án: Khối lượng nguyên tử của magie là 24.305. |
| Câu hỏi 2: Nguyên tố nào có khối lượng nguyên tử nhỏ nhất và lớn nhất trong bảng tuần hoàn? | Đáp án: Nguyên tố có khối lượng nguyên tử nhỏ nhất là hydro (1.008), nguyên tố có khối lượng nguyên tử lớn nhất là ôsmium (190.23). |
| Câu hỏi 3: Giải thích cách sử dụng bảng khối lượng nguyên tử trong việc tính toán hóa học. | Đáp án: Bảng khối lượng nguyên tử được sử dụng để tính toán khối lượng mol, tỷ lệ phần trăm nguyên tố và trong các phép tính hóa học khác. |