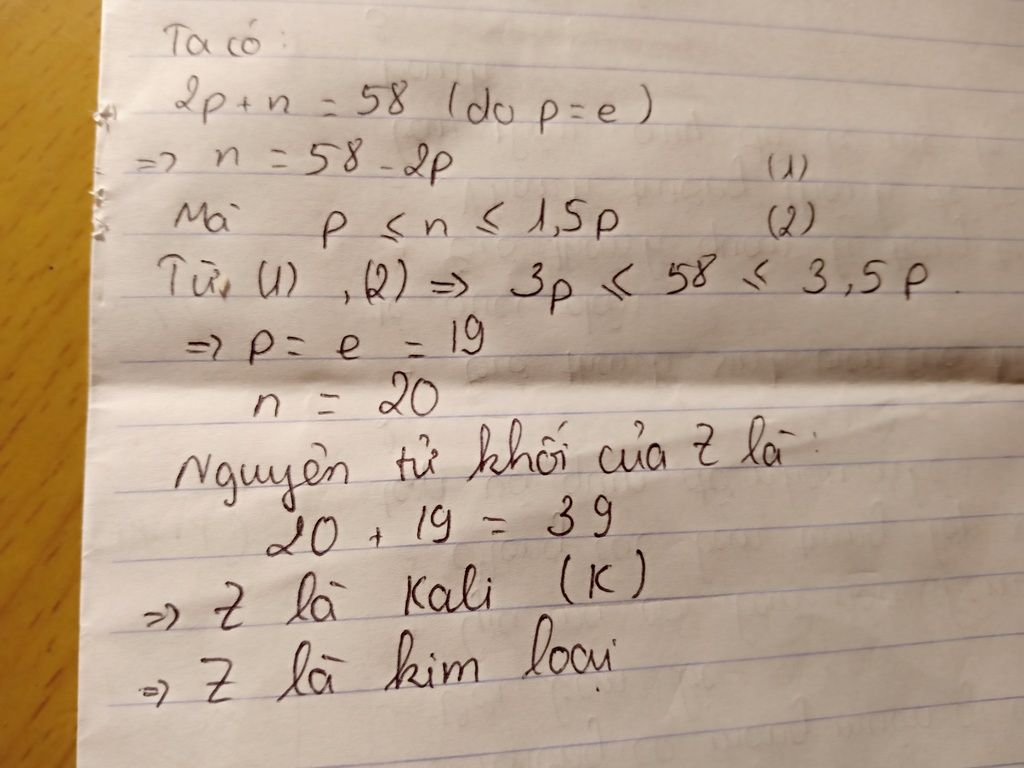Chủ đề kali số nguyên tử: Kali, với số nguyên tử 19, là một nguyên tố thiết yếu trong cuộc sống hàng ngày. Từ ứng dụng quan trọng trong nông nghiệp, công nghiệp đến vai trò không thể thiếu trong sức khỏe con người, kali mang lại nhiều lợi ích vượt trội. Trong bài viết này, chúng ta sẽ khám phá chi tiết về cấu trúc nguyên tử, tính chất vật lý và hóa học của kali, cũng như các ứng dụng và vai trò của nó trong tự nhiên và đời sống.
Mục lục
Nguyên Tử Kali và Ứng Dụng Trong Đời Sống
Kali (K) là một nguyên tố hóa học thuộc nhóm kim loại kiềm, có số nguyên tử là 19. Nguyên tử của Kali bao gồm 19 proton, 19 electron và 20 neutron, tạo nên nguyên tử khối trung bình là 39.0983 u.
Cấu Trúc Nguyên Tử Của Kali
- Ký hiệu hóa học: K
- Số nguyên tử: 19
- Nguyên tử khối: 39.0983 u
- Phân lớp electron: \(1s^2 2s^2 2p^6 3s^2 3p^6 4s^1\)
Tính Chất Vật Lý và Hóa Học Của Kali
- Kali là kim loại mềm, màu trắng bạc, dễ bị cắt bằng dao.
- Nhiệt độ nóng chảy của Kali là khoảng 63°C và nhiệt độ sôi là 760°C.
- Kali có tính khử rất mạnh, dễ phản ứng với oxi tạo thành oxit và với các phi kim khác tạo thành muối.
- Khi tác dụng với nước, Kali giải phóng khí hydro và tạo ra dung dịch kiềm mạnh.
Ứng Dụng Của Kali Trong Đời Sống
Kali đóng vai trò vô cùng quan trọng trong nhiều lĩnh vực khác nhau, bao gồm sức khỏe con người và các ngành công nghiệp:
- Trong sức khỏe con người: Kali giúp duy trì cân bằng điện giải, co bóp cơ bắp, và chức năng thần kinh.
- Trong nông nghiệp: Kali là thành phần chính trong phân bón NPK, giúp cây trồng phát triển khỏe mạnh.
- Trong công nghiệp: Kali được sử dụng trong sản xuất thủy tinh, xà phòng, và các hợp chất hóa học khác.
- Trong phòng thí nghiệm: Kali thường được dùng trong các phản ứng hóa học và điện phân.
Các Đồng Vị Của Kali
Kali có ba đồng vị tự nhiên:
- \(^{39}K\): chiếm 93,3%
- \(^{40}K\): chiếm 0,01%
- \(^{41}K\): chiếm 6,7%
Lưu Ý Khi Sử Dụng Kali
Dù không độc, Kali cần được xử lý cẩn thận vì tính chất phản ứng mạnh với nước và không khí. Khi sử dụng Kali, nên trang bị đầy đủ bảo hộ và tránh tiếp xúc trực tiếp để đảm bảo an toàn.
| Thông Tin | Chi Tiết |
|---|---|
| Ký hiệu hóa học | K |
| Số nguyên tử | 19 |
| Nguyên tử khối | 39.0983 u |
| Phân lớp electron | \(1s^2 2s^2 2p^6 3s^2 3p^6 4s^1\) |
| Nhiệt độ nóng chảy | 63°C |
| Nhiệt độ sôi | 760°C |

1. Giới Thiệu Về Nguyên Tố Kali
Kali, ký hiệu hóa học là \( K \), là một nguyên tố kim loại kiềm có số nguyên tử là 19. Kali là một nguyên tố thuộc nhóm 1 trong bảng tuần hoàn và có chu kỳ 4. Nguyên tố này có màu bạc và tồn tại dưới dạng rắn ở nhiệt độ phòng. Kali không có tính phóng xạ và có cấu trúc tinh thể lập phương tâm khối.
Kali có nguyên tử khối là 39,0983 u và cấu hình electron của nó được biểu diễn là \[ \text{[Ar]} 4s^1 \]. Điều này cho thấy kali có một electron duy nhất trong phân lớp 4s, làm cho nó rất phản ứng với các nguyên tố khác, đặc biệt là các phi kim. Trong điều kiện bình thường, kali rất mềm và có thể được cắt bằng dao.
Kali lần đầu tiên được tách ra vào năm 1807 bởi nhà hóa học người Anh Sir Humphry Davy thông qua quá trình điện phân kali hydroxit (\( KOH \)). Đây là kim loại đầu tiên được cô lập bằng phương pháp điện phân.
- Số proton: 19
- Số electron: 19
- Số nơtron: 20
- Trạng thái vật chất: Rắn
- Mật độ: \(0,862 \, \text{g/cm}^3\)
- Nhiệt độ nóng chảy: \(336,53 \, \text{K} \, (63,38^\circ \text{C})\)
- Nhiệt độ sôi: \(1032,15 \, \text{K} \, (759^\circ \text{C})\)
Kali rất quan trọng đối với sự sống trên Trái Đất. Nó là thành phần thiết yếu cho sự phát triển của thực vật và có mặt trong hầu hết các loại đất. Kali được sử dụng nhiều nhất trong phân bón để cung cấp dinh dưỡng cho cây trồng. Ngoài ra, kali còn có vai trò quan trọng trong sản xuất thuốc nổ (kali nitrat), sản xuất xà phòng mềm, và làm chất điện phân trong pin kiềm.
Một số đặc điểm nổi bật khác của kali bao gồm khả năng dẫn điện tốt và độ âm điện thấp (0,82 theo thang Pauling), khiến nó trở thành một trong những kim loại có tính phản ứng mạnh nhất trong nhóm kim loại kiềm.
2. Tính Chất Vật Lý và Hóa Học Của Kali
Kali (K) là một kim loại kiềm có số nguyên tử là 19. Dưới đây là các tính chất vật lý và hóa học nổi bật của nguyên tố này:
- Tính chất vật lý:
- Kali có màu trắng bạc khi bề mặt sạch và là một kim loại rất mềm, dễ cắt được bằng dao.
- Ở điều kiện thường, kali có khối lượng riêng nhỏ hơn nước, là kim loại nhẹ thứ hai sau liti.
- Nhiệt độ nóng chảy: \(336,53 \, K \, (63,38^\circ C, 146,08^\circ F)\).
- Nhiệt độ sôi: \(1032 \, K \, (759^\circ C, 1398^\circ F)\).
- Mật độ: \(0,862 \, g \cdot cm^{-3}\) (ở \(0^\circ C, 101,325 \, kPa\)).
- Nhiệt lượng nóng chảy: \(2,33 \, kJ \cdot mol^{-1}\), nhiệt bay hơi: \(76,9 \, kJ \cdot mol^{-1}\).
- Tính chất hóa học:
- Kali có tính khử rất mạnh, dễ phản ứng với các phi kim như oxy và clo.
- Khi đốt trong không khí hoặc oxy, kali cháy với ngọn lửa màu tím hoa cà đặc trưng và tạo ra các oxit như oxit kali (\(K_2O\)), peroxit kali (\(K_2O_2\)), và superoxit kali (\(KO_2\)).
- Kali phản ứng mãnh liệt với nước, giải phóng khí hydro và tạo dung dịch kiềm: \[2K + 2H_2O \to 2KOH + H_2 \uparrow.\]
- Kali phản ứng với axit như axit clohydric (HCl), tạo muối kali clorua và khí hydro: \[2K + 2HCl \to 2KCl + H_2.\]
- Kali phản ứng với hydro ở nhiệt độ cao (350-400°C) và áp suất lớn để tạo kali hidrua (KH): \[2K + H_2 \to 2KH.\]
Nhờ những tính chất vật lý và hóa học đặc biệt, kali có vai trò quan trọng trong nhiều ứng dụng công nghiệp và đời sống, đặc biệt là trong sản xuất phân bón và các hợp chất hóa học khác.

3. Ứng Dụng Của Kali Trong Đời Sống
Kali là một nguyên tố hóa học quan trọng trong nhiều lĩnh vực khác nhau của đời sống, từ nông nghiệp, công nghiệp đến y tế. Dưới đây là những ứng dụng chính của kali:
-
Nông nghiệp:
Kali là thành phần quan trọng trong các loại phân bón, đặc biệt là phân bón kali nitrat (KNO₃) và kali sunfat (K₂SO₄). Kali giúp cây trồng phát triển mạnh mẽ, cải thiện khả năng chống chịu của cây đối với các điều kiện thời tiết khắc nghiệt như khô hạn và sương giá, đồng thời tăng cường khả năng hấp thụ nước và dinh dưỡng từ đất.
-
Công nghiệp hóa chất:
Kali được sử dụng để sản xuất nhiều loại hợp chất hóa học như kali hydroxit (KOH), một chất kiềm mạnh được sử dụng trong sản xuất xà phòng, chất tẩy rửa và giấy. Kali cacbonat (K₂CO₃) được sử dụng trong sản xuất thủy tinh, đặc biệt là loại thủy tinh chịu nhiệt cao.
-
Y tế:
Kali là một chất điện giải quan trọng trong cơ thể con người, giúp điều chỉnh áp suất thẩm thấu của các tế bào, duy trì cân bằng acid-bazơ và hỗ trợ chức năng của cơ bắp và hệ thần kinh. Kali clorua (KCl) thường được sử dụng trong y học để điều trị hạ kali huyết (thiếu kali trong máu).
-
Công nghiệp năng lượng:
Kali được sử dụng trong các quá trình sản xuất năng lượng, bao gồm cả sản xuất pin và ắc quy. Hợp chất kali như kali perclorat (KClO₄) được sử dụng làm chất ôxy hóa trong sản xuất nhiên liệu tên lửa.
-
Ứng dụng khác:
Kali còn được sử dụng trong nhiều ứng dụng khác như sản xuất chất dẻo, dệt may và trong các phản ứng hóa học trong phòng thí nghiệm.

4. Vai Trò Của Kali Trong Tự Nhiên
Kali là một nguyên tố hóa học quan trọng và có vai trò đa dạng trong tự nhiên, bao gồm các lĩnh vực như sinh học, nông nghiệp và công nghiệp. Dưới đây là những vai trò quan trọng của kali trong tự nhiên:
- Trong cơ thể con người: Kali là một chất điện giải cần thiết để duy trì sự cân bằng nội môi trong cơ thể, tham gia vào nhiều chức năng sinh lý như điều chỉnh áp lực thẩm thấu, hỗ trợ hệ thống thần kinh và cơ bắp. Kali giúp duy trì nhịp tim ổn định và cải thiện sức khỏe tổng thể.
- Trong hệ thực vật: Kali là một trong ba nguyên tố cơ bản trong phân bón, có vai trò quan trọng trong sự phát triển của cây trồng. Nó giúp tăng cường quá trình quang hợp, tổng hợp protein, và làm cho cây trồng phát triển mạnh mẽ hơn. Kali còn giúp cây trồng tăng khả năng chống chịu với sâu bệnh và các điều kiện thời tiết khắc nghiệt.
- Trong công nghiệp: Kali được sử dụng rộng rãi trong sản xuất thủy tinh, xà phòng và chất tẩy rửa. Các hợp chất kali như kali nitrat (\(KNO_3\)) và kali clorua (\(KCl\)) được dùng trong sản xuất phân bón, giúp cải thiện chất lượng đất và tăng năng suất cây trồng.
- Trong y học: Kali clorua (\(KCl\)) được sử dụng để điều trị tình trạng thiếu kali, hỗ trợ các chức năng của hệ thần kinh và cơ bắp, và giúp điều chỉnh huyết áp, giảm nguy cơ mắc bệnh tim mạch và đột quỵ.
Kết luận, kali là một nguyên tố không thể thiếu trong đời sống và môi trường tự nhiên. Vai trò của kali không chỉ dừng lại ở việc hỗ trợ sức khỏe con người mà còn góp phần quan trọng trong nông nghiệp và công nghiệp, giúp cải thiện chất lượng cuộc sống và hiệu quả sản xuất.

5. Lưu Ý và An Toàn Khi Sử Dụng Kali
Kali (K) là một kim loại kiềm với tính chất hóa học mạnh, có khả năng phản ứng nhanh chóng với nhiều chất khác. Dưới đây là một số lưu ý quan trọng và các biện pháp an toàn khi làm việc với kali:
- Phản ứng với nước: Kali phản ứng mạnh với nước để tạo thành kali hydroxit (KOH) và khí hydro (H₂). Phản ứng này rất mãnh liệt và có thể gây nổ nếu không được kiểm soát đúng cách. Do đó, tuyệt đối không để kali tiếp xúc với nước hoặc hơi nước trong không khí.
- Bảo quản an toàn: Kali nên được bảo quản trong dầu hỏa hoặc dầu khoáng để ngăn chặn sự tiếp xúc với không khí và độ ẩm, giảm nguy cơ cháy nổ.
- Tránh tiếp xúc trực tiếp: Khi xử lý kali, luôn đeo găng tay, kính bảo hộ và quần áo bảo hộ để tránh tiếp xúc trực tiếp với kim loại này. Kali có thể gây bỏng da nghiêm trọng nếu tiếp xúc trực tiếp.
- Làm việc trong môi trường thoáng khí: Do kali có thể tạo ra khí hydro dễ cháy khi phản ứng, nên làm việc trong môi trường thoáng khí để tránh tích tụ khí nguy hiểm.
Các biện pháp an toàn trên giúp đảm bảo rằng việc sử dụng và xử lý kali được thực hiện một cách an toàn và hiệu quả, đồng thời giảm thiểu nguy cơ tai nạn lao động.
XEM THÊM:
6. Tài Liệu Tham Khảo và Nguồn Gốc
Kali, một nguyên tố hóa học quan trọng với số nguyên tử là 19, được nghiên cứu và sử dụng rộng rãi trong nhiều lĩnh vực khoa học và đời sống. Dưới đây là một số tài liệu tham khảo và nguồn gốc liên quan đến kali, nhằm cung cấp thông tin chi tiết và đầy đủ hơn về tính chất, vai trò và ứng dụng của nguyên tố này.
- Giáo trình hóa học: Các sách giáo khoa và giáo trình hóa học trung học và đại học cung cấp các thông tin cơ bản và nâng cao về tính chất hóa học, cách thức phản ứng, và vai trò của kali trong nhiều phản ứng hóa học khác nhau.
- Các bài báo khoa học: Những nghiên cứu và bài báo khoa học được công bố trên các tạp chí uy tín, bao gồm nghiên cứu về sự ảnh hưởng của kali đối với sức khỏe con người, tính chất hóa lý của kali, và cách thức sử dụng an toàn trong phòng thí nghiệm và sản xuất công nghiệp.
- Trang web và cổng thông tin: Nhiều trang web cung cấp các thông tin cập nhật về kali, bao gồm các tổ chức khoa học, giáo dục, như các cổng thông tin hóa học trực tuyến hoặc các trang web chuyên ngành.
- Tài liệu hướng dẫn sử dụng an toàn: Các tài liệu hướng dẫn từ các cơ quan an toàn lao động và y tế quốc tế, cung cấp các quy tắc và biện pháp cần thiết khi làm việc với kali, bao gồm cách lưu trữ, xử lý và vận chuyển nguyên tố này.
- Các bài báo công nghiệp: Thông tin từ các nhà sản xuất và công ty cung cấp kali, cùng với các bài báo chuyên ngành về các ứng dụng cụ thể của kali trong sản xuất phân bón, công nghiệp thủy tinh, hóa chất và nhiều ngành công nghiệp khác.
Việc sử dụng tài liệu từ nhiều nguồn đáng tin cậy giúp đảm bảo hiểu biết toàn diện về vai trò của kali trong tự nhiên và trong đời sống, đồng thời hướng dẫn cách thức sử dụng một cách an toàn và hiệu quả nhất.