Chủ đề k có nguyên tử khối là bao nhiêu: Bạn đang tìm kiếm thông tin về nguyên tử khối của Kali (K)? Bài viết này sẽ cung cấp chi tiết về nguyên tử khối của K, các tính chất hóa học, ứng dụng trong đời sống, và cách sử dụng an toàn Kali. Đừng bỏ lỡ cơ hội tìm hiểu sâu về một nguyên tố hóa học quan trọng này!
Mục lục
Nguyên Tử Khối Của Kali (K) Là Bao Nhiêu?
Nguyên tử khối của Kali (ký hiệu hóa học là \( \text{K} \)) là một kiến thức quan trọng trong lĩnh vực hóa học. Kali là một kim loại kiềm, có nhiều ứng dụng trong đời sống và sản xuất. Dưới đây là các thông tin chi tiết về nguyên tử khối của Kali và các tính chất liên quan.
1. Nguyên Tử Khối Của Kali
Kali có nguyên tử khối bằng \( \text{39} \, \text{amu} \) (đơn vị khối lượng nguyên tử).
2. Tính Chất Hóa Học
- Kali có tính khử mạnh: Khi tác dụng với các phi kim, Kali dễ dàng tạo thành các hợp chất như \( \text{KCl} \), \( \text{K}_2\text{O} \).
- Tác dụng với nước: Kali phản ứng mãnh liệt với nước, tạo thành dung dịch kiềm \( \text{KOH} \) và giải phóng khí hidro \( \text{H}_2 \).
- Ứng dụng trong sản xuất: Kali được sử dụng trong sản xuất phân bón, thủy tinh, và nhiều sản phẩm công nghiệp khác.
3. Ứng Dụng Của Kali Trong Đời Sống
Kali là một nguyên tố quan trọng trong nhiều lĩnh vực khác nhau:
- Trong nông nghiệp: Kali là thành phần chính của các loại phân bón, giúp cây trồng phát triển khỏe mạnh.
- Trong y học: Các hợp chất của Kali được sử dụng trong nhiều loại thuốc, đặc biệt là trong điều trị các bệnh về tim mạch.
- Trong công nghiệp: Kali được sử dụng để sản xuất thủy tinh có độ bền cao, cũng như trong các ứng dụng đặc biệt như sản xuất thuốc súng và hợp kim truyền nhiệt.
4. Đồng Vị Của Kali
Kali tồn tại dưới ba đồng vị tự nhiên:
| \( \text{K}^{39} \) | 93.3% |
| \( \text{K}^{40} \) | 0.01% |
| \( \text{K}^{41} \) | 6.7% |
5. Kết Luận
Kali là một nguyên tố có vai trò vô cùng quan trọng trong nhiều lĩnh vực của đời sống và công nghiệp. Việc hiểu biết về nguyên tử khối và các tính chất hóa học của Kali giúp chúng ta ứng dụng tốt hơn nguyên tố này trong sản xuất và đời sống hàng ngày.

2. Tính Chất Hóa Học Của Kali
Kali (K) là một kim loại kiềm có tính phản ứng rất mạnh, đặc biệt khi tiếp xúc với nước và không khí. Dưới đây là các tính chất hóa học đặc trưng của kali:
- Phản ứng với nước: Khi kali tiếp xúc với nước, nó tạo ra phản ứng mãnh liệt, giải phóng khí hydro \(\text{H}_2\) và tạo thành dung dịch kiềm là kali hydroxit \(\text{KOH}\). Phương trình phản ứng: \[ 2\text{K} + 2\text{H}_2\text{O} \rightarrow 2\text{KOH} + \text{H}_2 \uparrow \] Phản ứng này thường gây ra hiện tượng bùng cháy hoặc nổ nhỏ do lượng nhiệt sinh ra.
- Phản ứng với không khí: Kali dễ dàng bị oxi hóa khi tiếp xúc với không khí, tạo thành kali oxit \(\text{K}_2\text{O}\) hoặc kali superoxit \(\text{KO}_2\). Điều này làm cho kali phải được bảo quản trong dầu để tránh tiếp xúc với không khí. Phương trình phản ứng: \[ 4\text{K} + \text{O}_2 \rightarrow 2\text{K}_2\text{O} \]
- Phản ứng với axit: Kali phản ứng mạnh với axit, tạo thành muối kali và giải phóng khí hydro \(\text{H}_2\). Ví dụ, phản ứng với axit clohydric \(\text{HCl}\): \[ 2\text{K} + 2\text{HCl} \rightarrow 2\text{KCl} + \text{H}_2 \uparrow \]
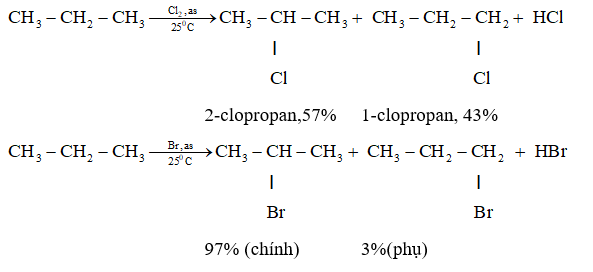
- Phản ứng với halogen: Kali dễ dàng phản ứng với các halogen như clo \(\text{Cl}_2\), brom \(\text{Br}_2\), hoặc iod \(\text{I}_2\) để tạo thành muối halogenua kali. Ví dụ, phản ứng với clo: \[ 2\text{K} + \text{Cl}_2 \rightarrow 2\text{KCl} \]
Nhờ vào các tính chất hóa học đặc trưng này, kali được sử dụng trong nhiều lĩnh vực, từ sản xuất hóa chất đến ứng dụng trong công nghiệp và nông nghiệp.
3. Ứng Dụng Của Kali Trong Đời Sống Và Công Nghiệp
Kali là một nguyên tố quan trọng với nhiều ứng dụng đa dạng trong đời sống và công nghiệp. Dưới đây là những ứng dụng nổi bật của kali:
- Trong nông nghiệp: Kali là một thành phần thiết yếu trong phân bón. Nó giúp cây trồng tăng cường sức đề kháng, thúc đẩy quá trình quang hợp và cải thiện chất lượng nông sản. Kali trong phân bón thường ở dạng kali clorua \(\text{KCl}\) hoặc kali sunfat \(\text{K}_2\text{SO}_4\).
- Trong công nghiệp hóa chất: Kali được sử dụng rộng rãi trong sản xuất các hợp chất hóa học như kali hidroxit \(\text{KOH}\) và kali cacbonat \(\text{K}_2\text{CO}_3\). Những hợp chất này được sử dụng trong nhiều ngành công nghiệp như sản xuất xà phòng, thủy tinh và thuốc nổ.
- Trong công nghiệp thực phẩm: Kali cũng được dùng làm chất phụ gia trong thực phẩm, giúp điều chỉnh độ pH và tăng cường hương vị. Kali sorbat \(\text{C}_6\text{H}_7\text{KO}_2\) là một chất bảo quản phổ biến được sử dụng để ngăn chặn sự phát triển của nấm mốc và vi khuẩn.
- Trong y tế: Kali đóng vai trò quan trọng trong việc điều hòa nhịp tim và hỗ trợ hoạt động của các cơ. Kali clorua \(\text{KCl}\) thường được sử dụng trong điều trị các bệnh liên quan đến sự thiếu hụt kali, giúp cân bằng điện giải trong cơ thể.
- Trong năng lượng: Kali superoxit \(\text{KO}_2\) được dùng trong các thiết bị cung cấp oxy trong môi trường khép kín như tàu ngầm hoặc tàu vũ trụ. Hợp chất này phản ứng với khí CO\(_2\) để tạo ra oxy, giúp duy trì không khí sạch.
Với những ứng dụng phong phú và quan trọng, kali là một nguyên tố không thể thiếu trong nhiều lĩnh vực của đời sống và công nghiệp.

5. Bảo Quản Và Sử Dụng An Toàn Kali
Kali là một kim loại kiềm có phản ứng mạnh với nước và không khí, do đó cần được bảo quản và sử dụng đúng cách để đảm bảo an toàn. Dưới đây là một số hướng dẫn cụ thể:
- Bảo quản:
- Kali nên được bảo quản trong các bình chứa kín, tốt nhất là trong dầu hỏa hoặc dầu khoáng để ngăn chặn tiếp xúc với không khí và hơi nước.
- Bảo quản ở nơi khô ráo, thoáng mát, tránh xa nguồn nhiệt và các chất dễ cháy nổ.
- Không bảo quản kali gần các axit mạnh hoặc chất oxy hóa để tránh phản ứng nguy hiểm.
- Sử dụng an toàn:
- Khi thao tác với kali, luôn đeo găng tay bảo hộ và kính bảo hộ để tránh tiếp xúc trực tiếp với da và mắt.
- Không để kali tiếp xúc với nước hoặc độ ẩm, vì điều này có thể gây ra phản ứng nổ.
- Nếu cần cắt nhỏ kim loại kali, sử dụng các dụng cụ chuyên dụng và làm việc trong môi trường có kiểm soát.
- Trong trường hợp xảy ra sự cố, không sử dụng nước để dập lửa, thay vào đó sử dụng cát khô hoặc bột hóa chất chuyên dụng.
- Xử lý chất thải:
- Kali dư thừa cần được xử lý theo quy định về chất thải nguy hại, không nên đổ bỏ vào hệ thống cống rãnh hoặc môi trường tự nhiên.
- Đóng gói cẩn thận và liên hệ với các đơn vị xử lý chất thải nguy hại để tiêu hủy một cách an toàn.
Việc bảo quản và sử dụng kali đúng cách không chỉ đảm bảo an toàn cho bản thân mà còn bảo vệ môi trường khỏi các nguy cơ ô nhiễm và cháy nổ.

6. Tìm Hiểu Thêm Về Các Hợp Chất Của Kali
Kali là một nguyên tố hóa học quan trọng, có mặt trong nhiều hợp chất khác nhau và được sử dụng rộng rãi trong đời sống cũng như các ngành công nghiệp. Dưới đây là một số hợp chất phổ biến của kali và ứng dụng của chúng:
6.1 Kali Hiđroxit (KOH)
Kali Hiđroxit (KOH), hay còn được gọi là potash ăn da, là một bazơ mạnh được sử dụng trong nhiều quy trình công nghiệp và hóa học.
- Sản xuất xà phòng và chất tẩy rửa: KOH được sử dụng để sản xuất xà phòng lỏng và các sản phẩm tẩy rửa vì tính kiềm mạnh và khả năng hòa tan tốt trong nước.
- Công nghiệp dệt và nhuộm: Kali hiđroxit được dùng để làm mềm vải và làm sạch trong quá trình xử lý vải.
- Sản xuất phân bón: Hợp chất này được sử dụng để điều chỉnh độ pH của đất và cung cấp nguồn kali cho cây trồng.
6.2 Kali Clorua (KCl)
Kali Clorua (KCl) là một muối kali phổ biến, được sử dụng rộng rãi trong nông nghiệp và y học.
- Phân bón nông nghiệp: KCl là một trong những loại phân bón kali thông dụng nhất, giúp cải thiện năng suất cây trồng bằng cách cung cấp kali - một chất dinh dưỡng cần thiết.
- Y học: Kali clorua được sử dụng trong y tế để điều chỉnh nồng độ kali trong máu của bệnh nhân. Nó cũng có vai trò quan trọng trong các dung dịch truyền dịch.
- Chất thay thế muối ăn: KCl thường được sử dụng như một chất thay thế muối natri (NaCl) cho những người cần hạn chế lượng natri trong chế độ ăn uống.
6.3 Các Hợp Chất Khác Của Kali
- Kali Nitrat (KNO3): Đây là một hợp chất được sử dụng trong phân bón, pháo hoa, và sản xuất thuốc nổ. Kali nitrat là nguồn cung cấp nitơ và kali cho cây trồng, giúp tăng cường quá trình quang hợp và tăng trưởng.
- Kali Sunfat (K2SO4): Hợp chất này được sử dụng làm phân bón, đặc biệt trong những trường hợp cây trồng nhạy cảm với clo, giúp cải thiện chất lượng nông sản.
- Kali Bicromat (K2Cr2O7): Được sử dụng trong ngành công nghiệp hóa chất để mạ kim loại, làm chất oxy hóa mạnh trong các phản ứng hóa học.
- Kali Permanganat (KMnO4): Hợp chất này được sử dụng làm chất khử trùng, chất tẩy màu trong công nghiệp dệt, và chất oxy hóa trong các quy trình phân tích hóa học.
Những hợp chất trên chỉ là một phần nhỏ trong số rất nhiều hợp chất của kali được sử dụng trong đời sống và công nghiệp. Mỗi hợp chất có những ứng dụng riêng biệt, đóng góp vào sự phát triển của nhiều lĩnh vực khác nhau.