Chủ đề cách làm mô hình nguyên tử của bo: Cách làm mô hình nguyên tử của Bo không chỉ là một bài học thú vị mà còn là cơ hội để bạn khám phá cấu trúc nguyên tử theo cách thực tế. Bài viết này sẽ hướng dẫn bạn từng bước tạo ra một mô hình chính xác và sinh động, giúp bạn nắm vững kiến thức và ứng dụng trong học tập hiệu quả.
Mục lục
Cách Làm Mô Hình Nguyên Tử Của Bo
Mô hình nguyên tử của Bo là một cách để hình dung và học hỏi về cấu trúc của nguyên tử dựa trên mô hình của nhà vật lý Niels Bohr. Dưới đây là hướng dẫn chi tiết cách làm mô hình nguyên tử của Bo, cụ thể là mô hình nguyên tử carbon.
Nguyên Liệu Chuẩn Bị
- Bìa carton hoặc giấy cứng
- Giấy màu vàng
- Viên bi nhựa to màu đỏ (đại diện cho proton và neutron)
- Viên bi nhỏ màu xanh (đại diện cho electron)
- Kéo, keo dán
- Dây nylon hoặc dây chun
Các Bước Thực Hiện
-
Chuẩn Bị Vật Liệu: Chuẩn bị các nguyên liệu như bìa carton, giấy màu, bi nhựa và các dụng cụ cần thiết.
-
Tạo Hạt Nhân Nguyên Tử:
Gắn các viên bi đỏ lại với nhau để tạo thành hạt nhân nguyên tử, bao gồm các proton và neutron. -
Vẽ Và Cắt Các Vòng Quỹ Đạo Electron:
Sử dụng giấy màu hoặc bìa carton để vẽ các vòng tròn đại diện cho các quỹ đạo của electron. Số lượng quỹ đạo phụ thuộc vào loại nguyên tử mà bạn muốn tạo. -
Gắn Electron Vào Các Vòng Quỹ Đạo:
Gắn các viên bi nhỏ màu xanh lên các vòng tròn đã vẽ để đại diện cho electron. Đảm bảo các electron được bố trí đúng vị trí theo mô hình nguyên tử Bo. -
Hoàn Thiện Mô Hình:
Gắn các phần đã chuẩn bị lại với nhau để tạo thành một mô hình hoàn chỉnh. Kiểm tra và điều chỉnh các chi tiết nếu cần thiết.
Ý Nghĩa Và Ứng Dụng
Mô hình nguyên tử của Bo không chỉ giúp hiểu rõ hơn về cấu trúc của nguyên tử mà còn có nhiều ứng dụng trong vật lý và hóa học hiện đại. Mô hình này giải thích được cấu trúc của nguyên tử hydro và là nền tảng cho việc phát triển lý thuyết cơ học lượng tử. Ngoài ra, mô hình Bo còn được sử dụng trong phân tích quang phổ, phát triển công nghệ laser và nghiên cứu vật liệu.
Mô Hình Toán Học
Trong mô hình Bo, electron chuyển động quanh hạt nhân theo các quỹ đạo xác định. Năng lượng của electron trong mỗi quỹ đạo được biểu diễn bằng công thức:
\[
E_n = - \frac{13.6 \text{ eV}}{n^2}
\]
Trong đó \(n\) là số nguyên dương đại diện cho mức năng lượng của electron. Quang phổ phát xạ của nguyên tử hydro được giải thích bằng sự chuyển dịch của electron giữa các quỹ đạo này.
Mô hình Bo, mặc dù có giới hạn trong việc giải thích các nguyên tử phức tạp, vẫn là một công cụ giáo dục quan trọng giúp học sinh và sinh viên hiểu về cấu trúc nguyên tử và các hiện tượng vật lý liên quan.
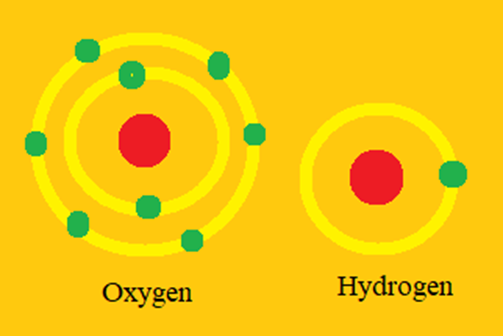
1. Giới thiệu về Mô Hình Nguyên Tử của Bo
Mô hình nguyên tử của Bo, được phát triển bởi nhà vật lý Niels Bohr vào năm 1913, là một bước đột phá trong việc hiểu biết về cấu trúc nguyên tử. Mô hình này giải thích cách các electron quay quanh hạt nhân nguyên tử trong các quỹ đạo cụ thể, giúp giải thích hiện tượng quang phổ phát xạ của nguyên tử hydro.
Trong mô hình Bo, các electron chỉ có thể tồn tại ở những quỹ đạo có mức năng lượng xác định và không thể tồn tại giữa các quỹ đạo này. Khi electron di chuyển từ quỹ đạo có năng lượng cao xuống quỹ đạo có năng lượng thấp hơn, nó phát ra một photon có năng lượng tương ứng với sự chênh lệch năng lượng giữa hai quỹ đạo. Nguyên lý này được diễn đạt bằng công thức:
\[
\Delta E = E_2 - E_1 = h \cdot \nu
\]
Trong đó, \(\Delta E\) là năng lượng của photon phát ra, \(E_2\) và \(E_1\) là năng lượng của các quỹ đạo cao và thấp, \(h\) là hằng số Planck, và \(\nu\) là tần số của photon. Mô hình Bo tuy đơn giản nhưng đã đặt nền móng cho sự phát triển của cơ học lượng tử và tiếp tục được giảng dạy rộng rãi trong giáo dục.
Mô hình này không chỉ giúp hiểu rõ hơn về cấu trúc nguyên tử đơn giản như hydro mà còn mở đường cho việc nghiên cứu các nguyên tử phức tạp hơn. Dù đã được thay thế bởi các mô hình phức tạp hơn trong cơ học lượng tử, mô hình Bo vẫn là một công cụ giáo dục quan trọng, giúp học sinh và sinh viên hình dung dễ dàng hơn về cấu trúc nguyên tử và các hiện tượng vật lý liên quan.
2. Nguyên Lý Hoạt Động Của Mô Hình Nguyên Tử Bo
Mô hình nguyên tử của Bo dựa trên nguyên lý rằng các electron quay quanh hạt nhân nguyên tử theo những quỹ đạo tròn với mức năng lượng cố định. Mỗi quỹ đạo tương ứng với một mức năng lượng riêng biệt và được gọi là "mức năng lượng".
Theo mô hình này, các electron không thể tồn tại ở khoảng cách giữa các quỹ đạo. Khi electron di chuyển từ quỹ đạo này sang quỹ đạo khác, nó phải hấp thụ hoặc phát ra một lượng năng lượng đúng bằng sự chênh lệch năng lượng giữa hai mức quỹ đạo. Điều này được biểu diễn bằng công thức:
\[
\Delta E = h \cdot \nu
\]
Trong đó:
- \(\Delta E\) là sự thay đổi năng lượng của electron khi chuyển từ quỹ đạo này sang quỹ đạo khác.
- \(h\) là hằng số Planck.
- \(\nu\) là tần số của photon được hấp thụ hoặc phát ra.
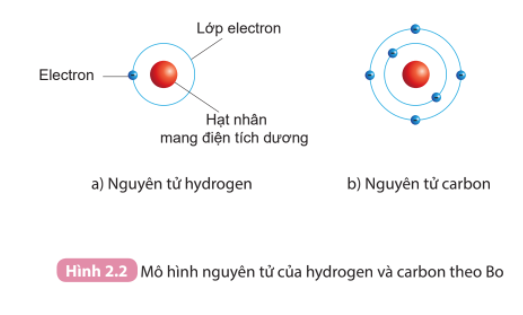
Các quỹ đạo của electron được đánh số theo thứ tự từ trong ra ngoài, với quỹ đạo gần hạt nhân nhất có mức năng lượng thấp nhất. Electron ở các quỹ đạo càng xa hạt nhân thì càng có mức năng lượng cao hơn.
Một trong những ứng dụng quan trọng của nguyên lý này là giải thích quang phổ phát xạ của nguyên tử. Khi một electron chuyển từ một quỹ đạo cao xuống một quỹ đạo thấp hơn, nó phát ra một photon ánh sáng với tần số nhất định, tạo nên các vạch phổ mà ta có thể quan sát được. Mô hình này đặc biệt thành công trong việc giải thích quang phổ của nguyên tử hydro.
Tuy nhiên, mô hình Bo cũng có những giới hạn. Nó chỉ chính xác cho các nguyên tử đơn giản như hydro và không thể giải thích được các hiện tượng phức tạp hơn liên quan đến các nguyên tử nặng hơn. Dù vậy, nguyên lý hoạt động của mô hình Bo vẫn là một nền tảng quan trọng trong việc nghiên cứu và giảng dạy về cấu trúc nguyên tử.

3. Hướng Dẫn Chi Tiết Làm Mô Hình Nguyên Tử Bo
Làm mô hình nguyên tử Bo là một dự án thú vị và dễ thực hiện, giúp học sinh hiểu rõ hơn về cấu trúc nguyên tử. Dưới đây là các bước chi tiết để làm mô hình này.
3.1 Chuẩn bị nguyên liệu và dụng cụ
- Bìa cứng hoặc xốp để làm nền
- Viên bi hoặc quả cầu nhỏ (màu đỏ cho proton, màu xanh cho neutron, và màu vàng cho electron)
- Dây kẽm hoặc dây cước để làm quỹ đạo cho electron
- Kéo, keo dán, và bút màu
- Thước kẻ để đo và cắt chính xác
3.2 Các bước thực hiện
-
Bước 1: Tạo hạt nhân nguyên tử
Dùng các viên bi màu đỏ để làm proton và viên bi màu xanh để làm neutron. Gắn chúng lại với nhau bằng keo để tạo thành hạt nhân nguyên tử. Đảm bảo rằng các viên bi được dán chắc chắn để tạo thành một khối đồng nhất.
-
Bước 2: Tạo các quỹ đạo electron
Sử dụng dây kẽm hoặc dây cước để tạo các vòng tròn bao quanh hạt nhân, đại diện cho các quỹ đạo của electron. Bạn có thể cắt dây theo chiều dài cần thiết và uốn thành hình tròn. Đảm bảo các quỹ đạo có kích thước khác nhau để biểu thị các mức năng lượng khác nhau.
-
Bước 3: Gắn electron vào quỹ đạo
Dùng các viên bi màu vàng để làm electron. Gắn chúng vào các quỹ đạo bằng keo. Mỗi quỹ đạo có thể có một hoặc nhiều electron, tùy thuộc vào cấu trúc của nguyên tử mà bạn muốn mô phỏng.
-
Bước 4: Hoàn thiện mô hình
Gắn các quỹ đạo electron vào hạt nhân bằng keo hoặc băng dính. Đảm bảo các quỹ đạo được cố định chắc chắn và cân đối xung quanh hạt nhân. Cuối cùng, trang trí mô hình nếu cần thiết để mô phỏng rõ ràng hơn cấu trúc nguyên tử.
3.3 Lưu ý khi thực hiện
- Đảm bảo an toàn khi sử dụng kéo và các dụng cụ sắc nhọn.
- Chọn vật liệu dễ tìm, an toàn và phù hợp với lứa tuổi của người thực hiện.
- Hiểu rõ lý thuyết về mô hình nguyên tử Bo trước khi bắt tay vào làm mô hình thực tế.
Sau khi hoàn thành, bạn sẽ có một mô hình nguyên tử Bo sinh động, giúp minh họa rõ ràng các khái niệm về cấu trúc nguyên tử và quỹ đạo electron, đồng thời nâng cao sự hiểu biết về vật lý nguyên tử.
4. Ứng Dụng Của Mô Hình Nguyên Tử Bo
Mô hình nguyên tử Bo đã góp phần quan trọng trong nhiều lĩnh vực, từ giáo dục đến nghiên cứu khoa học và công nghệ. Dưới đây là một số ứng dụng nổi bật của mô hình này.
4.1 Ứng dụng trong giảng dạy và học tập
Mô hình Bo là công cụ hữu ích trong giảng dạy các khái niệm cơ bản về cấu trúc nguyên tử. Nó giúp học sinh và sinh viên dễ dàng hình dung về các quỹ đạo electron và cách chúng tương tác với nhau. Ngoài ra, mô hình còn được sử dụng trong các bài thực hành, thí nghiệm hóa học và vật lý, giúp củng cố kiến thức lý thuyết.
4.2 Ứng dụng trong nghiên cứu khoa học
Mặc dù mô hình Bo có giới hạn, nhưng nó vẫn đóng vai trò quan trọng trong việc giải thích một số hiện tượng cơ bản trong vật lý nguyên tử, đặc biệt là trong nghiên cứu về nguyên tử hydro. Nhiều thí nghiệm và công trình nghiên cứu khoa học dựa trên các nguyên lý cơ bản của mô hình này để phát triển và mở rộng thêm kiến thức về cấu trúc nguyên tử và năng lượng.
4.3 Ứng dụng trong công nghệ và đời sống
Mô hình nguyên tử Bo cũng có các ứng dụng thực tế trong công nghệ, đặc biệt là trong lĩnh vực quang học và điện tử. Ví dụ, nó giúp hiểu rõ hơn về hoạt động của các thiết bị phát sáng như đèn LED, laser, và các cảm biến quang học. Các kiến thức này có thể được áp dụng để phát triển các sản phẩm công nghệ mới, cải tiến chất lượng và hiệu suất của các thiết bị điện tử.
Nhờ vào khả năng giải thích đơn giản nhưng hiệu quả các hiện tượng phức tạp, mô hình nguyên tử Bo vẫn là một phần quan trọng trong giáo dục và nghiên cứu, mở ra nhiều cơ hội ứng dụng trong các ngành khoa học và công nghệ hiện đại.

5. Phân Tích Và So Sánh Mô Hình Nguyên Tử Bo
Mô hình nguyên tử Bo là một trong những bước ngoặt quan trọng trong sự phát triển của lý thuyết nguyên tử, nhưng nó cũng có những hạn chế so với các mô hình khác. Dưới đây là phân tích chi tiết về ưu và nhược điểm của mô hình Bo, cũng như so sánh với các mô hình khác như mô hình nguyên tử của Rutherford và mô hình cơ học lượng tử hiện đại.
5.1 Ưu điểm của mô hình nguyên tử Bo
- Giải thích thành công quang phổ nguyên tử: Mô hình Bo giải thích một cách chính xác quang phổ vạch của nguyên tử hydro, một trong những thành tựu quan trọng nhất của nó. Đặc biệt, công thức tính năng lượng của các mức quỹ đạo electron là một bước tiến lớn trong vật lý nguyên tử.
- Đơn giản và dễ hiểu: Mô hình này giúp người học hình dung rõ ràng hơn về cách electron quay quanh hạt nhân, và sự phát ra hoặc hấp thụ năng lượng khi electron di chuyển giữa các quỹ đạo.
5.2 Nhược điểm của mô hình nguyên tử Bo
- Giới hạn trong phạm vi áp dụng: Mô hình Bo chỉ chính xác cho các nguyên tử đơn giản như hydro. Nó không thể áp dụng cho các nguyên tử phức tạp hơn hoặc các hệ thống có nhiều electron.
- Không giải thích được hiệu ứng Zeeman và Stark: Mô hình Bo không thể giải thích các hiện tượng như sự tách vạch quang phổ dưới tác dụng của từ trường (hiệu ứng Zeeman) hoặc điện trường (hiệu ứng Stark).
5.3 So sánh với các mô hình nguyên tử khác
| Mô hình | Đặc điểm chính | Ưu điểm | Nhược điểm |
|---|---|---|---|
| Mô hình Rutherford | Hạt nhân dương ở trung tâm, electron quay quanh | Đặt nền móng cho mô hình Bo | Không giải thích được quang phổ nguyên tử |
| Mô hình Bo | Electron quay quanh hạt nhân theo quỹ đạo cố định | Giải thích được quang phổ nguyên tử hydro | Không áp dụng cho các nguyên tử phức tạp |
| Mô hình cơ học lượng tử | Electron có tính chất sóng, không có quỹ đạo cố định | Áp dụng rộng rãi cho mọi nguyên tử và phân tử | Khó hình dung hơn |
Nhìn chung, mặc dù mô hình Bo có những hạn chế nhất định, nhưng nó đã đóng góp rất lớn vào sự hiểu biết của con người về cấu trúc nguyên tử và quang phổ nguyên tử. Mô hình này cũng là bước đệm quan trọng để phát triển các lý thuyết phức tạp hơn trong cơ học lượng tử.
XEM THÊM:
6. Kết Luận
Mô hình nguyên tử Bo là một bước tiến quan trọng trong lịch sử phát triển của lý thuyết nguyên tử. Dù có những hạn chế và không thể áp dụng cho mọi nguyên tử, mô hình này đã giúp định hình hiểu biết cơ bản về cấu trúc nguyên tử, đặc biệt là khả năng giải thích quang phổ của nguyên tử hydro. Nhờ sự đơn giản và trực quan, mô hình Bo trở thành một công cụ giáo dục hữu ích, giúp người học dễ dàng nắm bắt các khái niệm phức tạp về vật lý nguyên tử.
Qua các nghiên cứu và so sánh với những mô hình khác, mô hình Bo không chỉ cung cấp cái nhìn sâu sắc về nguyên tử mà còn mở đường cho các lý thuyết tiên tiến hơn trong cơ học lượng tử. Với những ứng dụng rộng rãi trong giáo dục, nghiên cứu khoa học và công nghệ, mô hình Bo tiếp tục đóng góp vào sự tiến bộ của khoa học hiện đại, đồng thời là một minh chứng cho tầm quan trọng của việc không ngừng tìm kiếm và khám phá những điều mới mẻ trong khoa học.
Tóm lại, mô hình nguyên tử Bo tuy đơn giản nhưng có vai trò vô cùng quan trọng, không chỉ trong việc giảng dạy và học tập mà còn trong nghiên cứu khoa học và các ứng dụng thực tế. Nó là một trong những bước đầu tiên đưa chúng ta đến với sự hiểu biết sâu rộng hơn về cấu trúc và tính chất của vật chất ở cấp độ nguyên tử.