Chủ đề 0 1 mol nguyên tử o: Bài viết này sẽ giúp bạn hiểu rõ về khái niệm 0,1 mol nguyên tử oxy, cách tính số nguyên tử, khối lượng cũng như những ứng dụng quan trọng trong các lĩnh vực hóa học, sinh học, và công nghiệp. Hãy cùng khám phá những thông tin chi tiết và hữu ích để nắm vững kiến thức này.
Mục lục
0,1 Mol Nguyên Tử Oxy
Trong hóa học, khái niệm "mol" được sử dụng để đo lượng chất. Một mol tương ứng với số lượng Avogadro, tức là khoảng \(6,022 \times 10^{23}\) hạt (nguyên tử, phân tử, ion, v.v.). Khi chúng ta nói về 0,1 mol nguyên tử oxy, chúng ta đang đề cập đến số lượng nguyên tử oxy trong một lượng chất có 0,1 mol.
Số Nguyên Tử Trong 0,1 Mol Oxy
Số lượng nguyên tử oxy trong 0,1 mol có thể được tính bằng cách nhân số mol với hằng số Avogadro:
Ứng Dụng Của 0,1 Mol Oxy
Việc tính toán số lượng nguyên tử trong một lượng chất nhất định như 0,1 mol oxy có ứng dụng trong nhiều lĩnh vực của hóa học, bao gồm:
- Xác định khối lượng của một chất cần thiết để phản ứng hoàn toàn với một chất khác trong phản ứng hóa học.
- Tính toán nồng độ của dung dịch.
- Thiết kế và tính toán trong các quá trình sản xuất công nghiệp.
Ví Dụ Thực Tế
Giả sử bạn có 0,1 mol nguyên tử oxy và bạn muốn biết khối lượng của lượng oxy này. Bạn có thể sử dụng khối lượng molar của oxy (\(16 \, \text{g/mol}\)) để tính toán:
Như vậy, 0,1 mol nguyên tử oxy tương đương với 1,6 gram oxy.
Kết Luận
Hiểu và sử dụng khái niệm mol và số Avogadro là rất quan trọng trong hóa học, giúp tính toán chính xác lượng chất và số lượng hạt vi mô trong các phản ứng và quá trình hóa học.

1. Giới Thiệu Về Mol và Nguyên Tử Oxy
Trong hóa học, mol là đơn vị đo lường lượng chất. Một mol tương ứng với số Avogadro, tức là khoảng \(6,022 \times 10^{23}\) hạt như nguyên tử, phân tử, hoặc ion. Khái niệm này giúp các nhà khoa học đo lường và so sánh các lượng chất trong các phản ứng hóa học.
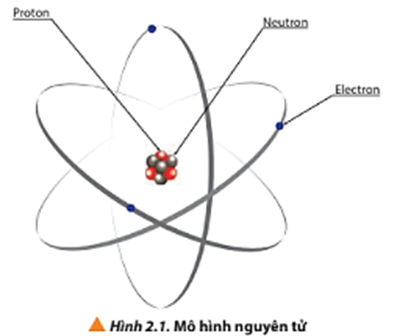
Nguyên tử oxy là một trong những nguyên tố cơ bản của hóa học, có ký hiệu là O và số nguyên tử là 8. Oxy tồn tại phổ biến trong tự nhiên và là thành phần chính trong nhiều hợp chất quan trọng.
Ví dụ, khi nói về 0,1 mol nguyên tử oxy, ta đang đề cập đến một lượng có \(0,1 \times 6,022 \times 10^{23}\) nguyên tử oxy, tức là khoảng \(6,022 \times 10^{22}\) nguyên tử.
- Mol: Đơn vị đo lường lượng chất trong hóa học.
- Nguyên tử Oxy: Nguyên tố hóa học cơ bản với ký hiệu O và số nguyên tử 8.
- Số Avogadro: \(6,022 \times 10^{23}\) hạt trong một mol chất.
Việc hiểu rõ về mol và nguyên tử oxy là rất quan trọng trong hóa học, giúp tính toán lượng chất, tỷ lệ phản ứng và các ứng dụng thực tế khác.
2. Tính Toán Số Nguyên Tử Oxy Trong 0,1 Mol
Để tính toán số nguyên tử oxy trong 0,1 mol, chúng ta cần sử dụng số Avogadro, được ký hiệu là \(N_A\), với giá trị khoảng \(6,022 \times 10^{23}\) hạt/mol. Số Avogadro biểu thị số hạt (như nguyên tử hoặc phân tử) trong một mol của bất kỳ chất nào.
Với 0,1 mol nguyên tử oxy, ta sẽ thực hiện phép tính sau:
- Số Avogadro: \(N_A = 6,022 \times 10^{23}\) hạt/mol.
- Số mol: \(n = 0,1\) mol.
- Số nguyên tử oxy trong 0,1 mol: \(n \times N_A = 0,1 \times 6,022 \times 10^{23} = 6,022 \times 10^{22}\) nguyên tử.
Như vậy, trong 0,1 mol nguyên tử oxy có khoảng \(6,022 \times 10^{22}\) nguyên tử oxy.
Việc tính toán này rất quan trọng trong việc xác định lượng chất trong các phản ứng hóa học và là cơ sở cho nhiều ứng dụng trong nghiên cứu và công nghiệp.

3. Khối Lượng Của 0,1 Mol Nguyên Tử Oxy
Để tính toán khối lượng của 0,1 mol nguyên tử oxy, trước tiên chúng ta cần biết khối lượng mol của nguyên tử oxy, ký hiệu là \(M_O\). Khối lượng mol của oxy được xác định là khoảng \(16 \, \text{g/mol}\).
Khối lượng của 0,1 mol nguyên tử oxy có thể được tính theo công thức:
- Khối lượng mol của oxy: \(M_O = 16 \, \text{g/mol}\).
- Số mol: \(n = 0,1\) mol.
- Khối lượng: \(m = n \times M_O = 0,1 \times 16 = 1,6 \, \text{g}\).
Như vậy, khối lượng của 0,1 mol nguyên tử oxy là \(1,6 \, \text{g}\). Điều này cho phép chúng ta hiểu rõ hơn về lượng chất và cách chúng tương tác trong các phản ứng hóa học, cũng như trong nhiều ứng dụng khác.

4. Vai Trò Của Oxy Trong Hóa Học
Oxy là một trong những nguyên tố quan trọng nhất trong hóa học, đóng vai trò thiết yếu trong nhiều phản ứng hóa học và quá trình sinh học. Dưới đây là một số vai trò chính của oxy trong hóa học:
- Phản ứng oxy hóa - khử: Oxy tham gia vào các phản ứng oxy hóa - khử, nơi nó thường đóng vai trò là chất oxy hóa, nhận electron từ các chất khác, dẫn đến sự hình thành các hợp chất mới. Ví dụ, quá trình đốt cháy là một dạng phản ứng oxy hóa phổ biến.
- Hô hấp tế bào: Trong sinh học, oxy là yếu tố quan trọng trong quá trình hô hấp tế bào, nơi nó được sử dụng để chuyển hóa glucose thành năng lượng dưới dạng ATP, hỗ trợ các hoạt động sống của cơ thể.
- Thành phần của nước: Oxy kết hợp với hydro tạo thành nước (\(H_2O\)), một hợp chất cần thiết cho sự sống và nhiều quá trình hóa học khác.
- Tham gia trong các hợp chất hữu cơ và vô cơ: Oxy là thành phần quan trọng của nhiều hợp chất hữu cơ (như rượu, axit carboxylic) và vô cơ (như oxit kim loại), có ứng dụng rộng rãi trong công nghiệp và đời sống.
Với vai trò đa dạng và quan trọng, oxy là một trong những yếu tố không thể thiếu trong việc duy trì sự sống và thúc đẩy các phản ứng hóa học, giúp mở rộng hiểu biết và ứng dụng trong nhiều lĩnh vực khác nhau.

5. Kết Luận
Oxy là một nguyên tố vô cùng quan trọng không chỉ trong hóa học mà còn trong đời sống hàng ngày. Việc hiểu rõ về khái niệm mol và cách tính toán số lượng nguyên tử trong một lượng mol nhất định giúp chúng ta có cái nhìn sâu sắc hơn về cấu trúc vật chất và các phản ứng hóa học. Qua các phần trên, chúng ta đã nắm bắt được cách tính toán và vai trò của oxy trong nhiều lĩnh vực, từ các phản ứng hóa học cơ bản đến ứng dụng trong đời sống.
0,1 mol nguyên tử oxy tương đương với một lượng cụ thể các nguyên tử oxy, đóng vai trò quan trọng trong nhiều phản ứng hóa học. Việc tính toán chính xác số lượng nguyên tử và khối lượng tương ứng giúp chúng ta áp dụng trong các bài toán thực tế, đồng thời nâng cao hiệu quả trong học tập và nghiên cứu hóa học.
Tóm lại, oxy không chỉ là một yếu tố quan trọng trong các phản ứng hóa học mà còn là chìa khóa mở ra hiểu biết sâu rộng hơn về bản chất của các chất và phản ứng hóa học. Việc nắm vững kiến thức về oxy và các tính toán liên quan là cơ sở để tiếp tục khám phá và phát triển trong lĩnh vực hóa học.