Chủ đề số đơn vị điện tích hạt nhân là gì: Số đơn vị điện tích hạt nhân là một khái niệm quan trọng trong hóa học và vật lý, giúp xác định vị trí của nguyên tố trong bảng tuần hoàn và đặc tính của chúng. Bài viết này sẽ cung cấp kiến thức đầy đủ và dễ hiểu về số đơn vị điện tích hạt nhân, từ khái niệm cơ bản đến ứng dụng thực tế, giúp bạn nắm vững chủ đề này.
Mục lục
- Số Đơn Vị Điện Tích Hạt Nhân Là Gì?
- 1. Khái niệm Số Đơn Vị Điện Tích Hạt Nhân
- 2. Cách Tính Số Đơn Vị Điện Tích Hạt Nhân
- 3. Ứng Dụng Của Số Đơn Vị Điện Tích Hạt Nhân
- 4. Mối Quan Hệ Giữa Số Đơn Vị Điện Tích Hạt Nhân và Số Khối
- 5. Tính Chất Hóa Học Liên Quan Đến Số Đơn Vị Điện Tích Hạt Nhân
- 6. Các Bài Tập Liên Quan Đến Số Đơn Vị Điện Tích Hạt Nhân
Số Đơn Vị Điện Tích Hạt Nhân Là Gì?
Số đơn vị điện tích hạt nhân của một nguyên tử, còn được gọi là số hiệu nguyên tử, là một đại lượng quan trọng trong hóa học và vật lý. Đây là con số biểu thị số lượng proton có trong hạt nhân của nguyên tử đó, và được ký hiệu bằng chữ cái Z.
Ý Nghĩa Của Số Đơn Vị Điện Tích Hạt Nhân
- Xác định nguyên tố hóa học: Mỗi nguyên tố hóa học có một số đơn vị điện tích hạt nhân duy nhất. Ví dụ, nguyên tố carbon có Z = 6, nghĩa là hạt nhân của nó có 6 proton.
- Xác định số electron: Trong một nguyên tử trung hòa về điện, số đơn vị điện tích hạt nhân cũng là số lượng electron quay quanh hạt nhân. Điều này có nghĩa là số proton bằng số electron.
- Vị trí trong bảng tuần hoàn: Số hiệu nguyên tử xác định vị trí của nguyên tố trong bảng tuần hoàn hóa học. Ví dụ, hydro có Z = 1 và nằm ở vị trí đầu tiên của bảng tuần hoàn.
Công Thức Tính Số Đơn Vị Điện Tích Hạt Nhân
Công thức để xác định số đơn vị điện tích hạt nhân của một nguyên tử là:
Trong đó:
- Z: Số đơn vị điện tích hạt nhân (số hiệu nguyên tử).
- p: Số lượng proton trong hạt nhân của nguyên tử.
Một Số Ví Dụ Về Số Đơn Vị Điện Tích Hạt Nhân
| Nguyên Tố | Ký Hiệu Hóa Học | Số Proton (Z) |
|---|---|---|
| Hydro | H | 1 |
| Cacbon | C | 6 |
| Oxi | O | 8 |
| Natri | Na | 11 |
Ứng Dụng Của Số Đơn Vị Điện Tích Hạt Nhân
- Xác định đồng vị: Các nguyên tố có cùng số đơn vị điện tích hạt nhân nhưng khác nhau về số neutron được gọi là các đồng vị.
- Sử dụng trong nghiên cứu: Số hiệu nguyên tử là thông tin cần thiết để xác định đặc tính hóa học và vật lý của một nguyên tố, cũng như để hiểu sâu hơn về cấu trúc nguyên tử.

1. Khái niệm Số Đơn Vị Điện Tích Hạt Nhân
Số đơn vị điện tích hạt nhân của một nguyên tử, còn được gọi là số hiệu nguyên tử, là số lượng proton có trong hạt nhân của nguyên tử đó. Đây là một đại lượng quan trọng giúp xác định đặc tính hóa học và vật lý của nguyên tử, đồng thời quyết định vị trí của nguyên tố trong bảng tuần hoàn.
Theo nguyên lý cơ bản của hóa học, mỗi nguyên tử của một nguyên tố hóa học cụ thể đều có số đơn vị điện tích hạt nhân cố định, được ký hiệu bằng chữ cái Z. Số này không thay đổi, bất kể trạng thái hóa học hay vật lý của nguyên tử.
Công thức tính số đơn vị điện tích hạt nhân được biểu diễn bằng:
- Z: Số đơn vị điện tích hạt nhân.
- p: Số lượng proton trong hạt nhân của nguyên tử.
Ví dụ, nguyên tử cacbon có 6 proton trong hạt nhân, do đó số đơn vị điện tích hạt nhân của cacbon là . Tương tự, nguyên tử oxy có 8 proton, nên số đơn vị điện tích hạt nhân là .
Số đơn vị điện tích hạt nhân cũng là yếu tố xác định tính chất hóa học của nguyên tố, như khả năng phản ứng, độ âm điện, và liên kết hóa học. Bằng cách biết số hiệu nguyên tử, ta có thể suy ra được cấu trúc electron và từ đó, dự đoán được hành vi hóa học của nguyên tố trong các phản ứng.
2. Cách Tính Số Đơn Vị Điện Tích Hạt Nhân
Số đơn vị điện tích hạt nhân, hay còn gọi là số hiệu nguyên tử, được xác định thông qua số lượng proton có trong hạt nhân của nguyên tử. Việc tính toán số đơn vị điện tích hạt nhân là một quá trình đơn giản và trực tiếp dựa trên thông tin về hạt nhân nguyên tử.
Công thức tính số đơn vị điện tích hạt nhân được biểu diễn như sau:
- Z: Số đơn vị điện tích hạt nhân (số hiệu nguyên tử).
- p: Số lượng proton trong hạt nhân của nguyên tử.
Để tính số đơn vị điện tích hạt nhân của một nguyên tử, bạn cần xác định số lượng proton trong hạt nhân của nó. Số proton này là một giá trị duy nhất cho mỗi nguyên tố hóa học và không thay đổi. Chẳng hạn, nếu một nguyên tử có 11 proton trong hạt nhân, thì số đơn vị điện tích hạt nhân của nó sẽ là:
Dưới đây là một bảng ví dụ về số đơn vị điện tích hạt nhân của một số nguyên tố phổ biến:
| Nguyên Tố | Ký Hiệu Hóa Học | Số Proton (Z) |
|---|---|---|
| Hydro | H | 1 |
| Cacbon | C | 6 |
| Oxy | O | 8 |
| Natri | Na | 11 |
Như vậy, việc tính toán số đơn vị điện tích hạt nhân là quá trình đơn giản, chỉ cần xác định số lượng proton trong hạt nhân nguyên tử để có được giá trị .

3. Ứng Dụng Của Số Đơn Vị Điện Tích Hạt Nhân
Số đơn vị điện tích hạt nhân không chỉ là một khái niệm cơ bản trong hóa học mà còn có nhiều ứng dụng quan trọng trong nhiều lĩnh vực khoa học và đời sống. Dưới đây là một số ứng dụng chính của số đơn vị điện tích hạt nhân:
- Xác định vị trí của nguyên tố trong bảng tuần hoàn: Số đơn vị điện tích hạt nhân xác định vị trí của một nguyên tố trong bảng tuần hoàn. Các nguyên tố được sắp xếp theo thứ tự tăng dần của số hiệu nguyên tử (Z), giúp dễ dàng nhận biết và phân loại các nguyên tố.
- Xác định tính chất hóa học của nguyên tố: Số đơn vị điện tích hạt nhân ảnh hưởng trực tiếp đến cấu trúc electron của nguyên tử, từ đó quyết định tính chất hóa học của nguyên tố. Ví dụ, nguyên tử có số Z khác nhau sẽ có số lượng electron khác nhau, dẫn đến tính chất hóa học khác nhau.
- Xác định đồng vị của nguyên tố: Các nguyên tố có cùng số đơn vị điện tích hạt nhân nhưng khác nhau về số neutron được gọi là các đồng vị. Việc xác định số hiệu nguyên tử giúp phân biệt các đồng vị khác nhau của cùng một nguyên tố.
- Sử dụng trong nghiên cứu vật lý hạt nhân: Trong lĩnh vực vật lý hạt nhân, số đơn vị điện tích hạt nhân là một thông số quan trọng để nghiên cứu cấu trúc và tính chất của hạt nhân nguyên tử. Nó cũng giúp các nhà khoa học hiểu rõ hơn về các phản ứng hạt nhân và sự phân rã của nguyên tử.
- Ứng dụng trong y học: Số đơn vị điện tích hạt nhân của các nguyên tố phóng xạ được sử dụng trong y học hạt nhân để chẩn đoán và điều trị bệnh. Ví dụ, các đồng vị phóng xạ được sử dụng trong xạ trị để tiêu diệt tế bào ung thư.
- Ứng dụng trong công nghiệp: Trong công nghiệp, số đơn vị điện tích hạt nhân được sử dụng để kiểm tra chất lượng vật liệu, đặc biệt là thông qua các kỹ thuật như quang phổ XRF (X-ray fluorescence) để phân tích thành phần hóa học của các vật liệu khác nhau.
Như vậy, số đơn vị điện tích hạt nhân đóng vai trò quan trọng trong việc xác định nhiều tính chất và ứng dụng khác nhau của nguyên tố, từ lý thuyết đến thực tiễn.
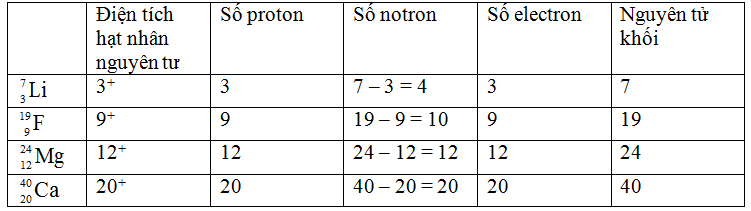
4. Mối Quan Hệ Giữa Số Đơn Vị Điện Tích Hạt Nhân và Số Khối
Số đơn vị điện tích hạt nhân (Z) và số khối (A) là hai đại lượng quan trọng trong việc xác định các đặc tính của nguyên tử. Chúng có mối quan hệ chặt chẽ với nhau và giúp xác định cấu trúc cũng như tính chất của nguyên tố.
- Số đơn vị điện tích hạt nhân (Z): Là số proton có trong hạt nhân của nguyên tử, quyết định bản chất hóa học của nguyên tố và vị trí của nó trong bảng tuần hoàn.
- Số khối (A): Là tổng số proton và neutron trong hạt nhân của một nguyên tử. Số khối được tính theo công thức:
- Z: Số đơn vị điện tích hạt nhân (số proton).
- N: Số neutron trong hạt nhân.
Do đó, số khối của một nguyên tử phản ánh tổng khối lượng của các hạt nhân hạ nguyên tử, trong khi số đơn vị điện tích hạt nhân xác định tính chất hóa học của nguyên tố đó. Ví dụ, nguyên tử Cacbon có Z = 6 và thường có A = 12, do có 6 neutron trong hạt nhân.
Mối quan hệ giữa Z và A là cơ sở để hiểu rõ hơn về các đồng vị của nguyên tố. Các đồng vị có cùng số đơn vị điện tích hạt nhân nhưng khác nhau về số khối, nghĩa là chúng có cùng số proton nhưng khác số neutron.
Ví dụ:
| Nguyên Tố | Số Proton (Z) | Số Neutron (N) | Số Khối (A) |
|---|---|---|---|
| Hydro-1 | 1 | 0 | 1 |
| Hydro-2 (Deuterium) | 1 | 1 | 2 |
| Carbon-12 | 6 | 6 | 12 |
| Carbon-14 | 6 | 8 | 14 |
Như vậy, số đơn vị điện tích hạt nhân và số khối không chỉ giúp xác định cấu trúc nguyên tử mà còn hỗ trợ trong việc phân biệt các đồng vị của cùng một nguyên tố. Điều này rất quan trọng trong nhiều lĩnh vực nghiên cứu khoa học và ứng dụng thực tiễn.

5. Tính Chất Hóa Học Liên Quan Đến Số Đơn Vị Điện Tích Hạt Nhân
Số đơn vị điện tích hạt nhân (Z) không chỉ xác định vị trí của nguyên tố trong bảng tuần hoàn mà còn ảnh hưởng trực tiếp đến các tính chất hóa học của nguyên tố. Các tính chất hóa học này bao gồm khả năng tạo liên kết, độ âm điện, và tính chất axit-bazơ, tất cả đều liên quan mật thiết đến cấu trúc electron của nguyên tử.
- Độ âm điện: Độ âm điện của một nguyên tố là khả năng hút electron của nó trong một liên kết hóa học. Độ âm điện tăng khi số đơn vị điện tích hạt nhân tăng, do lực hút giữa hạt nhân và các electron hóa trị mạnh hơn. Ví dụ, trong cùng một chu kỳ, fluor (Z = 9) có độ âm điện cao hơn nhiều so với natri (Z = 11).
- Năng lượng ion hóa: Năng lượng ion hóa là năng lượng cần thiết để loại bỏ một electron khỏi nguyên tử. Năng lượng ion hóa tăng khi số đơn vị điện tích hạt nhân tăng, vì lực hút giữa hạt nhân và electron trở nên mạnh hơn, đòi hỏi nhiều năng lượng hơn để tách electron ra khỏi nguyên tử. Điều này giải thích tại sao các nguyên tố thuộc nhóm khí hiếm có năng lượng ion hóa rất cao.
- Kích thước nguyên tử: Kích thước nguyên tử giảm khi số đơn vị điện tích hạt nhân tăng trong cùng một chu kỳ. Số proton tăng kéo các electron vào gần hạt nhân hơn, làm giảm bán kính nguyên tử. Kích thước này ảnh hưởng đến nhiều tính chất khác như tính kim loại và phi kim của nguyên tố.
- Tính chất axit-bazơ: Số đơn vị điện tích hạt nhân cũng ảnh hưởng đến tính chất axit-bazơ của các hợp chất. Ví dụ, oxit của các nguyên tố có số Z cao thường có tính axit, trong khi oxit của các nguyên tố kim loại kiềm có tính bazơ.
Như vậy, số đơn vị điện tích hạt nhân đóng vai trò quan trọng trong việc xác định và giải thích các tính chất hóa học của nguyên tố. Từ khả năng phản ứng đến tính chất vật lý, tất cả đều chịu ảnh hưởng mạnh mẽ bởi số proton trong hạt nhân của nguyên tử.
XEM THÊM:
6. Các Bài Tập Liên Quan Đến Số Đơn Vị Điện Tích Hạt Nhân
Dưới đây là một số bài tập giúp củng cố kiến thức về số đơn vị điện tích hạt nhân:
6.1. Bài tập tính số đơn vị điện tích hạt nhân
Bài tập 1: Tính số đơn vị điện tích hạt nhân của các nguyên tử sau:
- Nguyên tử Carbon (C): Biết rằng nguyên tử Carbon có 6 proton trong hạt nhân.
- Nguyên tử Neon (Ne): Biết rằng nguyên tử Neon có 10 proton trong hạt nhân.
Hướng dẫn:
- Số đơn vị điện tích hạt nhân (Z) chính là số proton trong hạt nhân nguyên tử. Do đó:
- Đối với Carbon, Z = 6.
- Đối với Neon, Z = 10.
6.2. Bài tập liên quan đến đồng vị
Bài tập 2: Xét hai đồng vị của nguyên tố Chlorine: 35Cl và 37Cl. Biết rằng tỷ lệ tự nhiên của 35Cl là 75.77% và của 37Cl là 24.23%. Tính nguyên tử khối trung bình của Chlorine.
Hướng dẫn:
- Áp dụng công thức tính nguyên tử khối trung bình:
\[
\text{Nguyên tử khối trung bình} = \frac{{75.77 \times 35 + 24.23 \times 37}}{{100}}
\]
- Tính toán cụ thể:
\[
\text{Nguyên tử khối trung bình} = \frac{{75.77 \times 35 + 24.23 \times 37}}{{100}} = 35.4846 \, \text{u}
\]
6.3. Bài tập ứng dụng thực tế
Bài tập 3: Một mẫu chất X có tổng số hạt (proton, neutron, electron) là 46, trong đó số proton bằng số neutron và nhiều hơn số electron là 1. Tìm ký hiệu hóa học của nguyên tố X.
Hướng dẫn:
- Gọi số proton là p, số neutron là n, số electron là e. Theo đề bài, ta có các phương trình:
- p + n + e = 46
- p = n
- p = e + 1
- Giải hệ phương trình này để tìm p, n, và e:
- p = 15, n = 15, e = 14.
- Suy ra nguyên tố X là Phosphorus (P), với ký hiệu 31P.