Chủ đề nguyên tố có năng lượng ion hóa nhỏ nhất là: Nguyên tố có năng lượng ion hóa nhỏ nhất là một trong những khái niệm quan trọng trong hóa học, ảnh hưởng đến nhiều phản ứng hóa học khác nhau. Bài viết này sẽ giúp bạn hiểu rõ hơn về nguyên tố này, tại sao nó có năng lượng ion hóa thấp nhất, và những ứng dụng thực tế của nó trong cuộc sống.
Mục lục
Nguyên Tố Có Năng Lượng Ion Hóa Nhỏ Nhất Là Gì?
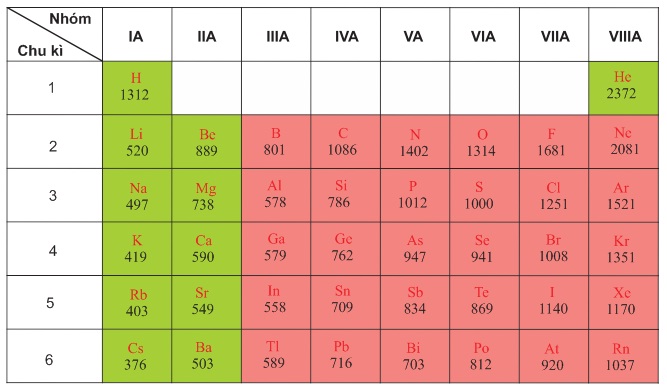
Năng lượng ion hóa là năng lượng cần thiết để tách một electron ra khỏi nguyên tử hoặc ion. Trong bảng tuần hoàn các nguyên tố hóa học, năng lượng ion hóa có xu hướng thay đổi theo một quy luật nhất định. Năng lượng ion hóa giảm dần từ trên xuống dưới trong một nhóm và tăng dần từ trái sang phải trong một chu kỳ.
Nguyên Tố Có Năng Lượng Ion Hóa Nhỏ Nhất
Theo quy luật này, nguyên tố có năng lượng ion hóa nhỏ nhất là Franxi (Fr). Đây là nguyên tố thuộc nhóm kim loại kiềm, nằm ở vị trí cuối cùng trong bảng tuần hoàn các nguyên tố. Năng lượng ion hóa đầu tiên của Franxi chỉ vào khoảng 400 kJ/mol, thấp nhất trong tất cả các nguyên tố. Điều này làm cho Franxi dễ dàng mất electron và trở thành ion dương.
Quy Luật Thay Đổi Năng Lượng Ion Hóa
- Năng lượng ion hóa giảm từ trên xuống dưới trong một nhóm: Điều này xảy ra do bán kính nguyên tử tăng, khiến lực hút giữa hạt nhân và electron yếu đi.
- Năng lượng ion hóa tăng từ trái sang phải trong một chu kỳ: Điều này là do số proton trong hạt nhân tăng lên, làm tăng lực hút giữa hạt nhân và electron.
Tác Động Của Năng Lượng Ion Hóa Đến Tính Chất Hóa Học
Năng lượng ion hóa ảnh hưởng trực tiếp đến tính chất hóa học của các nguyên tố. Những nguyên tố có năng lượng ion hóa thấp như Franxi dễ mất electron, khiến chúng rất hoạt động về mặt hóa học. Ngược lại, những nguyên tố có năng lượng ion hóa cao như Helium (He) rất khó bị ion hóa, khiến chúng khá ổn định.
Bảng So Sánh Năng Lượng Ion Hóa Của Một Số Nguyên Tố
| Nguyên Tố | Năng Lượng Ion Hóa (kJ/mol) |
| Franxi (Fr) | 400 |
| Cesium (Cs) | 376 |
| Helium (He) | 2372 |
Kết Luận
Việc hiểu rõ năng lượng ion hóa không chỉ giúp chúng ta biết được tính chất hóa học của các nguyên tố mà còn giúp dự đoán khả năng tham gia phản ứng của chúng. Franxi, với năng lượng ion hóa thấp nhất, là một ví dụ điển hình cho thấy tính chất hoạt động mạnh mẽ của các nguyên tố có năng lượng ion hóa thấp.
Tổng Quan Về Năng Lượng Ion Hóa
Năng lượng ion hóa là một khái niệm quan trọng trong hóa học, biểu thị năng lượng cần thiết để loại bỏ một electron từ nguyên tử hoặc ion, chuyển chúng từ trạng thái trung hòa thành ion dương. Hiểu rõ năng lượng ion hóa giúp chúng ta hiểu sâu hơn về tính chất hóa học và khả năng phản ứng của các nguyên tố.
- Định nghĩa: Năng lượng ion hóa là năng lượng cần thiết để tách một electron khỏi nguyên tử hoặc ion trong trạng thái khí.
- Đơn vị: Năng lượng ion hóa thường được đo bằng đơn vị kJ/mol.
Năng lượng ion hóa có thể được hiểu rõ hơn thông qua một số quy luật và yếu tố ảnh hưởng:
- Quy luật: Trong bảng tuần hoàn, năng lượng ion hóa thường tăng dần từ trái sang phải qua các chu kỳ và giảm dần từ trên xuống dưới trong cùng một nhóm.
- Yếu tố ảnh hưởng:
- Bán kính nguyên tử: Nguyên tử có bán kính càng lớn, lực hút giữa hạt nhân và electron ngoài cùng càng yếu, làm giảm năng lượng ion hóa.
- Số proton trong hạt nhân: Số lượng proton tăng làm tăng lực hút giữa hạt nhân và electron, làm tăng năng lượng ion hóa.
Việc nắm bắt năng lượng ion hóa không chỉ giúp hiểu rõ tính chất hóa học của các nguyên tố mà còn giúp dự đoán khả năng tham gia phản ứng của chúng. Các nguyên tố có năng lượng ion hóa thấp thường có xu hướng dễ dàng mất electron, trở thành ion dương và phản ứng mạnh mẽ với các chất khác.
| Nguyên tố | Năng lượng ion hóa (kJ/mol) |
| Helium (He) | 2372 |
| Hydrogen (H) | 1312 |
| Oxygen (O) | 1314 |
Qua bảng trên, chúng ta có thể thấy rằng các nguyên tố có năng lượng ion hóa cao như Helium rất khó mất electron và do đó rất bền vững về mặt hóa học.
So Sánh Năng Lượng Ion Hóa Giữa Các Nguyên Tố
Năng lượng ion hóa của các nguyên tố là một đại lượng quan trọng, giúp xác định khả năng của một nguyên tử mất electron và trở thành ion dương. Sự so sánh giữa các nguyên tố có thể tiết lộ nhiều thông tin về tính chất hóa học của chúng, đặc biệt là trong việc dự đoán khả năng phản ứng.
- Nguyên tố có năng lượng ion hóa nhỏ nhất: Như đã đề cập, Franxi (Fr) là nguyên tố có năng lượng ion hóa nhỏ nhất, chỉ cần một lượng năng lượng rất thấp để loại bỏ electron ngoài cùng.
- Nguyên tố có năng lượng ion hóa lớn nhất: Helium (He) có năng lượng ion hóa lớn nhất trong bảng tuần hoàn, điều này phản ánh sự ổn định của nó do lực hút mạnh giữa hạt nhân và electron.
Để so sánh cụ thể hơn, chúng ta có thể xem xét một số nguyên tố khác nhau và năng lượng ion hóa của chúng:
| Nguyên tố | Năng lượng ion hóa thứ nhất (kJ/mol) | Vị trí trong bảng tuần hoàn |
| Helium (He) | 2372 | Nhóm 18 |
| Lithium (Li) | 520 | Nhóm 1 |
| Oxygen (O) | 1314 | Nhóm 16 |
| Cesium (Cs) | 376 | Nhóm 1 |
| Franxi (Fr) | ≈380 | Nhóm 1 |
Các nguyên tố thuộc nhóm kim loại kiềm như Lithium (Li), Cesium (Cs) và Franxi (Fr) có năng lượng ion hóa rất thấp. Điều này là do electron ngoài cùng của chúng ở xa hạt nhân, làm giảm lực hút và dễ dàng bị loại bỏ.
- So sánh giữa các nhóm: Các nguyên tố thuộc cùng một nhóm thường có xu hướng giảm dần năng lượng ion hóa khi di chuyển từ trên xuống dưới do bán kính nguyên tử tăng lên.
- So sánh giữa các chu kỳ: Năng lượng ion hóa tăng dần từ trái sang phải trong cùng một chu kỳ, do lực hút giữa hạt nhân và electron ngoài cùng tăng lên khi số proton trong hạt nhân tăng.
Việc so sánh năng lượng ion hóa giữa các nguyên tố không chỉ giúp chúng ta hiểu rõ hơn về tính chất hóa học của chúng mà còn cung cấp thông tin quan trọng trong việc dự đoán phản ứng hóa học và sự ổn định của các hợp chất chúng tạo thành.

Ảnh Hưởng Của Năng Lượng Ion Hóa Đến Tính Chất Hóa Học
Năng lượng ion hóa là một yếu tố quan trọng ảnh hưởng trực tiếp đến tính chất hóa học của nguyên tố. Năng lượng này quyết định mức độ khó khăn trong việc loại bỏ electron khỏi nguyên tử, từ đó ảnh hưởng đến khả năng phản ứng của nguyên tố.
- Độ hoạt động của kim loại: Các nguyên tố có năng lượng ion hóa thấp như các kim loại kiềm (Li, Na, K) dễ dàng mất electron để tạo thành ion dương, do đó chúng có tính hoạt động hóa học mạnh. Ví dụ, Franxi (Fr) là kim loại có năng lượng ion hóa thấp nhất, dẫn đến tính hoạt động hóa học cao nhất trong nhóm.
- Tính chất của phi kim: Ngược lại, các phi kim như Oxygen (O) hay Fluor (F) có năng lượng ion hóa cao, khó mất electron hơn, và thường có xu hướng nhận electron để tạo thành ion âm. Điều này giải thích tại sao các phi kim có xu hướng tạo thành hợp chất ion với kim loại.
Khi so sánh các nguyên tố trong bảng tuần hoàn, năng lượng ion hóa không chỉ ảnh hưởng đến khả năng tạo ion mà còn đến độ âm điện và khả năng tạo liên kết. Năng lượng ion hóa càng cao, nguyên tố càng khó mất electron, dẫn đến tính chất hóa học ổn định hơn.
- Liên kết hóa học: Năng lượng ion hóa cao thường đi kèm với khả năng tạo liên kết cộng hóa trị mạnh, đặc biệt là trong các phân tử phi kim. Ngược lại, năng lượng ion hóa thấp thường thấy ở các nguyên tố tạo liên kết ion.
- Phản ứng hóa học: Nguyên tố có năng lượng ion hóa thấp thường tham gia phản ứng một cách dễ dàng, đặc biệt là các phản ứng oxy hóa khử, trong khi các nguyên tố có năng lượng ion hóa cao thường bền hơn và ít phản ứng hơn.
Như vậy, năng lượng ion hóa là một yếu tố quan trọng quyết định tính chất hóa học của nguyên tố, ảnh hưởng đến khả năng phản ứng, loại liên kết hóa học và tính chất của các hợp chất mà nguyên tố đó tham gia.
Ứng Dụng Của Năng Lượng Ion Hóa Trong Thực Tế
Năng lượng ion hóa không chỉ là một khái niệm quan trọng trong hóa học mà còn có nhiều ứng dụng thực tế trong đời sống và các ngành công nghiệp. Khả năng đo lường và sử dụng năng lượng ion hóa giúp các nhà khoa học và kỹ sư phát triển nhiều công nghệ tiên tiến.
- Ứng dụng trong phân tích hóa học: Năng lượng ion hóa được sử dụng trong các phương pháp phân tích như phổ khối lượng (Mass Spectrometry), nơi các ion được tạo ra từ mẫu chất cần phân tích để xác định thành phần và cấu trúc hóa học.
- Trong ngành công nghiệp bán dẫn: Năng lượng ion hóa đóng vai trò quan trọng trong quá trình cấy ion (Ion Implantation) vào các chất bán dẫn, điều chỉnh tính chất điện của chúng để chế tạo các vi mạch điện tử.
- Ứng dụng trong y học: Năng lượng ion hóa cũng được sử dụng trong thiết bị chẩn đoán và điều trị như các máy chụp X-quang và điều trị ung thư bằng xạ trị, nơi các tia ion hóa có thể tiêu diệt tế bào ung thư mà không gây tổn thương lớn đến mô xung quanh.
Ngoài ra, năng lượng ion hóa còn được ứng dụng trong các công nghệ xử lý nước, làm sạch không khí, và nghiên cứu môi trường. Nhờ hiểu biết về năng lượng ion hóa, con người có thể cải tiến các phương pháp xử lý và bảo vệ môi trường hiệu quả hơn.
- Xử lý nước: Năng lượng ion hóa được áp dụng trong các công nghệ như điện phân, giúp loại bỏ tạp chất và khử trùng nước.
- Làm sạch không khí: Máy lọc không khí sử dụng công nghệ ion hóa để loại bỏ bụi và các chất gây ô nhiễm, cải thiện chất lượng không khí trong nhà và văn phòng.
- Nghiên cứu môi trường: Các thiết bị đo năng lượng ion hóa được sử dụng để phân tích chất lượng môi trường, từ đó đưa ra các biện pháp bảo vệ và cải thiện môi trường sống.
Qua những ứng dụng này, có thể thấy năng lượng ion hóa không chỉ là một khái niệm lý thuyết mà còn có vai trò thiết yếu trong nhiều lĩnh vực thực tế, góp phần nâng cao chất lượng cuộc sống và thúc đẩy sự phát triển của khoa học công nghệ.

.png)