Chủ đề cấu hình electron của nguyên tử biểu diễn: Cấu hình electron của nguyên tử là nền tảng quan trọng trong hóa học, giúp giải thích nhiều tính chất và hiện tượng trong tự nhiên. Bài viết này sẽ cung cấp hướng dẫn chi tiết về cách biểu diễn cấu hình electron, cùng với các ví dụ minh họa và ứng dụng thực tế để người đọc dễ dàng nắm bắt và áp dụng.
Mục lục
Cấu Hình Electron của Nguyên Tử và Cách Biểu Diễn
Cấu hình electron của nguyên tử là một cách biểu diễn sự sắp xếp các electron trong các lớp và phân lớp xung quanh hạt nhân. Việc hiểu rõ cấu hình electron giúp giải thích nhiều tính chất hóa học của nguyên tố, như tính chất liên kết và khả năng phản ứng.
Cách Viết Cấu Hình Electron
- Nguyên tắc Hund: Các electron sẽ điền vào các orbital theo cách mà số electron độc thân là tối đa trước khi bắt cặp.
- Nguyên lý Pauli: Mỗi orbital chỉ chứa tối đa 2 electron với spin ngược chiều nhau.
- Quy tắc Aufbau: Các electron sẽ điền vào các orbital có mức năng lượng thấp hơn trước.
Các Dạng Biểu Diễn Cấu Hình Electron
- Biểu diễn theo dạng chuẩn: Dùng các ký hiệu \(\text{1s}^2\), \(\text{2s}^2\), \(\text{2p}^6\)... để mô tả số electron trong các lớp và phân lớp tương ứng.
- Biểu diễn theo ô orbital: Các ô orbital được biểu diễn dưới dạng các ô vuông hoặc hình chữ nhật, trong đó các electron được biểu diễn bằng các mũi tên ngược chiều nhau.
Ví Dụ Biểu Diễn Cấu Hình Electron
Ví dụ với nguyên tử có số hiệu nguyên tử \(Z = 8\) (Oxy):
Cấu hình electron: \(1s^2 2s^2 2p^4\)
Biểu diễn theo ô orbital:
| 1s | \(\uparrow \downarrow\) |
| 2s | \(\uparrow \downarrow\) |
| 2p | \(\uparrow \downarrow\) \(\uparrow\) \(\uparrow\) |
Ứng Dụng Của Cấu Hình Electron
Cấu hình electron được sử dụng để:
- Giải thích tính chất hóa học của nguyên tố.
- Dự đoán cấu trúc phân tử và hình dạng hình học của các hợp chất.
- Giải thích sự hình thành ion và liên kết hóa học.
Việc nắm vững cấu hình electron là nền tảng để hiểu sâu hơn về hóa học, giúp học sinh dễ dàng nắm bắt và vận dụng kiến thức trong thực tế.
Mục Lục Tổng Hợp Về Cấu Hình Electron
Cấu hình electron của nguyên tử là kiến thức quan trọng giúp hiểu rõ về cấu trúc và tính chất của các nguyên tố hóa học. Dưới đây là mục lục tổng hợp các nội dung liên quan đến cấu hình electron được trình bày chi tiết để bạn dễ dàng nắm bắt.
- Khái niệm cơ bản về cấu hình electron
- Nguyên tắc xây dựng cấu hình electron
- Cách biểu diễn cấu hình electron
- Ví dụ cụ thể về cấu hình electron
- Liên hệ giữa cấu hình electron và bảng tuần hoàn
- Ứng dụng của cấu hình electron trong hóa học
- Bài tập về cấu hình electron
- Những lỗi thường gặp khi học cấu hình electron
Cung cấp những kiến thức nền tảng về cấu hình electron, bao gồm cách các electron được sắp xếp trong các lớp và phân lớp xung quanh hạt nhân.
Trình bày chi tiết các nguyên tắc Pauli, Hund, và Aufbau trong việc điền electron vào các orbital. Giải thích vì sao các nguyên tắc này quan trọng trong việc xác định cấu hình electron chính xác.
Giới thiệu các phương pháp biểu diễn cấu hình electron như biểu diễn dạng chuẩn (ví dụ: \(1s^2 2s^2 2p^6\)) và biểu diễn bằng ô orbital với các mũi tên chỉ electron.
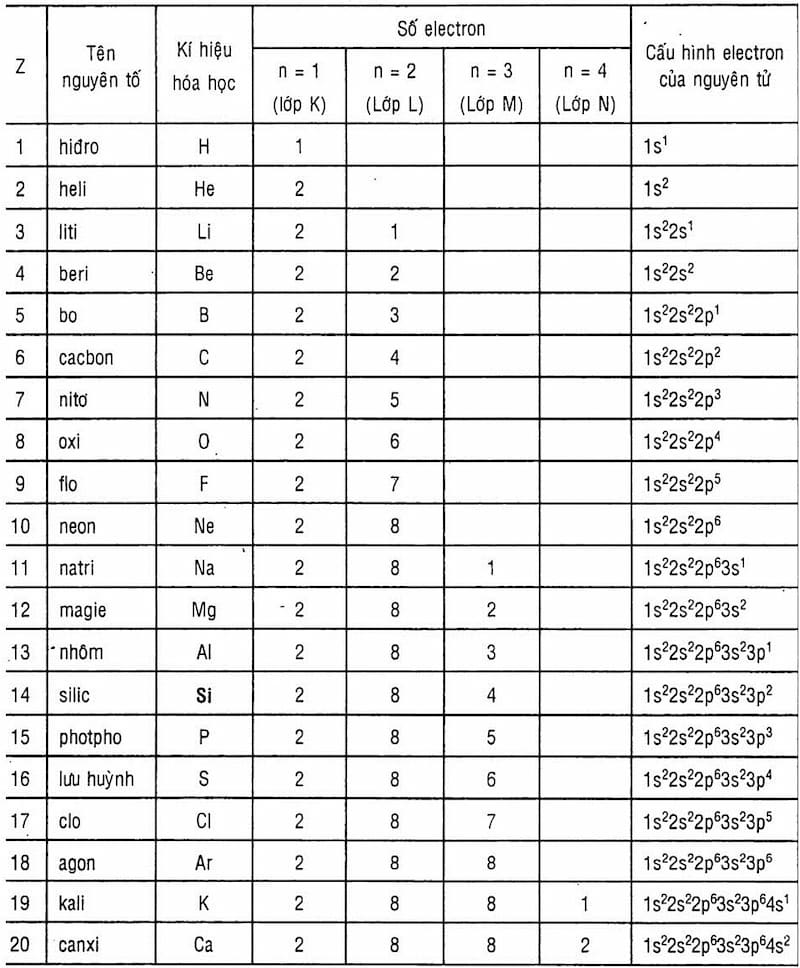
Cung cấp các ví dụ minh họa cho cấu hình electron của các nguyên tố phổ biến như Oxy, Natri, và các nguyên tố khác. Hướng dẫn từng bước để viết cấu hình electron cho mỗi nguyên tố.
Phân tích cách cấu hình electron quyết định vị trí của nguyên tố trong bảng tuần hoàn, cũng như cách nhóm và chu kỳ liên quan đến cấu hình electron.
Khám phá các ứng dụng thực tiễn của cấu hình electron trong việc dự đoán tính chất hóa học, cấu trúc phân tử, và phản ứng hóa học. Cung cấp ví dụ cụ thể về cách cấu hình electron được sử dụng trong nghiên cứu và công nghiệp.
Đưa ra các bài tập trắc nghiệm và tự luận về cấu hình electron để kiểm tra kiến thức. Kèm theo đó là hướng dẫn giải chi tiết và các mẹo làm bài.
Nhận diện các lỗi phổ biến mà học sinh thường mắc phải khi viết cấu hình electron, cùng với các gợi ý và phương pháp học hiệu quả để tránh những sai lầm này.
Phân Tích Chuyên Sâu Về Cấu Hình Electron
Cấu hình electron không chỉ đơn giản là cách sắp xếp các electron xung quanh hạt nhân, mà còn là chìa khóa để giải mã nhiều hiện tượng hóa học. Phân tích sâu hơn về cấu hình electron giúp chúng ta hiểu rõ hơn về tính chất của các nguyên tố, cũng như các quy luật tự nhiên mà chúng tuân theo.
- 1. Ảnh hưởng của cấu hình electron đến tính chất hóa học:
- 2. Vai trò của cấu hình electron trong việc xác định vị trí của nguyên tố trong bảng tuần hoàn:
- 3. Liên kết hóa học và cấu hình electron:
- 4. Cấu hình electron và tính chất từ của vật chất:
- 5. Những sai lầm phổ biến khi viết cấu hình electron:
- 6. Ứng dụng của cấu hình electron trong nghiên cứu và công nghiệp:
Cấu hình electron quyết định tính chất hóa học của nguyên tố, chẳng hạn như độ âm điện, năng lượng ion hóa, và bán kính nguyên tử. Các electron lớp ngoài cùng (electron hóa trị) đóng vai trò quan trọng trong các phản ứng hóa học, quyết định khả năng cho nhận electron của nguyên tử.
Cấu hình electron là cơ sở để xếp các nguyên tố vào các nhóm và chu kỳ trong bảng tuần hoàn. Các nguyên tố cùng nhóm có cấu hình electron hóa trị giống nhau, dẫn đến những tính chất hóa học tương tự. Ví dụ, các nguyên tố thuộc nhóm halogen đều có 7 electron ở lớp ngoài cùng.
Cấu hình electron của các nguyên tử trước và sau khi tham gia liên kết hóa học cho thấy sự thay đổi trong cấu trúc electron, từ đó giải thích sự hình thành các liên kết ion, liên kết cộng hóa trị, và liên kết kim loại. Chẳng hạn, liên kết ion hình thành khi nguyên tử kim loại nhường electron cho phi kim.
Các trạng thái từ tính của nguyên tố và hợp chất có liên quan chặt chẽ với cấu hình electron, đặc biệt là sự phân bố của các electron độc thân trong các orbital. Nguyên tố có electron độc thân thường có tính thuận từ, trong khi các nguyên tố không có electron độc thân thường là nghịch từ.
Việc nắm vững các nguyên tắc Pauli, Hund và Aufbau là cần thiết để tránh sai lầm khi viết cấu hình electron. Một lỗi phổ biến là không tuân thủ nguyên tắc Hund khi điền electron vào các orbital ngang bằng nhau, hoặc nhầm lẫn khi xác định số electron ở lớp vỏ ngoài cùng.
Hiểu rõ cấu hình electron cho phép dự đoán và điều chỉnh các tính chất của vật liệu, từ đó phát triển các hợp chất mới trong nghiên cứu hóa học và ứng dụng trong công nghiệp, như sản xuất chất bán dẫn, hợp kim, và các loại vật liệu tiên tiến khác.
















